偶氮苯类人工受体中间体的合成及1H NMR谱
2011-12-27赵小菁范圣第
赵小菁,田 甜,支 云,范圣第
(大连民族学院生命科学学院,辽宁大连 116605)
偶氮苯类人工受体中间体的合成及1H NMR谱
赵小菁,田 甜,支 云,范圣第
(大连民族学院生命科学学院,辽宁大连 116605)
在一种仿G蛋白耦合型信号转导的人工超分子系统中引入一类偶氮苯结构的化合物,用来模拟跨膜受体。以苯胺为原料,合成几种人工受体中间体-偶氮苯化合物,选取其中4,4’-二羧基偶氮苯与谷氨酸甲酯(GluOMe)进行连接,得到一种氨基酸甲酯偶氮苯衍生物(Azo-AAOMe),并对其1H NMR谱进行了研究。核磁谱图显示,所合成的化合物正是预期产物。
偶氮苯;人工受体;1H NMR谱
细胞信号转导过程与细胞周期调控、细胞分裂、细胞代谢、细胞增殖等紧密相关。研究细胞膜上各个重要环节蛋白质之间的相互作用及生物体系信号转导中重要分子事件的过程和机理,一直是生命科学研究的目标[1]。跨膜细胞信号转导过程与受体蛋白的结构与功能紧密相关,受体是位于细胞表面或细胞内亚细胞结构中的一种糖蛋白或糖脂分子,它能够选择性的识别外来信号,并与之结合,从而激活或启动一系列生化反应,产生特定的生物学效应,通常所说的受体是指膜受体。根据细胞膜表面受体信号转换机制和受体分子的结构特点,细胞膜表面受体分为激动剂控制的离子通道型受体、G蛋白耦合型受体和酶活性受体三类。
目前G蛋白耦合型和具有酶活性受体型仿生信号转导体系在模型的构建方面已经有了一些成功的报导[2]。一种在作为细胞膜模型的人工双层膜囊泡上使用能稳定插入囊泡双层膜中的合成固醇类化合物为受体,以邻羟基萘醛为信号分子的仿G蛋白耦合型信号转导超分子体系已经被构 建[3-4],如图1。

图1 仿G蛋白耦合型信号转导人工超分子体系示意图
本文试图在该系统中引入一类含有偶氮苯结构的化合物,用来模拟跨膜受体,可令系统接受光信号刺激后改变受体构象从而影响信号分子的传递,具体结构如图2。光致异构是指有机分子通过光的激发,其分子结构在两种不同形式之间的可逆转换。近年来国内外的不少研究小组利用有机材料这种性质,发展新型的光器件[5-10]。偶氮苯是一个典型的光致变色分子,在不同波长光照射下,其分子内的-N=N-基团会可逆地实现顺式 - 反式异构化[11-12]。
将偶氮苯类化合物引入生物体系的受体结构中,这在国内研究中尚属首次,在化学生物学的研究领域具有一定的意义。由于受体的基本结构单元是多肽且人工合成相对较难,所以选取偶氮苯化合物与氨基酸及其衍生物进行连接,作一个初步模拟的尝试,为此我们合成了几种偶氮苯类人工受体的中间体,合成路线如图3,并对化合物的1H NMR谱作了研究。根据核磁谱图可以判断所合成的化合物为预期产物,这为下一步的研究工作奠定了重要的基础。

图2 顺反偶氮苯结构示意图


图3 几种偶氮苯的合成路线示意图
1 材料与方法
1.1 仪器与试剂
DF-101S集热式恒温磁力搅拌器(河南巩义市英峪予华仪器厂);HR-200电子天平(OHAUS Adventurer);SHZ-D(Ⅲ)循环水式真空泵(河南巩义市英峪予华仪器厂);DHG-9070型电热恒温鼓风干燥箱(上海精宏实验设备厂);PHS-25 Bench PH/MV METER;Shimazu UV2450紫外-可见分光光度计;IWAKI ASAHI REN-1旋转蒸发仪;Mercury Vx 300核磁共振仪(300Hz)。试剂均为市售的化学纯或分析纯,苯丙氨酸甲酯为实验室自制。
1.2 4,4’-二羧基偶氮苯的合成
合成方法一:
(1)对碘苯胺的合成:将30 mL水,20 mmol NaHCO3(1.68 g)和9 mmol苯胺(0.92 g)混合,待固体全部溶解后,在激烈搅拌下分批加入10 mmol碘(2.5 g),室温下搅拌2 h,过滤,无水乙醇重结晶,得白色晶体,产率为70%。
(2)4,4’-二碘偶氮苯的合成:将13.7 mmol对碘苯胺(3 g),3.13 mmol KMnO4(5.1 g)和20.26 mmol CuSO4·5H2O(5.1 g) 溶解于 80 mLCHCl3中,室温下搅拌 3 d,过滤,粗产品以CH2Cl2为展开剂进行提纯,产率为15%。
(3)4,4’-二氰基偶氮苯的合成:在25 mL圆底烧瓶中,加入6 mmol4,4’-二碘偶氮苯,0.006 mmolPd(OAc)2,10 mLDMAC,1.2 mmol K4[Fe(CN)6]·3H2O和6 mmolNa2CO3,130℃下N2保护反应1.5 h,结束后,降至室温,加入20 mL乙酸乙酯,过滤,依次用15 mL水洗涤2次,15 mL 5%氨水洗涤1次,最后无水Na2SO4干燥,直接进入下一步实验。
(4)4,4’-二羧基偶氮苯的合成:100 mL单口瓶中,加入 14.0 g 乙二醇,0.33 mol水(6.0 g)和0.03 mol对苯甲基苯甲氰(5.8 g),加热搅拌,令苯甲氰分散于乙二醇水溶液中,迅速加入NaOH(20.0 g,0.50 mol),回流3.5 h,冷却后,反应混合物倾入400 mL水中稀释,滤去白色不溶物,滤液用盐酸调节到pH=2,析出黄色固体,水洗至中性,烘干后乙醇-水重结晶,产率为60%。
合成方法二:
在500 mL三颈瓶中依次加入38.9 mmol对硝基苯甲酸,625 mmol NaOH(25 g)和120 mL水,温度控制在50℃。将227.5 mmol葡萄糖(50 g)溶于75 mL的水中,30 min内滴入三颈瓶中,维持温度 50~60℃,反应 8 h后停止,冷却至室温。混合物用稀醋酸中和至pH=6左右,过滤,水洗,固体用热碳酸钾溶解,酸化,析出固体,抽滤,水洗至中性,100℃真空干燥24 h,得到浅黄色固体4.21 g,产率为80%。
1.3 4,4’-羟基偶氮苯的合成
在250 mL的三颈烧瓶中加入0.05 mol对氨基苯酚,12.5 mL 36%的盐酸溶液,7.5 mL36%的乙酸和37.5 mL水,将三口烧瓶置于冰盐浴中降温,待温度降到5℃以下时,开始用恒压滴液漏斗滴加30%的亚硝酸钠水溶液12.5 mL,滴加完毕后,保持温度5℃以下45 min,溶液颜色呈深红黑色。反应停止后,过量的亚硝酸钠用尿素除去,得紫红色重氮盐。
在另外的三口烧瓶中加入0.05 mol苯酚及12.5 mL水,35℃机械搅拌0.5 h,开始同时滴加重氮盐溶液和1.3 mol·L-1碳酸钠水溶液,保持相同的滴速。全部滴加完毕后,保持35℃继续反应4 h,pH维持在7~7.5,4 h后将温度升至60℃,反应2 h,溶液呈紫红色,停止反应,用稀盐酸酸化至pH=2,静置2 h,水洗过滤,所得紫红色固体真空干燥2 h,苯重结晶得红色固体,产率为70%。
1.4 4,4’-二谷氨酸甲酯偶氮苯(Azo-Glu-OMe)的合成
先称取0.51 g 4,4’-二羧基偶氮苯,0.50 g HoBt(1-羟基-苯并-三氮唑),0.76 g EDCHCl(1-乙基-(3-二甲基氨基丙基)羰二亚胺盐酸盐)以及50 mL二氯甲烷,放入圆底烧瓶中,0℃下搅拌0.5 h后,再加入0.51 g谷氨酸甲酯和0.59 g NMM(氮甲基吗啉),反应于室温下搅拌12 h后停止,旋蒸除去溶剂,得橙红色固体,用二氯甲烷(V)∶乙醚(V)=1∶0~1∶0.2作梯度淋洗剂,硅胶柱色谱提纯后,收集第二带即为所需产物,产率为65%。
2 结果与讨论
2.1 1H NMR 谱图1
H NMR谱图如图4。GluOMe和Azo-Glu-OMe的化学位移对比图如图5。


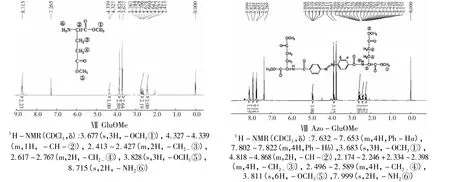
图4 偶氮苯类人工受体中间体的1H NMR谱图

图5 GluOMe和Azo-GluOMe的化学位移对比图
由图4可看出,对碘苯胺作为原料合成4,4’-二碘偶氮苯之后,3.675 ppm处的游离氨基峰消失,形成偶氮结构。原先氨基的给电子效应变成偶氮基团的强烈吸电子效应,与其相邻的苯环氢所受的屏蔽效应大大降低[13],化学位移从6.460~6.482变为7.858 ~7.878 ppm,与碘相邻的苯环氢也受到相应的影响,从7.395~7.416位移至7.635 ~7.656。进一步合成 4,4’- 二羧基偶氮苯之后,该产物在氯仿中的溶解度极低,因此采用氘代甲醇作为溶剂得到1H NMR谱图。对氨基苯酚与其产物4,4’-二羟基偶氮苯以及对硝基苯甲酸与其产物4,4’-二羧基偶氮苯,两者的原料与产物的1H NMR数据也具有明显区别,如图4之Ⅲ~Ⅵ所示。对氨基苯酚中的苯环a,b氢的化学位移非常接近,是由于其苯环上两个取代基均具有强给电子效应,但氨基的要大于羟基的,因此将6.625 ~6.647 ppm 归属于 a 氢,而 6.578 ~6.601 ppm则归属于b氢。当形成4,4’-二羟基偶氮苯后,化学位移相距较远。对硝基苯甲酸与其产物4,4’-二羧基偶氮苯则由于硝基和重氮基的拉电子效应大于羧基的,所以苯环a氢处于高场,b氢处于低场。
GluOMe和Azo-GluOMe的1H NMR谱图及标注如图4之Ⅶ和Ⅷ所示,而图5所示为反应前后两者的化学位移对比。可以看出,原料GluOMe反应生成Azo-GluOMe后,其在8.715 ppm处的自由氨基⑥的单峰消失,在7.999 ppm处出现了一个酰胺峰,是由于C=O键π电子环流使C=O键上下的锥体区域为屏蔽区,此时邻位NH上质子氢正处于这个区域,而其侧面的区域为去屏蔽区,因此与氨基相连的次甲基②上的质子氢由4.327~4.339 ppm 位移至 4.818 ~4.868 ppm。正是由于处在了邻位质子的侧面区域,屏蔽效应减弱,化学位移从高场向低场变化。酯基上的甲氧基质子氢发生的变化稍有不同,甲氧基①的化学位移从3.677 ppm变为3.683 ppm,而⑤的化学位移则从3.828 ppm变为3.811 ppm,这可能是由于谷氨酸甲酯的两个酯基所处的空间位置有差别所至。与次甲基相连的两个亚甲基均由低场向高场发生了位移,分别是亚甲基③从2.413~2.427 ppm 到2.174 ~2.246 ppm 和2.334 ~2.398 ppm,亚甲基④从 2.617 ~2.767 ppm 到 2.496 ~2.589 ppm。这意味着在氨基酸与偶氮苯分子连接在一起之后,共轭体系的增大引起的环电流效应增强,即环平面上、下的屏蔽效应增强,这些质子氢受到屏蔽,因此向着高场方向位移[14-15]。
2.2 合成与提纯
4,4’-二羧基偶氮苯的合成过程中,选用了两种方法。方法一是以苯胺为原料,通过一系列转化最后获得产品,该方法的优点是起始原料非常便宜易得,第一步合成步骤十分简单,但是从第二步开始所需的操作大大增加了难度,产率大大降低。因此,本研究选择了方法二。原料选用的是对硝基苯甲酸,葡萄糖作为偶合剂,合成步骤同样十分简单,最后产率也比较高。需要注意的关键点在于,合成结束后混合物用稀醋酸中和时所用酸的量必须要掌握好,否则产品极容易流失,导致产率大大降低。4,4’-二羟基偶氮苯的合成同样要注意最后稀盐酸中和时对使用的酸量有所控制。
4,4’-二羧基偶氮苯与谷氨酸甲酯是采用EDC缩合法,缩合反应的初始阶段需在0℃下进行,所以在谷氨酸甲酯加入前先控制反应在0℃下0.5 h。所得的红色产物需通过色谱柱进行拆分,这只能在实际操作中通过反复摸索才最后确定淋,洗剂的比例为:二氯甲烷(V)∶乙醚(V)=1∶0,1∶0.1,1∶0.2。之后再通过核磁检测,确定第二带为所需产品。
3 结论
合成了一种新型的氨基酸甲酯偶氮苯化合物,对合成过程进行了探索,选取了条件温和、产率较高的路线,并选取了柱色谱的提纯方法,经过反复摸索确定了梯度淋洗剂,并结合核磁共振波谱确定所需产品。用本方法可方便地扩大合成规模,为偶氮苯化合物与氨基酸连接,甚至与多肽的连接,从而引入受体结构的进一步研究奠定了基础,这对于实现受体的人工模拟有着重要的意义。
[1]孙大业,郭艳林,马力耕,等.细胞信号转导[M].北京:科学出版社,2001.
[2]HANCOCK J T.Cell Signaling[M].Harlow:Longman,1997.
[3]KIKICHI J,ARIGA K,SASAKI Y,et al.Control of enzymic activity by artificial cell- surface receptor[J].J.Mol.Catal.B.,2001,11:977 -984.
[4]TIAN W J,SASAKI Y,FAN S - D,et al.Intermolecular Communication on Lipid Bilayer Membrane[J].J.Supramol.Chem.2005,17,113-119.
[5]IKEDA T,TSUTSUMI O.Supplementary information accompanies this communication on[J].Nature's website.Science,1995,268:1873-1875.
[6]YU Y,NAKANO M,IKEDA T.Directed bending of a polymer film by light[J].Nature,2003,425:145 -156.
[7]HUGEL T,HOLLAND N B,CATTANI A,et al.Singlemolecule optomechanical cycle[J].Science,2002,296:1103-1106.
[8]XIE H,LIU Z,HUANG X,et al.Synthesis and non - linear optical materials[J].Eur.Polym.J.,2001,37:497-507.
[9]LI Y B,HE Y N,WANG X G.Photoinduced Deformation of Amphiphilic Azo Polymer Colloidal Spheres[J].J .Am.Chem.Soc.,2005,127(8):2402 -2403.
[10]WANG L,SCHULTZ P G.Expanding the genetic code[J].Angew.Chem.,2005,44:34 -66.
[11]KUMAR G S,NECKERS D C.Photochemistry of azobenzene - containing polymers[J].Chem.Rev.,1989,89:1915-1925.
[12]WU N,DEITERS A,CROPP T A,et al.A genetically encoded photocaged amino Acid[J].J.Am.Chem.Soc.2004,126,14306-14307.
[13]有机化合物的波谱解析[M].药明康德新药开发有限公司分析部,译.上海:华东理工大学出版社,2007.
[14] HAASE J,ECKERT D,SIEGEL H,et al.NMR in pulsed high magnetic fields[J].Physica B.,2004,346:514.
[15]张帆,胡一帆,胡泽宇,超强磁场中核磁共振信号与屏蔽效应的理论研究[J].波谱学杂志,2010,27(2):230.
Synthesis and1H NMR Property of Azo-benzene Artificial Receptor Intermediate
ZHAO Xiao-jing,TIAN Tian,ZHI Yun,FAN Sheng-di
(College of Life Science,Dalian Nationalities University,Dalian Liaoning 116605,China)
A series of Azo-compounds has been introduced into a G-pro Bio-inspired artificial signal transduction system,to simulating the transmembrane receptor of this system.The photoinduced isomerization of azobenzene between the extended(trans)and compact(cis)conformations has been reversibly triggered by light of two differing wavelengths.Using aniline as the material,a series of azo -benzene artificial receptor intermediate has been prepared.The 4,4’-dicarboxylazobenzene has been combinded with GluOMe,then a amino acid ester azobenzene derivatives has been synthesized.The1H NMR properties of these products have been studied.The results showed that the products are the right compounds.
Azo-benzene;artificial receptor;1H NMR property
O622
A
1009-315X(2011)05-0444-06
2011-03-28;最后
2011-06-22
国家自然科学基金资助项目(20872013):中央高校基本科研业务费专项资金资助项目(DC10040108)。
赵小菁(1977-),女,浙江兰溪人,副教授,博士,主要从事化学生物学研究。
(责任编辑 邹永红)
