安定在保存血液中的分解动力学研究1)
2011-06-09温昕娟朱培培张大明贠克明
温昕娟,曹 洁,朱培培,张大明,贠克明
安定是临床上常用的镇静催眠药,但长期服用或大量服用均可引起中毒,安定中毒的案例时有报道[1-3]。本研究建立安定灌胃中毒致死犬的动物模型,研究安定在保存犬血液中的分解动力学。
1 材料与方法
1.1 材料
1.1.1 仪器和试剂 T race DSQ气相色谱-质谱联用仪,美国Finnigan公司;岛津2010GC气相色谱仪,日本岛津公司;安定标准品(购于公安部二所);内标:SKF525(中国标准技术开发公司);其余试剂为国产分析纯。
1.1.2 实验动物 本地杂种犬6只,15 kg~20 kg,雄性,山西医科大学实验动物中心提供。
1.2 实验方法
1.2.1 溶液配制 安定、内标储备液的配制:分别精密称取安定、丙基解痉素(SKF525A,内标物)标准品适量,用无水乙醇溶解并定量稀释制成1.0 mg/mL的标准储备液。
1.2.2 色谱分析条件 气相色谱/质谱联用分析条件:DB-5MS(30 m×0.25 mm×0.25 mm)毛细管柱;载气为高纯氦气,恒流模式,流速1.0 mL/min;进样口温度 250℃;柱温为程序升温:200℃(1 min)→20℃/min→280℃(6 min);传输线温度 250℃;电子轰击电离源(EI),电子能量70 eV,离子源温度250℃;自动调谐方式,发射电流强度 100 μ A;扫描起始时间4 min,扫描范围50 amu~650 amu;分流进样,分流比为10∶1。气相色谱分析条件:DB-5(30 m×0.25 mm×0.25 mm)毛细管柱;载气为高纯氮气,恒压模式,压力150 kPa;进样口温度:250℃;柱温:200℃(1 min)→20℃/min→280℃(6 min);NPD检测器,温度 300℃;不分流进样。
1.2.3 提取分离与检测 血液 1 mL,加水3 mL,加入内标物SKF52510 μ g,硼酸缓冲溶液调pH 为10,5 mL乙醚萃取,振荡10 min,离心,取上清液4 mL置于干燥离心管中。乙醚重新萃取一次,合并有机相,40℃恒温水浴中挥干。残渣加20 μ L乙醇定容,取1 μ L进样。保留时间结合特征离子峰定性,内标法和标准曲线法(气相色谱)定量。
1.2.4 保存犬血中的分解动力学 雄性犬6只,插胃管,2 min内注入2 LD50剂量安定[4],每只犬血分4等份置于20℃、4℃、-20℃、20℃(加氟化钠至浓度为1%)中,于0、7d、14d、28d,60 d、90 d、150 d、210 d检测血液中安定含量。采用 WinNorLin药代动力学软件处理平均药物浓度,拟合分解动力学方程,计算分解半衰期。
2 结 果
2.1 GC和GC/MS检测 安定与内标物及内源性杂质分离良好。详见图1~2。
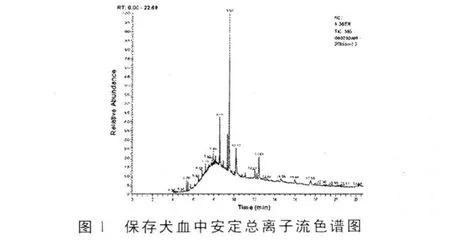
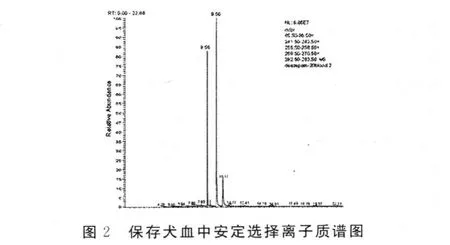
2.2 工作曲线 取空白血分别添加安定0.1、0.2、0.4、0.8、1.0、2.0、4.0、8.0、12.0、24.0、32.0、48.0 μ g 按前述 2.1方法提取测定。所建立的血中安定检测工作曲线、线性范围、相关系数、最低检出限分别为Y=3.0519X-2.8942(X为安定和内标物峰面积比值 ;Y为安定含量 ,μ g/mL或μ g/g)、0.1~ 32μ g/mL、0.998 8μ g/mL 、0.05μ g/mL 。
2.3 回收率及精密度 精密吸取15份空白全血1 mL,分为3组,分别加水3 mL,混匀。每组分别加入安定0.5、1.0、4.0 μ g,按2.1全血样品处理项方法处理测定。同时取1 d内5次测定结果计算日内相对标准差,以3 d内5次测定结果计算日间相对标准差。详见表1。
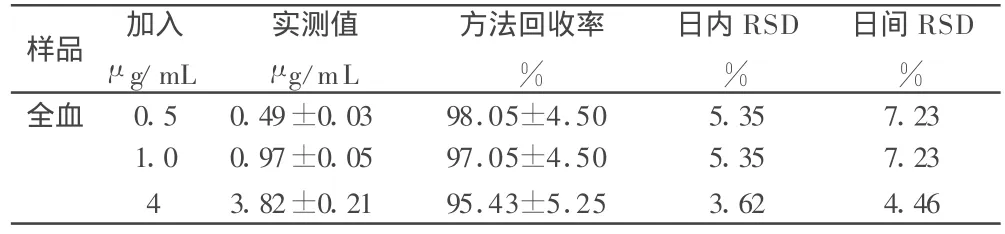
表1 安定提取回收率及精密度(n=5)
2.4 分解动力学研究
2.4.1 温度对保存血液中安定浓度的影响(见表 2、表3)
表2 温度对保存血液中安定浓度的影响(±s)μ g/mL 或μ g/g

表2 温度对保存血液中安定浓度的影响(±s)μ g/mL 或μ g/g
时间(d)20℃ 4℃ -20℃ 20℃(1%NaF)0 102.376±8.560 102.376±8.560 102.376±8.560 102.376±8.560 102.205±6.078 78.724±7.870 87.258±6.620 113.112±4.382 28 90.128±5.637 67.507±5.3921) 64.951±3.0581) 95.906±1.466 56 56.874±2.1351) 31.511±4.4521) 18.520±1.0851) 41.235±6.3711)90 28.560±1.6331) 27.156±3.6401) 15.593±4.1091) 29.748±4.2381)150 26.357±4.4291) 19.632±1.5471) 12.155±3.4241) 19.839±2.0251)210 19.121±4.7991) 26.077±7.9191) 15.529±8.8161) 21.056±8.2331)方差分析,bonferroni法与0时相比,1)P<0.05 7
表3 温度对保存血液中安定下降百分比的影响(±s)%

表3 温度对保存血液中安定下降百分比的影响(±s)%
时间(d)20℃ 4℃ -20℃ 20℃(1%NaF)0 100.0±8.3 100.0±8.3 100.0±8.3 100.0±8.3 99.8±6.1 76.8±7.6 85.2±6.4 110.4±4.2 28 88.0±5.5 65.9±5.21) 63.4±2.91) 93.6±1.4 56 55.5±2.11) 30.7±4.31) 18.0±1.01) 40.2±6.21)90 28.5±1.61) 26.5±3.51) 15.2±4.11) 29.2±4.11)150 27.8±1.51) 19.1±1.51) 11.8±3.31) 19.3±1.91)210 18.6±4.61) 25.4±7.71) 15.1±7.51) 20.5±8.01)方差分析,bonferroni法与0时相比,1)P<0.05 7
2.4.2 分解动力学参数和方程 采用WinNorLin药代动力学软件处理平均药物浓度-时间数据。其分解符合一级动力学过程,可用 Ct=C1e-αt+C2e-βt(Ct 为时间 t测得的含量;C1、C2表示初始含量;t表示时间,单位:天;α、β为一级分解速率常数)。分解动力学方程和参数见表4。根据此方程计算的理论值与实测值符合情况见表4。

表4 不同保存条件下血液中安定分解动力学参数
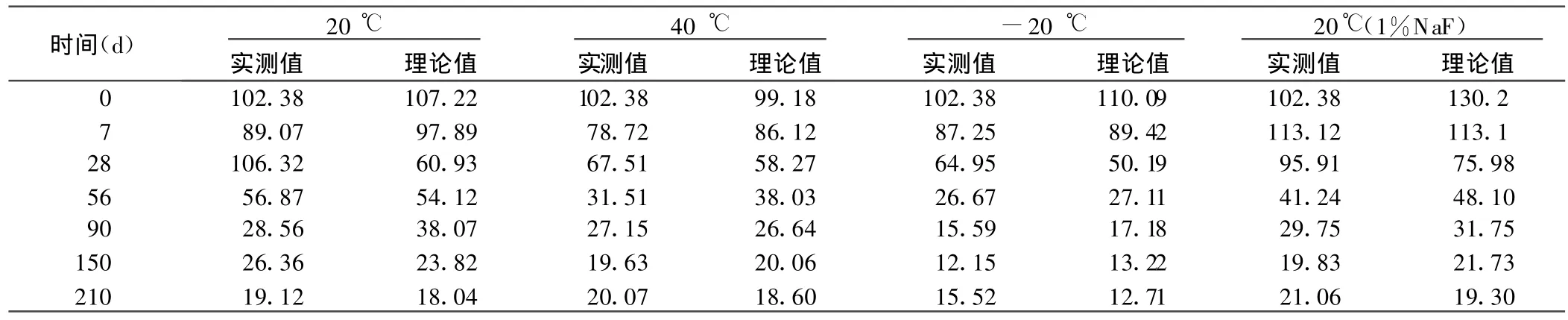
表5 20℃、4℃、-20℃条件下血液中安定理论值与实测值比较
3 结 论
苯骈二氮杂卓类药物在生物检材中的稳定性视母体药物及其代谢物的结构、存储条件和防腐剂的添加有关[6]。室温下血液和组织标本中安定、氟安定以及氟安定的分解产物N-1-脱羟基氟安定在几个月内是稳定的,而安定的分解产物去甲安定不稳定[7]。本实验结果显示,保存28 d~56 d时,犬血中安定含量下降至其初始浓度的55.5%~65.9%,保存210 d时下降至初始浓度的15.2%~25.5%。说明安定等苯骈二氮杂卓类药物在全血和血浆中均可分解。
3.1 温度对保存血液中安定浓度的影响 温度对全血中苯骈二氮杂卓类药物稳定性的影响已有研究[8-10]。本实验结果表明,室温、4℃、-20℃保存210 d犬血中安定含量下降为其初始浓度的15.2%~25.5%,但三个温度间无统计学意义。说明在室温、4℃、-20℃保存时温度对全血中安定稳定性的影响不大。
3.2 防腐剂对保存血液中安定浓度的影响 本实验结果显示,-20℃添加1%氟化钠保存28 d~150 d犬血中安定含量显著高于4℃、-20℃保存犬血中安定浓度,但保存210 d时各组间无统计学意义。说明抑菌剂对保存血液样本安定稳定性也有较小影响,可轻度抑制其中安定的分解。这也可能与本研究采用活体采血,血样细菌污染少有关。
3.3 WinNorLin软件拟合结果分析 血中平均药物浓度-时间数据拟合结果显示,保存全血中安定的分解动力学符合一级动力学过程,可用 Ct=C1e-αt+C2e-βt表示。用此公式计算的安定血浓度理论值与实测值非常接近,说明应用血中安定分解动力学数学模型和参数,可以推测血中药物浓度的经时变化,推断中毒死亡当时或检材采集当时尸体或检材中药物含量,指导选择最佳检材存放条件,正确分析和使用毒物分析结果。
本实验证明安定在保存血液样品中可分解,保存温度和抑菌剂对其影响较小。安定中毒案件法医学鉴定中所采血样应于28 d内送检和检验,否则可用其分解动力学方程和参数推断中毒死亡或检材采集当时的血药浓度。
[1]Wolf CE,Poklis A.A rapid HPLC procedure for analysis of analgesic pharmaceutical mixtures for quality assurance and drug diversion testing[J].Anal T oxicol,2005,29(7):711-714.
[2]郑虎.药物化学[M].北京:人民卫生出版社,2005:100.
[3]陆基宗.学生滥用安定类药物有害[J].家庭医学,2006,2:16.
[4]邓小明,朱科明.常用实验动物麻醉[M].上海:第二军医大学出版社,2001:21.
[5]李玉兰,徐建宁,刘耀.生物试样中安定、利眠宁、舒宁药物及其代谢降解物的GC/MS分析[J].现代仪器,1999(5):12-15.
[6]李云,贠克明.生物检材中常见法医毒物的分解动力学[M].第四届全国法医毒物分析学术交流会论文选,海潮出版社,2008:100-103.
[7]谭家镒,姜兆林.肝、尿中安定等4种药物的固相萃取-紫外导数光谱检测法[J].分析化学,1999,27(11):1317-1319.
[8]Skopp G,Potsch L,Konig I,et al.A preliminary study on the stability of benzodiazepines in blood and plasma stored at 4 degrees C[J].International J Legal Med,1998,111(1):1-5.
[9]ElM ahjoub A,Staub C.Stability of benzodiazepines in whole blood samples stored at varying temperatures[J].J Pharmaceutical&Biomedical Analysis,2000,23(6):1057-1063.
[10]Robertson MD,Drummer OH.Postmortem distribution and redistribution of nitro benzodiazepines in man[J].Forensic Sci,1998,43(1):5-13.
