恩诺沙星混悬液在猪体内残留消除规律研究
2011-03-07刘小艳吴海坤方炳虎袁照红杨利军
刘小艳,吴海坤,方炳虎*,袁照红,杨利军
(1.广东大华农动物保健品股份有限公司,广东新兴527400;2.华南农业大学兽医学院,广东广州510642)
恩诺沙星是动物专用的广谱喹诺酮类抗菌药物,具有杀菌活性强、体内分布广、与其他抗菌药物无交叉耐药性等特点,对细菌、支原体均有效,临床常用于肠炎、肺炎、乳房炎、皮肤及软组织感染的治疗[1]。因恩诺沙星味苦,现研制出恩诺沙星(口服)混悬液以改善猪的适口性以利于治疗猪的黄白痢等肠道疾病。本试验的目的在于研究恩诺沙星(口服)混悬液在猪组织中的残留消除规律,为该制剂在猪的临床使用上提供依据。
1 材料与方法
1.1 材料
1.1.1 试验用动物 选取健康二元杂交猪40头,公母兼有,体重71.3 kg±4.5 kg。试验前饲养观察5 d。本次试验猪均无异常表现,生长状况良好。
1.1.2 试验药品与试剂 恩诺沙星混悬液,含量50 mL/L,批号20090107,由广东大华农动物保健品股份有限公司提供。恩诺沙星对照品,含量99.9%,批号H0080306;盐酸环丙沙星对照品,含量100.0%,批号H010105,均由中国兽医药品监察所提供。乙腈、甲醇为色谱纯试剂,其他试剂为分析纯,水符合GB/T6682规定的二级水。
1.1.3 主要仪器 Agilent1200高效液相色谱系统,配备四元梯度泵、自动进样器、柱恒温系统、荧光检测器、色谱工作站,美国安捷伦公司。
1.1.4 主要试液配制 0.05 mol/L磷酸/三乙胺溶液:取850 g/L磷酸3.4 mL,用水稀释至1 000 mL,搅拌下滴加三乙胺,调pH至2.4;磷酸盐缓冲液(用于肌肉、脂肪组织):取磷酸二氢钾6.8 g,加水使溶解并稀释至500 mL,调pH至7.0;磷酸盐缓冲液(用于肝脏、肾脏组织):取磷酸二氢钾6.8 g,加水溶解并稀释至500 mL,pH为4.0~5.0;恩诺沙星、环丙沙星标准储备液(1 000 μ g/mL):分别精密称取恩诺沙星50.05 mg、盐酸环丙沙星对照品55.22 mg于50 mL的棕色容量瓶,用甲醇定容至刻度,即成1 000 μ g/mL的恩诺沙星、环丙沙星标准储备液,置于4℃冰箱保存,使用期为3个月。
1.2 方法
1.2.1 给药与采样 每头猪按10 mg/kg体重的单次剂量,通过经口灌服方式给药,连续给药3 d,每天1次。在停药后的第0、1、3、5、7、10、14、21天各时间点宰杀5头猪,分别采取臀部肌肉、肝脏、肾脏和脂肪共4种样品,样品采集后立即做好标记、包装,保存于—20℃冰箱,待测。
1.2.2 组织样品预处理 按参考文献[2]进行。
1.2.2.1 提取 准确称取2.0 g已匀浆的各组织样品并分别加磷酸盐缓冲液10.0 mL,10 000 r/min匀浆1 min。匀浆液振荡混合5 min,4 000 r/min离心10 min,用磷酸盐缓冲液10.0 mL冲洗残渣,振荡、离心,合并上清液,备用。
1.2.2.2 净化 C18固相萃取柱依次用2 mL甲醇活化、2 mL磷酸盐缓冲液润洗,润洗完毕后,准确量取5 mL备用液过柱,用2 mL水淋洗,挤干。加1 mL流动相洗脱,挤干,收集洗脱液,摇匀,经滤膜过滤后作为试样溶液,取20 μ L试样溶液进样,供高效液相色谱分析。
1.2.3 色谱条件及工作指标 色谱柱:phenomenex luna-C18,4.6 mm×250 mm,5 μ m;流动相:0.05 mol/L磷酸溶液/三乙胺-乙睛(82+18),用前过0.45 μ m滤膜;流速:0.8 mL/min;检测波长:激发波长280 nm;发射波长450 nm;进样量20 μ L。
1.2.4 各组织标准曲线与线性范围 准确称取2.0 g已匀浆的各空白组织置于50 mL离心管中,再加入100 μ L恩诺沙星、环丙沙星标准系列溶液,涡旋混匀,使得各样品中恩诺沙星、环丙沙星浓度为20 μ g/kg~2 000 μ g/kg。按组织样品预处理方法处理后,进行HPLC分析,将测得的色谱峰面积(S)与药物浓度(C)作直线回归,求得标准曲线的回归方程和相关系数。
1.2.5 组织中恩诺沙星、环丙沙星回收率和变异系数的测定 准确称取2 g已匀浆的各空白组织于50 mL离心管中,加入100 μ L不同浓度的混合标准溶液,其中脂肪与肌肉组织添加浓度为50、100、200 μ g/kg,肝脏组织添加浓度为100、200、400 μ g/kg,肾脏组织添加浓度为150、300、600 μ g/kg,涡旋混匀后放置30 min,按“1.2.2”方法处理,计算回收率及变异系数。
1.2.6 各组织中恩诺沙星与环丙沙星浓度测定各时间点所采猪组织按“1.2.2”方法处理,进行HPLC分析处理,求得恩诺沙星和环丙沙星峰面积,按各组织标准曲线方程求得恩诺沙星及环丙沙星浓度,进而得到各时间点猪各组织中恩诺沙星和环丙沙星的残留含量总和。
1.2.7 休药期的确定 根据农业部有关动物源食品中恩诺沙星和环丙沙星的最高残留限量,获得恩诺沙星混悬液在猪临床应用的休药期。
2 结果
2.1 恩诺沙星和环丙沙星的色谱图
恩诺沙星、环丙沙星标准溶液,空白组织、空白添加样品、连续给药后样品色谱分析图(图1~图4)。
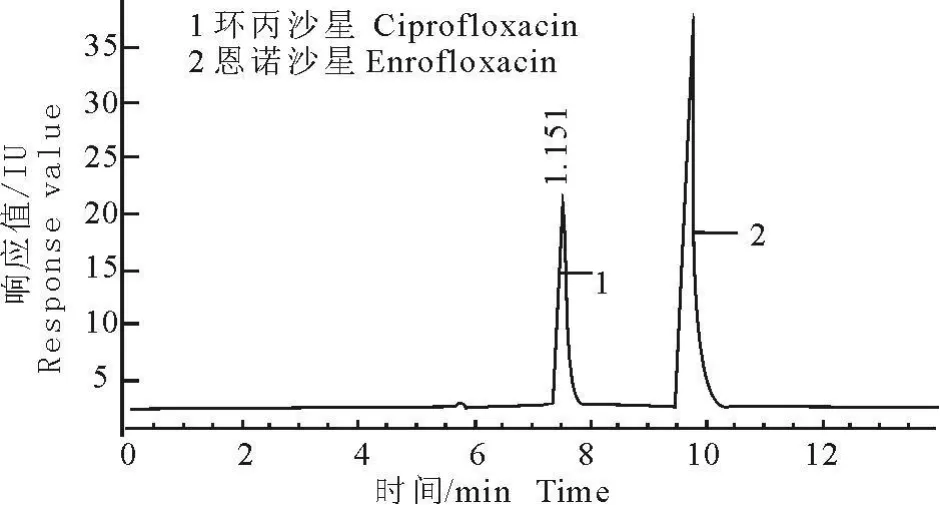
图1 恩诺沙星和环丙沙星标准溶液样(0.25 μ g/mL)色谱图Fi g.1 The chromatogram of 0.25 μ g/mL standard solutions of enrofloxacin and ciprofloxacin
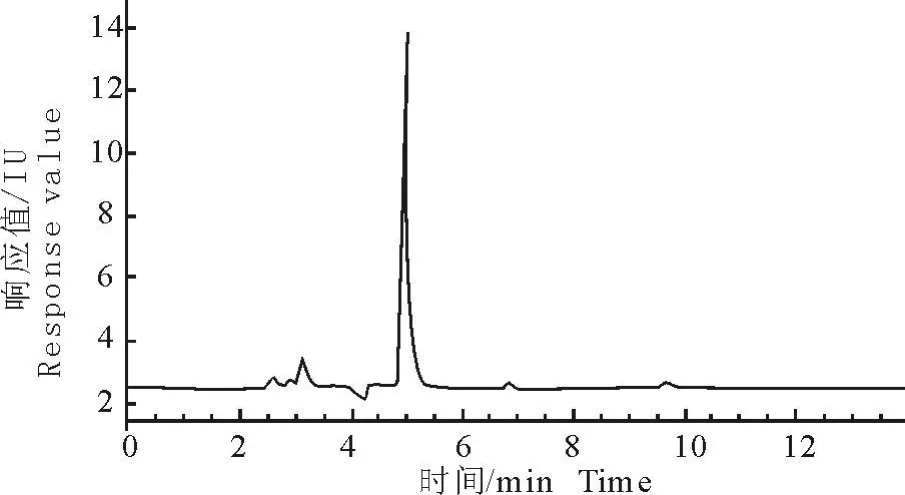
图2 空白肌肉色谱图Fig.2 The chromatog ram of the blank muscle
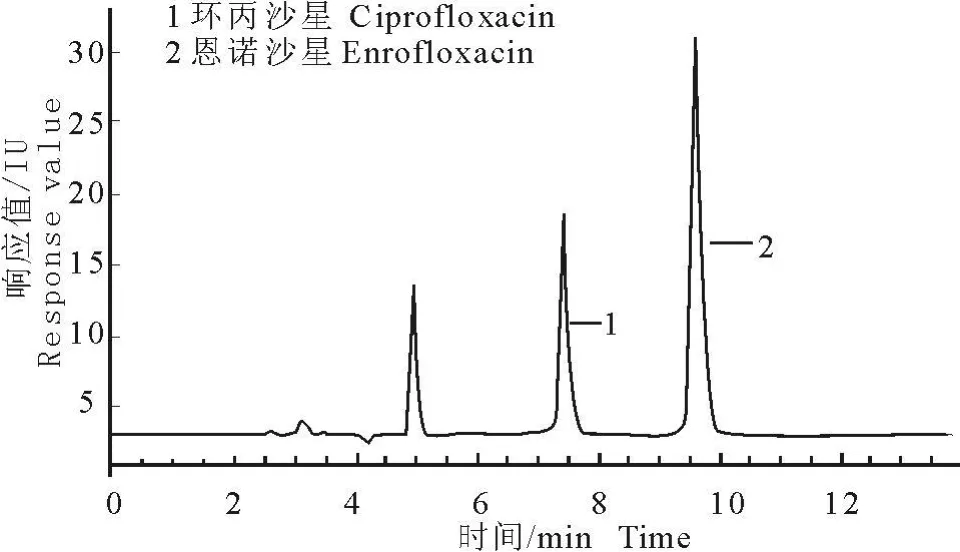
图3 空白肌肉添加恩诺沙星(500 μ g/kg)和环丙沙星(500 μ g/kg)色谱图Fig.3 The chromatogram of the blank muscle adding enrofloxacin(500 μ g/kg)and ciprofloxacin(500 μ g/kg)
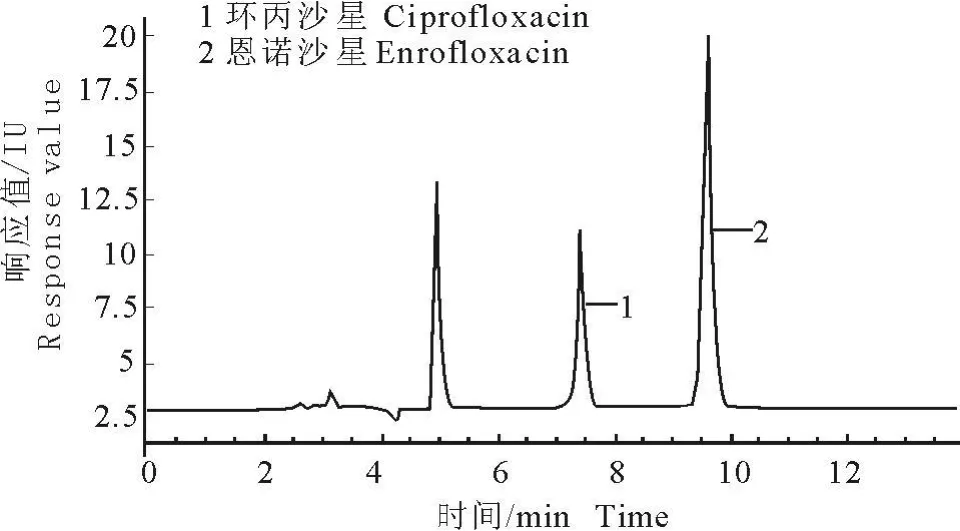
图4 肌肉中恩诺沙星和环丙沙星残留色谱图(1 d) Fig.4 The chromatog ram of enroflox acin and ciprofloxacin of the muscle afer administration 1 d
在以上检测条件下,能将恩诺沙星、环丙沙星与组织中的其他组分分开,干扰少。恩诺沙星、环丙沙星的出峰保留时间分别在9.6 min和7.4 min左右。本次检测方法最低检测限为20 μ g/kg,符合残留检测需要。
2.2 各组织中恩诺沙星和环丙沙星测定的标准曲线与线性范围
2.3 恩诺沙星、环丙沙星回收率和变异系数的测定
在20 μ g/kg~2 000 μ g/kg添加浓度下,各组织的回收率为70.0%~90.0%,变异系数<10.0%,表明该方法灵敏、准确,具有较好的重现性。
2.4 停药后猪各组织中恩诺沙星与环丙沙星残留测定
猪各组织中恩诺沙星和环丙沙星的残留含量总和结果见表2。
2.5 休药期确定
根据农业部公告[3],恩诺沙星给药后以恩诺沙星及其主要代谢物环丙沙星残留量之和为标志残留物,规定在猪各组织中的最高残留限量(maximum residue limit,MRL):肌肉100 μ g/kg,脂肪100 μ g/kg,肝脏200 μ g/kg,肾脏300 μ g/kg。由本次试验结果表明,恩诺沙星混悬液按每头猪10 mg/kg体重剂量,通过灌服方式进行给药,连续使用3 d,以恩诺沙星及其主要代谢物环丙沙星残留之和为标示残留物,残留在肌肉、脂肪中的恩诺沙星和环丙沙星消除较快,第3天总残留量已下降至检测限以下;肝和肾脏中的残留药物消除较缓慢,第3天肾中药物总残留量为185.70 μ g/kg。综合各组织中总残留量和MRL规定,建议恩诺沙星混悬液在猪上的休药期为5 d。
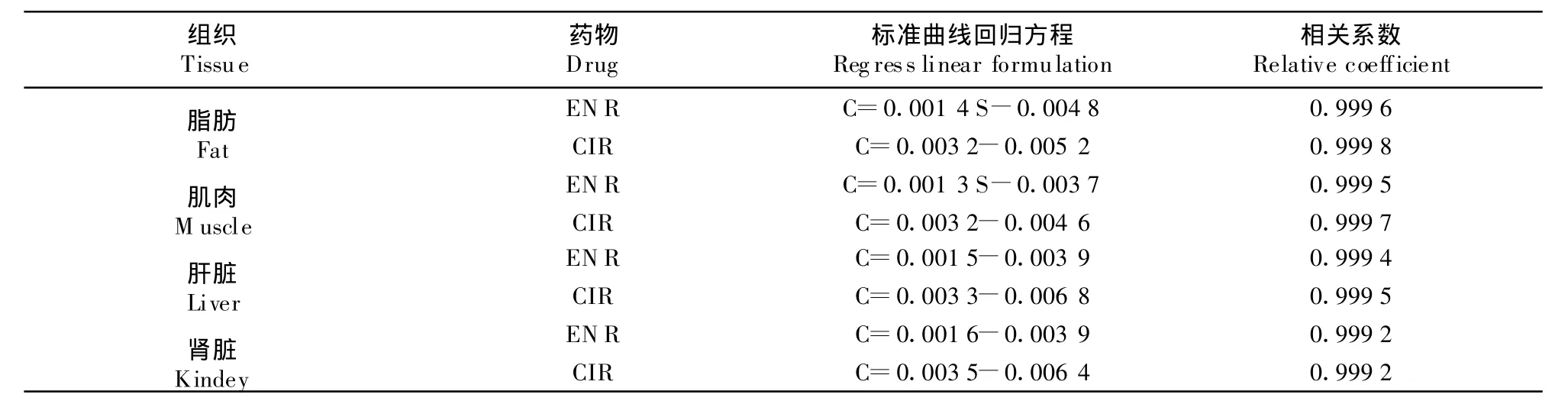
表1 猪各组织中恩诺沙星和环丙沙星的回归方程与相关系数Table 1 Regress linear formulation and relative coefficient of enrofloxacin and ciprofloxacin in pig tissues
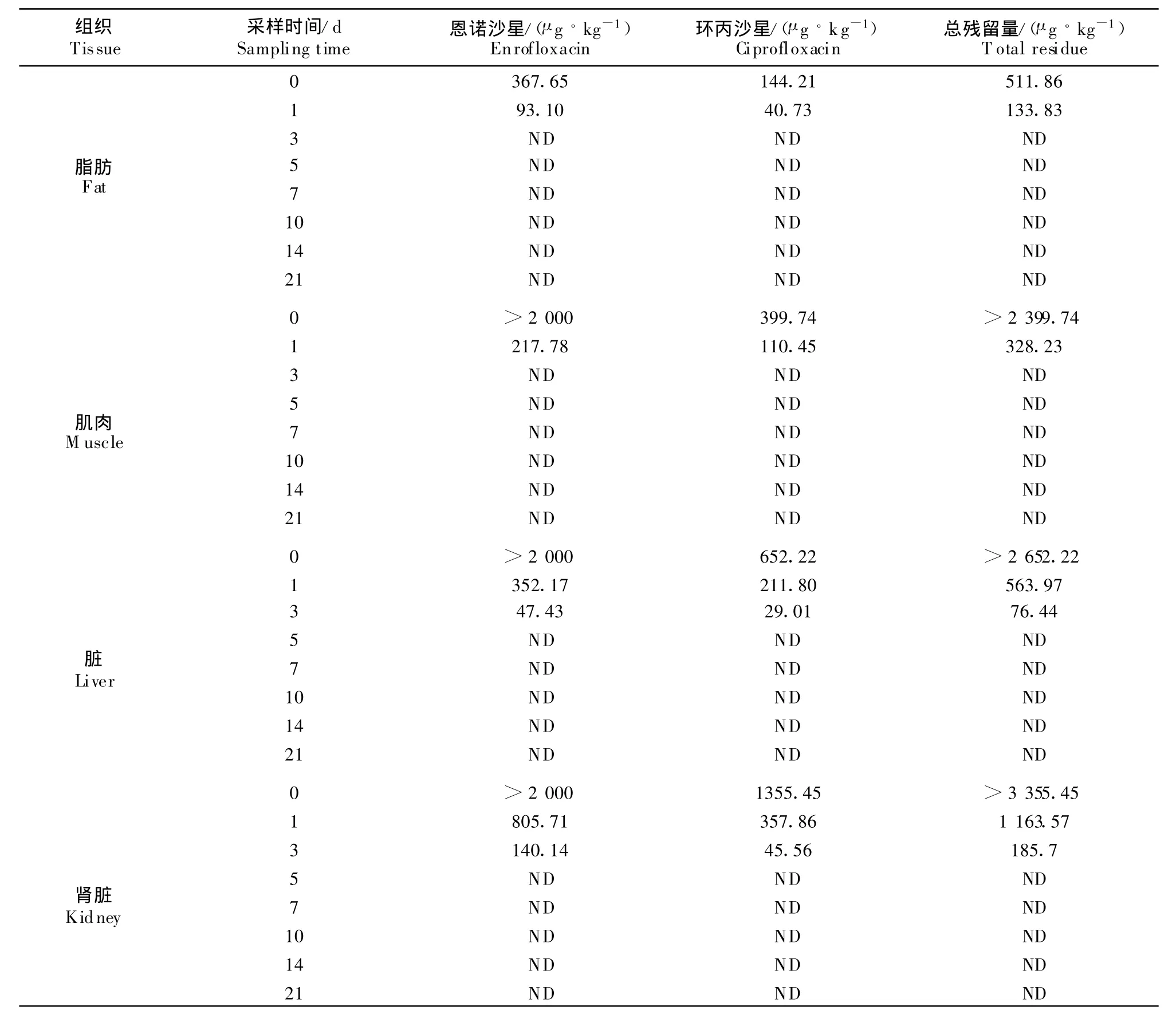
表2 各时间点猪组织中的恩诺沙星和环丙沙星残留量Table 2 Residues of enroflxacin and ciprofloxacin in pig tissues in different sampling time
3 讨论
恩诺沙星和环丙沙星在肌肉和脂肪中代谢消除较快、残留量下降迅速[4-6],这与报道一致。吴海坤等[5]用恩诺沙星混悬液以恩诺沙星计以75 mg/L水给60日龄鸡自由饮水,连续用药5 d后休药,休药第5天,肌肉、肝脏及皮肤+脂肪组织中药物总残留量(恩诺沙星+环丙沙星)分别为(11.12±10.53)、(79.29±28.86)、(50.08±22.09)μ g/kg,而肾脏组织未检出;休药第8天,肌肉、肾脏、肝脏组织中均未检出恩诺沙星及环丙沙星,皮肤+脂肪的总残留量为13.84 μ g/kg±10.82 μ g/kg;罗雅劲等[6]用恩诺沙星微囊按以恩诺沙星计以200 g/t饲料给猪混饲,连续给药7 d,停药后第5天,在肌肉、脂肪中的恩诺沙星和环丙沙星消除较快,第5天总残留量已下降至检测限以下;肝和肾脏中的残留药物消除较缓慢,第7天肾中药物总残留量为91.48 μ g/kg确定恩诺沙星微囊制剂休药期为7 d。本次试验与以上参考文献结果存在差异,可能与使用的动物、给药方式、药物的剂型有很大关系,本研究为以后恩诺沙星新剂型的开发提供了一定的基础。
[1] 刘小艳,方炳虎,杨利军,等.恩诺沙星口服混悬液的研制及其对仔猪黄白痢疗的效观察[J].动物医学进展,2009,30(9):120-122.
[2] 中华人民共和国农业部公告第236号.动物性食品中恩诺沙星和环丙沙星残留检测方法-高效液相色谱法[S].2003.
[3] 中华人民共和国农业部公告第235号.动物性食品中兽药最高残留限量[S].2002.
[4] 仲 锋,郭筱华,黄齐颐,等.恩诺沙星在猪组织中残留消除规律研究[J].中国兽药杂志,2005(2):6-9.
[5] 吴海坤,方炳虎,时书宁,等.恩诺沙星混悬液的研制及其在鸡组织中的残留研究[J].动物医学进展,2010,31(4):47-52.
[6] 罗雅劲,孙永学,李小娜,等.恩诺沙星微囊制剂在猪体内残留消除规律研究[J].中国畜牧兽医,2010,37(2):129-131.
