重金属对海岸带沉积物中菊酯生物降解的影响
2010-12-15田晶
田 晶
(秦皇岛经济技术开发区环境保护监测站,河北秦皇岛066004)
重金属对海岸带沉积物中菊酯生物降解的影响
田 晶
(秦皇岛经济技术开发区环境保护监测站,河北秦皇岛066004)
通过考察Cu2+、Cd2+对渤海海岸带沉积物中甲氰菊酯、氯氰菊酯和溴氰菊酯的缺氧生物降解的影响,发现:外加Cu2+和Cd2+均对渤海海岸带沉积物中甲氰菊酯、氯氰菊酯和溴氰菊酯的缺氧生物降解有抑制作用,且随着外加金属离子浓度的增大,抑制作用更为明显。与Cu2+相比较,Cd2+对渤海沉积物中拟除虫菊酯缺氧生物降解的抑制作用更大,这跟Cu、Cd在渤海海岸带沉积物中的存在形态和对生物的毒性不同有密切的关系。
拟除虫菊酯;缺氧生物降解;重金属;沉积物
拟除虫菊酯是在天然除虫菊酯化学结构研究基础上发展起来的继有机氯、有机磷农药以来的第三代农药。最近研究表明,此类农药有蓄积性[1],即使长期低剂量接触也会引起慢性疾病[2];特别是对鱼类等水生生物属高毒[3~4],将会导致水生态系统结构改变和功能破坏。拟除虫菊酯有很强的疏水性和较高的辛醇水分配系数,属于高亲脂性农药,进入水环境中易被颗粒物或油滴吸附,从而向沉积层迁移,最终沉降在沉积物中。
沉积物是重金属污染物的载体和“蓄积库”,重金属是一种重要的持久性污染物,不容易被微生物降解,具有累积效应。通过各种途径进入水体的重金属,绝大部分迅速地由水相转入固相,即迅速地结合到悬浮物和沉积物中。结合到悬浮物中的重金属在被水流搬运过程中,当其负荷超过搬运能力时,最终也转入沉积物中[5],对沉积物中有机物的生物降解产生一定的影响。重金属对有机物降解的影响不仅仅可能是抑制作用,在一定环境条件下也可能是促进作用,还可能是几乎无影响[6]。
本文选取生态风险较高的Cu和Cd两种典型重金属为对象,通过研究外加Cu2+、Cd2+时沉积物中拟除虫菊酯的缺氧生物降解特性,分析渤海海岸带沉积物中重金属对生物降解拟除虫菊酯的影响作用,以期通过生物修复技术为重金属污染的沉积物进行“人工修复”和“强化自然净化”提供重要科学依据。
1 材料与方法
1.1 实验仪器与化学试剂
HEQ-C恒温摇床、TDL-50B低速离心机、KQ-100超声波发生仪、Agilent7890GC(ECD检测器、HP-5毛细管柱)。
甲氰菊酯、溴氰菊酯、氯氰菊酯(纯度99.5%、94.7%、99.5%,国家标准物质网提供);石油醚(分析纯,沸程30~60℃);丙酮(分析纯);硫酸铜(CuSO4分析纯);硫酸镉(CdSO4,分析纯)。
1.2 样品采集
海水及沉积物均采自渤海流域秦皇岛市河北大街户段,经测定其p H值为8.37。沉积物样品采自距海岸带沉积物表层10~20cm处,采集后密封放入冰箱冷藏,以备实验使用。沉积物的化学组成见表1。

表1 沉积物理化性质
1.3 实验方法
在一系列100mL的具塞磨口三角瓶中加入11.6g新鲜的海岸带沉积物(相当于干重10g)和10mL海水,然后加入甲氰菊酯、氯氰菊酯和溴氰菊酯的混合标准样品溶液(针尖插入沉积物中,浓度如下:甲氰菊酯290μg/kg沉积物,氯氰菊酯1600μg/kg沉积物,溴氰菊酯1775μg/kg沉积物)。分别在不同的三角瓶中加入1mL不同浓度的硫酸铜溶液和硫酸镉溶液(折合硫酸铜浓度为200μg/g沉积物和1000μg/g沉积物,硫酸镉浓度为5μg/g沉积物和23μg/g沉积物)。置于恒温摇床上振荡2h(200r/min),达到吸附平衡后,连续吹入氮气5min,加塞密封(聚四氟乙烯生料带),置于恒温培养箱中培养((25±1)℃),然后定期取样分析。
1.4 分析方法
在待测样品中加入20mL有机萃取剂萃取(石油醚:丙酮=1∶1),在恒温摇床上振荡2h(200r/min),然后用超声波发生仪超声萃取30min,再离心分离20min(2000r/min),将上清液用去离子水萃取2次,有机相经无水硫酸钠脱水后浓缩定容,用Agilent7890A型气相色谱仪进行定量分析。
Agilent7890A型气相色谱仪操作条件:采用不分流进样,进样量为1μL;恒压方式,柱前压为50kPa;载气为高纯氮气,流速40mL/min;进样口的温度为270℃,检测器的温度为320℃;柱一级升温程序:初始温度210℃,保持1min;以10℃/min升至285℃,保持10min。
2 结果与讨论
2.1 外加铜离子对沉积物中菊酯缺氧生物降解的影响
本文研究了未加重金属离子、外加低浓度CuSO4(200μg/g沉积物)和高浓度CuSO4(1000μg/g沉积物)时,在温度为25℃甲氰菊酯、氯氰菊酯和溴氰菊酯在渤海海岸带沉积物中的缺氧生物降解特性。
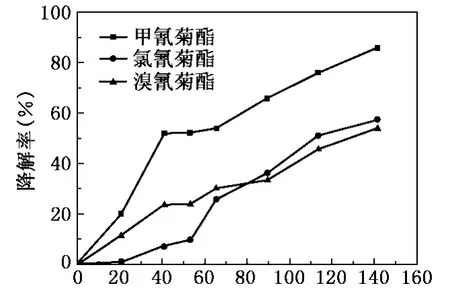
图1 无外加金属离子时菊酯缺氧生物降解曲线
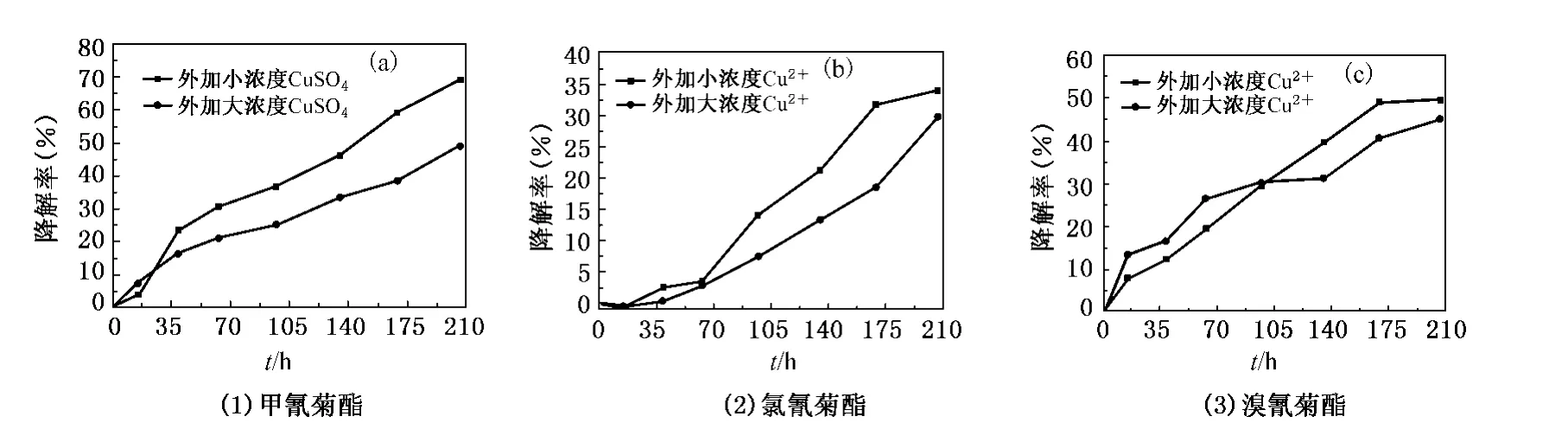
图2 外加Cu2+时菊酯缺氧生物降解曲线
无外加CuSO4时甲氰菊酯、氯氰菊酯和溴氰菊酯在渤海海岸带沉积物中的缺氧生物降解曲线如图1所示。由图中可以看出,在无外加CuSO4时,三种菊酯在沉积物中均有一定程度的生物降解。外加低浓度CuSO4(200μg/g沉积物)和高浓度CuSO4(1000μg/g沉积物)时,甲氰菊酯、氯氰菊酯和溴氰菊酯在渤海海岸带沉积物中的缺氧生物降解曲线如图2所示,未加和外加CuSO4时菊酯的缺氧生物降解动力学方程见表2。
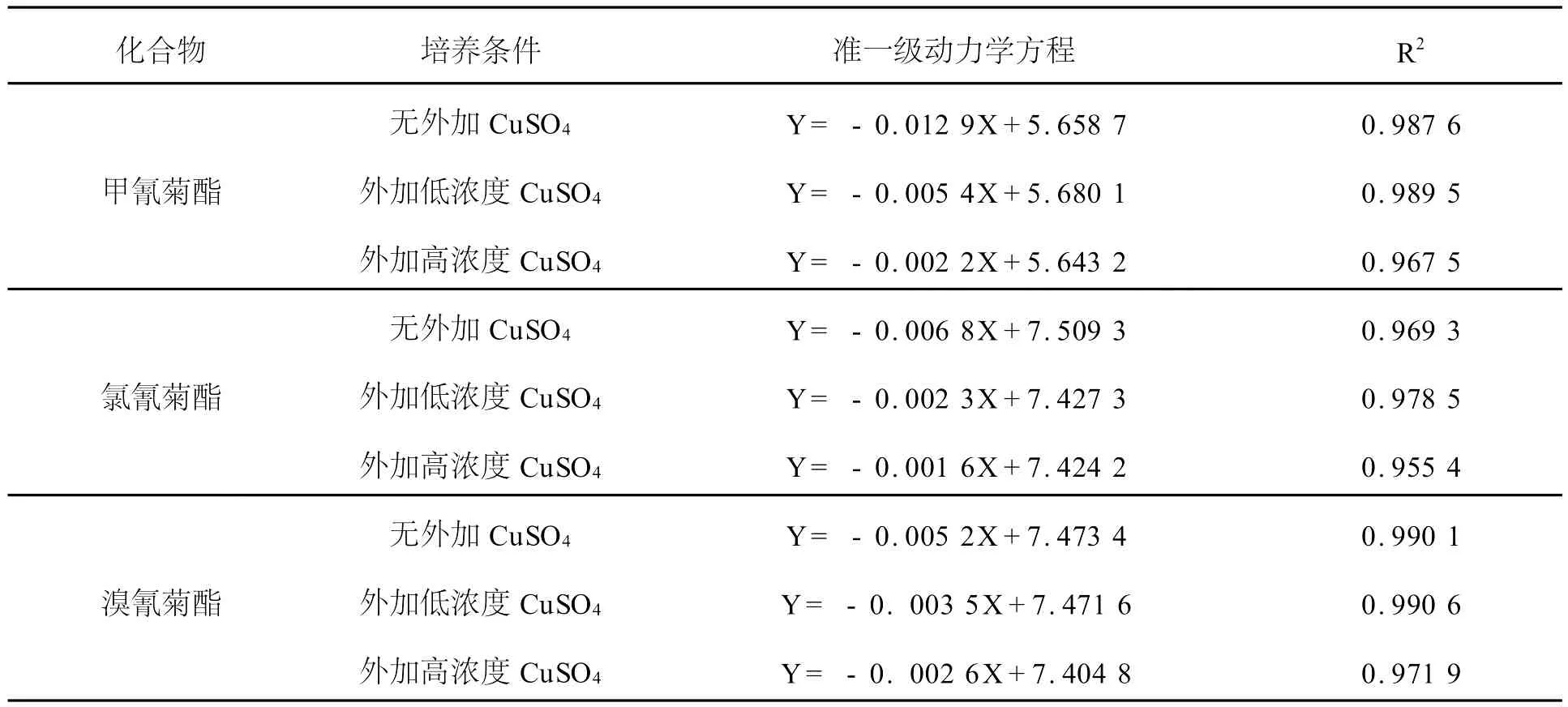
表2 未加和外加CuSO4时菊酯的缺氧生物降解动力学方程
由表2可以看出,无外加CuSO4和外加Cu-SO4时,甲氰菊酯、氯氰菊酯和溴氰菊酯的缺氧生物降解符合准一级动力学,经过F检验,9个准一级动力学方程的相关性在α=0.01水平上十分显著。外加低浓度CuSO4时,甲氰菊酯、氯氰菊酯和溴氰菊酯的缺氧降解速率常数分别为:外加高浓度CuSO4时,其缺氧降解速率常数分别为:,均远远小于无外加CuSO4时的缺氧降解速率常数:,由此可知外加CuSO4对甲氰菊酯、氯氰菊酯和溴氰菊酯在海岸带沉积物中的缺氧生物降解有抑制作用。当外加高浓度CuSO4时菊酯缺氧生物降解受到的抑制作用更为明显,即随着重金属浓度的增加,抑制效果也愈突出,这可能是重金属离子与沉积物中微生物酶分子活性部位相结合,形成较为稳定的络合物,产生与底物的竞争性抑制,酶活性降低,使得代谢缓慢;亦或是通过抑制一些具有降解菊酯能力的微生物的生长和繁殖,从而抑制了沉积物中菊酯的生物降解作用。
2.2 外加镉离子对沉积物中菊酯缺氧生物降解的影响
本文研究了外加低浓度CdSO4(5μg/g沉积物)和高浓度CdSO4(23μg/g沉积物)时,25℃下甲氰菊酯、氯氰菊酯和溴氰菊酯在渤海海岸带沉积物中的缺氧生物降解特性,其降解曲线见图3。未加和外加CdSO4时菊酯的缺氧生物降解动力学方程见表3。
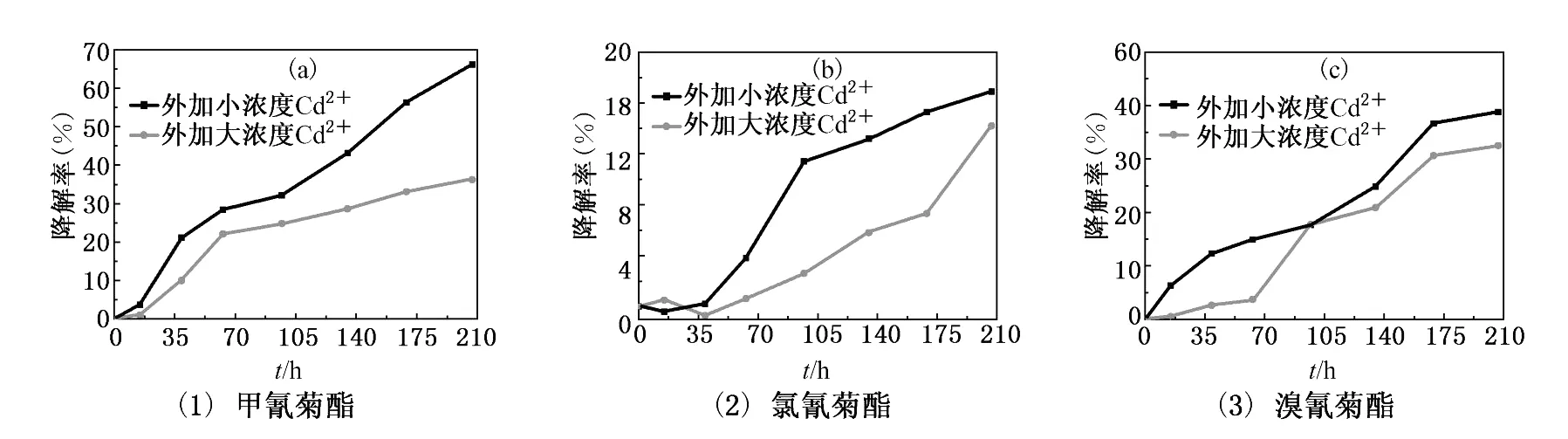
图3 外加Cd2+时菊酯缺氧生物降解曲线
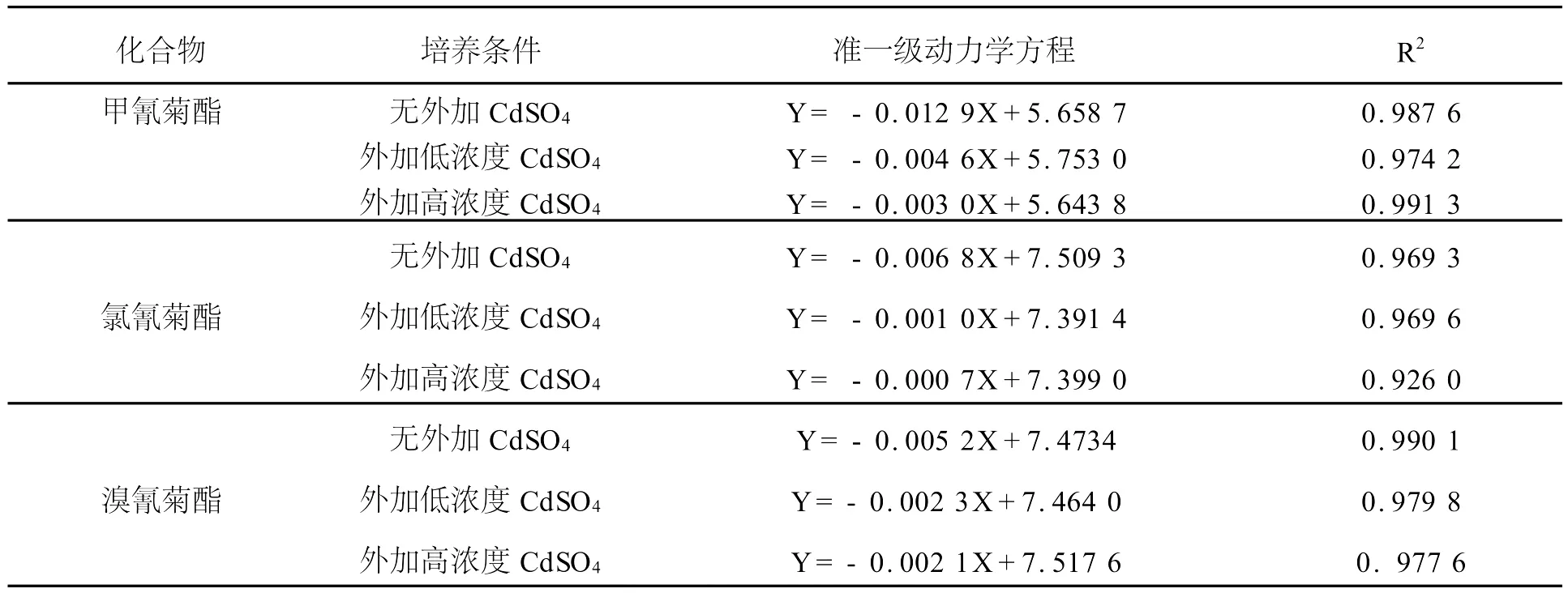
表3 未加和外加CdSO4时菊酯的缺氧生物降解动力学方程
由表3可以看出,无外加CdSO4和外加Cd-SO4时,甲氰菊酯、氯氰菊酯和溴氰菊酯的缺氧生物降解符合准一级动力学,经过F检验,9个准一级动力学方程的相关性在α=0.01水平上十分显著。外加低浓度CdSO4时,甲氰菊酯、氯氰菊酯和溴氰菊酯的缺氧降解速率常数分别为:外加高浓度CdSO4时,其缺氧降解速率常数分别为,均远远小于无外加CdSO4时的缺氧降解速率常数:。从而可知外加CdSO4对甲氰菊酯、氯氰菊酯和溴氰菊酯在渤海海岸带沉积物中的缺氧生物降解有抑制作用,且当外加高浓度CdSO4时对三种菊酯缺氧生物降解的抑制作用更为显著,即随着重金属浓度的增加,抑制效果也愈突出。
2.3 外加Cu2+与Cd2+时沉积物中菊酯缺氧生物降解动力学比较
由表2、表3和图2、图3综合可以看出,外加低浓度和高浓度Cu2+与Cd2+时对沉积物中甲氰菊酯、氯氰菊酯和溴氰菊酯缺氧生物均有抑制作用,且高浓度的抑制作用更为明显。两种外加重金属离子相比较,Cd2+对渤海海岸带沉积物中甲氰菊酯、氯氰菊酯和溴氰菊酯的的抑制作用更为明显。
重金属在沉积物中以不同的化学形态存在,不同的形态会表现出不同的环境地球化学行为和毒性特征。金属离子一般以离子交换态、碳酸盐结合态、络合态等形式存在,重金属的存在形式是不稳定的,易受p H和氧化还原电位等环境因素的影响。与Cu2+相比,Cd2+对沉积物中三种菊酯缺氧生物降解的抑制作用更为明显,这可能是因为渤海海岸带沉积物中Cd多以离子可交换态存在,对降解两种菊酯的微生物毒性较大,从而使得菊酯在沉积物中缺氧生物降解速率减慢,因此其对三种菊酯的缺氧生物降解的抑制作用较大。而Cu2+的抑制作用相对较小,这可能与Cu具有相对较强的络合能力有关,更容易与沉积物中的腐殖质等有机物形成络合物或螯合物,从而被沉积物附着,因而其对沉积物中生物的毒性作用较小。
3 结论
(1)外加CuSO4与CdSO4均对渤海海岸带沉积物中甲氰菊酯、氯氰菊酯和溴氰菊酯的缺氧生物降解有抑制作用,且随着添加浓度增加,抑制作用更为明显。
(2)与外加Cu2+相比,Cd2+对沉积物中甲氰菊酯、氯氰菊酯和溴氰菊酯缺氧生物降解的的抑制作用更为明显,这与两种重金属在沉积物环境中的存在形态和对生物的毒性有很大的关系。
[1]H.K.Makkawy,M.D.Madbouly.Persistence and Accumulation of Organic Insecticides in Nile Water and Fish[J].Resources Conservation and Recycling,1999,27(1-2):102-115.
[2]J.H.Kolaczinski,C.F.Curtis.Chronic Illness as a Result of Low-level Exposure to Synthetic pyrethroid Insecticides:a Review of the Debate[J].Food and Chemical Toxicology,2004,42(5):697-706.
[3]Wang Ligang,Jiang Xin,Yan Dongyun et al.Comparison of two procedures for extraction and clean-up of organophosphorus and pyrethroid pesticides in sediment[J].Pedosphere,2004,14(2):229-234.
[4]张征,李今,梁威,等.拟除虫菊酯杀虫剂对水生态系统的毒性作用[J].长江流域资源与环境,2006,15(1):126-128.
[5]蒋炳言,汪琳琳.中国水系沉积物重金属污染研究现状[J].科技信息.2009,(9):83-84.
[6]Muftah H,El-Naas,Shaheen A,Al-Muhtaseb,Souzan Makhlouf.Biodegadation of phenol by Pseudomonas putida immobilized in poyvinyl alcohol(PVA)gel[J].Journal of Hazardous Materials,2009,164(2/3):720-725.
Effects of Heavy Metal on Biodegradation of Pyrethroids in Coastal Sediment
Tian Jing
(Environmental Monitoring Station of Qinhuangdao Economic&Technological Development Zone,Qinhuangdao Hebei066004)
In this paper,the effects of Cu2+,Cd2+on the anoxic biodegradation of fenpropathrin,cypermethrin and deltamethrin in coastal sediment of the Bohai Sea were studied.The results showed that the additional Cu2+and Cd2+restrained the anoxic biodegradation of fenpropathrin,cypermethrin and deltamethrin in the coastal sediment.Furthermore,the inhibition effects became greater with the increasing of concentration of additional metal iron.Compared with the Cu2+,the inhibition of additional Cd2+was more prominent on the anoxic biodegradation of pyrethroids in the coastal sediment,which were closely related to the existence form and biotoxicity of Cu and Cd in the coastal sediment of the Bohai Sea.
pyrethroids;anoxic biodegradation;heavy metal;sediment
X503.2
A
1008-813(2010)05-0068-05
10.3969/j.issn.1008-813X.2010.05.022
2010-09-12
田晶(1978—),女,河北饶阳人,毕业于西北农林科技学院环境工程系,现任秦皇岛经济技术开发区环境保护监测站助理工程师,研究环境监测方法分析、数据处理、行政执法等课题。
