老年2型糖尿病小鼠记忆损害和大脑内proBDNF-p75NTR表达
2022-08-09熊静邢维昊李舒婷张晓琳刘凤巫晓宇
熊静 邢维昊 李舒婷 张晓琳 刘凤 巫晓宇
(昆明医科大学第二附属医院神经内科,云南 昆明 650101)
痴呆已经成为老年人群致死和致残的主要疾病之一。中国现有痴呆患者约1 000万,到2050年,痴呆患者预计达到4 000万〔1,2〕。2型糖尿病(T2DM)是阿尔茨海默病(AD)和血管性痴呆的重要危险因素。T2DM患者AD发病率是非T2DM者的1.5倍,对老年人影响更为明显〔3〕。T2DM 发病增加,加上年龄增长和肥胖的代谢后果,显著增加了认知能力下降和痴呆的发病〔4〕。T2DM、肥胖和AD 存在着胰岛素抵抗、脑小血管损伤、炎症和氧化应激等共同的病理生理机制〔5〕,但T2DM与认知损害之间的分子机制仍不清楚。近年来,连接大脑、内分泌胰腺、脂肪组织的神经信号通路功能障碍越来越受到重视〔6〕。脑源性神经营养因子(BDNF)在哺乳动物脑内含量丰富〔7〕,也存在于外周神经、骨骼肌、平滑肌、肝脏、淋巴细胞、内分泌系统、胰腺、内皮细胞和脂肪组织中〔8〕。BDNF在学习和记忆中有重要的作用,与AD等神经变性疾病密切相关〔9〕。BDNF在内质网中先合成BDNF前体蛋白(proBDNF),proBDNF在细胞内和细胞外经过一系列蛋白酶剪切形成成熟型BDNF(mature BDNF)〔7,10〕。研究表明,proBDNF和mature BDNF分别通过p75神经营养因子受体(p75NTR)和酪氨酸激酶受体(Trk)B结合,在学习和记忆中起相反的生物学作用〔7,9,10〕。
研究发现肥胖、T2DM、神经变性疾病患者血清中BDNF基因表达水平降低〔11,12〕。T2DM损害学习和记忆的部分原因是通过下调BDNF表达,改变了突触可塑性〔13〕。目前,还没有研究报道T2DM对脑内proBDNF水平或proBDNF与mature BDNF比值及其相应的受体p75NTR和TrkB的影响。本研究采用高脂饮食喂养8周龄C57BL/6小鼠,建立T2DM模型,并持续到小鼠老年期,测定T2DM小鼠短期记忆和空间参考记忆损伤和脑内proBDNF-p75NTR和mature BDNF-TrkB的表达。
1 材料与方法
1.1实验动物 8周龄C57BL/6雌性小鼠,分为T2DM组(n=8)和对照组(n=8)。T2DM组给予高脂饮食,对照组给予标准饮食,喂养30 w至小鼠38周龄。标准无菌条件,室温22℃,湿度55%,12 h∶12 h光照-黑暗周期饲养。
1.2主要试剂和仪器 主要试剂:proBDNF和mature BDNF酶联免疫吸附试验(ELISA)试剂盒(澳大利亚南澳大学周新富教授赠送),p75NTR ELISA试剂盒(美国R&D公司),TrkB ELISA试剂盒(Sino Biological Inc.),TRIzoL试剂盒(美国 Invitrogen公司),逆转录试剂盒和RT-PCR试剂盒(美国 Qiagen公司),引物(Invitrogen公司合成)。主要仪器:ABI 7300实时PCR系统(Applied Biosystems)。
1.3小鼠体重、空腹血糖、葡萄糖耐量测定(GTT)和胰岛素耐量测定(ITT) 小鼠入组时测定基础体重和空腹血糖,之后每周测量体重,每4周测量空腹血糖。空腹血糖在禁食过夜16 h后,尾静脉采血测定。小鼠38 w时,进行GTT和ITT。GTT在小鼠禁食16 h后进行,测量空腹血糖后给予腹腔内注射葡萄糖(1 g/kg),分别于注射后15、30、60、90、120 min重复测定。ITT在小鼠禁食5 h后进行,测定基线血糖后,给予胰岛素腹腔注射(0.75 U/kg),分别于注射后15、30、60、90和120 min重复测定。
1.4Y迷宫空间识别实验和自发交替实验 采用Y迷宫空间识别实验和自发交替实验测定小鼠的短期记忆。Y迷宫由3个完全相同的臂组成,形成Y形。中央处各有一个可移动的隔板。Y迷宫空间识别实验步骤简述如下:3个臂随机设为新异臂、起始臂和其他臂。实验的第1个阶段(训练期),用隔板挡住新异臂,开放起始臂和其他臂,将小鼠自起始臂放入,在两个开放的臂中自由活动探索3 min。2 h后进行第2阶段(回忆期),打开新异臂,将小鼠自起始臂放入,在3个臂中自由活动3 min。Anymaze软件记录小鼠在各臂中的活动时间和进入次数,计算新异臂中活动时间的百分比,进入新异臂次数的百分比。3 d后进行Y迷宫自发交替实验,测试前将Y迷宫旋转45°,将小鼠自任意一臂中放入,自由活动5 min,Anymaze软件记录小鼠进入各个臂的顺序和次数,计算自发交替百分比。
1.5Morris水迷宫实验 用Morris水迷宫测试来测量空间参考记忆。水迷宫装置由一个圆形聚丙烯池(直径120 cm×高45 cm),池周有4种不同图案提示,以帮助小鼠定位。水温保持在(23±1)℃,加入无毒的白色涂料使水不透明。第1天为适应期,将小鼠平台所在象限(目标象限)面向池壁放入水中,自行游泳2 min。第2天进行可见平台实验,使平台露出水面0.5 cm,观察小鼠分别从四个象限的某一固定点入水至爬上平台的时间,小鼠若超过60 s找不到平台,可引导其找到平台。第3~6天进行定位航行实验:将平台隐入水下1 cm,再将小鼠面向并靠近池壁分别从四个不同象限入水,Anymaze软件记录小鼠从入水到爬上平台的游泳时间(逃避潜伏期)和在目标象限内的游泳时间。第7天进行空间探索实验,移除平台,给予小鼠60 s探索时间,Anymaze软件记录小鼠在原平台所在位置区域的时间和穿越原平台位置的次数。
1.6RT-PCR检测小鼠脑组织BDNF、TrkB和p75NTR mRNA表达 采用CO2窒息法,人道处死小鼠,取出脑组织,液氮中速冻后贮存于-80℃冰箱备用。用TRIzoL试剂提取小鼠大脑总RNA,逆转录合成cDNA,RT-PCR测定BDNF、p75NTR、TrkB基因在小鼠脑组织中的转录水平。RT-PCR的反应程序为:95℃ 10 min,95℃ 15 s,循环40次,60℃ 1 min,引物序列:BDNF正向:5′-TACTTTGGTTGCATGAAGGCTGCC-3′,反向:5′-ACTTGACTACTGAGCA-TCACCCTG-3′;p75NTR正向:5′-GTGGGACAGA-GTCTGGGTGT-3′,反向:5′-AAGGAGGGGAGGTGATAGGA-3′;TrkB正向:5′-AGGGCAACCCGCCCACGGAA-3′,反向:5′-GGATCGGTCTGGGGAAAAG-3′;β-actin正向:5′-CGGGAAATCGTGCGTGAC-3′,反向:5′-TGGAAGGTGGACAGCGAGG-3′。RT-PCR检测结果通过β-actin结果进行矫正,应用2-ΔΔCt法对数据进行分析〔14〕。
1.7ELISA测定小鼠脑组织proBDNF、成熟(mature)BDNF、TrkB和p75NTR蛋白 用放射免疫沉淀试验(RIPA)蛋白裂解液提取脑组织蛋白。Mature BDNF ELISA测定〔14,15〕简述如下:G蛋白纯化的小鼠抗-mature BDNF单克隆抗体(工作浓度1 μg/ml)包被酶标板,37℃ 1 h。磷酸盐缓冲液(PBS)洗板,3%牛血清白蛋白(BSA)室温封闭1 h。加样:标准品为重组mature BDNF蛋白,倍比稀释加入,范围在0~2 000 pg/ml,加入脑组织样本(浓度250 μg/ml),37℃,1 h,PBST洗板,加入检测抗体—生物素标记的羊抗mature BDNF抗体(工作浓度0.15 μg/ml),37℃,1 h。PBST洗板,加入链霉亲和素-辣根过氧化物酶(HRP),37℃,1 h,PBST洗板,加入新鲜配制的TMB底物,室温避光,10~15 min内显色。加入0.1 mol/L Hcl终止反应,用Model 2550 EIA reader于450 nm读取OD值。 ProBDNF测定步骤同mature BDNF〔15〕。包被抗体为G蛋白纯化的羊抗-proBDNF单克隆抗体(工作浓度为5 μg/ml),标准品为重组proBDNF蛋白,范围在0~2 000 pg/ml,脑组织样品浓度为250 μg/ml,检测抗体为生物素标记的羊抗proBDNF抗体(工作浓度0.15 μg/ml)。P75NTR和TrkB测定按照试剂盒说明书进行。
1.8统计学分析 采用SPSS17.0软件进行独立样本t检验。
2 结 果
2.1高脂饮食诱导C57BL/6小鼠建立T2DM模型 T2DM组平均体重〔(54.36±2.68)g〕明显高于对照组〔(23.66±1.62)g,t=11.40,P<0.01〕。T2DM组平均空腹血糖〔(8.22±0.41)mmol/L〕明显高于对照组〔(4.45±0.22)mol/L,t=36.69,P<0.01〕。GTT实验显示,与对照组相比,T2DM组葡萄糖耐量受损,注射葡萄糖后血糖升高的峰值延迟,60 min达到峰值,之后缓慢下降,至注射后120 min时,血糖仍明显高于对照组(P<0.01)。ITT中,与对照组相比,T2DM小鼠对胰岛素的敏感性降低。T2DM组给予胰岛素腹腔注射后,血糖水平降低的幅度更小,并且更快地开始恢复,注射胰岛素后120 min,T2DM组血糖明显高于对照组(P<0.05)。见表1、表2。
2.2Y迷宫实验中T2DM组小鼠短期工作记忆下降 T2DM组在新异臂内活动时间百分比、进入新异臂的次数占总次数百分比、自发交替率较对照组均明显减少(P<0.05)。见表3。
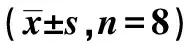
表1 两组GTT结果
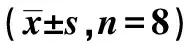
表2 两组ITT结果
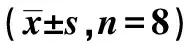
表3 两组Y迷宫结果
2.3Morris水迷宫测试中T2DM小鼠空间参考记忆下降 定位航行实验显示,随着训练时间的延长,对照组逃跑潜伏期逐渐缩短,在目标象限的时间逐渐增加,T2DM组小鼠的比对照组小鼠长,在目标象限中的时间更短(P<0.05)。表明T2DM小鼠学习速度下降。见表4。空间探索试验显示,移除平台后,T2DM小鼠在之前平台所在区域的时间〔(1.73±0.04)s〕明显少于对照组〔(1.93±0.04)s,P<0.05〕;T2DM小鼠进入之前平台所在区域的次数〔(3.00±0.21)次〕明显少于对照组〔(4.12±0.22)次,P=0.003〕,说明T2DM小鼠的空间参考记忆受损。
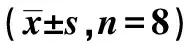
表4 两组水迷宫定位航行实验结果
2.4T2DM小鼠脑内BDNF、TrkB和p75NTR mRNA表达变化 与对照组相比,T2DM组BDNF mRNA、TrkB mRNA均显著下调(P<0.01),而p75NTR mRNA显著上调(P<0.01)。见表5。
2.5T2DM组大脑中proBDNF、mature BDNF、TrkB和p75NTR蛋白的变化 T2DM组proBDNF、p75NTR水平明显高于对照组(P<0.01),T2DM组mature BDNF、TrkB水平明显低于对照组(P<0.01)。见表6。

表5 两组脑BDNF、TrkB和

表6 两组脑内proBDNF、mature BDNF、TrkB和p75NTR蛋白浓度比较
3 讨 论
高脂饮食喂养C57BL/6小鼠建立的T2DM模型,表现为肥胖、血糖升高和胰岛素抵抗。这个模型被认为是一个非常有效的胰岛素抵抗和T2DM模型〔16〕。既往研究认为,T2DM对认知的损伤在老年期更明显〔3〕,因此本研究持续到小鼠老年期(38周龄)。本研究结果说明T2DM促进了老年小鼠的短期工作记忆和空间参考长期记忆的下降。有研究表明,肥胖、T2DM、神经退行性疾病患者血清中BDNF水平较低〔11,17〕。T2DM患者血清BDNF 浓度与延迟记忆损伤相关〔12〕,而伴有T2DM的痴呆患者BDNF 平均水平最低〔18〕。BDNF水平降低可能在T2DM患者的认知障碍病理生理学改变中发挥重要作用〔19〕。因此,T2DM引起小鼠脑中BDNF基因转录下调,与小鼠的短期和空间参考记忆损伤有关。
BDNF基因转录后,先合成proBDNF,proBDNF在细胞内由furin蛋白酶或前蛋白转化酶剪切形成mature BDNF。分泌到细胞外proBDNF由组织纤维蛋白溶解酶(tPA)或基质金属蛋白酶(MMPs)转化形成mature BDNF〔7,10〕。两种BDNF有相反的生物学作用,proBDNF/mature BDNF平衡对神经元可塑性和神经元连续更新有重要作用〔10,20〕。
和mature BDNF促进神经元的存活、增加突触可塑性、促进记忆〔9〕的作用相反,proBDNF是一种强大的神经退行性疾病促进因子〔21〕。AD患者内嗅皮层及额叶皮质中的proBDNF水平降低,皮层区总BDNF水平与海马区Aβ淀粉样蛋白呈负相关,血清proBDNF与pTau染色呈正相关,TrkB水平下降,与同一区域的Aβ和pTau水平呈负相关〔22〕。proBDNF诱导海马神经元凋亡,促进海马神经元的长时程抑制〔21〕。BDNF肽链上furin位点突变,引起小鼠大脑海马区proBDNF水平升高,导致树突分化减少和棘突密度降低,海马体积变小,损害初级突触传递功能,增强长时程抑制功能。向高龄老鼠海马内注射proBDNF后,海马区新生神经细胞减少,相反,给予proBDNF抗体可抵消这种不良影响〔23,24〕。
proBDNF是一个强大的神经退行性疾病促进因子,通过激活p75NTR 和sortilin受体复合物,显著抑制神经干细胞增殖、减少神经元分化、少突胶质细胞和星形胶质细胞的数量,导致神经突起塌陷、神经元凋亡和抑制神经发生〔21〕,损害认知功能〔7,10〕。研究表明,T2DM患者出现高血糖水平时,血管内皮细胞中p75NTR水平增加〔25〕。研究发现,BDNF参与了体重和糖代谢的调节。BDNF通过TrkB,增加能量消耗,控制体重增加,改善血糖平衡,提高胰岛素敏感性〔6〕。动物研究发现,p75NTR参与了调节葡萄糖代谢和胰岛素抵抗。p75NTR基因敲除小鼠,胰岛素敏感性增加,能量消耗增加〔26〕。综上,T2DM可引起老年小鼠脑内mBDNF、proBDNF及其受体的异常调节,与T2DM相关的记忆障碍有关。有必要在今后的研究中,探索调节proBDNF和mature BDNF的生物合成过程,如改变饮食和运动,增加mature BDNF的正性作用或降低proBDNF负性作用,或阻断p75NTR信号通路,能否同时改善T2DM合并认知障碍。
