紫外分光光度法测定阿司匹林有效期的教学实验设计
2022-04-06倪亚楠李宇杰张胜红
倪亚楠, 李宇杰, 冯 蕊, 沈 彤, 张胜红
(北京石油化工学院化学工程学院,化学化工国家级实验教学示范中心,北京 102617)
0 引 言
随着我国在2016年正式加入国际工程联盟的“华盛顿协议”,国内工科高校的本科教学更加重视创新能力和工程实践能力的培养,而实验教学是培养学生创新意识和实践能力的重要环节[1]。基于工程教育专业认证的理念和标准,大学实验课程不仅要加深学生对工程基础和专业知识的理解,更重要的是要培养学生基于科学原理和方法解决实际工程问题的研究能力,如设计实验、分析和解释数据、并通过信息综合得到合理有效的结论。
具体到制药工程专业的物理化学实验课程,传统的验证性动力学实验,如蔗糖水解和乙酸乙酯皂化反应动力学参数的测定,在工程教育专业认证背景下已难以有效支撑相应的毕业要求指标点。为此,设计了具有制药专业特色的动力学综合化学实验——阿司匹林水解反应动力学参数及其有效期的测定。阿司匹林,又名乙酰水杨酸,是一种常见的非甾体药物,广泛用于解热、阵痛、抗炎和抗血栓等方面[2]。阿司匹林的合成、制剂、溶出、鉴别和质量分析是药物化学及相关专业的经典实验内容[3-7]。作为阿司匹林实验教学中的重要一环,其水解反应不仅有助于学生深度理解酯水解反应机理和动力学,而且是阿司匹林有效期预测和药物剂型设计的理论基础。
1 实验设计思路
乙酰水杨酸水解反应通常用作阿司匹林定量分析的一个手段[8],尚未发展为一个独立的化学反应动力学教学实验。究其原因,阿司匹林水解反应动力学参数的测定主要基于络合显色法[9-11]:即采用可溶性Fe3+盐与其水解产物形成稳定的紫色络合物,然后监测该络合物在~525 nm波长处的吸光度来间接测定阿司匹林的含量。络合显色法需要pH值为2.5~3.5的弱酸性环境稳定水杨酸铁络合物,因此难以模拟阿司匹林溶液的近中性存储环境;此外,该方法操作过程繁琐且耗时较长,无法满足4~8 h的物理化学实验学时要求。张彩云等[12]采用双波长紫外分光光度法消除水杨酸对阿司匹林的干扰,在加速实验条件下测定了阿司匹林水解反应的动力学参数。遗憾的是,该方法忽略了产物水杨酸(pKa=2.98)对溶液pH值以及阿司匹林水解速率的影响,理论上存在瑕疵。
借鉴上述研究成果,本实验采用近中性的NaH2PO4-Na2HPO4缓冲溶液(pH=6.85,25℃)模拟阿司匹林溶液的存储环境,采用紫外分光光度法监测产物水杨酸的吸光度以及阿司匹林水解反应的进度。通过测定50~80℃范围内阿司匹林水解反应的速率常数k计算该反应的平均表观活化能Ea并推测室温下(25℃)阿司匹林溶液水解反应的速率常数和有效期。
2 实验实施
2.1 实验教学方法
本实验采用问题导向的探究性教学。首先启发学生思考:为什么常见的阿司匹林药品是片剂而不是针剂或者口服液?然后引出化学稳定性是影响药物剂型的重要因素,进而介绍药品有效期的概念并引导学生思考如何通过加速实验法测定阿司匹林水解反应的动力学参数和药物有效期。
2.2 实验安排
本实验项目定位为综合性或开放性物理化学实验,也可进一步融入药学相关的专业综合实验。实验时长为8学时,教学组织方面可以采用2人1组或4人1组,要求学生共同设计实验方案并分工协作。第1阶段(4学时),任课教师讲解实验原理、仪器操作和实验注意事项,重点引导学生检讨并修订实验内容和方案。学生配制相关溶液,确定紫外可见光谱仪的工作波长并测定70和80℃时阿司匹林水解反应的动力学参数。第2阶段(4学时):学生测定50和60℃时阿司匹林水解反应的速率常数。
2.3 实验原理
阿司匹林在水溶液中不稳定,易于水解生成水杨酸和醋酸。

其中,酸和碱(尤其是H+和OH-离子)都能够催化该水解反应,尽管碱催化阿司匹林水解反应的速率远高于酸催化或自水解反应速率[13]。因此,实际测得的速率是同步发生的各水解反应速率的总和[14],即
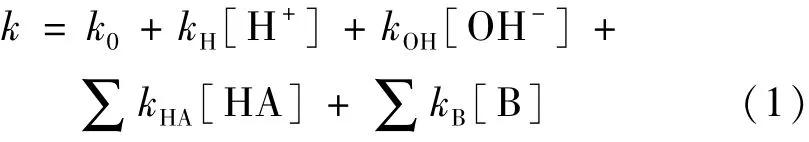
式中:k0,kH和kOH分别为阿司匹林自水解、H+和OH-离子催化阿司匹林水解反应的速率常数;而kHA和kB分别为其他广义酸(HA)和碱(B)催化该反应的速率常数。
尽管阿司匹林水解反应可能存在不同的路径,但在pH值恒定的实际反应中该过程通常只由一种机理主导,并且该反应在水介质中可以按准一级反应处理[14]。因此,阿司匹林水解反应速率与其浓度呈正比,即

式中:c为时间t时阿司匹林的浓度;k为速率常数。
将式(2)积分得:
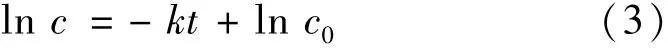
式中,c0为阿司匹林的初始浓度。
根据Lambert-Beer定律,在选取的工作波长(如水杨酸的最大吸收波长)处,反应未开始、达到平衡和任意t时刻的溶液吸光度(记作A0,A∞和At)可以分别采用下式表示:

式中:b为石英比色皿的内部宽度;ε和ε′分别为阿司匹林和水杨酸在选定波长下的摩尔吸光系数。
此外,鉴于阿司匹林水解反应的平衡常数远大于106,可以合理假设反应达到平衡时阿司匹林完全水解并采用浓度为c0的水杨酸溶液的吸光度数值替代A∞[14]。
将式(4)~(6)联立,得:

进一步将式(7)和(8)代入式(3)得:
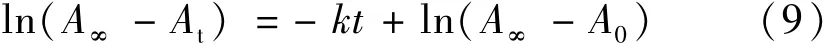
以ln(A∞-At)对t作图,由拟合直线的斜率即可求得反应在不同温度时的速率常数k。假设该反应的表观活化能Ea在50~80℃区间内为定值,依据

中的Arrhenius方程以lnk对1/T作图并由拟合直线的斜率即可得到水解反应的Ea值。
进一步假设该反应的Ea在20~80℃范围内为常数,将式(10)外推至298 K即可计算25℃时阿司匹林水解反应的k值。药品的有效期通常是指药物有效组分损失10%所需的时间(τ0.9)。相应地,阿司匹林水溶液的τ0.9值可以根据25℃时水解反应的k值由下式进行计算:

2.4 主要试剂及仪器
试剂:乙酰水杨酸(阿司匹林),水杨酸,醋酸,NaH2PO4·2H2O和Na2HPO4,均为分析纯,上海阿拉丁生化科技股份有限公司。
仪器:G-10双光束紫外可见分光光度计(让奇仪器科技有限公司);SYC-15c超级恒温水浴(南京桑力电子设备厂);电子分析天平,容量瓶,100 mL磨口锥形瓶。
2.5 实验步骤和注意事项
(1)溶液配制。首先配制NaH2PO4和Na2HPO4浓度均为25 mmol/L的缓冲溶液1 L并以此为溶剂配制浓度为0.1 mmol/L的阿司匹林溶液,以及等浓度的水杨酸和醋酸溶液。
(2)确定工作波长。待紫外可见分光光度计稳定后,以缓冲溶液为参比测定阿司匹林、水杨酸和醋酸溶液在210~600 nm波长范围内的紫外可见吸收光谱,选择阿司匹林和醋酸干扰较小的水杨酸最大吸收波长为工作波长。
(3)测定阿司匹林水解反应速率常数。将盛有适量新鲜配制的阿司匹林溶液的带塞锥形瓶分别置于50、60、70和80℃的恒温水浴槽中并开始计时。每隔10 min吸取少许反应液滴入石英比色皿中并置于大量室温水浴中冷却2 min,然后以缓冲溶液为参比测定该反应液的吸光度。其中,50、60、70和80℃恒温水浴反应的时长分别控制为180、180、120和90 min。
注意事项:阿司匹林溶液要现用现配,配制过程可以采用超声辅助溶解;水浴加热过程中锥形瓶磨和磨口之间可以夹持细滤纸条,在保证实验安全的情况下尽可能地减少溶剂的挥发。
细节对于小说的情节发展和人物塑造有着至关重要的作用,这一点在虚构文学作品中显而易见。而放到“非虚构”作品中,它却常常被人所忽略。诚然,任何“非虚构文学”都不可能没有一点虚构的成分,适当合理的虚构是必要的,也恰恰是将“非虚构文学”推向成功的必然因素之一。显然宁肯清楚的认识到了这一点,并成功的将其熟稔掌握,为小说文本增添了许多张力。
3 结果与讨论
3.1 工作波长的确定
乙酰水杨酸、水杨酸和醋酸的pKa分别为3.57、2.98和4.75,在近中性的NaH2PO4-Na2HPO4缓冲溶液中3者主要以离子的形式存在且对光的吸收集中在紫外区,如图1所示。其中,水杨酸及其共轭离子的最大吸收波长为296 nm,阿司匹林和醋酸的共轭酸碱对在此波长理论上均不存在吸收[14]。由于常温下阿司匹林水溶液的轻微水解,实际测得的A0和A∞分别为0.007 8和0.401 4。因此,实验中可以忽略阿司匹林和醋酸的影响,采用296 nm波长处的吸光度A监测水杨酸的浓度以及阿司匹林水解反应的进度。
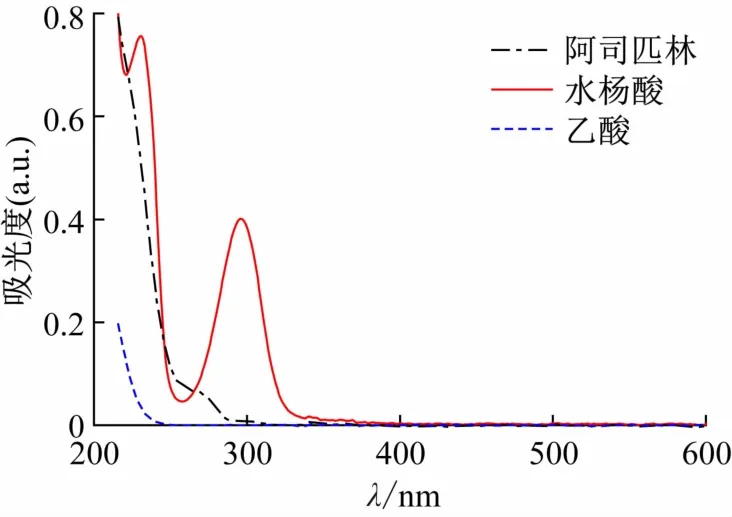
图1 阿司匹林及其水解产物的紫外-可见吸收光谱
3.2 阿司匹林水解反应的速率常数
图2所示给出了不同温度和反应时长时阿司匹林水解反应液在296 nm处的吸光度。随着反应时间的延长,吸光度的数值逐步增大,表明阿司匹林逐渐转化为水杨酸;此外,随反应温度从50℃提高到80℃,吸光度的递增明显加剧,表明升高温度能够加快阿司匹林水解反应进程。

图2 温度和时间对阿司匹林溶液吸光度的影响
为降低原始数据点散乱性引起的误差,利用Origin软件中的ExpGro1型指数递增函数拟合吸光度数据并采用拟合的At值以ln(A∞-At)对t作图,结果如图3所示。ln(A∞-At)与t高度线性相关,证实阿司匹林水解遵从一级反应动力学。由拟合直线斜率得到阿司匹林水解反应在50、60、70和80℃的速率常数分别为1.67×10-3、4.06×10-3、8.02×10-3和1.70×10-2min-1。

图3 不同温度下阿司匹林水解溶液的ln(A∞-A t)~t曲线
3.3 阿司匹林水解反应的表观活化能
基于不同温度下阿司匹林水解反应的k值,以lnk对1/T作图并进行线性拟合,结果如图4所示。拟合直线的线性回归决定系数R2为0.998,较好地吻合Arrhenius方程。由拟合直线斜率得到的Ea为72.6 kJ/mol,符合68.6~73.6 kJ/mol的文献值[15],同时也接近传统络合显色法测得的弱酸性介质中阿司匹林水解反应的活化能(69.8~73.0 kJ/mol)[9-11],表明此实验方法具有较高的准确性。

图4 温度对阿司匹林水解反应速率常数的影响
将图4中的拟合直线进一步外推可得25℃时阿司匹林水解反应的k为1.75×10-4/min,这一数值与Baker[16]的研究结果(1.54×10-4/min,22.5℃)吻合。相应地,阿司匹林在NaH2PO4和Na2HPO4缓冲溶液中的有效期τ0.9为602 min,即10 h。如此短的药物有效期表明阿司匹林不宜采用溶液型注射剂的形式保存。
3.4 阿司匹林水解反应机理
阿司匹林水解反应的机理与溶液的pH值密切相关。文献[13-14]中详细研究了不同pH值下的阿司匹林水解反应,发现在pH值为4.5~8.5时其水解反应速率几乎不变且反应机理以Brønsted碱(B碱)辅助的水分子亲核加成为主,即:
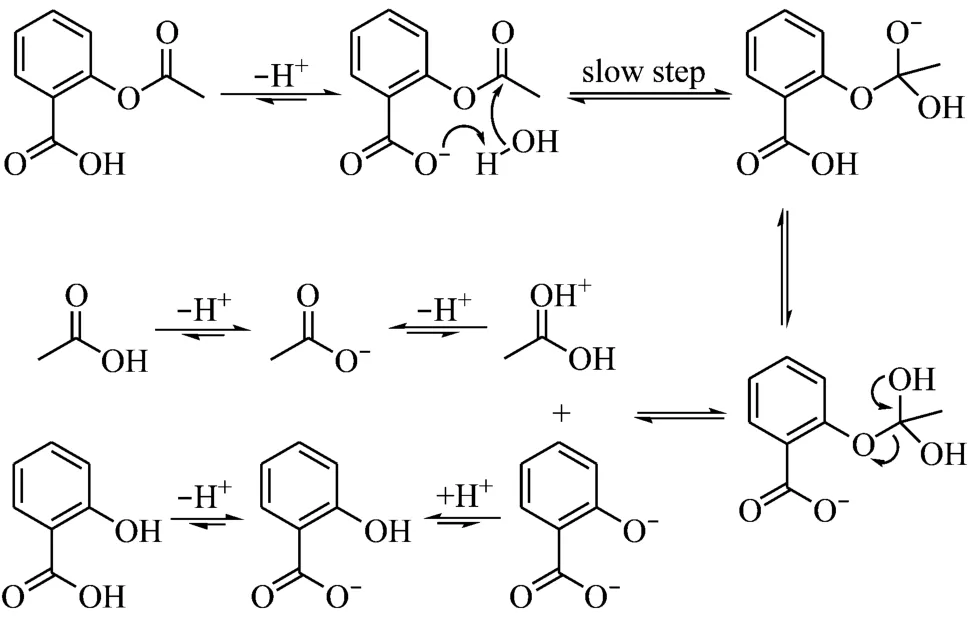
水分子不是一个活泼的亲核试剂,在中性环境中难以进攻酯羰基碳并引发酰氧键的断裂(反应决速步)。但阿司匹林的羧基在pH值大于4.5的环境中主要以羧酸根离子(B碱)的形式存在,能够诱导水分子的去质子化并赋予其更强的亲核能力[14]。因此,中性环境中阿司匹林水解反应的机理主要为分子内B碱辅助的水分子亲核加成。
4 结 语
阿司匹林有效期的测定是一个以化学反应动力学为主,同时涵盖紫外分光光度法、酯水解反应机理和药物剂型设计等相关知识点的短学时综合化学实验。该实验以学生感兴趣的真实问题为导向,能够有效激发学生的学习主动性并训练其综合运用所学理论知识分析和解决实际问题的能力。此外,该实验反应条件温和、试剂使用量少、不产生酸碱废液且不涉及大型高端仪器的使用,有望替代传统的蔗糖水解和乙酸乙酯皂化反应动力学实验在普通高等院校物理化学实验教学中推广。
