缬苯那嗪类似物P109人肝微粒体中代谢产物鉴定及酶表型研究
2022-01-25张雨沐于大伟孙钰菲刘兴华王文艳
张雨沐,李 鑫,于大伟,孙钰菲,刘兴华,王文艳
(1.烟台大学药学院,新型制剂与生物技术药物研究山东省高校协同创新中心,分子药理和药物评价教育部重点实验室,山东 烟台 264010;2.山东绿叶制药有限公司长效和靶向制剂国家重点实验室,山东 烟台 264010)
缬苯那嗪(VBZ)是突触囊泡单胺转运体2(VMAT2)抑制剂,通过阻断VMAT2发生作用,抑制其活性,从而减少单胺类物质从细胞质到突触前囊泡中的摄取和储存,使单胺类物质在细胞质中被单胺氧化酶代谢,导致释放到突触中的单胺类物质浓度降低,抵消多巴胺系统活性增强[1-2]。VBZ于2017年4月11日获美国食品药品监督管理局(FDA)批准在美国上市,商品名为 Ingrezza,是首个用于迟发性运动障碍成年患者的药物[3-4]。VBZ是丁苯那嗪代谢产物中活性最强的(+)-α-DHTBZ的缬氨酸酯(前药)[5-7],其在口服后经水解代谢为(+)-α-DHTBZ,是主要的活性物质[8]。VBZ在体内主要经氧化代谢为单氧化缬苯那嗪,活性降低;另外形成脱甲基代谢产物失去活性[9-10]。
P109是VBZ结构改造产物,其在9位进行了环丙烷甲基取代,在体内转化为活性化合物P105,结构示于图1,其具有与(+)-α-DHTBZ相似的药理活性。
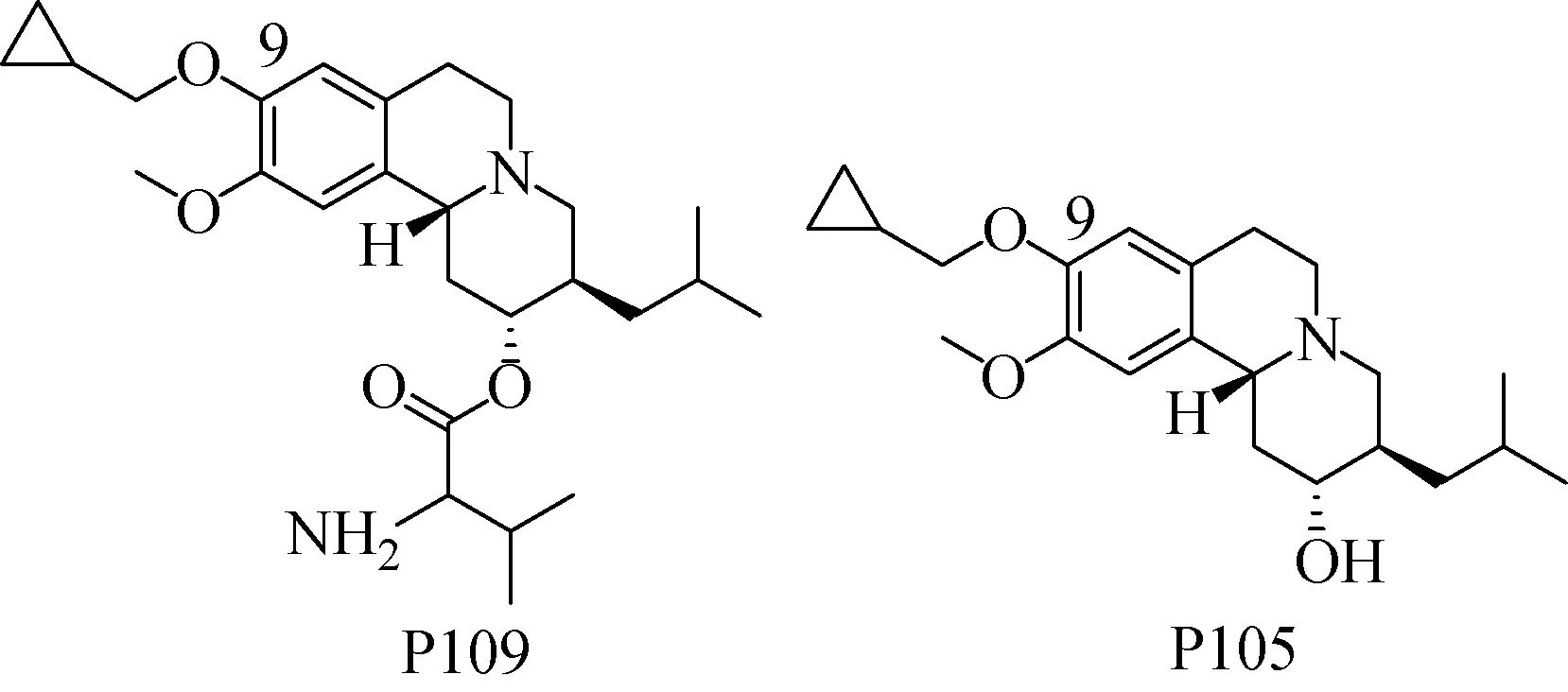
图1 P109、P105结构示意图Fig.1 Structural diagrams of P109 and P105
在早期的药物-药物相互作用确定中,体外肝微粒体孵育体系是研究药物代谢的重要模型[11-12],虽然与体内样品相比,体外孵化样品中药物代谢物的谱图通常较简单[13],但适宜条件下,体内外代谢产物具有较好的相关性[14]。高效液相色谱-高分辨质谱(HPLC-HRMS)联用技术具有灵敏度高、检测速度快和质量准确度高的特点,是药物代谢产物分析的有力手段[15-16]。本研究拟采用人肝微粒体体外孵育模型,利用超高效液相色谱-高性能台式四极杆-轨道阱质谱(UHPLC-Q ExactiveTMOrbitrap MS)技术,在正离子模式下研究P109在人肝微粒体中的代谢产物,利用高效液相色谱-三重四极杆质谱(LC-MS/MS)联用技术研究P109代谢酶表型,旨为新药的开发和可能的药物相互作用研究提供科学数据。
1 实验部分
1.1 仪器与装置
Vanquish Flex高效液相色谱仪与Q ExactiveTMOrbitrap质谱仪(配有加热电喷雾离子化源(HESI)和Xcalibur4.2工作站)、Ultimate 3000高效液相色谱仪与TSQ Quantum Access 质谱仪(配有电喷雾离子化源(ESI),Xcalibur4.1工作站)、Legend Micro 21R微量台式离心机:美国Thermo Scientific公司产品;XW-80A型旋涡混合器:上海精科实业有限公司产品;HSC-24A型氮吹仪:天津市恒奥科技发展有限公司产品;XS105型电子分析天平(十万分之一):德国Mettler-Toledo公司产品;MDF-U4186S型医用低温箱:日本三洋公司产品; DKB-501A型超级恒温水槽:上海精宏实验设备有限公司产品。
1.2 材料与试剂
P109、P105:纯度大于99%,由山东绿叶制药有限公司合成;7-OH香豆素(批号BCBZ4431,纯度99%)、甲酸(批号SHBJ0951,规格500 mL,96%):美国Sigma-Aldrich公司产品;甲醇、乙腈:色谱级,德国Meker公司产品;还原型辅酶Ⅱ(NADPH)(批号36554423,规格100 mg,98%):美国Rocheroche Diagnositics GmbH公司产品;磷酸缓冲盐(批号SLBX1022):美国Sigma公司产品;人肝微粒体(批号JPXY,规格 20 g/L):瑞德肝脏疾病研究所(上海)有限公司产品;娃哈哈纯净水:杭州娃哈哈集团有限公司产品。
1.3 实验条件
1.3.1色谱条件 色谱柱:Waters Eclipse Plus-C18柱(150 mm×2.1 mm×3.5 μm);流动相:0.1%甲酸水(A)-0.1%甲酸乙腈(B);梯度洗脱程序:0~1.0 min(95%A),1.0~5.0 min(90%A),5.0~8.0 min(80%A),8.0~12.0 min(70%A),12.0~15.0 min(5%A),15.0~20.0 min(95%A);流速0.4 mL/min;柱温30 ℃;进样量5 μL。
1.3.2Q ExactiveTMOrbitrap质谱条件 电喷雾离子源(HESI),正离子模式检测;喷雾电压3.5 kV;毛细管温度350 ℃;鞘气压力206.85 kPa,辅助气压力68.95 kPa。样品采用高分辨全扫描(Full MS/dd-MS2),一级扫描分辨率70 000,二级扫描分辨率17 500,碰撞电压(NCE)分别为20、40、60 eV,质量扫描范围m/z100~1 000。
1.3.3TSQ Quantum Access质谱条件 电喷雾离子源(ESI),正离子模式检测;喷雾电压4.0 kV;毛细管温度350 ℃;鞘气压力206.85 kPa,辅助气压力34.475 kPa。样品采用全扫描(Full scan)、二级离子全扫描(MS2scan)。根据代谢产物鉴定所得的质谱图确定监测离子对,列于表1。
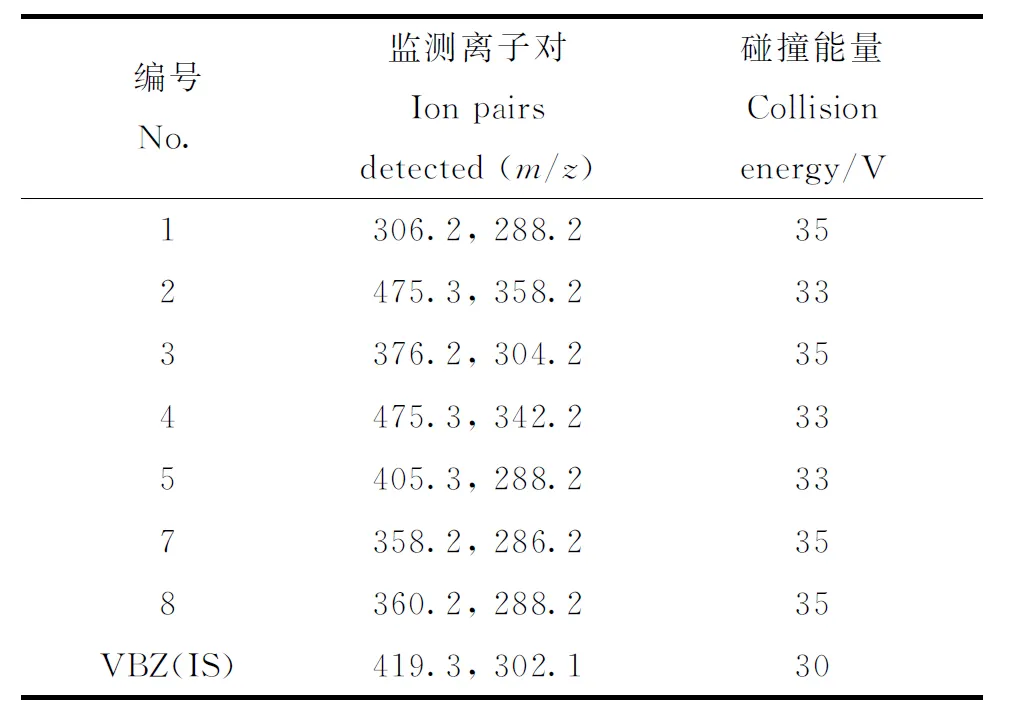
表1 HPLC-MS/MS监测P109/P105代谢产物离子对Table 1 Ion pairs of P109/P105 metabolites in human liver microsomes detected by HPLC-MS/MS
1.4 人肝微粒体温孵体系
实验分为实验组、阳性对照组和阴性对照组3组(n=3)。实验组为含P109的孵育体系;阳性对照组为含阳性探针底物(非那西丁、安非他酮、阿莫地奎、双氯芬酸、S-美芬妥英、右美沙芬和咪达唑仑)孵育体系,确定孵育体系活性;阴性对照组孵育体系中不含NADPH,确定P109在体系中的稳定性。
1.4.1代谢产物鉴定温孵体系 温孵管中先加入P109,氮气吹干,然后加入肝微粒体混合体系,涡旋30 s,置于37 ℃水浴预孵育5 min,加入NADPH启动反应,孵育体系中各成分终浓度为:P109为10 μmol/L,肝微粒体为1 g/L,NADPH为1 mmol/L,总孵育体积为200 μL。分别于加入NADPH启动反应后0和1 h,加入400 μL乙腈溶液终止反应。将终止反应的孵育样品涡旋振荡2 min,4 ℃下以13 000 r/min离心10 min,将上清液全部移取至1.5 mL离心管,氮气吹干,100 μL流动相复溶,即为待检样品。
1.4.2代谢产物酶表型研究温孵体系 在温孵管中先加入P109/P105和抑制剂(α-萘黄酮、盐酸噻氯匹定、孟鲁斯特纳、磺胺苯吡唑、S-(+)-N-3苄基苯乙基内酰脲、奎尼丁、酮康唑),氮气吹干,加入肝微粒体混合体系,涡旋30 s,置于37 ℃水浴预孵育5 min,加入NADPH启动反应,孵育体系中各成分终浓度为:P109/P105为1 μmol/L,肝微粒体为0.2 g/L,NADPH 为1 mmol/L,总孵育体积为100 μL。分别于加入NADPH启动反应后0和20 min,加入400 μL乙腈溶液终止反应。后续同1.4.1节。
1.5 数据处理
1.5.1代谢产物鉴定 质谱扫描得到总离子流色谱图(TIC),利用Xcaliber4.2工作站,先用精确分子质量推测可能的元素组成,再结合质谱裂解碎片信息进行数据处理,通过分子式预测模块,预测母离子和碎片离子的分子式,鉴定P109的体外代谢产物结构,质量精度误差在5×10-6以内。
1.5.2代谢产物酶表型研究 将数据导入Excel软件,用以下公式进行计算:代谢产物产量=20 min的代谢产物产量-0 min的代谢产物产量;抑制率%=(1-含有抑制剂的代谢产物产量/不含抑制剂的代谢产物产量)×100%,根据计算结果绘制柱状图。
2 结果与讨论
2.1 P109裂解规律推断
在正离子模式下,P109的保留时间为10.4 min,准分子离子峰为[M+H]+m/z459.320 28,分子式为C27H42N2O4,经碰撞裂解,母离子丢失C2位上的缬氨酸,形成碎片离子[M+H-VAL]+m/z342.241 46,后丢失C9位上的环丙烷甲基,形成基峰[M+H-VAL-C4H6]+m/z288.194 64。此外,还形成碎片离子m/z405.273 19(脱环丙烷甲基)、m/z360.252 41(VAL C—O键断裂)、m/z232.132 19(脱3位2-甲基丙基)、m/z178.085 51(环裂解)、m/z151.074 83(环裂解),参考异喹啉生物碱裂解途径[17-19],推断其裂解途径示于图2。这些碎片离子信息可用于后续代谢产物的鉴定和分析。
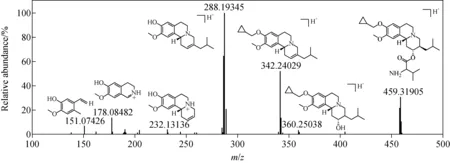
图2 P109可能的裂解规律Fig.2 Fragmentation pathways of compound P109
2.2 P109代谢产物分析与鉴定
在NADPH存在的体外人肝微粒体孵育体系中共筛选并鉴定出1个原型和8个代谢产物,离子流图示于图3,代谢产物信息列于表2。
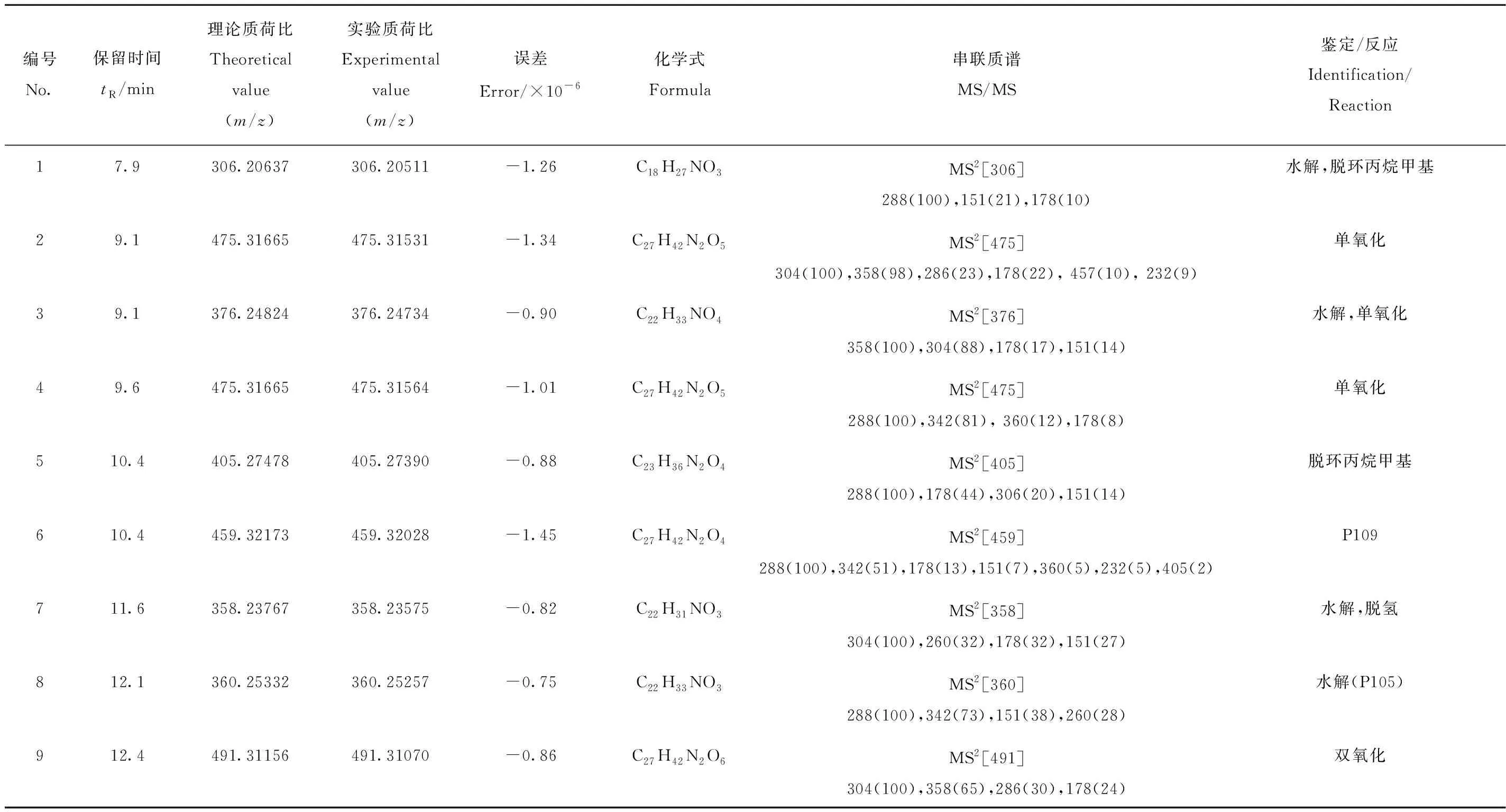
表2 UHPLC-Q ExactiveTM Orbitrap MS检测P109的肝微粒体代谢产物表征Table 2 Characteristic fragment ions of compound P109 metabolites in human liver microsomes by UHPLC-Q ExactiveTM Orbitrap MS
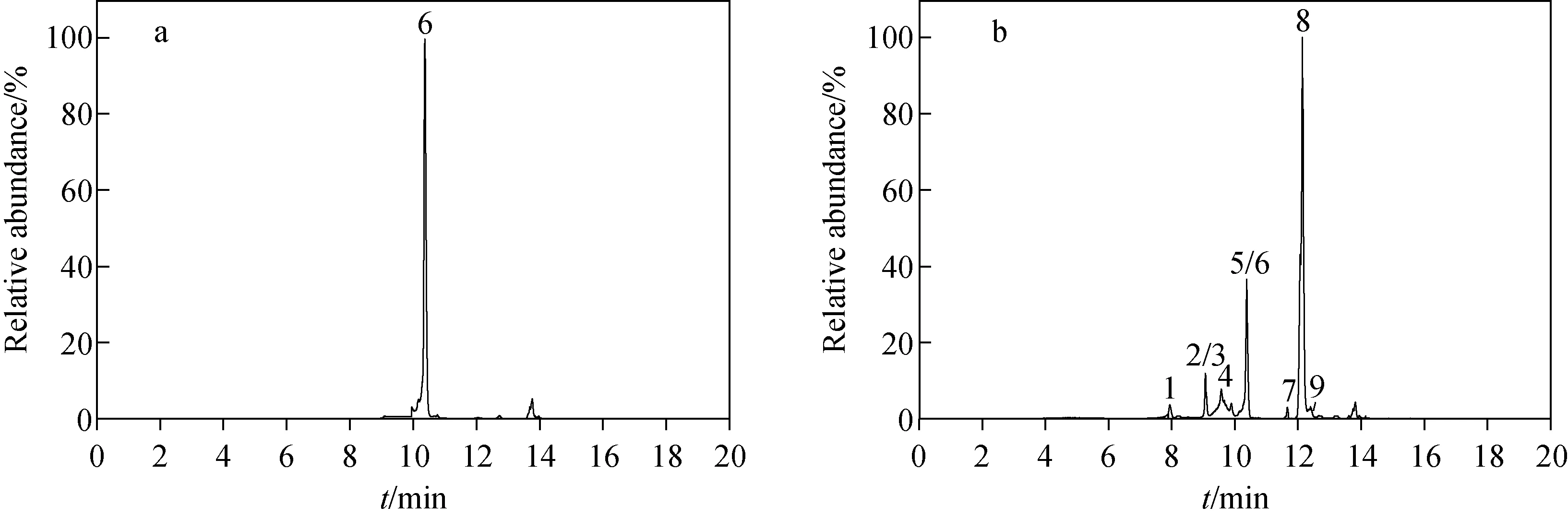
注:a.孵育0 h;b.孵育1 h
代谢产物1的保留时间为7.9 min,准分子离子峰为[M+H]+m/z306.205 11(-1.26×10-6,C18H27NO3),比P109低153 u,且产生的m/z288、178、151与P109二级碎片离子峰相同,推测为酯键水解为羟基(-99 u)且脱环丙烷甲基(-54 u)形成的产物。
代谢产物2和4的保留时间分别为9.1、9.6 min,准分子离子峰分别为[M+H]+m/z475.315 31(-1.34×10-6,C27H42N2O5)、[M+H]+m/z475.315 64(-1.01×10-6,C27H42N2O5),推测代谢产物2、4为单氧化(+16 u)产物。代谢产物2丢失1个水分子形成二级碎片离子m/z457,且具有二级碎片离子m/z304、286,推测氧化部位位于2-甲基丙基,脱去水分子使该部位质荷比减小2 u,脱去该部位后形成的碎片离子m/z178、232与P109一致。代谢产物4具有二级碎片离子m/z288、342、360、178,与P109二级碎片离子相同,推测氧化部位位于缬氨酸酯,酯基水解为羟基时随酯基一起脱去。
代谢产物3的保留时间为9.1 min,准分子离子峰为[M+H]+m/z376.248 24(-0.90×10-6,C22H33NO4),且生成二级碎片离子m/z358、304、178、151,与代谢产物2相同,为2-甲基丙基氧化后脱水形成一系列碎片离子,推测代谢产物3为酯基水解为羟基(-99 u)同时单氧化(+16 u)形成的产物。
代谢产物5的保留时间为10.4 min,准分子离子峰为[M+H]+m/z405.273 90(-0.88×10-6,C23H36N2O4),比P109低54 u,推测为脱环丙烷甲基(-54 u)产物。
代谢产物6的保留时间为10.4 min,准分子离子峰为[M+H]+m/z459.320 28(-1.45×10-6,C27H42N2O4),保留时间与碎片离子峰均与P109对照品一致,推测为P109。
代谢产物7的保留时间为11.6 min,准分子离子峰为[M+H]+m/z358.235 75(-0.82×10-6,C22H31NO3),比P109低101 u,推测为酯基水解(-99 u)后脱氢(-2 u)产物。
代谢产物8的保留时间为12.1 min,准分子离子峰为[M+H]+m/z360.252 57(-0.75×10-6,C22H33NO3),比P109低99 u,且保留时间和碎片离子峰均与化合物P105对照品一致,推测为酯基水解(-99 u)产物。
代谢产物9的保留时间为12.4 min,准分子离子峰为[M+H]+m/z491.310 70(-0.86×10-6,C27H42N2O6),比P109高32 u,推测为双氧化(+33 u)产物。
2.3 P109代谢途径分析
根据原型化合物及代谢产物的质谱裂解信息,推测P109的代谢途径示于图4。
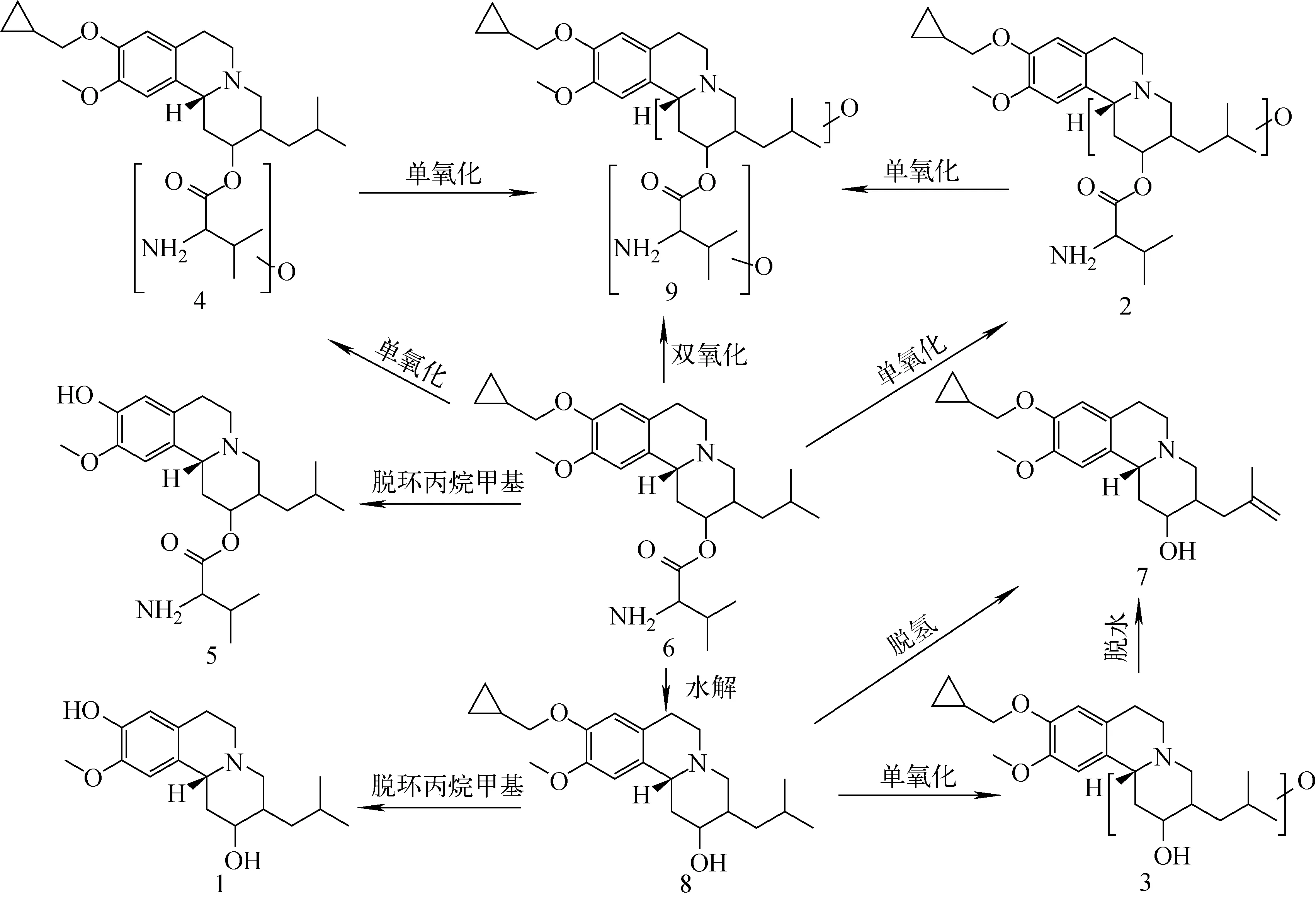
图4 P109经人肝微粒体的代谢途径Fig.4 Metabolic pathways of P109 in liver microsomal samples
P109体外主要经历3个代谢途径:1) 发生氧化反应生成化合物2、4和9,P109在2-甲基丙基或缬氨酸酯上发生单氧化形成代谢产物2和4,同时发生双氧化反应或代谢产物2、4进一步氧化形成代谢产物9;2) 发生水解反应生成代谢产物1、3、7和8,P109缬氨酸酯水解为羟基生成代谢产物8,进一步发生脱环丙烷甲基、单氧化、脱氢反应,生成代谢产物1、3和7;3) 发生脱环丙烷甲基反应生成代谢产物5。经药理研究发现,P109与VBZ相似,是前药,其在体内缬氨酸酯键断裂形成的代谢产物8(P105)具有VMAT2抑制作用,且对VMAT2的亲和力远高于前药P109,是主要的活性物质。
2.4 P109代谢产物酶表型研究
对P109温孵样品监测代谢产物2、4、5、8(P105),P105温孵样品监测代谢产物1、3、7,双氧化代谢产物因生成量过少不予监测,计算各代谢产物不同亚型CYP酶抑制率,示于图5。
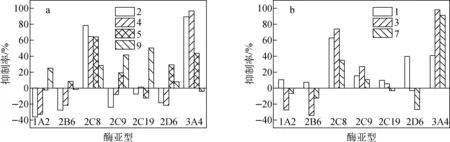
图5 特异性化学抑制剂对人肝微粒体中P109(a)和P105(b)代谢产物产生的抑制作用Fig.5 Inhibitory effect of specific chemical inhibitors on metabolism of P109 (a) and P105 (b) in human liver microsomes
研究表明,CYP3A4参与50%以上临床用药的Ⅰ相代谢[20];CYP2D6参与代谢的药物占总P450代谢药物的30%[21];CYP2C8负责至少5%的临床药物代谢,主要包括紫杉醇6-α羟基化反应和阿莫地喹N-脱烷基化反应[22]。结合本实验结果可知,氧化代谢产物2、3、4,脱氢代谢产物7主要经CYP3A4代谢,CYP2C8为其次要代谢亚型酶;脱环丙烷甲基代谢产物1、5主要经CYP2C8代谢,次要代谢亚型为CYP3A4和CYP2D6。水解代谢产物8涉及多种亚型酶,且在孵育体系中会发生进一步代谢,主要代谢亚型暂时无法推断,需进一步研究。
3 结论
本研究应用UHPLC-Q ExactiveTMOrbitrap MS技术快速筛选并鉴定了P109经人肝微粒体体外代谢的产物,对筛选出的8个代谢产物进行初步鉴别,均为无明显毒性结构的Ⅰ相代谢产物,并阐述了P109的肝微粒体代谢规律以及各代谢产物的代谢酶表型。P109为前药型新化合物,本研究有助于阐明药物的体内代谢途径,对于药动学、药效学和药物的安全性评价等研究具有重要意义,同时为体外实验的结果外推至体内实验提供了理论支持。
