正交试验优选抗风止痛宁提取工艺*
2021-12-15王景媛曾永成高佳蓉强选萍史亚军
晏 菲,王景媛,曾永成,高佳蓉,强选萍,史亚军
(陕西中医药大学药学院·陕西省中药基础与新药研究重点实验室,陕西 咸阳 712046)
类风湿关节炎(RA)属中医痹证范畴。《黄帝内经·素问·痹论》曰:“风寒湿三气杂至,合而为痹也。”风、寒、湿、热等外邪侵袭人体,邪留关节,经脉气血闭阻不通,不通则痛。RA 患者疼痛、水肿、四肢麻木等体征大都表露于体肤,针对寒湿痹阻症患者,以中药外用,如熏洗、外敷、蜡疗、艾灸等[1-4],直接作用于皮肤或黏膜,吸收更快,直达病所,发挥舒筋活血、通络止痛、驱邪外出的作用[5]。抗风止痛宁酊剂是我校附属医院治疗寒湿痹阻型RA 的临床经验方,由丹参、红花、三七、全蝎、生川乌、伸筋草等药材组方,原工艺采用传统制备方法,将上述药材用白酒(规定浓度)浸泡地藏1 ~3 个月而得,此法生产周期较长,提取工艺缺乏科学的评价手段和方法。为进一步规范制剂的制备工艺,本研究中采用正交试验法,以乙醇为提取溶剂,丹参酮ⅡA、羟基红花黄色素A 和总固体含量为综合评价指标,优化抗风止痛宁的提取工艺,为其现代制剂开发提供参考。现报道如下。
1 仪器与试药
1.1 仪器
U-3000 型高效液相色谱仪(美国 Thermo Fisher公司);BT-25S 型电子天平(赛多利斯<上海>贸易有限公司,精度为十万分之一);DHG-9140 型电热恒温鼓风干燥箱(上海一恒科技有限公司)。
1.2 试药
丹参酮ⅡA对照品(批号为 110766 -201721,含量≥99.5%),羟基红花黄色素A 对照品(批号为111637-201810,含量≥93.1%),均购自中国食品药品检定研究院;乙醇为分析纯,甲醇、乙醇、乙腈均为色谱纯,水为娃哈哈纯净水。丹参、红花、三七、全蝎、生川乌、伸筋草饮片(陕西兴盛德饮片有限公司,批号分别为20180107,20180825,20180921,20180910,20180910,201800927)。
2 方法与结果
2.1 丹参酮ⅡA 含量测定
2.1.1 色谱条件
色谱柱:Agilent TC -C18柱(250 mm ×4.6 mm,5 μm);流动相:甲醇 - 水(75 ∶25,V / V);流速:1.0 mL /min;检测波长:270 nm;柱温:25 ℃;进样量:10 μL。
2.1.2 溶液制备
取丹参酮ⅡA对照品 6.13 mg,精密称定,置50 mL 容量瓶中,以甲醇溶解并定容,即得质量浓度为122.6 μg/mL 的丹参酮ⅡA对照品溶液。采用浸渍法提取,将浸出液滤过,浓缩至每100 mL 相当于原饮片10 g(总处方量),即得样品溶液;精密量取样品溶液25 mL,减压回收溶剂,残渣加甲醇溶解并定容至25 mL,即得供试品溶液。
2.1.3 方法学考察
系统适用性试验:取 2.1.2 项下丹参酮ⅡA对照品溶液和供试品溶液各适量,按2.1.1 项下色谱条件进样测定,记录色谱图。结果理论板数按丹参酮ⅡA计应不低于3 000,分离度大于1.5,基线分离良好。详见图1。
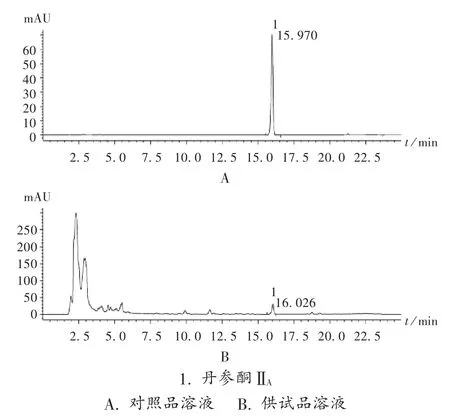
图1 丹参酮ⅡA 高效液相色谱图1. tanshinone ⅡAA. Reference solution B.Test solutionFig.1 HPLC chromatograms of tanshinone ⅡA
线性关系考察:精密量取丹参酮ⅡA对照品溶液0,0.5,1.0,1.5,2.0,2.5,3.0 mL,分别置 10 mL 容量瓶中,加甲醇定容,按2.1.1 项下色谱条件进样测定,记录峰面积。以丹参酮ⅡA质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程 Y =134.19 X + 28.911(r = 0.999 7,n =7)。结果表明,丹参酮ⅡA质量浓度在 6.13 ~ 36.78 μg /mL 范围内与峰面积线性关系良好。
检测限确定:精密量取 2.1.2 项下丹参酮ⅡA对照品溶液适量,倍比稀释,并按2.1.1 项下色谱条件进样测定,以信噪比( S / N)为 3 ∶1 时计算检测限。结果丹参酮ⅡA的检测限为 0.01 μg/mL。
精密度、稳定性、重复性、加样回收试验:按规定方法进行试验。结果精密度试验的 RSD 为0.71%,表明仪器精密度良好;稳定性试验的 RSD 为1.91%,表明室温下供试品溶液在12 h 内稳定;重复性试验的 RSD为1.25%,表明方法重复性良好;平均加样回收率为99.03%,RSD 为 0.96%(n =6),表明方法准确度良好。
2.2 羟基红花黄色素A 含量测定
2.2.1 色谱条件
色谱柱:BD Hypersil C18柱(250 mm ×4.6 mm,5 μm);流动相:甲醇 - 乙腈 - 0.7% 磷酸水溶液(26 ∶2 ∶72,V / V / V);流速:1.0 mL /min;检测波长:403 nm;柱温:30 ℃;进样量:10 μL。
2.2.2 溶液制备
取羟基红花黄色素 A 对照品 3.07 mg,精密称定,置 50 mL 容量瓶中,以甲醇溶解并定容;取1 mL置50 mL 容量瓶中,以甲醇定容,即得质量浓度为12.28 μg /mL 的羟基红花黄色素 A 对照品溶液。精密量取2.1.2 项下样品溶液1 mL,减压回收溶剂,残渣加甲醇溶解并定容至100 mL,即得供试品溶液。
2.2.3 方法学考察
系统适用性试验:取2.2.2 项下羟基红花黄色素A对照品溶液和供试品溶液各适量,按2.2.1 项下色谱条件进样测定,记录色谱图。结果理论板数以羟基红花黄色素A 计应不低于 3 000,分离度大于1.5,基线分离良好。详见图2。
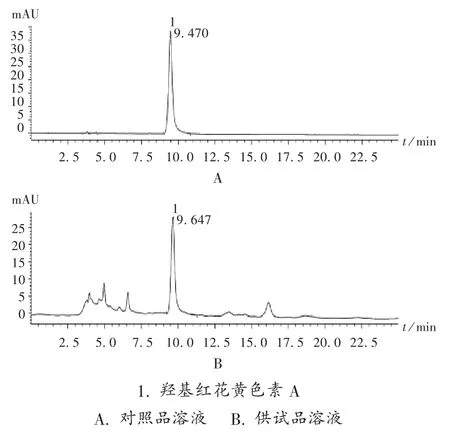
图2 羟基红花黄色素A 高效液相色谱图1. hydroxysafflor yellow AA. Reference solution B.Test solutionFig.2 HPLC chromatograms of hydroxysafflor yellow A
线性关系考察:精密吸取羟基红花黄色素A 对照品溶液 0,0.5,1.0,2.0,3.0,4.0,5.0 mL,分别置 10 mL容量瓶中,加甲醇定容,按2.2.1 项下色谱条件进样测定,记录峰面积。以羟基红花黄色素 A 质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程 Y =26.767 X -1.364 4(r =0.999 8,n =7)。结果表明,羟基红花黄色素 A 的质量浓度在0.61 ~ 6.14 μg /mL 范围内与峰面积线性关系良好。
定量限与检测限确定:精密量取2.2.2 项下羟基红花黄色素A 对照品溶液适量,倍比稀释,并按2.2.1 项下色谱条件进样测定,以信噪比(S / N)分别为 10 ∶1 和3∶1 时计算定量限和检测限。结果,羟基红花黄色素A 的定量限和检测限分别为 0.012 μg /mL 和 0.005 μg /mL。
精密度、稳定性、重复性、加样回收试验:按规定方法进行试验。结果精密度试验的 RSD 为0.86%,表明仪器精密度良好;稳定性试验的 RSD 为1.78%,表明室温下供试品溶液在12 h 内稳定;重复性试验的 RSD为2.31%,表明方法重复性良好;平均加样回收率为101.75%,RSD 为 1.16%(n =6),表明方法准确度良好。
2.3 总固体含量测定
参照2020 年版《中国药典(四部)》通则“固体总量测定法”,计算总固体含量(%)。精密量取样品溶液25 mL,置已干燥至恒重的蒸发皿中,水浴蒸干,于105 ℃干燥3 h,置干燥器中冷却30 min,迅速精密称定质量,计算供试品中总固体含量(%)。
2.4 单因素考察
乙醇体积分数:取处方量药材粗粉5 份,分别加10倍量50%,60%,70%,80%,90%乙醇浸渍3 d,综合评分显示,在乙醇体积分数为70%时达到最大值。故选择乙醇体积分数因素的三水平分别为60%,70%,80%。
乙醇用量:取处方量药材粗粉5 份,分别加入5,10,15,20,25 倍 70%乙醇浸渍 3 d,综合评分显示,随着乙醇用量的增加,综合评分逐渐升高,但当乙醇用量超20 倍后增加不明显。故选择乙醇用量的三水平分别为15,20,25 倍。
浸渍时间:取处方量药材粗粉5 份,加入10 倍量70% 乙醇,分别浸渍 1,2,3,4,5 d,综合评分显示,在提取1 ~3 d 时逐渐升高,4 d 以上时基本无变化。综合提取次数的影响,从提高效率方面考虑,故选择浸渍时间的三水平分别为 2,3,4 d。
提取次数:取处方量药材粗粉5 份,分别加入10 倍量 70%乙醇,浸渍 3 d 为 1 次,分别考察提取 1,2,3,4,5 次的情况。综合评分显示,在提取1 ~3 次时升高,提取3 次后基本无变化,说明3 次时已基本提取完全。故选择提取次数的三水平分别为1,2,3 次。
2.5 正交试验
以丹参酮ⅡA含量(Ⅰ)、羟基红花黄色素A 含量(Ⅱ)、总固体含量(Ⅲ)及综合评分(Ⅳ)为评价指标,采用综合加权评分法[6],根据影响提取工艺因素的大小、权重系数分别记为 0.4,0.4,0.2,综合评分 =丹参酮ⅡA含量 /丹参酮ⅡA含量max×0.4 ×100 +羟基红花黄色素A含量 /羟基红花黄色素 A 含量max×0.4×100 +总固体含量 /总固体含量max×0.2×100。以乙醇体积分数(A)、乙醇用量(B)、浸渍时间(C)、提取次数(D)为考察因素,设计 L9(34)正交试验。结果见表1 至表3。

表1 L9(34)正交试验因素水平表Tab.1 Factors and levels the L9(34) orthogonal test
由表2 和表3 可知,各因素对提取效果的影响强度依次为乙醇体积分数>提取次数>浸渍时间>乙醇用量,最佳参数为A2B3C2D3;仅A 因素对提取有显著影响。从节约能源和提高效率的角度出发,选择最佳提取工艺为A2B1C2D3,即加15 倍量70%乙醇,浸渍3 次,每次3 d,将浸出液滤过、浓缩,调整至含醇量为70%,且每100 mL 相当于原饮片(总处方量)10 g。
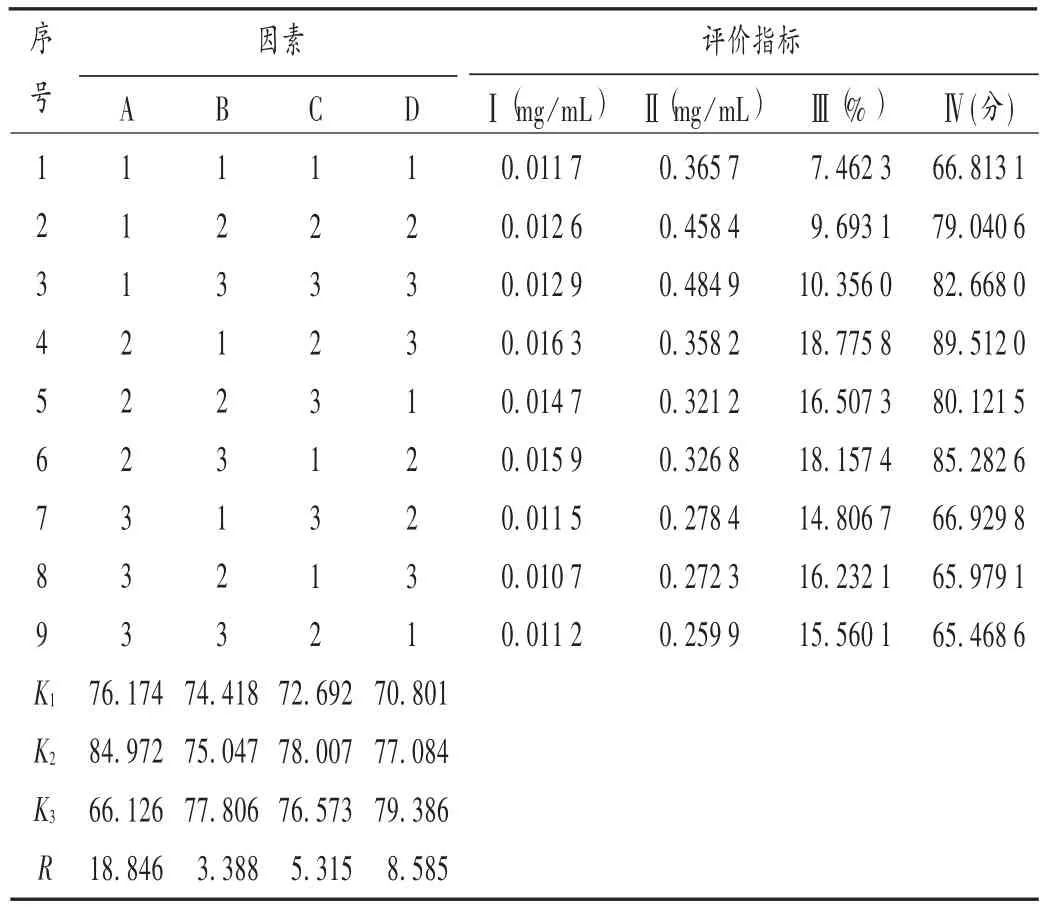
表2 L9(34)正交试验设计方案及结果Tab.2 Design and results of the L9(34)orthogonal test
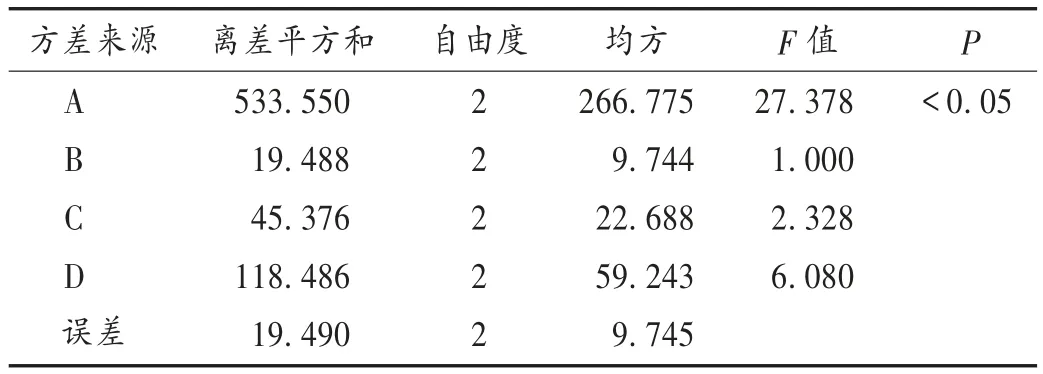
表3 方差分析结果Tab.3 Results of ANOVA
2.6 验证试验
按最佳提取工艺进行6 次平行试验,并测定丹参酮ⅡA、羟基红花黄色素A 及总固体含量。结果丹参酮ⅡA、羟基红花黄色素A 和总固体的平均含量分别为0.016 2 mg/mL(RSD 为 1.23% )、0.485 5 mg /mL(RSD 为 1.38% )和18.81%(RSD 为 2.06%)。结果表明,该工艺合理可行。
3 讨论
该制剂处方药材的主要有效成分为丹参中丹参酮类、红花中黄酮类、三七中皂苷类、川乌和伸筋草中生物碱类等,为了确保有效成分提取率,参考文献[7-8]和原工艺白酒浸泡地藏方法,本研究中采用乙醇浸渍提取。主药丹参、红花为经典药对,为活血化瘀之要药。丹参中丹参酮ⅡA具有抗血小板聚集、抗炎、抗氧化等作用[9-11],红花中羟基红花黄色素A 具有抗血小板聚集、抗炎、镇痛及抑制软骨细胞凋亡的作用[12-16],二者为主要指标性成分,总固体含量测定在中药提取物质量和制剂有效成分含量控制上具有重要意义,故选择丹参酮ⅡA、羟基红花黄色素A 及总固体含量作为工艺优化的评价指标。
优化工艺中用70%乙醇提取,有利于有效成分的浸出,且乙醇无毒、价低易得,适合用于工业化大生产,在确保有效成分含量的同时大大提高了制剂效率、制剂质量和疗效。临床应用的大部分中药制剂以经验配制为主,多数尚未完善提取工艺和质量标准,对其成分缺乏科学监测,该类制剂提取工艺的考察能较好地解决这一问题,也为今后制剂配制的规范化与工业化生产提供了依据。
