荧光光谱法研究萘普生和壳聚糖之间的相互作用
2021-02-16孙杰张冰卫徐光富李博南京市食品药品监督检验院南京98中国药科大学药学院南京0009中国药科大学理学院南京98
孙杰,张冰卫,徐光富,李博*(. 南京市食品药品监督检验院,南京 98;. 中国药科大学药学院,南京 0009;3. 中国药科大学理学院,南京 98)
壳聚糖(chitosan)是氨基葡萄糖和乙酰氨基葡萄糖组成的多糖,它是天然糖类中唯一大量存在的碱性氨基多糖[1-2]。目前壳聚糖已经被应用于食品、药用辅料、生物医学材料等多个领域,在缓控释制剂、生物医学材料等方面扮演着越来越重要的角色[3-6]。
萘普生(naproxen)是非甾体消炎镇痛药,通过抑制前列腺素合成而起到抗炎镇痛作用[7]。近年来已有利用壳聚糖等对萘普生进行包封[8-9],开发缓控释制剂等的报道,以改善萘普生的吸收及降低其不良反应。在制剂中,辅料与药物之间可能通过静电力、范德华力、疏水性作用力、氢键作用力等形成包合物、共晶、分散体、复合物等,因此在药物制剂研发过程中,对药物与辅料间相互作用的考察不可缺少[10]。热分析法、红外光谱法、X 衍射法等是常用的药物与辅料相互作用研究方法[11]。
荧光光谱法常用于蛋白质和小分子之间相互作用的研究,利用小分子对蛋白质荧光猝灭,通过Stem-Volmer 方程计算荧光猝灭常数Ksv,并计算结合常数和结合位点数以及相应的热力学参数ΔS 和ΔG,研究结合常数和作用力类型[12]。课题组前期对大分子猝灭剂与小分子荧光物之间的相互作用模型进行了完善,比较了小分子荧光药物与大分子之间相互作用研究模型[13]。本文利用荧光光谱法研究萘普生和壳聚糖之间相互作用的结合常数,推测壳聚糖与萘普生作用的基本原理,从而为壳聚糖与药物的相互作用的研究和应用提供理论基础,也为壳聚糖作为辅料的应用提供基础。
1 材料
F4600 荧光分光光度计(日本日立);2004-21 智能型超级恒温水槽(常州国华电器有限公司);pH 计(pHS-3B,上海仪电科学仪器股份有限公司)。萘普生(含量:99.9%,批号:100198-201004,中国食品药品检定研究院),壳聚糖(4 ~296 kD,中国药科大学药剂教研室;410 kD,江南大学),其他试剂为分析纯,水为二次蒸馏水。
2 方法
2.1 溶液配制
2.1.1 萘普生溶液(NPS) 称取10 mg 萘普生于10 mL 的量瓶中,甲醇溶解并定容,得萘溶液浓度为1.74×10-4mol·L-1的NPS 溶液,于4℃保存。
2.1.2 壳聚糖溶液(CTS) 称取0.25 mg 壳聚糖于25 mL 量瓶中,水溶解并定容,得浓度为2.44×10-7mol·L-1的CTS 溶液,于4℃保存。
2.1.3 Britton-Robinson(BR)缓冲液 取0.04 mol·L-1的磷酸、乙酸、硼酸混合酸液,用0.2 mol·L-1氢氧化钠调节pH 至5。
2.2 激发波长和发射波长的确定
移取0.1 mL 的NPS 溶液于5 mL 量瓶中,加1.5 mL BR 缓冲液,用水定容,置1 cm×1 cm 的石英比色皿中,扫描激发光谱和发射光谱,确定最大激发波长(262 nm)和发射波长[(355±0.5)nm]。荧光激发和发射波长狭缝宽度皆为5 nm,扫描速度为1200 nm·min-1,扫描电压为400 V。
2.3 荧光光谱分析
在5 mL 量瓶中,依次加入0.1 mL NPS 溶液、1.5 mL BR 缓冲液,用水定容,摇匀,298 K(25℃)恒温水浴10 min,固定激发波长262 nm,在250 ~ 450 nm 扫描NPS 的荧光光谱图。
在5 mL 量瓶中,依次加入0.1 mL NPS 溶液、1.5 mL BR 缓冲液和不同体积的CTS 溶液,用水定容,摇匀,配制系列NPS 和CTS 混合溶液。将该混合溶液置298 K(25℃)恒温水浴10 min,固定激发波长262 nm,在250 ~450 nm 内分别扫描复合物的荧光光谱图,记录各溶液的荧光强度。
2.4 结合常数测定
根据Lineweaver-Burk 双倒数曲线(公式1),以NPS 溶液355 nm 处荧光强度为F0,NPS 和CTS 混合溶液的355 nm 处荧光强度为F,将CTS浓度[Q]对荧光猝灭与F0/F进行线性回归,计算CTS 与NPS 的相互作用的结合常数Ka。

3 结果与讨论
3.1 荧光光谱特征
如图1 所示,NPS 的荧光发射波长和激发波长分别为355 nm 和262 nm。因此后续试验中,分别以355 nm 和262 nm 为荧光发射波长和激发波长。

图1 萘普生的荧光激发光谱图和发射光谱图Fig 1 Fluorescence excitation and emission spectrogram of NPS
3.2 体系pH 值对荧光猝灭的影响
分别在pH 4、5、6、7、8、9、10 的条件下测定NPS 溶液(1.74×10-4mol·L-1)、CTS 溶液(2.44×10-7mol·L-1)、NPS-CTS 结合物的荧光强度值。结果如图2 所示,CTS 在各个pH值下荧光强度均很弱,与NPS 的荧光强度相比,可以忽略不计;NPS 的荧光强度随着pH 值的变化没有明显的变化。

图2 pH 值对荧光猝灭的影响Fig 2 Influence of pH on fluorescence quenching
当pH 值为5 时,NPS-CTS 的荧光强度最弱,此时pH 值条件下CTS 对NPS 的荧光猝灭程度最大,而对于NPS 和CTS 自身的荧光强度没有明显的影响。因此选择与NPS 的pKa值相近的pH 5为测定的pH 值。由图3 得出,在pH 5 时,NPS和CTS 相互作用的结合常数相对最大。
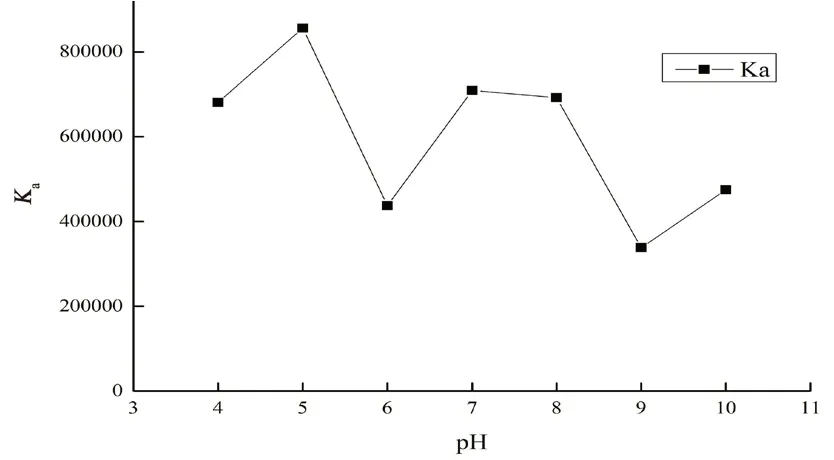
图3 pH 值对结合常数的影响Fig 3 Influence of pH on binding constants
3.3 缓冲液的用量对荧光猝灭的影响
确定BR 缓冲液的pH 值为5.0,考察NPS、CTS、NPS-CTS 在不同用量缓冲液(0.5、1.0、1.5、2.0、2.5、3.0、3.5 mL)条件下荧光强度值的变化,结果发现缓冲液用量对荧光强度的影响不大,综合选择1.5 mL 作为试验条件。
3.4 水浴时间的考察
确定缓冲液的pH 为5.0,用量为1.5 mL,取NPS 0.7 mL,加BR 缓冲液10.5 mL,加CTS 0.7 mL,用纯净水补足至35 mL,在25 ℃恒温水浴中水浴加热,于0 ~67 min 时间点取样测定荧光强度,结果显示在0 ~67 min 内,体系猝灭程度基本不变,复合物在测定时间内稳定,综合选择水浴时间为10 min。
3.5 荧光猝灭类型
荧光猝灭分为动态猝灭和静态猝灭两种,动态猝灭是猝灭剂和荧光物质的激发态分子之间的碰撞等导致的猝灭,而静态猝灭是猝灭剂和荧光分子在基态时生成不发光的复合物,从而导致荧光强度降低。在研究分子间相互作用,计算结合常数和结合位点数时,静态猝灭是关键的前提条件。所以首先要对其猝灭类型进行判断。试验考察了不同温度对NPS 和CTS 相互作用情况的影响。图4 为NPS 在288、298 和303 K 与CTS 相互作用的Stem-Volmer(公式2)曲线图,表1 为各温度计算的Ksv。

图4 不同温度下NPS 与CTS 相互作用的Stem-Volmer 曲线图Fig 4 Stem-Volmer curve of interaction between NPS and CTS

表1 不同温度下CTS-NPS 的Ksv 常数Tab 1 Ksv of CTS-NPS at different temperatures

如图4 和表1 所示,各温度下Stem-Volmer曲线呈现良好的线性关系(r>0.99),随着温度的升高,Stem-Volmer 曲线图斜率下降,Ksv常数不断变小,这是因为对于静态猝灭在温度升高时可能引起复合物的稳定性下降,从而减小了静态猝灭的程度,因此可以判断本文研究猝灭属于静态猝灭。在实际操作过程中,为了避免温度太高使得分子热运动加剧从而导致体系在静态猝灭的同时发生动态猝灭,同时为了试验的易于进行,最终选择298 K 作为试验条件。
3.6 结合常数测定
取1.74×10-4mol·L-1NPS 溶液,加入不同浓度的CTS,加1.5 mL BR 缓冲液,用水定容到5 mL。激发波长262 nm,于200 ~500 nm 内扫描得到萘普生的荧光猝灭光谱(见图5)。

图5 298 K 时不同浓度CTS 对萘普生的荧光猝灭光谱图Fig 5 Fluorescence quenching of NPS with series concentration of CTS at 298 K
如图5 的猝灭曲线所示,不同浓度CTS-NPS溶液的最大发射波长均为355 nm,表明CTS 能够与NPS 发生相互作用进而猝灭NPS 的荧光。以355 nm 处的荧光强度,按Lineweaver-Burk 曲线进行线性回归,得到图6 的回归曲线图,以截距与斜率的比值计算Ka,得到CTS 与NPS 的结合常数Ka为8.29×105L·mol-1;按公式(3)对双对数曲线进行线性回归,得到图7 的回归曲线图,其斜率为结合位点数n,得CTS 与NPS 的结合位点数为1.12,可见 CTS 与NPS 基本上是1∶1 结合的。

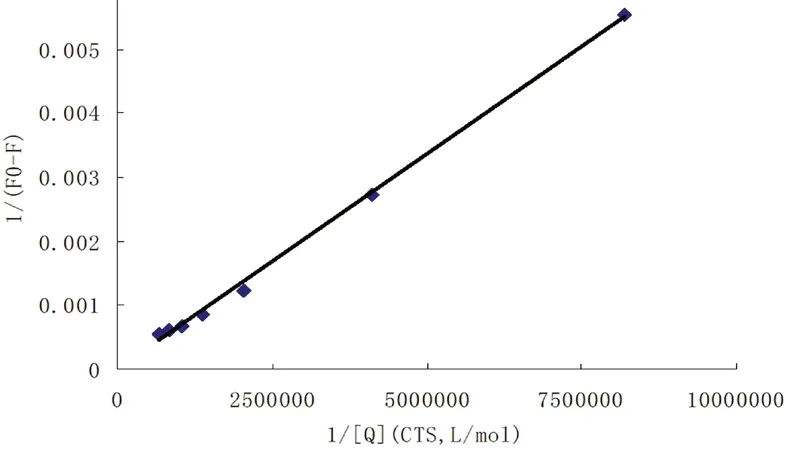
图6 NPS 和CTS 相互作用的Lineweaver-Burk 曲线图Fig 6 Lineweaver-Burk curve of NPS and CTS

图7 NPS 和CTS 相互作用的双对数曲线图Fig 7 Double logarithmic curve of MET and CTS
3.7 作用力的推测
由不同温度下的结合常数Ka, 通过Arrhenius 方程计算壳聚糖与萘普生相互作用的热力学参数,结果见表2。

表2 壳聚糖与萘普生相互作用的热力学参数Tab 2 Thermodynamic parameter of reaction between NPS and CTS
从表2 中可以看到,NPS 与CTS 相互作用的ΔH <0,ΔS >0。由于ΔS >0 可能是疏水和静电作用力,ΔH <0 且较小时为静电作用力,因此CTS 和NPS 之间的作用力主要为静电作用力。又因为ΔS 对ΔG 的贡献比ΔH 大,所以还含有疏水作用。表明作用力主要是CTS 的-NH3+与NPS 的-COO-以静电力结合,1∶1 作用形成分子量较大的复合物而使NPS 的荧光变弱。同时两者反应的自由能ΔG <0,表明反应在正方向上是自发进行的。
3.8 壳聚糖分子量对相互作用的影响
分别考察了分子量为4、6、8、10、30、50、100、240、296、410 kD 的CTS 与NPS 的相互作用,结果如表3 所示,随着壳聚糖分子量(MW)的逐渐增大,CTS 与NPS 的结合常数线性增大,回归方程Ka=2.165 MW-155.5,相关系数r为0.9900;同时结合仍为1∶1 结合。

表3 不同分子量壳聚糖与萘普生的相互作用Tab 3 Interaction of CTS with different weight and NPS
3.9 壳聚糖脱乙酰度对相互作用的影响
分别比较对脱乙酰度74.4%~88.8%的CTS与NPS 的相互作用,结果见表4。

表4 脱乙酰度对壳聚糖与萘普生相互作用的影响Tab 4 Effect of degree of deacetylation on the interaction of CTS and NPS
如表4 所示,CTS 的脱乙酰度(DD)对结合常数影响非常显著,脱乙酰度与结合常数的回归方程为Ka=7.370×104DD-5.263×106,相关系数为0.9926。结合位点数除了脱乙酰度为82.9%的点其他没有明显改变,仍为1∶1 结合。在脱乙酰度为74.4%的较低的脱乙酰度的情况下,CTS对NPS 产生的荧光猝灭极弱,且随着CTS 浓度的增加没有呈现荧光猝灭增强的规律,说明当CTS的脱乙酰度较低,游离的-NH2数较少时,其与NPS 的作用很弱,导致NPS 的荧光没有明显的被猝灭现象,从也无法准确计算其结合常数和结合位点数;当CTS 的脱乙酰度逐渐增加时,游离的-NH2数逐渐增多,其与NPS 的相互作用增强,荧光猝灭现象明显。由此可见,NPS 与CTS 的相互作用主要是静电作用,CTS 的脱乙酰度对其与NPS 的相互作用影响较大,且CTS-NPS 结合的Ka值与脱乙酰度呈线性相关,相关系数r为0.9926。
4 结论
本文利用荧光光谱法证实NPS 与CTS 可发生相互作用,在pH 5.0、温度298 K 时,两者的结合比例为1∶1,结合常数为8.29×105L·mol-1;其相互作用以静电作用为主。同时进一步发现CTS的分子量和脱乙酰度与其和NPS 的结合常数成正比,且脱乙酰度影响更为显著,表明两者的静电作用通过CTS 的氨基发生;而结合比例基本不受CTS 的分子量和脱乙酰度影响。本研究为CTSNPS 等复合物的制备及CTS 作为药物缓控释材料的研究提供基础。
