LC-MS/MS自身内标法测定人血浆中达比加群浓度
2021-02-16王峰何昕钱懿轶中南大学湘雅二医院药学部长沙400云南省阜外心血管病医院药剂科昆明650000昆明医科大学研究生院昆明650500
王峰,何昕,钱懿轶(. 中南大学湘雅二医院药学部,长沙 400;2. 云南省阜外心血管病医院药剂科,昆明 650000;. 昆明医科大学研究生院,昆明 650500)
达比加群酯是一类新型口服抗凝剂(novel oral anticoagulants,NOACs),属非肽类直接凝血酶抑制剂。因其与传统抗凝药如华法林相比,给药剂量相对固定,治疗过程中无需频繁进行剂量调整和凝血功能监测,用药依从性较高[1-2],所以于2013年在国内上市后广泛用于非瓣膜性房颤成人患者的卒中和全身性栓塞预防[3]。然而,抗凝治疗本身具有长期性、个体差异性和出血高风险性等特点,达比加群酯导致的出血风险也随着该药的逐渐应用而受到广泛关注。美国食品药品监督管理局建议将达比加群血药浓度控制在40 ~200 ng·mL-1[4],提示达比加群血药浓度水平或可作为预测该药疗效和不良反应的有效指标。液相色谱串联质谱法(LC-MS/MS)具有良好的灵敏度和准确性[5],本研究拟建立一种人血浆中达比加群浓度的LC-MS/MS 测定法,并引入一种阀切换技术,以自身为内标,达到快速、准确检测并易于推广的效果,为促进达比加群酯安全合理用药,优化抗凝策略提供科学依据。
1 材料
达比加群对照品(加拿大Toronto Research Chemicals 公司,纯度>98%,批号:1-JYS-153-1);甲醇、乙腈为色谱级(美国Anaqua Chemicals公司);甲酸、氨水为分析纯(国药集团化学试剂有限公司);实验用水为去离子水;空白马血清(北京政博伟业生物科技有限公司,批号:180824)。
LCMS-8050 型三重四级杆质谱仪(日本岛津公司);色谱系统包括LC-30AD 型色谱泵、SIL-30AC 型自动进样器、CBM-20A 型控制器;MSMate 9600 全自动二维液相色谱串联质谱耦合仪(湖南德米特仪器有限公司);Milli-Q plus 纯水仪(美国Millipore 公司)。
2 方法与结果
2.1 色谱条件
色谱柱:Aston SN 苯基柱(2.1 mm×50 mm,5 μm);流动相:甲醇-水(含4 mmol·L-1甲酸、氨水)=33∶67(V/V);流速:0.8 mL·min-1;柱温:45℃;进样量:1 μL;等度洗脱。
每份待测样品自动进样的同时,二维液相色谱串联质谱耦合仪自动抽去设定剂量的样品溶液作为内标储存于耦合仪中,再通过阀切换装置,在进样后0.4 min,将预先储存在耦合仪中的内标溶液(6.24 ng·mL-1)注入色谱柱中分析,进而达到待测物和内标为同一物质,但在不同时间出峰的效果,第一个为目标峰,第二个为自校内标峰。
2.2 质谱条件
采用电喷雾离子化源(ESI)正离子模式检测;多反应监测模式(MRM)扫描;定性分析检测离子对:m/z472.15/172.05,碰撞电压:-25 V;定量分析检测离子对:m/z472.15/289.10,碰撞电压:-20 V;驻留时间:497 ms;脱溶剂气温度:250℃;接口温度:300 ℃;加热块温度:350℃;雾化气(氮气)流速:3 L·min-1;加热气:氮气流速10 L·min-1,空气流速10 L·min-1;碰撞气(氩气)压力:270 kPa;接口电压:4 kV。
2.3 溶液配制与血浆样品处理
2.3.1 溶液配制 精密称取达比加群对照品5.31 mg,用甲醇定容至50 mL,制备104.08 μg·mL-1的达比加群储备液。储备液先用空白马血清制备成5.204 μg·mL-1的达比加群标准溶液,再用空白马血清逐步稀释为5.204、26.02、52.04、104.08、260.2、520.4 ng·mL-1的标准血浆样品和低、中、高3 种浓度(10、100、400 ng·mL-1)的质控样品。另取储备液,用甲醇制备成6.24 ng·mL-1的内标工作液。上述溶液均保存于-20 ℃冰箱。
2.3.2 人血浆/马血清样本处理 精密吸取人血浆/马血清样品200 μL 置于1.5 mL EP 管中,精密加入蛋白沉淀剂(乙腈-甲醇=80∶20,V/V)500 μL,室温下涡旋振荡1 min 后,14 500 r·min-1离心8 min,取500 μL 上层清液转移至进样瓶中待测分析。
2.4 方法学考察
2.4.1 专属性 分别制备空白溶剂、空白马血清、空白人血浆、空白马血清+达比加群对照品(30 ng·mL-1,50 ng·mL-1)、用药患者给药后血浆样本,按“2.3.2”项下方法操作,进样分析。典型色谱图见图1,空白试剂、空白马血清和空白人血浆在待测物和内标峰处无干扰,待测物和内标保留时间分别为1.26 min 和1.81 min,峰形良好。
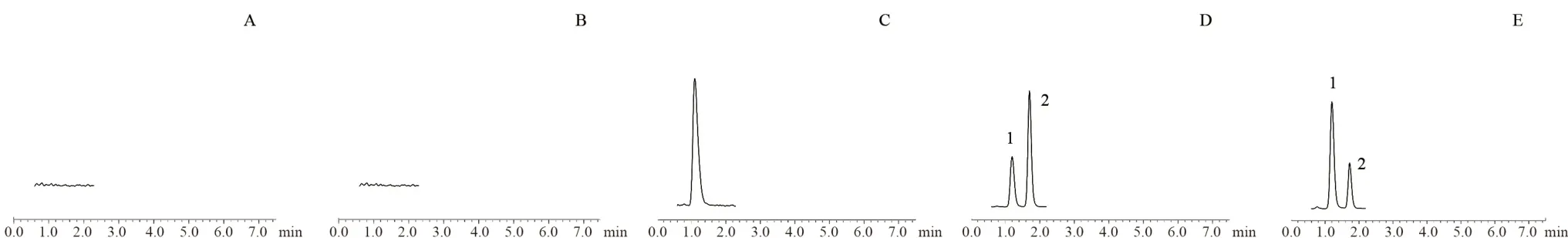
图1 典型色谱图Fig 1 Typical chromatograms
2.4.2 标准曲线与定量下限 按“2.3.1”项下方法配制标准血浆样品,再按“2.3.2”项下方法处理后进行分析,以达比加群待测物质量浓度(ng·mL-1)为横坐标(x)、待测物与内标峰面积比值为纵坐标(y),采用加权最小二乘法进行线性回归,得回归方程为y=0.0092x+0.0358(r=0.9997),表明达比加群在5.204 ~520.4 ng·mL-1与峰面积线性关系良好,定量下限为5.204 ng·mL-1。
2.4.3 精密度与准确度 取“2.3.1”项下高(400 ng·mL-1)、中(100 ng·mL-1)、低(10 ng·mL-1)质量浓度质控样品和5.204 ng·mL-1的标准血浆样品(作为定量下限浓度样品),按“2.3.2”项下方法处理,每个浓度制备5 份样品,连续测定3 d,根据当日标准曲线计算质控样品的测定浓度,计算得质控样品和定量下限浓度样品日内、日间精密度RSD分别为1.4%~2.5%和1.0%~2.9%,准确度分别为92.72%~111.54%和91.75%~113.16%。
2.4.4 提取回收率和基质效应 按“2.3.2”项下方法处理高、中、低浓度质控样品,每个浓度平行测定5 份,测得待测物峰面积为A;另取空白马血清处理后取上清液,加入与高、中、低浓度质控样品相对应的对照品溶液,每个浓度制备5份样品,测得待测物峰面积为B;取同体积超纯水代血浆,按“2.3.1”项下方法配制高、中、低相应浓度的样品,直接进样分析,每个浓度平行测定5 份,测得待测物峰面积为C。按下列公式计算:提取回收率=A/B×100%,基质效应=B/C×100%。结果见表1,表明本测定法提取回收率较高,测定过程无明显基质效应。

表1 提取回收率和基质效应考察结果(n =5)Tab 1 Extraction recovery and matrix effect (n =5)
2.4.5 稳定性 高、中、低浓度质控样品,每个浓度制备5 份样品,分别于不同条件下放置,再按“2.3.2”项下方法处理并分析,每个浓度平行测定5 份,考察不同条件下稳定性。考察条件及结果见表2。

表2 不同条件下达比加群的稳定性考察结果(n =5)Tab 2 Stability of dabigatran under various conditions (n =5)
2.5 方法学应用
将本测定法应用于20 例(男11 例,女9例)平均年龄(66.05±9.32)岁、服用达比加群酯胶囊患者的血药浓度测定。所有患者以“110 mg q12 h”方案用药,在末次给药后10 ~14 h 空腹采血并立即分离血浆,按“2.3.2”项下方法处理并分析。测得20 例患者达比加群血药浓度为25.1 ~257.0 ng·mL-1,平均值为(92.60±49.90)ng·mL-1。具体结果见表3。

表3 达比加群血药浓度监测结果及临床应用Tab 3 Blood drug concentration monitoring and clinical practice of dabigatran
3 讨论
3.1 方法先进性
内标法是LC-MS/MS 对生物样本进行定量分析时常采用的方法[6],通过引入内标校正样品预处理造成的损失、进样体积差异、基质效应对离子化过程的影响等因素造成的误差。按照理想内标应与待测物具备相似物理化学性质这一原则,内标可分为同位素内标、待测物的结构类似物以及与待测物质谱行为相近的物质[7]。其中,同位素内标与待测物在色谱保留、质谱裂解等方面几乎一致,因而应用最为广泛,已发表的LC-MS/MS 测定法,以达比加群-d3和[13C]-达比加群为内标者居多[8-11]。但同位素内标往往价格高昂、获取难度大,测定成本较高,不利于实现常规化监测。本研究参考“多维”概念,借助二维液相色谱串联质谱耦合仪,引入阀切换技术,首次建立了一种以待测物达比加群自身为内标的人血浆中达比加群浓度LC-MS/MS 测定法,以固定浓度的达比加群标准溶液为内标,实现待测样品和内标的“二维”进样和“一维”色谱分离。同时本法采用等度洗脱,简化了色谱条件,待测物和内标保留时间分别为1.26 min 和1.81 min,每份样品从样品进样、内标进样和分析时长仅为2.4 min,与文献方法相比缩短了分析时间,提升了分析效率,较好地实现了经济、快速、高效测定的目的,有利于临床常规化开展达比加群血药浓度监测的推广。
3.2 达比加群血药浓度监测的临床意义探索
从本研究选取的20 例服用达比加群酯的患者血药浓度数据分析,以110 mg q12 h 方案服用达比加群酯的患者,用药6 次后,血药浓度变异较大,且临床观察到的凝血指标异常升高不良事件有可能与高血药浓度有关,从患者的既往出血/栓塞不良事件史考虑,相同用法用量达比加群用于不同患者,或者同一患者不同时期以相同用法用量达比加群酯治疗,均有可能存在疗效和安全性的差异,提示患者在后续用药过程中,有必要进行达比加群血药浓度监测。虽然目前国内外文献报到了一些达比加群血药浓度的监测方法[12-14],但对临床应用价值尚无探索。RE-LY 研究[15]数据提示达比加群酯活性代谢物浓度存在较大个体差异与CES1和ABCB1基因多态性相关,提示达比加群血药浓度监测对进一步揭示药效学差异,促进临床合理用药具有重要的意义,且该方法有希望成为一个相较于肌酐清除率和凝血检查指标如部分凝血活酶时间(APTT)、蛇毒凝血时间(ECT)、稀释凝血时间(dTT)、凝血酶时间(TT)和稀释的蝰蛇毒时间(dRVVT)等指标更精准、快速和经济的监测方法[16]。随着达比加群酯的特异性拮抗剂idarucizumab 获批上市[17],除了为达比加群酯用药安全性和药效提供评估依据之外,达比加群血药浓度还有可能为特异性拮抗剂的个体化用药提供指引,同时随着我国药品一致性评价政策[18]的推进,达比加群血药浓度监测也有助于同类国产新药的研发。
4 结论
本研究首次以达比加群自身为内标,以LCMS/MS 方法测定达比加群血药浓度并初步应用于临床,方法新颖,样品处理简单,分析过程快速、高效,测定结果准确,适用于达比加群血药浓度的测定。该方法的初步临床应用结果显示,有较好的临床应用前景并更好地促进达比加群酯的个体化用药。
