磁微粒吖啶酯化学发光法检测AMH的性能评估及成年女性AMH参考区间的建立
2021-02-05岳朝艳段朝晖罗晓红张倩岚应春妹
岳朝艳,段朝晖,章 迪,韦 婕,罗晓红,张倩岚,伍 勇,应春妹
(1.复旦大学附属妇产科医院,上海 200011;2.中山大学孙逸仙纪念医院,广东 广州 510120;3.中南大学湘雅三医院,湖南 长沙 410205 )
抗苗勒管激素(anti-mullerian hormone,AMH)是转化生长因子β超家族的一员,由2个相对分子质量为72 000的二聚体单体组成,通过二硫键连接。女性AMH由卵泡颗粒细胞合成,是调节卵泡成熟的关键激素。AMH反映了卵巢窦状卵泡和窦前卵泡的数量,也有助于评估卵巢功能[1]。目前,检测AMH的方法主要为酶联免疫吸附试验和化学发光法。酶联免疫吸附试验结果易受多种因素影响[2-4],随着检测需求的增多,自动化免疫学方法可能更适用临床。本研究依据美国临床实验室标准化协会(the Clinical and Laboratory Standards Institute,CLSI)发布的EP系列文件对国产磁微粒吖啶酯化学发光法检测AMH的性能进行验证和评估,并建立我国成年女性AMH的参考区间。
1 材料和方法
1.1 研究对象
选取2018年1—12月女性健康体检者1 089名,其中349名来自复旦大学附属妇产科医院、464名来自中南大学湘雅三医院、276名来自中山大学孙逸仙纪念医院。180例用于相关性分析的样本包括104名健康女性、21例卵巢早衰患者、55例多囊卵巢综合征患者。健康女性来自复旦大学附属妇产科医院体检中心,卵巢早衰和多囊卵巢综合征均为复旦大学附属妇产科医院生殖内分泌门诊确诊患者。健康女性纳入标准:女性;年龄20~60岁;无自身免疫性疾病或炎症性疾病;近3个月内无激素治疗史,如雌激素、孕激素或口服避孕药物;无卵巢切除手术史;无多囊卵巢综合征;体质量指数(body mass index,BMI)<26.9 kg/m2。
1.2 方法
1.2.1 仪器和试剂 iFlash 3000化学发光免疫分析仪(深圳市亚辉龙生物科技股份有限公司)及配套AMH试剂(磁微粒吖啶酯化学发光法)。cobas e601全自动电化学发光免疫分析仪及配套AMH试剂(电化学发光法)。
1.2.2 样本采集 采用分离胶/促凝剂采血管采集所有对象静脉血5 mL,静置30 min,1 000×g离心15 min。所有样本均在采集后2 h内处理完毕,-80 ℃保存,统一检测。所有样本均仅解冻1次。
1.2.3 性能评估 性能评价项目包括空白限、检测限、定量限、精密度(重复性、批间精密度和总不精密度)及与电化学发光法的比对。所有性能评估实验均在复旦大学附属妇产科医院检验科完成。空白限、检测限和定量限根据CLSI EP17-A2文件[5]的要求确定。精密度根据CLSI EP5-A3文件[6]的要求确定。在CLSI EP6-A文件[7]要求的基础上,采用多项回归分析进行线性范围验证,线性验证实验结果为一阶方程式判定为线性,检测样本的最低值和最高值之间为线性区间。
1.2.4 方法学比对和偏移评估 以电化学发光法为参比方法,磁微粒吖啶酯化学发光法为实验方法。采用2种方法同时检测104名健康女性、21例卵巢早衰患者、55例多囊卵巢综合征患者的血清AMH水平。2种方法的相关性采用线性回归方程Y=bX+a评估。偏移评估:将给定的医学决定水平(Xc)代入线性回归方程,计算实验方法(Y)与参比方法(X)之间的系统误差(systematic error,SE)和相对偏移(SE%),SE=Yc-Xc,SE%=SE/Xc×100%。方法学评估的SE%低于室间质量评价允许误差范围,则认为不同检测系统间的测定结果具有可比性。
1.2.5 不同样本类型的比较 分别采用不同的采血管[无抗凝剂真空管、分离胶促凝剂管、肝素锂抗凝管、柠檬酸钠抗凝管、乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA)抗凝管]采集11名健康体检者全血,进行配对比较,计算不同抗凝管样本与无抗凝剂真空管样本之间的Passing-Bablok回归方程及平均偏差。试验均在复旦大学附属妇产科医院检验科完成。
1.2.6 血清样本在不同保存时间和保存温度下的稳定性 收集11名健康体检者的血清样本,立即采用磁微粒吖啶酯化学发光法检测AMH,以此作为基线水平,AMH范围为0.68~18.48 ng/mL。然后将每份血清等分为17份,分别保存于室温(20~25℃)、4 ℃、-20 ℃和-80 ℃,每天检测1份样本,共检测7 d。计算不同时间、不同保存温度的样本的检测结果与基线水平的平均百分差值。试验均在复旦大学附属妇产科医院检验科完成。
1.2.7 磁微粒吖啶酯化学发光法成年女性AMH参考区间的建立 将1 089名健康体检女性按年龄分组(20~24岁、25~29岁、30~34岁、35~39岁、40~44岁、45~49岁和≥50岁),采用磁微粒吖啶酯化学发光法检测血清AMH水平。检测分别在复旦大学附属妇产科医院检验科、中南大学湘雅三医院检验科和中山大学孙逸仙纪念医院检验科完成,检测系统校准合格,室内质控在控。选择AMH检测结果的第2.5百分位数(P2.5)~第97.5百分位数(P97.5)作为参考区间。
1.3 统计学方法
采用GraphPad Prism 5.0软件和MedCalc 11.4软件进行统计分析。呈正态分布的数据以±s表示,2个组之间比较采用独立样本t检验,多组间比较采用方差分析。呈非正态分布的数据以中位数(M)[四分位数(P25~P75)]表示,组间比较采用非参数Mann-WhitneyU检验,Z值<Z*值表示不需分组。以P<0.05为差异有统计学意义。
2 结果
2.1 磁微粒吖啶酯化学发光法检测性能的验证
磁微粒吖啶酯化学发光法检测AMH的空白限为0.001 ng/mL,检出限为0.02 ng/mL,定量限为0.08 ng/mL。低值样本的重复性为1.3%、批间精密度为2.2%、总不精密度为3.2%。高值样本的重复性为1.6%、批间精密度为2.1%、总不精密度为3.1%、线性范围为0.02~27.22 ng/mL。2种方法的检测性能见表1。

表1 磁微粒吖啶酯化学发光法和电化学发光法检测AMH的性能
2.2 磁微粒吖啶酯化学发光法与电化学发光法的相关性
磁微粒吖啶酯化学发光法与电化学发光法的线性回归方程为Y=0.998 8X+0.179 5(r=0.975 3,P<0.05),2种方法的相关性良好。
2.3 磁微粒吖啶酯化学发光法与电化学发光法检测AMH的偏移评估
以电化学发光法为参比方法,磁微粒吖啶酯化学发光法检测AMH低值(1 ng/mL)的相对偏移为17.8%,绝对偏差为0.178 3 ng/mL,可满足临床需求。其他浓度的相对偏移和绝对偏差均在允许范围内。2种方法的一致性较好。见表2。

表2 磁微粒吖啶酯化学发光法与电化学发光法检测AMH的偏移评估
2.4 不同抗凝管样本与无促凝剂真空管样本的比较
不同抗凝管样本与无促凝剂真空管样本比较,检测结果均呈线性相关。因此,血清和血浆均可作为磁微粒吖啶酯化学发光法检测AMH的样本。见表3。

表3 不同抗凝管样本与无促凝剂真空管样本的比较
2.5 不同保存时间和保存温度的稳定性比较
血清样本在室温(20~25 ℃)条件下可稳定3 d,在4、-20、-80 ℃条件下可稳定7 d,见图1。

图1 AMH检测的稳定性
2.6 成年女性AMH参考区间及变化趋势
成年女性AMH参考区间的建立基于多中心研究,本研究覆盖了3个不同的地区,结果显示,3个地区AMH水平差异均无统计学意义。见表4。
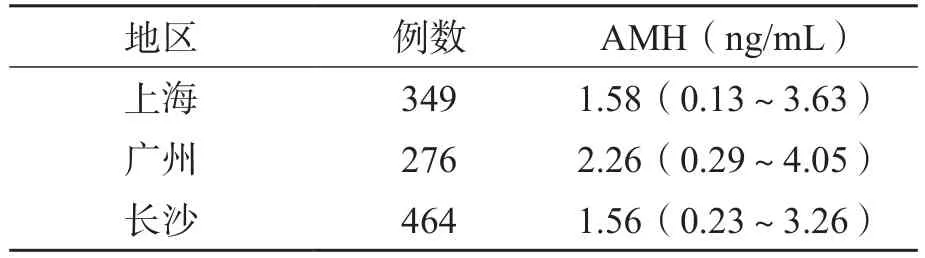
表4 各地区AMH水平比较 M(P25~P75)
按年龄分组后显示,50岁以上的妇女AMH水平很低,因此归为1个年龄组。以检测结果的P2.5~P97.5作为参考范围。20~24岁、25~29岁、30~34岁、35~39岁、40~44岁、45~49岁和≥50岁的成年女性的AMH参考区间分别为1.20~10.21、1.14~9.17、0.55~8.18、0.25~7.02、0.07~4.59、0.01~2.11、<0.39 ng/mL,见表5。回归模型显示血清AMH水平随年龄的增长而下降,见图2。
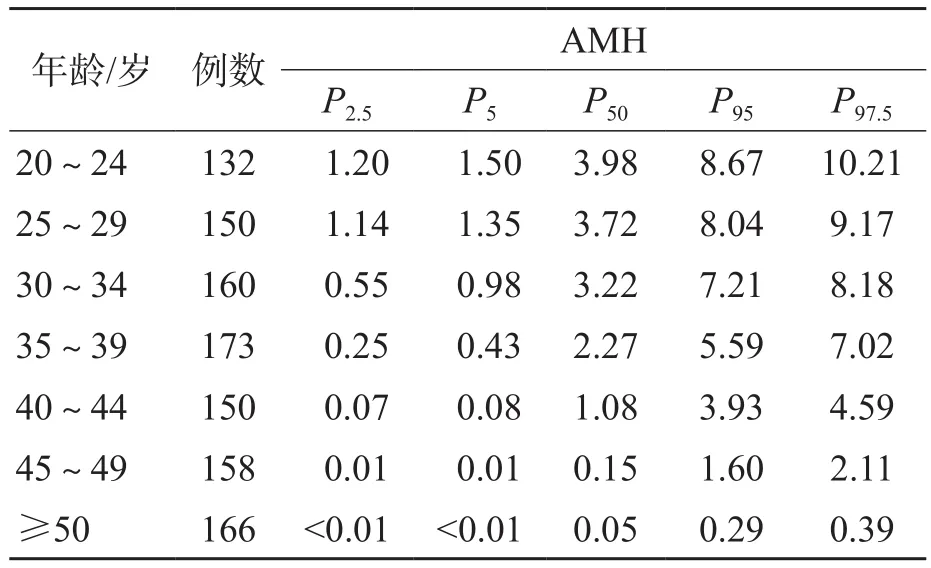
表5 成年女性血清AMH的参考区间 ng/mL
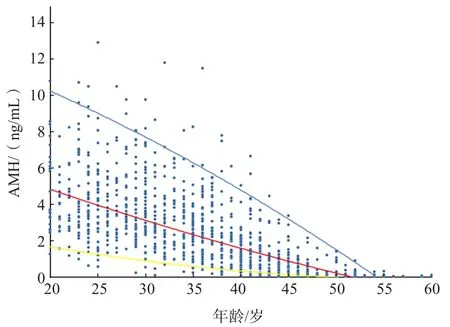
图2 AMH随年龄变化的趋势
3 讨论
血清AMH水平可以准确反映窦状卵泡的储备,是评估卵巢储备功能的可靠指标。AMH与经阴道超声评估的窦状卵泡数有强相关性,AMH和窦状卵泡数与存在于卵巢组织中的原始卵泡数量之间也有良好的相关性[8-9]。AMH水平能够反映卵细胞以及卵泡池随着年龄增加不断下降的趋势,因此可用于判断卵巢老化程度及更年期预测[10-11]。在卵巢储备功能降低、早发性卵巢功能不全和卵巢早衰出现症状之前,AMH是目前最早、最准确的血清学诊断指标之一[12]。AMH在卵巢功能不全时显著降低,提示卵泡池过早耗尽。AMH除了预测生殖寿命之外,还可用于优化生育治疗,在进行体外受精联合胚胎移植术时可用AMH来预测结果,其中最重要的是预测卵巢反应情况,有助于判定卵巢超刺激的个体化方案。AMH还有助于评估早期诊断卵巢功能失调,特别是多囊卵巢综合征,为临床决策提供合理参考。虽然AMH在临床上应用广泛,但目前国内尚无统一的血清AMH参考区间。根据ISO15189:2003(E)标准的要求,实验室必须为临床提供本地区检验项目可靠的参考区间,以便为临床上区分健康与患病、诊断、预防及治疗提供高质量的保证。
本研究使用的AMH检测试剂(磁微粒吖啶酯化学发光法)使用了2个小鼠单克隆抗体,分别针对AMH分子上的pro-和mature-区域。样本中的AMH、抗AMH包覆的顺磁性微粒与吖啶标记的抗AMH共轭反应形成“三明治”复合物,同时检测AMH的非共价复合物形式和未切割的pro-AMH;该方法使用的抗体只特异性地与人源性的AMH结合,避免了其他种属的干扰,可以有效提高检测的敏感性和特异性[13-14]。
准确的AMH参考区间是其临床应用的必要条件。美国贝克曼库尔特公司和瑞士罗氏公司的AMH检测系统可以溯源至AMH GEN Ⅱ酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)。虽然美国贝克曼库尔特公司的化学发光法与瑞士罗氏公司的电化学发光法具有可比性,但这2种方法的检测结果与ELISA的检测结果有一定差异。美国贝克曼库尔特公司新的化学发光法使用了与AMH GEN ⅡELISA方法类似的校正材料,其AMH检测结果仍比AMH GEN Ⅱ ELISA平均低22%[15]。然而,DEMIRDJIAN等[11]的研究结果显示,美国贝克曼库尔特公司的化学发光法AMH检测结果与AMH GEN Ⅱ ELISA具有可比性[16]。这些互相矛盾的结论可能是由于ELISA的准确性和重复性较低所致。虽然AMH GEN Ⅱ ELISA已被广泛应用,但使用相同单克隆抗体的试剂盒相对不稳定。为此,美国贝克曼库尔特公司发布了一份“现场安全通知”(FSN-20434-3),内容涉及在将样本添加到反应板之前与稀释液预混合,该程序可消除补体干扰。
血液中AMH由pro-AMH和AMHNC 2个部分组成,前者为非活性的未裂解前体,后者为酶裂解、受体活性形式。AMH GEN Ⅱ ELISA可同时检测出重组pro-AMH和AMHNC[16]。瑞士罗氏公司和美国贝克曼库尔特公司的AMH检测抗体使用了2种小鼠单克隆抗体,第1种是生物素标记的AMH特异性小鼠单克隆抗体(Mab F2B/12H;IgG2a亚类),第2种是磺基钌标记的AMH小鼠检测单克隆抗体(Mab F2B/7A;IgG2b亚类)。这2种单克隆抗体都来自美国贝克曼库尔特公司。抗体优先与AMH mature-区域(Mab F2B/12H)和AMH pro-区域(Mab F2B/7A)结合[16-18]。AMH标准品的缺乏是导致AMH检测结果出现差异的重要因素,因此目前迫切需要对AMH标准品达成一致,以便对AMH的检测系统进行校准,避免检测报告与结果解释的混乱。美国贝克曼库尔特公司的化学发光法和瑞士罗氏公司的电化学发光法AMH检测结果可以溯源至AMH GEN Ⅱ ELISA。本研究使用的磁微粒吖啶酯化学发光法可溯源至罗氏的化学发光法Elecsys AMH[19]。
综上所述,磁微粒吖啶酯化学发光法检测AMH的性能参数(空白限、检出限、定量限、精密度、线性范围)均符合验证要求,与电化学发光法有较高的相关性,且血清样本在不同储存时间和不同贮藏温度下检测AMH均有较好的稳定性,可提供可靠的检验结果。另外,本研究还初步建立了成年女性AMH的参考区间,可为临床正确解释AMH水平提供更可靠的参考,为AMH项目在临床上的广泛开展提供科学依据。
