氨氮降解菌的筛选及降解氨氮条件研究*
2020-11-15蔡尽忠张慧美邱彩玲范淑捷
蔡尽忠,张慧美,邱彩玲,范淑捷,邓 盈
(1 厦门华厦学院 环境与公共健康学院,福建 厦门 361024;
近年来,随着城市化和工农业生产的发展,大量富含氮、磷等营养物质的城市污水、工农业废水流入自然水域,进而导致水体的富营养化[1]。同时因富营养化水中含有硝酸盐和亚硝酸盐,人畜长期饮用这些物质含量超过一定标准的水,也会中毒致病[2-3]。随着水环境污染和水质富营养问题的日益尖锐以及公共环境意识的日益增强,污水脱氮问题在全球范围内引起了广泛的重视。因此采取一定措施降低水中的氨氮含量对于城镇居民生活环境的治理有着重要作用。处理氨氮的方法一般有物理、化学、生物等处理方法。鲁秀国等[4]使用解氨剂-超重力法处理氨氮废水,探索了处理脱氮过程的最佳工艺条件,论证了解氨剂-超重力法处理氨氮废水技术上的可行性。在化学沉淀法处理氨氮废水方面,华南理工大学、兰州化学工业公司环保所等进行了较系统研究,处理后的废水氨氮含量小于1×10-6,沉淀物可以作为复合肥回收利用。生物降解法中常用的添加剂是微生态制剂,由于它安全高效、绿色环保,不仅仅能改善水体环境,还可以减少动物因饮用此类富营养化水体而造成疾病的发生。由于生物降解方法成本低、运作简单、不会造成二次污染、安全环保等特点,备受大众的青睐与推崇[5]。本研究从厦门华厦学院天鹅湖底泥中,分离筛选出能降解氨氮的菌株,研究菌株降解氨氮的最适条件,为水体氨氮污染的生物降解提供应用基础。
1 实 验
1.1 实验材料
1.1.1 培养基
富集培养基(g): 葡萄糖 5.0,NaCl 2.0,(NH4)2SO42.0,K2HPO41.0,FeSO4·7H2O 0.4,MgSO4·7H2O 0.5,水1000 mL。
分离培养基(g): 葡萄糖 5.0,NaCl 2.0,(NH4)2SO42.0,K2HPO41.0,FeSO4·7H2O 0.4,MgSO4·7H2O 0.5,琼脂粉15.0,水1000 mL。
1.1.2 仪 器
7230可见分光光度计,厦门星鲨;CT15RT多用途冷冻离心机,厦门莱胜;PHX-280H生化培养箱,宁波莱福;SHZ-82A气浴恒温震荡器,常州华普达。
1.2 实验方法
1.2.1 氨氮降解菌的富集
取1 g厦门华厦学院天鹅养殖处天鹅湖中的水底污泥加入9 mL无菌水制成悬液,接种至100 mL富集培养基中,在转速为120 r·min-1,温度为30 ℃的摇床中培养7 d,这期间每天向培养基中加入1 mL5%的(NH4)2SO4溶液,用于富集可以利用氨氮的微生物。
1.2.2 降解氨氮菌的分离纯化及降解氨氮效率检测
将富集培养后的菌液稀释至合适的浓度后在分离培养基中涂布,放置于30℃的生化培养箱中倒置培养至长出菌落后,用连续划线法接种到分离培养基中,反复分离纯化至同一平皿只出现同种形态的菌落。将筛选分离后的各菌株分别接种到含有氨氮含量为120 mg·L-1的液体筛选培养基(模拟高浓度氨氮水样),在温度为30 ℃、转速为120 r·min-1摇瓶培养24 h后取培养液放置于离心机中以3000 r·min-1离心10 min,取其上清液,采用纳氏试剂分光光度法[6]测氨氮含量,计算出各个降解菌的氨氮降解率。选出一株降解能力最强的氨氮降解菌株作进一步研究。

1.2.3 培养时间对氨氮降解能力的影响
将筛选出的最优菌种在转速120 r·min-1,温度30 ℃的摇床中培养24 h。每隔2~4 h对培养基进行一次氨氮含量的检测,研究降解氨氮的最佳培养时间。
单一语种词典可以给学习者提供更为准确的释义,其中包括翻译无法完美而彻底地传达的含义,但是由于没有学习者的母语,它不太适合初学者。双语词典可以给初学者提供一目了然的解释,但是词语的释义囿于目的语的缘故,很多词的文化内涵不能完美阐释。
1.2.4 培养条件对氨氮降解能力的影响
将最优菌株接种到20 mL筛选培养基中,分别在不同温度(26.0、28.0、30.0、33.0、35.0、37.0 ℃),不同初始 pH值(5.0、6.0、7.0、8.0、9.0、10.0),不同摇床转速(90、120、150、180、200 r·min-1) 的条件下,培养1.2.3确定的时间后测定氨氮降解率,确定最佳氨氮降解条件。在最佳氨氮降解条件下测定其对模拟高浓度氨氮水样和厦门华厦学院天鹅湖实际水样的氨氮降解率。
1.2.5 数据分析
采用Microsoft Excel 2010和SPSS18.0进行数据处理和分析,均值差异性分析采用LSD法,显著性水平为P< 0.05。
2 结果与讨论
2.1 氨氮降解菌的分离与筛选结果
天鹅湖水底污泥经富集、分离、纯化,获得7株氨氮降解菌,编号分别为TEH-03、TEH-04、TEH-05、TEH-06、TEH-08、TEH-12、TEH-13。这7株菌对氨氮的降解率如图1所示,TEH-03菌株对氨氮的降解率显著高于其它菌株(P<0.05),因此对该菌株作进一步研究。

图1 7株氨氮降解菌的氨氮降解率
2.2 最优菌TEH-03的氨氮降解能力的初步测定
通过图2的TEH-03菌株对氨氮的降解率曲线,可以发现该菌从14h以前对氨氮的降解率快速升高,14 h以后对氨氮的降解率差异不显著(P>0.05),确定降解氨氮的最佳培养时间为14 h。
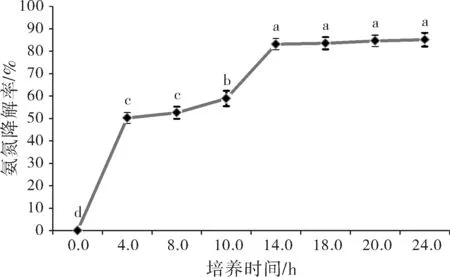
图2 培养时间对最优菌TEH-03氨氮降解能力的影响
2.3 温度对氨氮降解能力的影响
从图3可知氨氮降解能力随温度变化出现先缓慢升高后快速降低的趋势,这可能是菌株TEH-03会产生大量的活性酶,温度升高有利于提高微生物酶活性,但过高的温度会使酶活性降低甚至失活。在温度为30 ℃时对氨氮的降解率最高,但是26、28和30 ℃条件下对氨氮的降解率差异不显著(P>0.05),考虑到节约能源,将最适培养温度确定为26 ℃。
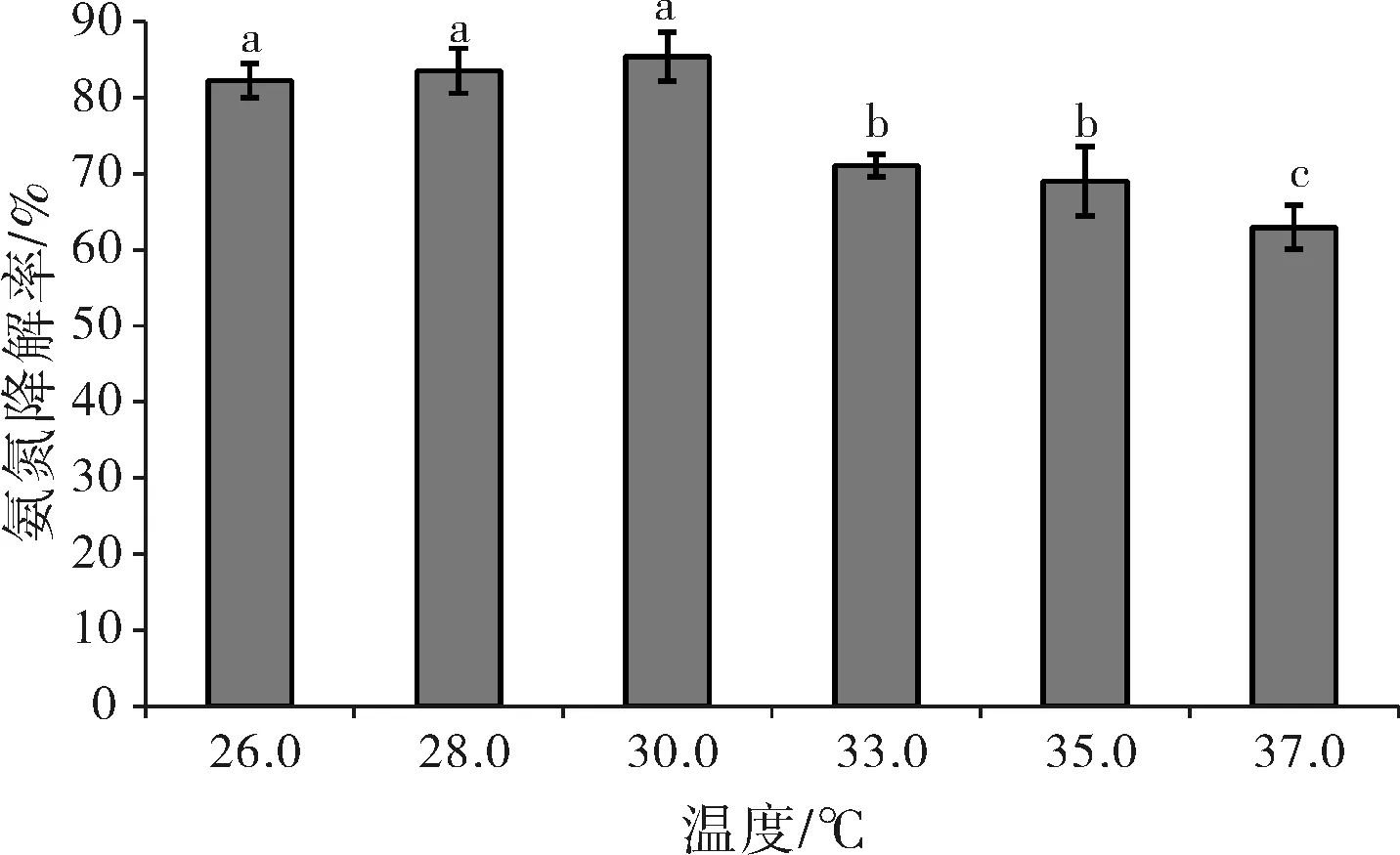
图3 温度对氨氮降解能力的影响
2.4 初始pH 值对氨氮降解能力的影响
从图4可知菌株对氨氮的降解率随pH值变化出现快速升高后又快速降低的趋势,当外界环境中的氢离子浓度高于或低于微生物酶的适应范围,不仅会抑制酶的活性还会降低酶促反应效率,并且微生物对营养物质的吸收也会变弱,代谢功能也会受到影响。当pH值为7.0时菌株TEH-03对氨氮的降解率显著高于其它pH条件(P<0.05),因此初始pH值应控制在7.0最佳。
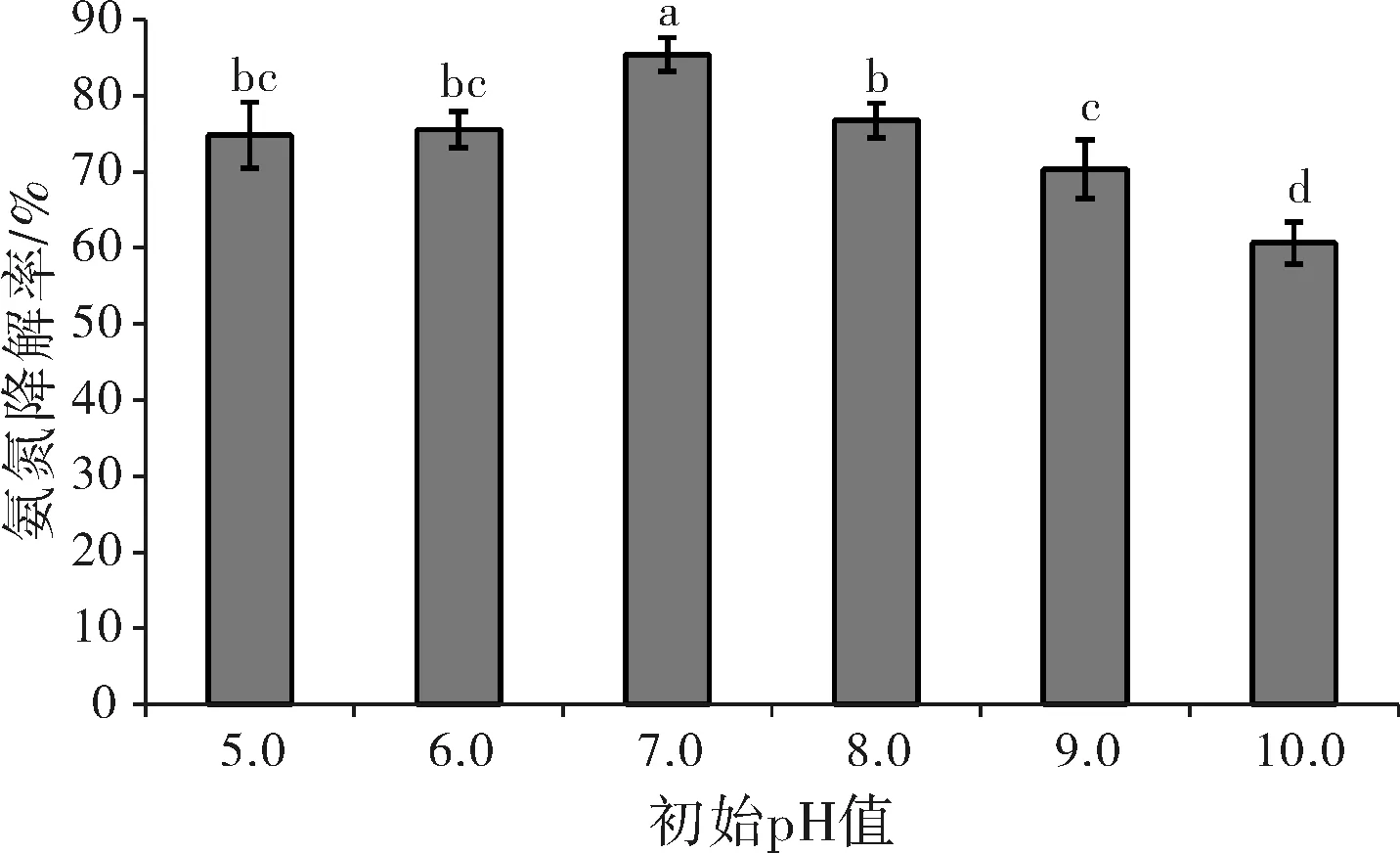
图4 初始pH值对氨氮降解能力的影响
2.5 转速对氨氮降解能力的影响
由图5可以看出随着转速的增加,菌株对氨氮的降解率出现快速升高后又快速降低的趋势,过高或者过低的氧气量都不利于菌株TEH-03降解氨氮。当转速达到120 r·min-1时对氨氮的降解效率显著高于其它转速 (P<0.05),因此最佳转速为120 r·min-1。
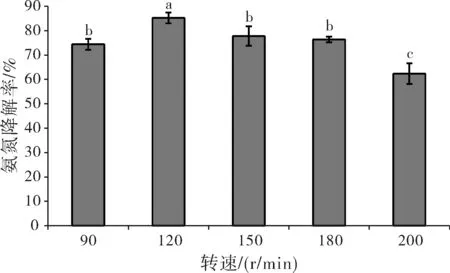
图5 转速对氨氮降解能力的影响
2.6 最适培养条件下对模拟水样和实际水样的氨氮降解率
将TEH-03菌株在最适培养条件即温度为26 ℃、pH为7.0、转速为120 r·min-1下培养14小时后测定其对模拟高浓度氨氮水样的降解率为86.83%,但是对厦门华厦学院天鹅养殖处天鹅湖实际水样的氨氮降解率仅为77.78%,其原因可能是由于模拟水样中的氨氮含量较高,菌株可以高效的发挥其降解效果,而天鹅湖水样中可能含有其它有毒物质对菌株产生抑制作用,从而降低菌株在实际水样中的适应性,使得对氨氮降解效果不如模拟水样。
3 结 论
本实验通过对厦门华厦学院天鹅湖中的污泥微生物分离纯化,以硫酸铵为唯一氮源筛选得到1株对氨氮具有较好降解作用的菌株TEH-03。研究结果表明TEH-03菌株的最适降解条件为温度26 ℃,初始pH值为7.0,转速为120 r·min-1,该菌在14 h 就可达到最佳的对氨氮降解率达到86.83%。以天鹅湖的污水作为实际水样,菌株TEH-03对实际水样中氨氮降解率为77.78%,该菌株是对自然水体的治理有一定效果的,但如果用于改善城市、工业污水还得进一步优化条件提高该菌株对氨氮降解的效率。
