生物法合成α-酮戊二酸及其衍生物的研究进展
2020-05-12朱福周董解荣张成林
朱福周,董解荣,陈 宁,张成林,2*
(1.天津科技大学 生物工程学院,天津 300457;2.菱花集团有限公司,山东 济宁 272073)
α-酮戊二酸(α-ketoglutarate,α-KG)是三羧酸循环的重要中间产物之一,参与生物体内氨基酸、维生素和有机酸的合成及能量代谢[1-2]。α-酮戊二酸经转氨基作用形成L-谷氨酸进入氮代谢中,是连接细胞内碳代谢和氮代谢的关键节点[1]。常见的α-酮戊二酸衍生物包括γ-氨基丁酸(γ-aminobutyric acid,GABA)、5-氨基乙酰丙酸(5-aminolevulinic acid,5-ALA)以及由α-酮戊二酸依赖的羟化酶催化生成的羟化物如4-羟基异亮氨酸(4-hydroxyisoleucine,4-HIL)等。迄今为止,α-酮戊二酸及其衍生物已被广泛应用于化工、食品、医药、日化等诸多领域[3-6],具有非常广泛的应用前景。
工业化生产α-酮戊二酸、γ-氨基丁酸及5-氨基乙酰丙酸主要采用化学合成法,4-羟基异亮氨酸主要采用是提取法。然而,上述工艺多存在生产工艺复杂、分离困难收率低、易引起环境污染等不足,限制其大规模生产和应用[2,7-9]。相比而言,生物合成法具备成本低、效率高、环境友好等优势。但总体而言,生物法合成α-酮戊二酸及其衍生物尚处于起步阶段。基于此,本文从α-酮戊二酸及其衍生物的应用、生物合成途径及其代谢调控、生物法合成策略等方面进行了综述,以期为其生产菌株的代谢工程构建和工艺开发提供借鉴。
1 α-酮戊二酸的应用
1.1 α-酮戊二酸在医药领域中的应用
α-酮戊二酸作为合成多种药物的重要前体物质被广泛应用于医药领域。α-酮戊二酸可与5-羟甲基糠醛合成抗氧化剂,具有提高抗氧压的功能[10];能与丙三醇、1,2,4-丁三醇或1,2,6-己三醇通过聚合反应生成三醇-α-酮戊二酸聚合物,从而增强其机械性能和化学特性,广泛应用于组织工程学和药物传递等领域[11]。此外,α-酮戊二酸还具有缓解尿毒症、有效促进术后伤口愈合、治疗营养不良以及控制血脂水平等功能[6,12]。
1.2 α-酮戊二酸在食品领域中的应用
α-酮戊二酸作为运动类饮料的营养成分可用于提供能量,其被吸收后与运动员体内过多的氨结合以防止氨中毒,同时还用作饮料中的抗菌剂。α-酮戊二酸还可与精氨酸结合形成精酮合剂,具有补充能量、抗疲劳、提高其训练时表现的功能[13]。此外,α-酮戊二酸盐还具有增强奶酪和腊肠等发酵食品风味的功能,被广泛应用于食品工业中[5]。
1.3 α-酮戊二酸在畜牧业和农业中的应用
α-酮戊二酸具有促进牲畜生长、增加骨骼密度、增强免疫功能、提高抗应激能力以及提高繁殖率等功能,因此作为营养强化剂应用于动物饲料中[14]。α-酮戊二酸是植物氨同化必需的碳架及信号分子,广泛参与碳和氮代谢及其调节。在农业中,α-酮戊二酸常用于增强农作物抗干旱性能[15]。
除用于上述领域外,α-酮戊二酸还可用作化妆品的主要成分,具有清除自由基、缓解褐斑等功效。
2 α-酮戊二酸的合成方法
目前α-酮戊二酸的合成方法主要包括化学合成法、酶法和微生物发酵法。但工业上主要采用化学合成法,该方法是以琥珀丁二酸二乙酯、草酸二乙酯等为原料,经缩合、水解、蒸馏浓缩、结晶等工艺合成α-酮戊二酸,收率最高为75%[16-17]。该技术在多步复杂的合成反应过程中会产生大量副产物,其中包括氰化物等剧毒品、重金属污染物以及易爆物等,不仅加大了分离难度、降低了生产率,同时也增加了生产的危险性[16-17]。
早期酶催化法生产α-酮戊二酸是利用谷氨酸脱氢酶(glutamate dehydrogenase,GDH)以谷氨酸为底物合成,但由于谷氨酸脱氢酶对α-酮戊二酸的亲和力高于谷氨酸且该反应需要辅酶烟酰胺腺嘌呤二核苷磷酸(nicotinamide adenine dinucleotide phosphate,NADP+),因此未被工业化应用[18]。近年来,有研究者利用L-谷氨酸氧化酶(L-glutamate oxidase,GLOD)以谷氨酸为底物合成α-酮戊二酸[19],但该方法在反应过程中产生的过氧化氢严重抑制酶活性[20]。尽管添加过氧化氢酶(catalase,CAT)可消除过氧化氢,但因生产工艺复杂化并增加生产成本未被工业化应用[20]。
与化学合成法、酶催化法相比,微生物发酵法具有成本低、收率高、污染轻及副产物少等优点,具有很大的工业化生产的潜力[21]。目前已发现荧光假单胞菌(Pseudomonas fluorescens)、铜绿假单胞菌(P.aeruginosa)、粘质沙雷氏菌(Serratia marcescenss)、石蜡节杆菌(Arthrobacter paraffineus)、谷氨酸棒杆菌(Corynebacterium glutamicum)、解脂亚洛酵母(Yarrowia lipoytica)及光滑球拟酵母(Torulopsis glabrata)等多种微生物能够过量合成α-酮戊二酸,其中谷氨酸棒杆菌、解脂亚洛酵母及光滑球拟酵母生产性能最好。解脂亚洛酵母发酵生产α-酮戊二酸具有发酵周期长、产酸速率低、副产物过高等不足,限制了其工业化应用[17]。谷氨酸棒杆菌因具有安全稳定及遗传背景清晰的特性被广泛用于氨基酸、有机酸及核苷的发酵生产。谷氨酸棒杆菌因三羧酸循环(tricarboxylic acid cycle,TCA)中柠檬酸至α-酮戊二酸代谢流较强的性能[2]。尽管利用该菌株合成α-酮戊二酸的发酵周期大幅度缩短,但其生产效率还需进一步提高。
3 α-酮戊二酸的生物合成途径及其代谢调控
3.1 α-酮戊二酸的生物合成途径
α-酮戊二酸是微生物三羧酸循环中的中间代谢产物,葡萄糖进入细胞后经糖酵解途径生成丙酮酸,其在丙酮酸脱氢酶复合体(pyruvate dehydrogenase complex,PDHC)的作用下形成乙酰辅酶A。后者与草酰乙酸依次在柠檬酸合酶(citrate synthase,CS)、顺乌头酸酶(cis-aconitase,ACO)、异柠檬酸脱氢酶(isocitrate dehydrogenase,IDH)的作用下生成α-酮戊二酸。α-酮戊二酸可在α-酮戊二酸脱氢酶复合体(α-ketoglutarate dehydrogenase complex,OGDC)的作用下生成琥珀酰辅酶A以完成三羧酸循环[22];亦可在谷氨酸脱氢酶的作用下生成谷氨酸[23];此外还可与谷氨酰胺经谷氨酸合酶(glutamate synthase,GOGAT)催化生成谷氨酸(见图1)。
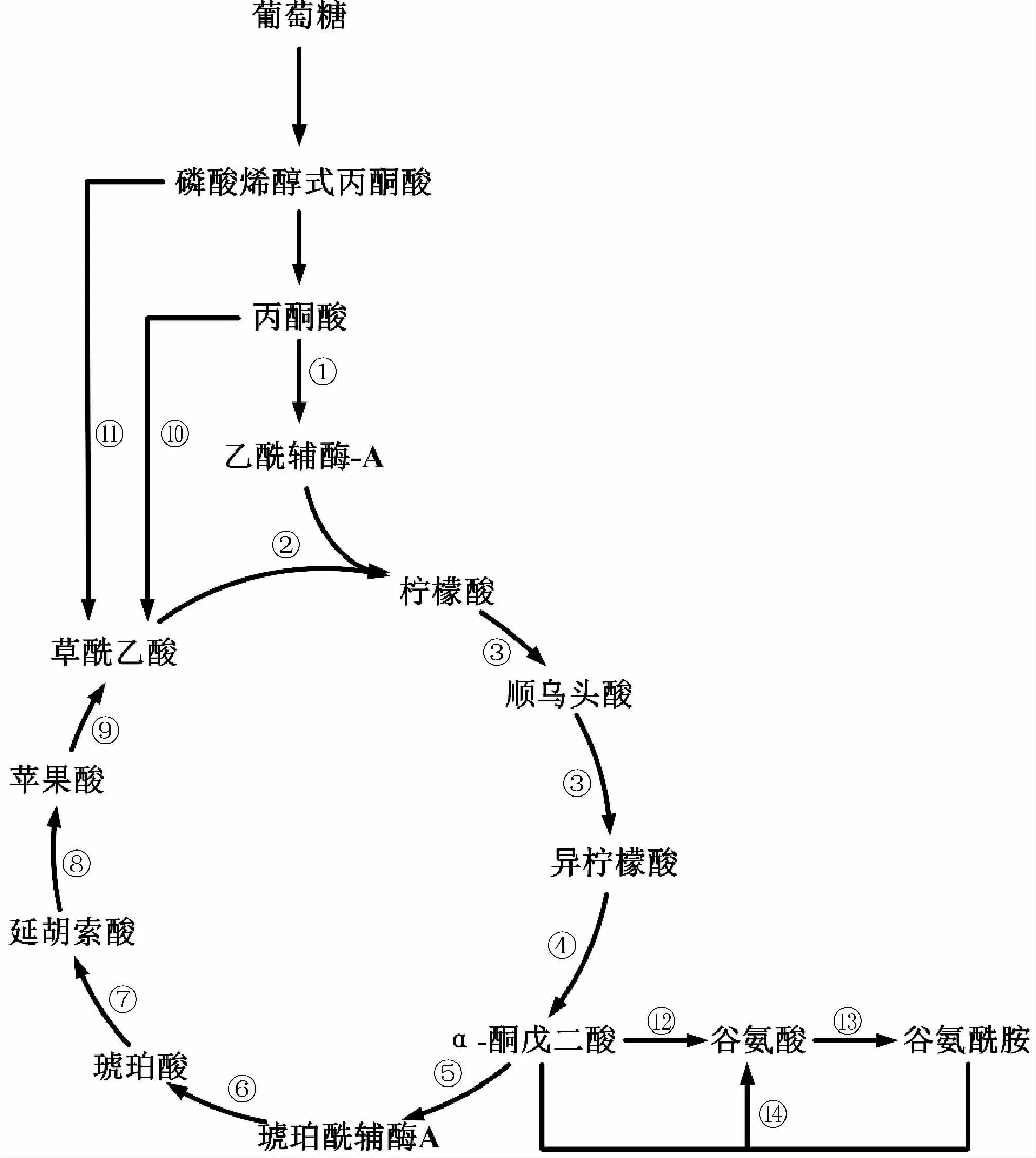
图1 α-酮戊二酸的生物合成途径Fig.1 Biosynthetic pathway of α-ketoglutarate
3.2 α-酮戊二酸生物合成的代谢调控
α-酮戊二酸的生物合成途径中有3个重要代谢节点,分别为磷酸烯醇式丙酮酸-丙酮酸-草酰乙酸节点、柠檬酸节点和α-酮戊二酸节点[23]。草酰乙酸是合成α-酮戊二酸的重要前体物质,除来源于三羧酸循环外,还可通过回补途径(replenishment pathway,RP)获得,分别由丙酮酸经丙酮酸羧化酶(pyruvate carboxylase,PC)和磷酸烯醇式丙酮酸经磷酸烯醇式丙酮酸羧化酶(phosphoenolpyruvate carboxylase,PEPC)催化生成。其中前者以生物素为辅酶,后者通常受天冬氨酸和α-酮戊二酸的反馈抑制。不同微生物含有上述1种或2种羧化酶,如大肠杆菌仅含磷酸烯醇式丙酮酸羧化酶、枯草芽孢杆菌及解脂亚洛酵母仅含丙酮酸羧化酶、谷氨酸棒杆菌同时含有磷酸烯醇式丙酮酸羧化酶和丙酮酸羧化酶。
柠檬酸节点是控制三羧酸循环代谢流量的重要代谢节点,柠檬酸合酶是该节点的关键酶,其活性往往受柠檬酸、腺嘌呤核苷三磷酸(adenosine triphosphate,ATP)及NADP的反馈抑制[24]。α-酮戊二酸节点决定其代谢去向,α-酮戊二酸分别在α-酮戊二酸脱氢酶和谷氨酸脱氢酶的催化下合成琥珀酰辅酶A和谷氨酸。α-酮戊二酸脱氢酶以硫胺素为辅酶。因此,当培养基中硫铵素不足时,α-酮戊二酸会因三羧酸循环代谢流减弱而流向谷氨酸。在谷氨酸棒杆菌中,α-酮戊二酸脱氢酶的活性除受硫铵素调节外,还受抑制蛋白(oxoglutarate dehydrogenase inhibitor,OdhI)的抑制作用。OdhI与α-酮戊二酸脱氢酶结合后使其丧失活性,但OdhI第14位苏氨酸被丝氨酸/苏氨酸蛋白激酶PknG磷酸化后不能与α-酮戊二酸脱氢酶结合,从而该抑制作用被解除。但当培养基中生物素充足时,OdhI不能被PknG磷酸化从而恢复其抑制作用[24]。
目前共发现3种谷氨酸脱氢酶,分别以NADH(EC 1.4.1.2)、NADPH(EC 1.4.1.4)以及NADPH或NADH(EC 1.4.1.3)为辅酶。不同微生物含谷氨酸脱氢酶种类不同,如大肠杆菌含EC 1.4.1.4、枯草芽孢杆菌含EC 1.4.1.2、谷氨酸棒杆菌含EC 1.4.1.3和EC 1.4.1.4、解脂亚洛酵母含EC 1.4.1.2和EC 1.4.1.4。研究发现,谷氨酸棒杆菌中EC 1.4.1.4起主要作用,但其对α-酮戊二酸的米氏常数(Km值)(5.7 mmol/L)高于α-酮戊二酸脱氢酶(0.02~0.13 mmol/L)[25]。前期研究发现,在谷氨酸棒杆菌培养过程中减少生物素或NH4+后,α-酮戊二酸脱氢酶和谷氨酸脱氢酶活性被抑制,α-酮戊二酸大量积累[26]。
4 发酵法生产α-酮戊二酸的研究进展
4.1 α-酮戊二酸生产菌种的选育
发酵法生产α-酮戊二酸最早始于LOCKWOOD L B等[27]利用荧光假单胞菌生物合成α-酮戊二酸的研究,随后多种微生物均被发现可以过量合成α-酮戊二酸[4,28]。谷氨酸棒杆菌及解脂亚洛酵母和光滑球拟酵母等酵母菌因具有生理和遗传特性清晰、生长快速、底物谱宽等特性被认为是发酵法生产α-酮戊二酸的理想菌株。因此,α-酮戊二酸生产菌种的选育研究主要集中在上述3种微生物,其主要策略包括增强α-酮戊二酸前体物的供应以及弱化竞争代谢支路。
4.1.1 增强α-酮戊二酸前体物的供应
陈坚等[29]于解脂亚洛酵母(Y.lipoytica)WSH-Z06过表达丙酮酸脱氢酶E1编码基因PDA1以提高其活性。结果表明PDA1过表达菌株胞内丙酮酸含量显著降低,经发酵144 h,其α-酮戊二酸产量由37.6 g/L提高至43.3 g/L。VENELINA Y等[30]于解脂亚洛酵母(Y.lipolytica)H355过量表达了NADP+依赖型的异柠檬酸脱氢酶编码基因IDP,以增强α-酮戊二酸前体物异柠檬酸的供应。经发酵117 h,重组菌株Y.lipolyticaH355Aα-酮戊二酸产量达到167.6 g/L,较出发菌株提高6.8%,副产物丙酮酸的积累量显著下降。孙兰超等[31]于谷氨酸棒杆菌(C.glutamicum)GDK-10过表达磷酸烯醇式丙酮酸羧化酶编码基因ppc以增加其草酰乙酸供应,重组菌株GDK-12的单位菌体产量出发菌株提高38.59%。
4.1.2 弱化竞争代谢支路
JO J H等[32]以谷氨酸棒杆菌(C.glutamicum)HH109为出发菌株,敲除其异柠檬酸裂解酶编码基因aceA、谷氨酸脱氢酶编码基因gdh和谷氨酸合酶编码基因gltB,以阻断异柠檬酸的消耗及α-酮戊二酸向谷氨酸的代谢,获得的重组菌株谷氨酸棒杆菌(C.glutamicum)JH107α-酮戊二酸产量达到51.1 g/L,较出发菌株提高68%。赵岩等[33]以谷氨酸棒杆菌(C.glutamicum)GDK-10为出发菌株,通过敲除乳酸脱氢酶编码基因ldh、乙酸激酶编码基因ackA、丙酮酸醌氧化还原酶编码基因pqo,以减少副产物乳酸、乙酸和丙酮酸积累量。结果表明,ldh和pqo基因敲除菌株C.glutamicumGDK-14和C.glutamicumGDK-15的α-酮戊二酸产量分别为40.18 g/L和31.94 g/L,较出发菌株降低8.54%和27.9%;ackA基因敲除菌株(C.glutamicum)GDK-16的α-酮戊二酸产量为47.88g/L,较出发菌株提高8.99%。LIY等[26]以谷氨酸棒杆菌C.glutamicumGKG-047为出发菌株,敲除其谷氨酸脱氢酶编码基因gdh1和gdh2,获得的重组菌(C.glutamicum)GKGDα-酮戊二酸产量达到45.6 g/L。薛宁等[34]以谷氨酸棒杆菌C.glutamicumGKGD为出发菌株,分别敲除异柠檬酸裂解酶编码基因aceA和谷氨酸合酶编码基因gltB,以减少异柠檬酸向乙醛酸循环的代谢流量及α-酮戊二酸的消耗。获得的重组菌株GKGD-1和GKGD-2摇瓶条件下α-酮戊二酸产量分别为12.86 g/L和13.81 g/L,较出发菌株提高14.72%和7.39%,转化率分别提高9.76%和5.43%。
4.2 发酵法生产α-酮戊二酸的工艺优化
4.2.1 培养基优化
韩洪军等[35]向培养基中添加玉米浆和表面活性剂吐温60以增加生长因子供应并增强细胞膜通透性,并考察其对谷氨酸棒杆菌GKGD发酵生产α-酮戊二酸的影响。结果表明,在初始发酵培养基中添加6 mL/L的玉米浆、在发酵10 h添加1 mL/L的吐温60,α-酮戊二酸的产量达到17.9 g/L,较未优化前提高了198%。
ZENG W等[36]研究了不同初始浓度甘油对解脂亚洛酵母(Y.lipolytica)WSH-Z06细胞生长和α-酮戊二酸合成的影响。发现当培养基中初始甘油质量浓度为50 g/L时,α-酮戊二酸的产量为67.4 g/L,丙酮酸产量达到39.1 g/L,较优化前分别提高了9.6%和176.8%,实现了α-酮戊二酸和丙酮酸联产。彭小雨等[37]考察了氮源浓度以及硫铵素浓度对解脂亚洛酵母(Y.lipolytica)WSH-Z06 C3联产酮酸的影响。结果表明,大豆蛋白粉和硫铵素质量浓度分别为4 g/L和0.2 μg/L时,α-酮戊二酸和丙酮酸的总产量最高(78.2 g/L),较优化前提高了57.9%。
4.2.2 发酵条件优化和过程控制
CHERNYAVSKAYA O G等[38]以乙醇为碳源,考察了溶氧对解脂亚洛酵母(Y.lipolytica)N1发酵生产α-酮戊二酸的影响。发现低溶氧(5%)时菌株对NH4+的利用速率比高溶氧(50%)时快,低溶氧条件下的产量为49 g/L,较高溶氧条件下提高了22.5%。进一步发现溶氧水平极大的影响Y.lipolyticaN1对NH4+的利用速率,进而影响α-酮戊二酸的积累。
YU Z等[39]考察了pH对解脂亚洛酵母(Y.lipolytica)WSH-Z06合成α-酮戊二酸的影响。发现低pH有利于α-酮戊二酸的合成,当pH维持在3.0时,α-酮戊二酸的产量达到53.4 g/L,较优化前提高了142%。王炫等[40]对α-酮戊二酸生产菌谷氨酸棒杆菌(C.glutamicum)KGA-3的发酵条件进行系统优化,分别研究了pH控制方式、初始糖质量浓度、发酵温度、摇瓶装液量等因素对α-酮戊二酸产量的影响,最终确定培养基初始pH为7.0,初始糖质量浓度为90 g/L,发酵温度为32 ℃,摇瓶装液量为25 mL/500 mL,优化后α-酮戊二酸的产量和转化率分别为25.8 g/L和35.1%,较优化前分别提高了45.5%和11.5%。张海林等[41]通过动力学分析确定了通过调控pH控制菌体浓度促进α-酮戊二酸积累的策略,发酵初期控制pH值为6.0,菌体质量浓度达到10 g/L后pH自然降至3.0并保持至发酵结束,α-酮戊二酸产量为54 g/L,产量和生产强度分别较未优化前提高19.3%和17.8%。
5 α-酮戊二酸主要衍生物的应用及生物合成进展
5.1 γ-氨基丁酸及其生物合成
γ-氨基丁酸是天然非蛋白质氨基酸,广泛存在于动物、植物以及微生物中。γ-氨基丁酸可以抑制大脑中神经递质的传递,进而影响到对压力的应激反应[42]。此外,γ-氨基丁酸还可以提高生长激素水平,参与大脑中蛋白质的合成,具有降血压、利尿、治疗糖尿病等功能[43]。
目前已报道的生物法合成γ-氨基丁酸的菌株主要包括乳酸菌、大肠杆菌和谷氨酸棒杆菌。α-酮戊二酸在谷氨酸脱氢酶和谷氨酸脱羧酶的催化下生成γ-氨基丁酸。其生产菌株的代谢工程改造策略包括过表达磷酸烯醇式丙酮酸羧化酶或丙酮酸羧化酶编码基因及敲除苹果酸脱氢酶编码基因以增强草酰乙酸供应[7]、过表达谷氨酸脱羧酶编码基因以促进γ-氨基丁酸的合成[44-45]、敲除γ-氨基丁酸转氨酶编码基因以阻止其降解以及过表达转氨酶透过酶编码基因以增强其输出[46]。
5.2 5-氨基乙酰丙酸及其生物合成
5-氨基乙酰丙酸亦属于天然非蛋白质氨基酸,是亚铁血红素、叶绿素、微生素B12合成的重要前体。5-氨基乙酰丙酸被广泛应用于癌症的光动力学诊断和治疗,还可用作杀虫剂和植物生长调节剂[8,47]。
5-氨基乙酰丙酸的生物合成包括C4途径和C5途径。其中C5途径以α-酮戊二酸为前体物质依次在谷氨酸脱氢酶(glutamte dehydrogenase,GDH)、谷氨酰-转移核糖核酸合成酶(glutamyl-transfer ribonucleic acid synthetase,GluRS)、谷氨酰-转移核糖核酸还原酶(glutamyl-tRNA reductase,GluRR)以及谷氨酸-1-半醛氨基转移酶(glutamate-1-semialdehyde aminotransferase,GluSA)催化作用下生成5-氨基乙酰丙酸。目前已报道的利用C5途径合成5-氨基乙酰丙酸的菌株主要包括大肠杆菌和谷氨酸棒杆菌。其生产菌株的代谢工程改造策略包括过表达柠檬酸合酶编码基因以增强柠檬酸供应[48]、弱化α-酮戊二酸脱氢酶编码基因以减少α-酮戊二酸消耗[48]、过表达谷氨酰-tRNA还原酶和谷氨酸-1-半醛氨基转移酶编码基因以强化5-氨基乙酰丙酸的合成[49-51]、弱化5-氨基乙酰丙酸脱水酶编码基因以减少5-氨基乙酰丙酸降解[52]、过表达输出蛋白编码基因以增强其输出[50]、敲除乳酸脱氢酶和乙酸激酶编码基因以减少副产物乳酸和乙酸的积累等[53]。
5.3 4-羟基异亮氨酸及其生物合成
羟基氨基酸是重要的氨基酸衍生物,可由α-酮戊二酸和Fe2+依赖的氨基酸羟化酶催化氨基酸和α-酮戊二酸生成。4-羟基异亮氨酸是常见的羟基氨基酸,由异亮氨酸和α-酮戊二酸经异亮氨酸羟化酶催化生成[54]。4-羟基异亮氨酸具有血糖浓度依赖的促进胰岛素分泌的活性以及增加葡萄糖耐受性、促进脂肪代谢和保护肝脏等功能[55]。
目前已报道的生物法合成4-羟基异亮氨酸的菌株主要包括大肠杆菌和谷氨酸棒杆菌。其生产菌株的代谢工程改造策略包括过表达异亮氨酸羟化酶以构建4-羟基异亮氨酸合成途径[56]、过表达磷酸烯醇式丙酮酸羧化酶或丙酮酸羧化酶编码基因以增强草酰乙酸供应[54]、过表达柠檬酸合酶和异柠檬酸脱氢酶编码基因以增强α-酮戊二酸供应[57]、敲除异柠檬酸裂解酶编码基因以减少异柠檬酸的消耗[57]、敲除(或弱化)α-酮戊二酸脱氢酶编码基因以减少α-酮戊二酸消耗[58]、过表达NAD激酶和6-磷酸葡萄糖脱氢酶编码基因为异亮氨酸合成提供NADPH[9]等。
6 展望
近年来,随着生物技术尤其是生物信息学、合成生物学及酶工程技术的不断进步,α-酮戊二酸及其衍生物的生物合成水平逐渐提高,工业化进程也在加快,其应用范围和领域逐渐扩大。如前所述,α-酮戊二酸脱氢酶和谷氨酸脱氢酶竞争α-酮戊二酸,其产物琥珀酰-辅酶A(coenzyme A,CoA)和谷氨酸参与多种生物反应,因此动态调节其活性以平衡其合成代谢将是实现α-酮戊二酸高效合成的关键。随着成簇的规律间隔的短回文重复序列干扰(clustered regularly interspaced short palindromic repeats interference,CRISPRi)技术的应用以及生物感应器(biosensor)的开发和应用,将为解决该关键问题提供重要支撑。
