服用扶正抗癌方后非小细胞肺癌晚期患者CD8+T细胞表达NKG2D和NKG2A受体的变化①
2019-11-20吴姗姗王柏山李志静
吴姗姗 王柏山 严 峰 张 宁 张 程 李志静
(辽宁中医药大学附属医院临床检验中心,沈阳110032)
肺癌是目前全世界发病率和死亡率最高的恶性肿瘤,吸烟、肺部持续慢性感染、遗传等因素均可导致肺癌的发生。约有85%的病例属于非小细胞肺癌(NSCLC),包括鳞癌、腺癌、腺鳞癌和大细胞肺癌等,多数病例在发现时已有局部浸润或已发生转移[1,2]。尽管在过去的几十年已经开发了多种化疗和靶向治疗方案,但是多数NSCLC仍会发生转移或复发[3]。一些研究发现扶正抗癌方联合化疗药物治疗,能够增加化疗药物敏感性并且降低其毒性[4,5]。扶正抗癌方具有扶正补虚,提高机体免疫力抗癌抑瘤的作用。但是具体免疫学机制尚不清楚。T细胞是机体抗肿瘤免疫的重要效应细胞,并且通过功能各异的细胞亚群来完成免疫调控机能。成熟T细胞分为 CD4+T和CD8+T细胞。CD8+T细胞又称为细胞毒性T细胞,主要发挥对肿瘤细胞的免疫监视作用。CD8+T细胞通过T细胞受体(TCR)与靶细胞上的抗原肽-MHC-Ⅰ类分子结合,传导活化信号并直接作用于靶细胞使其溶解。CD8+T细胞也可表达一些NK相关受体,有活化性受体NKG2D和抑制性受体NKG2A等,通过识别其相应的配体传递抑制或活化信号,抑制与活化信号发生整合,最终决定CD8+T细胞能否杀伤靶细胞[6]。
NKG2D是一种广泛表达于免疫效应细胞(如NK细胞、CD8+αβT细胞、NKT细胞等)的活化性细胞表面受体,T细胞上的NKG2D是作为TCR激活的一个重要共刺激分子[7]。而且有研究发现结肠癌患者的CD8+T细胞可以分别通过TCR或NKG2D受体识别自体和同种异体的肿瘤细胞[8]。食道癌Ⅲ/Ⅳ期患者的CD8+T细胞NKG2D受体表达显著低于Ⅰ/Ⅱ期患者,说明其表达与肿瘤疾病的严重程度密切相关[9]。人类患宫颈癌时CD8+T细胞表达NKG2A上调使CD8+T细胞释放穿孔素明显减少,而且细胞毒性试验表明NKG2A表达的上调可抑制CD8+T细胞的细胞毒作用[10]。无论是小鼠还是人类当阻断抑制性的NKG2A受体时,可以通过提升CD8+T和NK细胞的效应功能从而加强对肿瘤的免疫作用[11]。由此可见,通过观察CD8+T细胞表面NKG2D和NKG2A表达的高低,可以预测肿瘤疾病的严重程度。本研究旨在探索晚期NSCLC患者按疗程规范服用扶正抗癌方前后CD8+T细胞表面NKG2D和NKG2A的表达情况。
1 材料与方法
1.1材料
1.1.1研究对象 本研究通过本院伦理委员会审批以及患者的知情同意。选择我院2018年5月至2019年1月期间收治的有病理学明确诊断的31例NSCLC晚期患者,其中男18例,女13例;年龄35~79岁,平均年龄为(45.5±3.8)岁,其中鳞癌14例,腺癌17例;TNM分期Ⅲa期8例,Ⅲb期11例,Ⅳ期12例。上述患者为治疗组,根据服用扶正抗癌方前后分别定义为治疗前组和治疗后组。
1.1.2病例入选标准 入选标准:①患者符合原发性非小细胞肺癌诊断标准[12]且无其他肿瘤史;②患者不伴发自身免疫性疾病,如系统性红斑狼疮、风湿性骨关节病等;③患者未服用激素类药物或接受免疫抑制剂的治疗;④排除活动性(病毒)感染。Karnofsky评分≥70分。选择与患者性别年龄相匹配的健康人21例即健康对照组,其中男11例,女10例;年龄32~77岁,平均(42.3±3.5)岁。
1.1.3药物干预 治疗组服用院内扶正抗癌方(基本组成:苦参15 g,生白术12 g,生甘草5 g,半夏15 g,大贝20 g,半枝莲15 g,白花蛇草30 g,茯苓20 g,陈皮15 g,生苡仁30 g);辨证加减:反复咳嗽并痰中带血可加三七和仙鹤草等;胸痛者可加枳壳、香附、延胡索等;阴虚者可加沙参和麦冬等;阳虚者加巴戟天、肉苁蓉和杜仲等。上述中药由我院药房提供并按正规流程制备,每日1剂水煎至150 ml,分3次服用,连续服用30日为1个疗程。
1.2实验方法
1.2.1T 淋巴细胞绝对数量检测 完全依照1997年美国CDC颁布的CD4+T细胞和CD8+T细胞绝对值检测指导方法严格执行。具体步骤:将20 μl CD4FITC/CD8PE/CD3PerCP试剂加入BD公司TruCOUNT管中,逆向加样法加入50 μl EDTA抗凝血,室温避光15 min,加入经10倍稀释的免洗溶血素450 μl,室温避光15 min,样本溶血充分后流式细胞仪FACSCalibur检测,MULTISET 软件进行分析。
1.2.2CD8+T细胞表面NKG2D和NKG2A的表达 具体步骤:采用荧光标记的单克隆抗体组合CD3 PE-Cy7/CD8 Percp-Cy5.5/NKG2D APC/NKG2A PE 对治疗组和健康对照组的外周静脉血进行表面染色,即每个研究对象均有一管按上述组合染色的样本管,另设一管同型对照管。样本管内加入100 μl EDTA抗凝全血,按上述组合的单克隆抗体分别加入样本管内,室温避光25 min后加入溶血素3 ml,继续室温避光8 min溶血充分后,300 g离心10 min弃上清。加入3 ml PBS进行洗涤,室温下300 g离心10 min后弃上清,共洗涤两次。最终加入含有1% 多聚甲醛的PBS 200 μl悬浮,BD FACSCalibur流式细胞仪检测,CELLQUEST软件进行分析。
1.2.3生存质量评价 根据Karnofsky评分评价患者的生存质量。提升:比治疗前评分升高≥10分;平稳:治疗前后评分变化幅度≤10分;降低:比治疗前评分减少≥10分[13]。
1.3统计学处理 采用SPSS20.0软件进行分析,计量资料用中位数的95%可信区间表示。各组间两两比较采用Mann-WhitneyU检验,相关性采用Spearman 秩相关检验,P<0.05为差异具有统计学意义。
2 结果
2.1CD4+T和CD8+T细胞绝对值在NC组、治疗前组和治疗后组的差别 NC组的CD4+T细胞绝对值显著高于治疗前组和治疗后组(P<0.01);治疗前组和治疗后组的CD4+T细胞绝对值无显著性差异,见表1。NC组的CD8+T细胞绝对值显著高于治疗前组和治疗后组(P<0.01);治疗后组的CD8+T细胞绝对值显著高于治疗前组(P<0.01),见表1和图1A。
2.2CD8+T细胞表面NKG2D和NKG2A在NC组、治疗前组和治疗后组所占百分比
2.2.1CD8+T细胞表面NKG2D+NKG2A-在NC组、治疗前组和治疗后组占百分比 NC组的NKG2D+NKG2A-CD8+T细胞的百分比显著高于治疗前组和治疗后组(P<0.01);治疗后组NKG2D+NKG2A-CD8+T细胞的百分比显著高于治疗前组(P<0.01),见表1、图1B和图 2,流式细胞图见图3。
2.2.2CD8+T细胞表面NKG2D-NKG2A+在NC组、治疗前组和治疗后组所占百分比 NC组的NKG2D-NKG2A+CD8+T细胞的百分比显著低于治疗前组(P<0.01);NC组也显著低于治疗后组(P<0.05);而治疗前组和治疗后组无显著性差异,见表1、图1C和图 2,流式细胞图见图3。
2.2.3CD8+T细胞表面NKG2D+NKG2A+在NC组、治疗前组和治疗后组占百分比 NC组的NKG2D+NKG2A+CD8+T细胞的百分比显著低于治疗前组(P<0.01);在其余各组间无显著性差异,见表1、图1D和图 2,流式细胞图见图3。
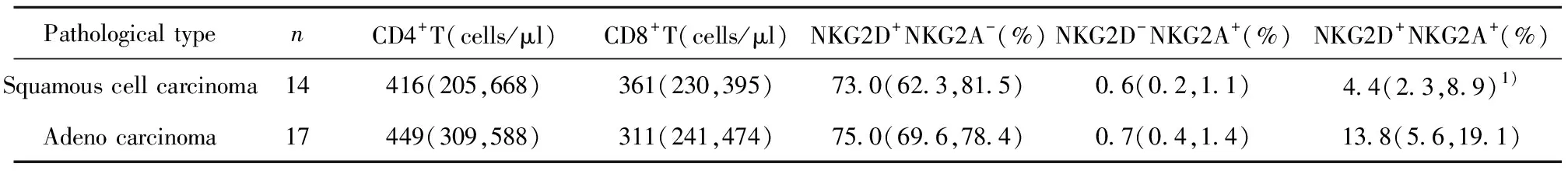
2.3治疗前组不同病理类型上述指标的差别 治疗前组包含鳞癌14例,腺癌17例。鳞癌NKG2D+NKG2A+CD8+T细胞的百分比显著低于腺癌(P<0.05);CD4+T、 CD8+T细胞绝对值以及NKG2D+NKG2A-CD8+T(%)、NKG2D-NKG2A+CD8+T(%)在鳞癌患者和腺癌患者间并无显著性差异,见表2。



GroupsnCD4+T(cells/μl)CD8+T(cells/μl)NKG2D+NKG2A-(%)NKG2D-NKG2A+(%)NKG2D+NKG2A+(%)Pre31449(268,623)347(241,437)2)74.7(66.2,78.7)2)0.7(0.2,1.1)2)8.6(2.7,15.1)2)Post31495(343,672)426(366,547)2)81.9(69.6,86.3)2)0.5(0.1,0.9)1)5.4(1.6,10.8)NC21946(746,1 138)679(527,863)93.1(87.8,94.0)0.1(0,0.2)2.8(2.2,4.9)
Note:Compared with NC group,1)P<0.05,2)P<0.01.

图1 治疗前、治疗后和NC组的CD8+T细胞绝对值、NKG2D+NKG2A-CD8+T(%)、NKG2D-NKG2A+CD8+T(%)、NKG2D+NKG2A+CD8+T(%)的差异Fig.1 Comparison percentage of NKG2D+NKG2A-CD8+T cells, NKG2D-NKG2A+CD8+T cells,NKG2D+NKG2A+CD8+T cells and absolute counts of CD8+ T cells among Pre-treatment group,Post-treatment group and NC three groupsNote: A.The comparison of the absolute counts of CD8+T cells;B.The comparison of the percentage of NKG2D+NKG2A-CD8+T cells;C.The comparison of the percentage of NKG2D-NKG2A+CD8+T cells;D.The comparison of the percentage of NKG2D+NKG2A+CD8+T cells.

图2 治疗前、治疗后和NC组NKG2D+NKG2A-CD8+T(%)、NKG2D-NKG2A+CD8+T(%)、NKG2D+NKG2A+CD8+T(%)以及NKG2D-NKG2A-CD8+T(%)Fig.2 Percentage of NKG2D+NKG2A-CD8+T cells, NKG2D-NKG2A+CD8+T cells,NKG2D+NKG2A+CD8+T cells and NKG2D-NKG2A-CD8+T cells among Pre-treatment group,Post-treatment group and NC three groups

图3 各组CD8+T细胞表达NKG2D和NKG2A不同亚群所占百分比的流式细胞图Fig.3 Representative flow cytometric graphs of NKG2D+/-NKG2A+/-CD8+T cells in Pre-treatment group,Post-treatment group and NC group


Pathological typenCD4+T(cells/μl)CD8+T(cells/μl)NKG2D+NKG2A-(%)NKG2D-NKG2A+(%)NKG2D+NKG2A+(%)Squamous cell carcinoma14416(205,668)361(230,395)73.0(62.3,81.5)0.6(0.2,1.1)4.4(2.3,8.9)1)Adeno carcinoma17449(309,588)311(241,474)75.0(69.6,78.4)0.7(0.4,1.4)13.8(5.6,19.1)
Note:Compared with Adenocarcinoma group,1)P<0.05.



TNMnCD4+T(cells/μl)CD8+T(cells/μl)NKG2D+NKG2A-(%)NKG2D-NKG2A+(%)NKG2D+NKG2A+(%)Ⅲ19581(449,643)2)391(278,466)1)77.4(75.0,82.5)2)0.4(0.2,0.8)2)8.6(3.7,13.9)Ⅳ12248(191,335)267(185,357)61.5(53.4,67.4)1.1(0.8,2.4)9.8(2.6,25.9)
Note:Compared with Phase Ⅳ group,1)P<0.05,2)P<0.01.

图4 Ⅲ期、Ⅳ期患者CD4+和CD8+T细胞绝对值、NKG2D+NKG2A-CD8+T(%)以及NKG2D-NKG2A+CD8+T(%)的差异Fig.4 Comparison the percentage of NKG2D+NKG2A-CD8+T(%),NKG2D-NKG2A+CD8+T(%),absolute counts of CD4+ T cells and absolute counts of CD8+ T cells between Phase Ⅲ and Phase ⅣNote: A.The comparison of the absolute counts of CD4+T cells;B.The comparison of the absolute counts of CD8+T cells;C.The comparison of the percentage of NKG2D+NKG2A-CD8+T cells;D.The comparison of the percentage of NKG2D-NKG2A+CD8+T cells.



GendersnCD4+T(cells/μl)CD8+T(cells/μl)NKG2D+NKG2A-(%)NKG2D-NKG2A+(%)NKG2D+NKG2A+(%)Males18472(329,601)315(256,470)75.5(70.5,79.0)0.6(0.2,1.0)9.0(6.6,18.8)Females13437(299,633)360(218,395)71.8(61.3,79.0)0.8(0.4,1.4)8.7(6.2,18.3)

图5 NSCLC患者治疗前和治疗后NKG2D+NKG2A-CD8+T(%)和NKG2D-NKG2A+CD8+T(%)的相关性(A和B)Fig.5 Correlation analysis of percentage of NKG2D+NKG2A-CD8+T cells and percentage of NKG2D-NKG2A+CD8+T cells between Pre-treatment group and Post-treatment groupNote: A.The correlation analysis of the percentage of NKG2D+NKG2A-CD8+T cells and percentage of NKG2D-NKG2A+CD8+T cells in pre-treatment group;B.The correlation analysis of the percentage of NKG2D+NKG2A-CD8+T cells and percentage of NKG2D-NKG2A+CD8+T cells in post-treatment group.
2.4治疗前组不同TNM分期患者上述指标的差别 治疗前组包含Ⅲ期19例,Ⅳ期12例。Ⅲ期的CD4+T细胞绝对值显著高于Ⅳ期(P<0.01),见表3和图4A;Ⅲ期的CD8+T细胞绝对值显著高于Ⅳ期(P<0.05),见表3和图4B;Ⅲ期的NKG2D+NKG2A-CD8+T(%)显著高于Ⅳ期(P<0.01),见表3和图4C;Ⅲ期的NKG2D-NKG2A+CD8+T(%)显著低于Ⅳ期(P<0.01),见表3和图4D。
2.5治疗前组不同性别上述指标的差别 治疗前组包含女性10例,男性11例,CD4+T、CD8+T细胞绝对值以及NKG2D+NKG2A-CD8+T(%)、NKG2D-NKG2A+CD8+T(%)、NKG2D+NKG2A+CD8+T(%)在女性和男性间并无显著性差异,见表4。
2.6相关性分析 治疗前组NKG2D+NKG2A-CD8+T(%)与NKG2D-NKG2A+CD8+T(%)呈负相关(P<0.01,R=-0.66),见图5A。
治疗后组NKG2D+NKG2A-CD8+T(%)与NKG2D-NKG2A+CD8+T(%)也呈负相关(P<0.01,R=-0.54),见图5B。
2.7治疗后生存质量评价 共31例患者治疗前后Karnofsky评分的变化,其中7例患者评分升高≥10分,占总体的22.0%;19例患者评分变化幅度≤10分,占总体的61.2%;5例患者评分减少≥10分,占总体的16.1%。83.9%的患者治疗后生存质量都稳中有升。
3 讨论
中医定义肺癌是一种全身属虚,局部属实,本虚标实之病证,邪毒聚结,最易耗伤人体正气,随着邪长正消,正气受戕益甚。可见正虚是肺癌的内因,也是推动肺癌发展的关键,扶正培本以及时时顾护正气是中医对肺癌进行辨证施治的核心。中医的正气主要由先天的元气和后天的中气构成。有研究发现通过补中益气不仅可以改善非特异性免疫,特异性免疫也会有所改善[14]。中医学的正气理论与现代医学的免疫理论有相通之处但是不能等同,二者的关联有待深入研究,本研究旨在探索按疗程规范服用扶正抗癌方前后,NSCLC晚期患者CD8+T细胞表面表达NKG2D和NKG2A的变化。
CD4+T细胞又称为辅助性T细胞,可以调控或辅助其他淋巴细胞发挥功能。本研究发现NSCLC晚期患者CD4+T细胞绝对值显著低于NC组,在按疗程规范服用扶正抗癌方前后患者CD4+T细胞绝对值无显著性变化。众多研究表明,细胞毒性T细胞可以抑制恶性实体瘤的生长[15]。NSCLC晚期患者CD8+T细胞绝对值显著低于NC组,应用扶正抗癌方后患者CD8+T细胞绝对值较治疗前明显升高。应用扶正抗癌方后NSCLC晚期患者CD8+T细胞绝对值显著升高,有利于抑制患者体内肿瘤的生长。
肿瘤浸润的NKG2D+CD8+T细胞可以识别并消除表达NKG2D配体的肿瘤细胞[16]。Lin等[17]的研究发现:与肿瘤细胞共同孵育后,CD8+T细胞表达NKG2D显著下调。当阻断NKG2D或其配体可抑制CD8+T细胞杀伤肿瘤的活性。其研究显示NKG2D受体可能是胃癌的有利预后指标,并推测NKG2D表达下降是肿瘤的免疫逃逸机制[17]。有数据表明NSCLC晚期患者较早期患者CD8+T细胞表达NKG2D显著下降[18]。相似的结果在本研究同样得到了印证,本研究发现NSCLCⅢ期患者的NKG2D+NKG2A-CD8+T占百分比显著高于Ⅳ期,随着肿瘤疾病的进展CD8+T细胞表达NKG2D会明显减少。患者服用扶正抗癌方后,83.9%的患者生存质量评价稳中有升,只有16.1%的患者生存质量评价下降。与其相对应的我们发现治疗后NKG2D+NKG2A-CD8+T占百分比较治疗前显著升高但是仍然显著低于NC组。结果表明患者在服用扶正抗癌方后CD8+T细胞表达NKG2D显著上调,可能有利于体内CD8+T细胞识别并杀伤肿瘤细胞,从而使患者的一般状况得到改善,二者之间存在因果关联。
NKG2A是一种带有酪氨酸抑制性基序(ITIM)的NK相关抑制性受体,既表达于NK细胞又表达于T细胞[19]。在健康个体的外周血中约有5%的CD8+T细胞表面可稳定表达NKG2A,当有慢性抗原刺激时这种表达可以上调[20]。NKG2A/CD94形成的异二聚体可与人类非经典的MHCⅠ类分子复合物HLA-E结合,传导抑制信号从而抑制NK和CD8+T细胞的活性[21]。最新研究发现:通过阻断CD8+T细胞而非NK细胞表面的NKG2A受体,可以提高机体对治疗性肿瘤疫苗的临床反应[22]。Yu等[18]的研究发现NSCLC晚期患者较早期患者CD8+T细胞表达NKG2A显著升高。本研究发现NSCLCⅢ期患者的NKG2D-NKG2A+CD8+T占百分比显著低于Ⅳ期,随着肿瘤疾病的进展CD8+T细胞表达NKG2A增多。我们的结果与Yu等[18]的研究结果相符。患者服用扶正抗癌方后,大部分患者生存质量保持稳中有升的状态。我们发现治疗后NKG2D-NKG2A+和NKG2D+NKG2A+CD8+T两群细胞的百分比,较治疗前虽有下降的趋势但并无统计学差异。我们推测之所以没有产生统计学差异,可能是由于本研究的样本量偏小。患者生存质量的改善还是与CD8+T细胞表达NKG2A减少的趋势相对应的,但是CD8+T细胞对肿瘤细胞的杀伤功能是否有改善则需要进一步的研究证实。
NKG2D和NKG2A受体可同时表达于CD8+T细胞,CD8+T细胞的活性取决于上述两个受体叠加的效果。本研究的相关性结果显示无论在治疗前还是治疗后,NSCLC晚期患者NKG2D+NKG2A-CD8+T和NKG2D-NKG2A+CD8+T两群细胞的百分比呈负相关,说明CD8+T细胞表达NKG2D和NKG2A受体呈现互为消长的状态。免疫活化和免疫抑制之间存在平衡,可以间接反映免疫监视的效果,在肿瘤微环境中免疫活化和免疫抑制信号的比例可以更好地预测免疫治疗的结果[23]。我们的结果也再次印证这种CD8+T细胞上免疫活化和免疫抑制的平衡理论。
本研究的NSCLC晚期患者包含鳞癌14例、腺癌17例,鳞癌NKG2D+NKG2A+CD8+T细胞的百分比显著低于腺癌患者,其他细胞群无显著性差异。而之前Yu等[18]的研究发现鳞癌CD8+T细胞表达NKG2D和NKG2A有低于腺癌的趋势但无显著性差异,之所以结果会有差异,我们推测可能是由于患者构成的不同引起上述的差异,Yu等[18]的研究包含23例早期患者和17例晚期患者,而我们的患者全部是晚期患者。NKG2D和NKG2A同时表达于同一个CD8+T细胞,二者可能处于一种博弈状态,CD8+T细胞是否能够杀伤肿瘤细胞主要取决于肿瘤细胞表面何种受体的配体处于优势,但仍有待于进一步的研究证实。本研究发现NSCLC晚期患者CD8+T细胞表达NKG2D和NKG2A的水平无性别差异,这与Yu等[18]的研究结果一致。
综上所述,NSCLC晚期患者按照辨证施治的原则,服用扶正抗癌方一个月大部分患者生存质量稳中有升,与之相对应的CD8+T细胞表达NKG2D升高和NKG2A降低,我们推测扶正抗癌方的应用可能激活体内CD8+T细胞杀伤肿瘤细胞的活性,有利于改善患者预后。可以成为手术、放化疗以及靶向治疗的辅助疗法,而且众多研究已经证实服用扶正抗癌方可增加放化疗敏感性同时降低放化疗引起的不良反应。
