一测多评法同时测定清解颗粒中3 种成分
2019-10-16肖望重夏新华
唐 林, 肖望重, 黄 莉, 雷 昌, 夏新华
(1.湖南中医药大学第一附属医院,湖南 长沙410007;2.中药粉体与创新药物省部共建国家重点实验室培育基地,湖南 长沙410208;3.湖南中医药大学药学院,湖南 长沙410208)
清解颗粒为湖南中医药大学第一附属医院的院内制剂,临床用于治疗小儿急性支气管炎和小儿慢性支气管炎的急性发作,疗效显著,该制剂由生石膏、苦杏仁、防风、焦山楂等12 味中药组成,具有解表清热、化痰止咳的功效[1],苦杏仁、防风为方中君药,其中苦杏仁苷为前者指标性成分,升麻素苷,5-O-甲基维斯阿米醇苷为后者指标性成分,三者均具有明显的止咳、祛痰、平喘、抗炎、抗病毒等药理作用[2-4]。课题组前期对清解颗粒提取工艺进行研究,建立HPLC 法测定指标成分含有量,但该方法操作繁琐,成本较高[5]。
近年来,一测多评法在中药多指标质量评价过程中受到重视,其优势为采用相对校正因子,在仅使用1 个对照品(易得、价廉、稳定)的情况下实现多指标成分同步测定,成为一种适合中药特点的多指标质量评价新模式[6],已在丹参、黄连、金银花、人参、三七、复方丹参片、栀子金花丸等多种中药及复方制剂的多指标质量控制中得到了应用[7-9]。因此,本实验建立一测多评法,以含有量最高、廉价易得的苦杏仁苷为内标,建立其与升麻素苷、5-O-甲基维斯阿米醇苷之间的相对校正因子,探讨该方法用于清解颗粒成分含有量测定的可行性,同时也可为该制剂质量控制提供依据。
1 材料
1.1 仪器 Agilent 1260 高效液相色谱仪,配置DEAB806546 高压四元泵、DEAAC12853 自动进样器、DEACN13975 柱温箱、DEAAX03328DAD 检测器、Agilent 1260 series 色谱工作站(美国Agilent Technologies 公司);Waters e2695 高效液相仪,配置Waters 2489 UV 检测器、Empower 3 色谱数据工作站(美国Waters 公司);Hei-Vap Advantage 型旋转蒸发仪(德国Heidolph 公司);AL-204 型分析天平[梅特勒-托利多仪器(上海) 有限公司];SK-7200HP 超声波清洗器(上海科导超声仪器有限公司)。
1.2 试药 白芍、柴胡等中药饮片均购自康美药业股份有限公司,经湖南中医药大学药学院刘塔斯教授鉴定为正品,符合2015 年版《中国药典》 项下规定。苦杏仁苷(批号110820-201506,含有量93.4%)、5-O-甲基维斯阿米醇苷(批号111523-201509, 含 有 量 95.8%)、 升 麻 素 苷 (批 号111522-201511,含有量94.8%) 对照品均购自中国食品药品检定研究院。甲醇、乙腈、冰醋酸为色谱纯(德国默克公司);其他试剂均为分析纯;水为超纯水(法国威立雅有限公司Purelab Option Q15 超 纯 水 机 制 备)。 清 解 颗 粒 样 品 (批 号20180401、20180501、20180801),由湖南省中医药研究院中药研究所制备。
2 方法与结果
2.1 溶液制备
2.1.1 对照品溶液 精密称取苦杏仁苷、升麻素苷、5-O-甲基维斯阿米醇苷对照品适量, 置于25 mL量瓶中,甲醇溶解定容,得到贮备液(三者质量浓度分别为1.236、0.748、0.396 mg/mL),于冰箱中冷藏备用。精密量取适量,加甲醇稀释,即 得 (每 1 mL 分 别 含 三 者 0.247、 0.150、0.079 mg)。
2.1.2 供试品溶液 取颗粒2 g,研细,精密称取适量, 置于250 mL 具塞锥形瓶中, 精密加入50 mL甲醇,称定质量,超声(功率250 W、频率50 kHz) 提取30 min,放冷,甲醇补足减失的质量,摇匀,滤过,精密量取续滤液25 mL,浓缩至干,残渣加甲醇溶解,转移至10 mL 量瓶中,稀释至刻度, 摇匀, 续滤液过0.45 μm 微孔滤膜,即得。
2.1.3 阴性样品溶液 按处方比例和制备工艺分别制备缺苦杏仁、防风的阴性样品,按“2.1.2”项下方法制备,即得。
2.2 色谱条件 依利特C18色谱柱 (4.6 mm×250 mm,5 μm);流动相甲醇(A) -乙腈(B) -0.1%冰醋酸(C),梯度洗脱,程序见表1;体积流量1 mL/min;检测波长210 nm(0 ~20 min,苦杏仁苷)、254 nm(20 ~40 min,升麻素苷、5-O-甲基维斯阿米醇苷);柱温30 ℃;进样量5 μL。在上述色谱条件下,各成分分离度良好,阴性无干扰,色谱图见图1。

表1 梯度洗脱程序Tab.1 Gradient elution programs
2.3 方法学考察
2.3.1 线性关系考察 精密量取对照品贮备液适量,按一定比例配制成6 个质量浓度,在“2.2”项色谱条件下进样测定。以峰面积为纵坐标(Y),溶液质量浓度为横坐标(X) 进行回归,结果见表2,可知各成分在各自范围内线性关系良好。

表2 各成分线性关系Tab.2 Linear relationships of various constituents
2.3.2 精密度试验 精密量取供试品 (批号20180801) 溶液5 μL,在“2.2” 项色谱条件下进样测定6 次,测得苦杏仁苷、升麻素苷、5-O-甲基维斯阿米醇苷峰面积RSD 分别为0.72%、0.44%、0.39%,表明仪器精密度良好。
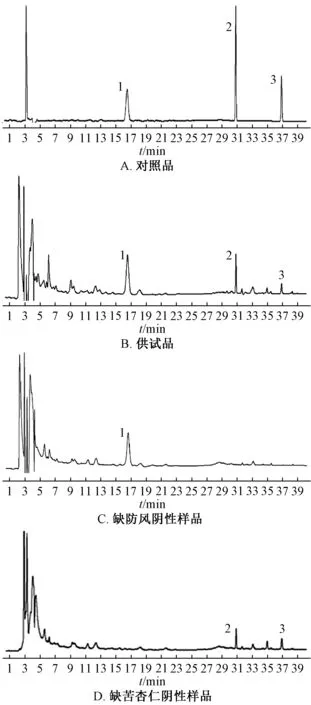
图1 各成分HPLC 色谱图Fig.1 HPLC chromatograms of various constituents
2.3.3 稳定性试验 精密量取供试品 (批号20180801) 溶液5 μL,于0、2、4、8、12、24 h在“2.2” 项色谱条件下进样测定,测得苦杏仁苷、升麻素苷、5-O-甲基维斯阿米醇苷峰面积RSD分别为0.77%、2.24%、2.35%,表明溶液在24 h内稳定性良好。
2.3.4 重复性试验 取同一批样品 (批号20180801),按“2.1.2” 项下方法制备6 份供试品溶液,在“2.2” 项色谱条件下进样测定,测得苦杏仁苷、升麻素苷、5-O-甲基维斯阿米醇苷含有量RSD 分别为2.87%、1.65%、2.10%,表明该方法重复性良好。
2.3.5 加样回收率试验 精密称取同一批样品(批号20180801)约1 g(含苦杏仁苷7.60 mg、升麻素苷1.22 mg、5-O-甲基维斯阿米醇苷0.44 mg),共6 份,精密加入苦杏仁苷对照品溶液(3.259 4 g/mL)2 mL、升麻素苷对照品溶液(0.322 mg/mL)4 mL、5-O-甲基维斯阿米醇苷对照品溶液(0.35 mg/mL)1.60 mL,按“2.1.2” 项下方法制备供试品溶液,在“2.2” 项色谱条件下进样测定,计算回收率,结果见表3。

表3 各成分加样回收率试验结果(n=6)Tab.3 Results of recovery tests for various constituents(n=6)
2.4 相对校正因子测定 采用多点校正法。取“2.1.1” 项下对照品溶液,在“2.2” 项色谱条件下进样测定,以苦杏仁苷为内标,计算其他2 种成分相对 校正因子fk/m, 公式 为(Ak为内标峰面积,Wk为内标质量浓度,Am为组分m 峰面积,Wm为组分m 质量浓度)[10],结果见表4。
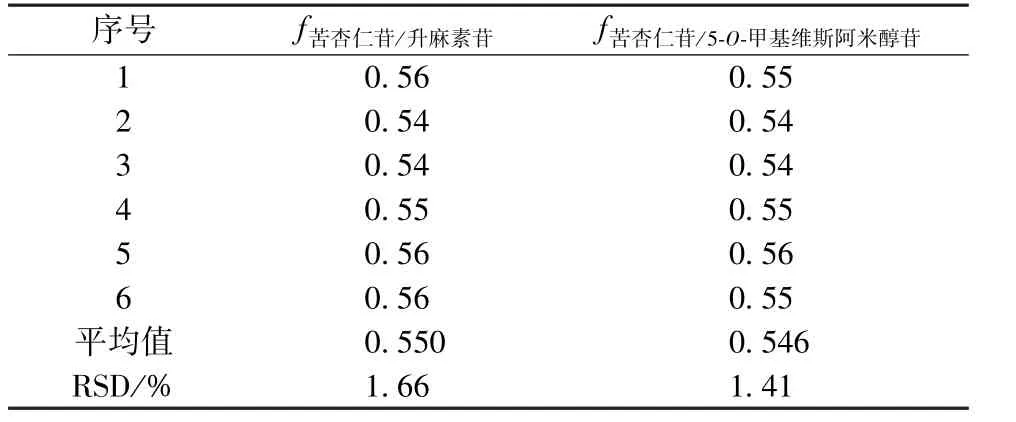
表4 各成分相对校正因子Tab.4 Relative correction factors of various constituents
2.5 耐用性考察
2.5.1 不同仪器、色谱柱 取“2.1.1” 项下对照品溶液,在“2.2” 项色谱条件下进样测定,考察不同仪器(Waters e2489、Agilent 1260)、色谱柱(依利特C18、Agilent SB-C18、Agilent HC-C18)对相对校正因子的影响,结果见表5,可知均无明显影响,耐用性良好(RSD<3.0%)。

表5 不同仪器、色谱柱对相对校正因子的影响Tab.5 Effects of different instruments and columns on relative correction factors
2.5.2 柱温 取“2.1.1” 项下对照品溶液,在“2.2” 项色谱条件下测定柱温25、30、35、40 ℃时的相对校正因子,结果见表6,可知均无明显影响,重复性良好(RSD<3.0%)。
2.5.3 色谱峰定位 以苦杏仁苷为内标,考察其他2 种成分相对保留时间(待测成分与内标成分保留时间之比,tR) 和保留时间差(待测成分与内标成分保留时间之差,Δt),结果见表7,可知以tR为 定 位 标 准 时, 各 成 分 差 异 较 大 (RSD >3.0%);以Δt 为定位标准时,各成分差异较小(RSD<3.0%),即可将其用于色谱峰定位。
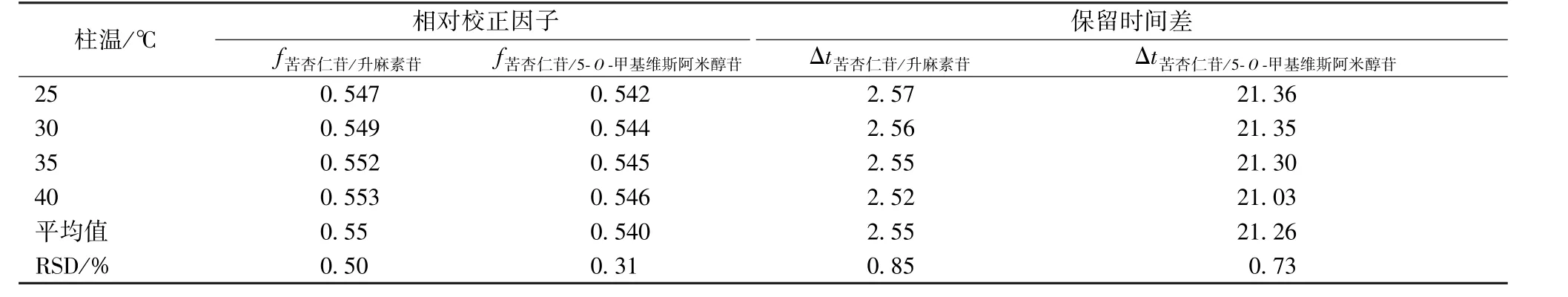
表6 不同柱温对相对校正因子的影响Tab.6 Effects of different column temperatures on relative correction factors

表7 各成分相对保留值、保留时间差Tab.7 Relative retention values and retention time differences for various constituents
2.6 样品含有量测定 分别采用外标法和一测多评法测定3 批样品含有量,结果见表8,可知2 种方法所得结果无明显差异。

表8 各成分含有量测定结果(mg/g)Tab.8 Results of content determination of various constituents(mg/g)
3 讨论
本实验检测波长根据《中国药典》 确定,即苦杏仁苷为210 nm,升麻素苷、5-O-甲基维斯阿米醇苷为254 nm,故采用二极管阵列检测器的波长切换功能,具有较高的灵敏度、准确度、专属性。在选择流动相时,比较了甲醇-水、乙腈-水、甲醇-乙腈-水、甲醇-乙腈-盐 (0.1%冰醋酸、0.1%磷酸、0.1%甲酸) 的洗脱效果,发现甲醇-水洗脱苦杏仁苷分离效果较好,乙腈-水洗脱5-O-甲基维斯阿米醇苷分离效果较好,而甲醇-乙腈-水洗脱各成分时基本达到基线分离,但升麻素苷存在轻微拖尾,故考虑在水相中加入弱酸来改善峰形拖尾,由于甲醇-乙腈-0.1%冰醋酸洗脱时成分分离度较好,峰形对称,故以其为流动相。
前期分别以苦杏仁苷、升麻素苷、5-O-甲基维斯阿米醇苷为内标,比较其相对校正因子,发现苦杏仁苷最稳定(RSD<2%),而且较易分离获得,对照品价格便宜, 含有量最高, 故选择其作为内标。
对于一测多评法的色谱峰定位,主要是采用相对保留时间[11-12]。但本实验所测成分的相对保留时间在不同色谱柱中明显不同,可能是因为它们与内标色谱峰保留时间的差异较大[13-14],故选择保留时间差进行定位。
