HPLC-MS法测定大鼠血浆中广藿香酮衍生物PPCl浓度及其药动学研究
2019-06-01张岚彭成程芳陈婕妤潘媛韩波张若琪
张岚 彭成 程芳 陈婕妤 潘媛 韩波 张若琪
(成都中医药大学药学院,中药资源系统研究与开发利用省部共建国家重点实验室培养基地,成都 611137)
广藿香为唇形科植物广藿香Pogostemon cablin[(Blanco) Benth]的地上干燥部分[1],广藿香酮为其主要有效成分之一。本实验室前期就广藿香酮的药理活性以及药动学进行了研究,发现其具有显著的抗真菌活性和良好的生物利用度[2-4]。但由于广藿香酮侧链处于一个较大的疏水空腔,致使其与抗菌关键作用靶点为四硝季戊四醇还原酶结合不紧密,影响其抗菌效应。为改善其抗菌活性,提高药物与靶点的结合能力,本实验室在广藿香酮的侧链引入大位阻的疏水官能团,合成一系列广藿香酮衍生物,其中广藿香酮衍生物PPCl抗菌作用显著,具有较大的开发前景[5]。
广藿香酮衍生物PPCl为3(2E,4E)-5-(4-氯代苯基)戊-2,4-烯酰基)-4-羟基-6-甲基-2H-吡喃-2-酮 (3(2E,4E)-5-(4- chlorophenyl) penta-2, 4-dienoyl)-4-hydroxy-6-methyl-2H-pyran-2-one),是本实验室以脱氢乙酸和有机醛为原料,利用Alodl加成反应,二苯基脯氨醇三甲基硅醚为催化剂合成,其结构如图1所示。前期研究表明PPCl具有良好的抗菌活性,对革兰阳性菌的抑制活性较强,尤其对金黄色葡萄球菌效果明显,MIC值为4μg/mL。其抗菌机制可能是通过破坏细菌DNA结构、抑制胞内酶活性、抑制细菌核酸、蛋白质和ATP等[5-7]。由此可见,PPCl抗菌效果佳,具有良好的开发前景,本实验通过研究该药物的药动学参数,为PPCl进一步研究和开发奠定基础。
1 实验材料
1.1 实验药物和试剂
广藿香酮衍生物PPCl(纯度≥95%,由成都中医药大学药学院韩波教授提供);大黄素对照品(纯度≥98%,批号为150422,成都克洛玛生物科技有限公司);乙腈(色谱级,美国Fisher公司)、甲醇(色谱级,美国Fisher公司)、醋酸铵(色谱级,美国Fisher公司)、水(色谱级,美国Fisher公司)、乙酸乙酯(分析纯,成都市科龙化工试剂厂)。
1.2 实验仪器
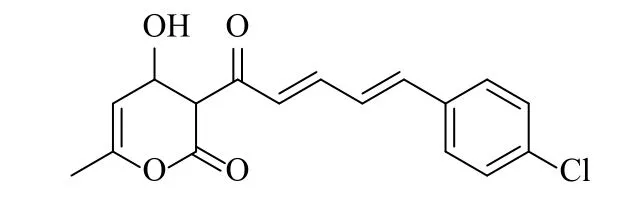
图1 广藿香酮衍生物(PPCl)结构图Fig.1 Structural of pogostone derivative (PPCl)
高效液相色谱仪(Agilent1260型号,包括四元梯度泵,在线脱气机,自动进样器),三重四级杆液质联用仪(Agilent 6410C,包括ESI电离源,Mass Hunter工作站软件系统);电子分析天平(型号BP-211D,德国Sartorius公司);涡旋振荡器(型号:2E-179277,美国Vortex-Genie公司);Allegra X-30系列离心机(型号:ALZ138033,贝克曼库尔特商贸(中国)有限公司);氮气吹扫仪(型号:MD200,杭州奥盛仪器有限公司);超声清洗波器(型号:KQ-5200E,昆山市超声仪器有限公司)。
1.3 实验动物
SD大鼠8只(SPF级,雌雄各半),体重200~220g,成都达硕实验动物有限公司,合格证号:SYXK(川)2015-030。
2 实验方法与结果
2.1 色谱和质谱条件
色谱柱:InfinityLab Poroshell 120 ECC18(3mm×100mm, 2.7μm);保护柱:InfinityLab Poroshell 120 EC-C18(3mm×5mm, 2.7μm);流动相A为5mmol/L醋酸铵水,流动相B为乙腈;梯度洗脱:0~1min:55%乙腈,1~3min:55%~80%,乙腈,3~8min:80%乙腈;流速:0.3mL/min;柱温:25℃;进样量:5μL。
离子源:ESI,负离子模式,以氮气做干燥气,流速:12L/min,脱溶剂温度:300℃,雾化室压力:45.0psi,毛细管电压:4000V,碰撞能量:11V,碎裂电压:90V,扫描方式:多重反应监测模式(MRM)。PPCl和大黄素的检测离子分别为:m/z315→231和m/z268.9→239.8,268.9→224.9。
2.2 溶液的配制
精密称取适量广藿香酮PPCl对照品和大黄素对照品,用甲醇分别稀释溶解定容成浓度为308μg/mL的PPCl贮备液和190μg/mL的大黄素贮备液;用甲醇分别稀释PPCl贮备液和大黄素贮备液,依次配制成:30800、23100、15400、9240、4620、1386、415.8、83.16和33.26ng/mL的PPCl标准工作溶液和浓度为3800ng/mL的内标溶液。
2.3 血浆样品处理方法
分别取50μL内标溶液和50μL PPCl标准工作溶液加入到50μL空白血浆中,混匀后加入1.3mL乙酸乙酯,涡旋混匀3min后,离心(12000r/min,4℃,10min),取上清液,常温下氮气吹干,用流动相复溶后,涡旋1min,超声10s后离心(12000r/min,4℃,10min),取上清液进行分析,进样量:5μL。
2.4 方法和结果
2.4.1 专属性考察
按“2.3”项方法操作,分别制备空白血浆样品、加入PPCl工作溶液和大黄素溶液的血浆样品以及大鼠灌胃给药后的血浆样品,得到色谱图A~C。结果表明PPCl和大黄素的出峰时间分别为6.3min和4.8min,二者分离性良好,血浆中的杂质不影响样品的测定,专属性良好,结果如图2所示。
2.4.2 标准曲线和定量下限
按“2.3”项方法操作,于空白血浆中分别精密加入PPCl工作液和内标溶液,配成浓度为30800、23100、15400、9240、4620、1386、415.8、83.16和33.26ng/mL的血浆样品,内标的血浆浓度为3800ng/mL。以“2.1”项色谱质谱方法测定PPCl的浓度,以PPCl的浓度为横坐标,PPCl与大黄素峰面积的比值为纵坐标做回归运算,得到标准曲线:y=0.0011x+0.0184,r=0.997(权重=1/W1.5)。PPCl在33.26~30800ng/mL范围内线性关系良好,定量下限为33.26ng/mL。
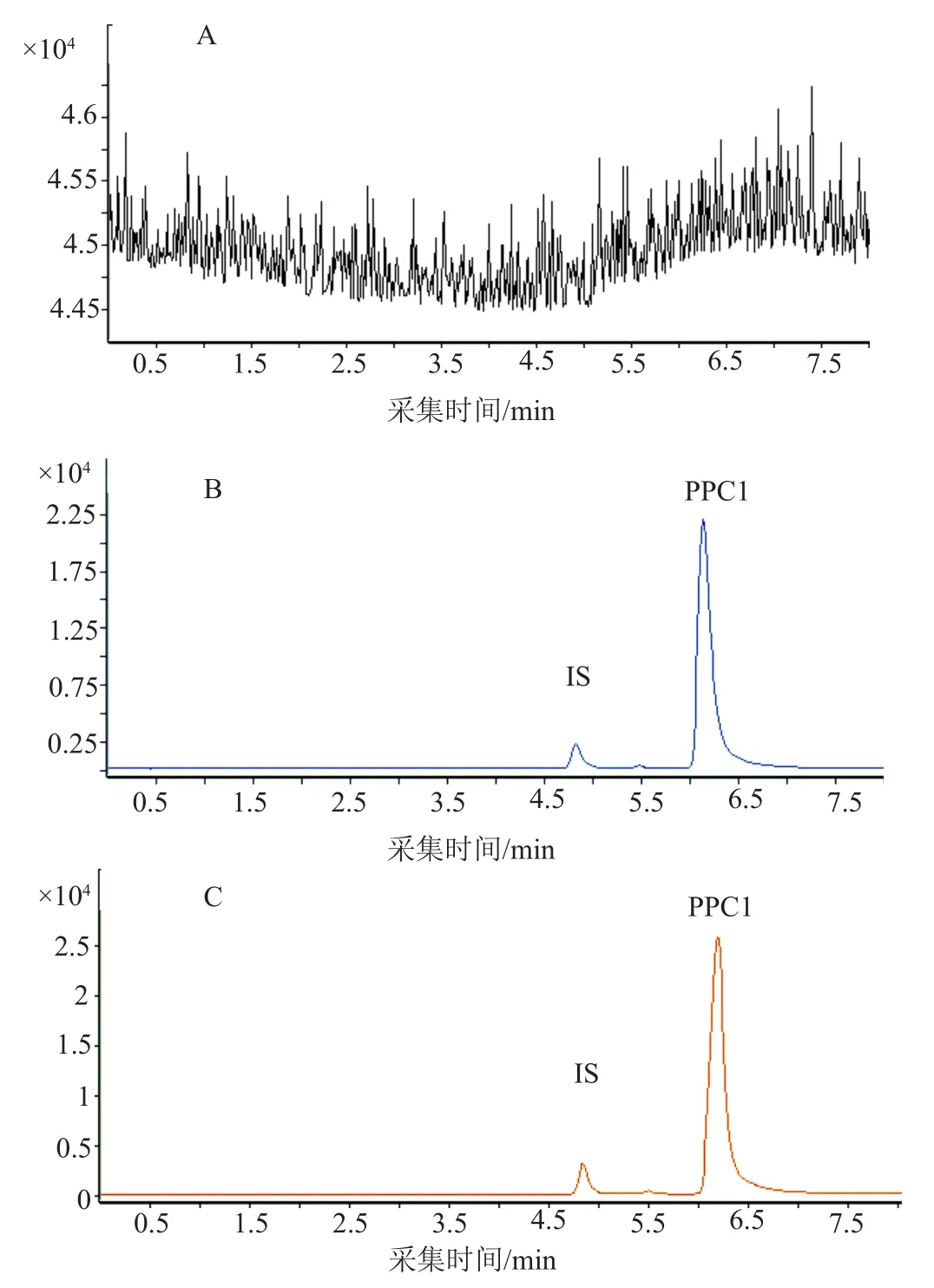
图2 PPCl和内标在大鼠血浆中的MRM色谱图Fig.2 The MRM chromatograms of PPCl and IS in rat plasma
2.4.3 精密度与准确度
按“2.3”项方法操作,在空白血浆中加入浓度为33.26、83.16、4620和23100ng/mL的工作溶液,制备质控样本,每个浓度做6个样本。连续测定3个分析批,计算该方法的日内和日间精密度和准确度,结果见表1。结果表明此方法下PPCl的日内、日间精密度和准确度均符合《药物非临床药代动力学研究技术指导原则要求》。
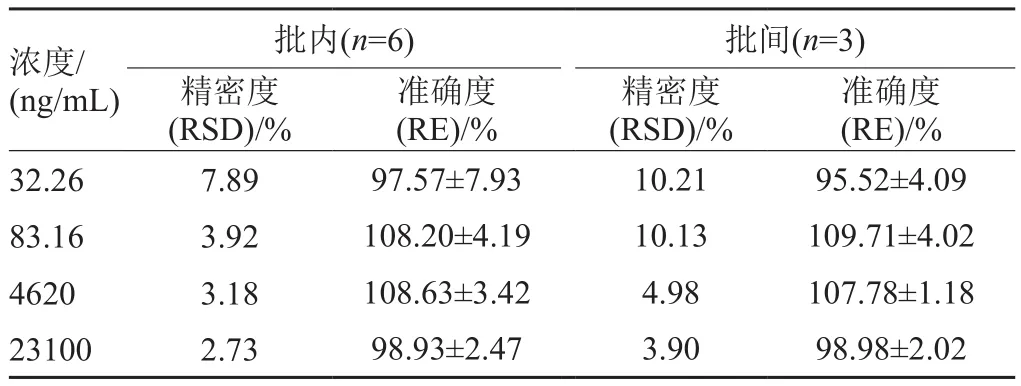
表1 PPCl大鼠血浆样品的精密度和准确度Tab.1 Precision and accuracy for PPCl in rat plasma
2.4.4 提取回收率
按“2.3”项方法操作,分别制备83.16、4620和23100ng/mL 3个浓度的血浆样品,每个浓度5个样本,按照“2.1”项色谱质谱条件下测得PPCl和大黄素的峰面积之比,记为A1;另取空白血浆按照“2.3项处理后,取上清液,加入质量浓度分别为83.16、4620和23100ng/mL的PPCl工作溶液和浓度为3800ng/mL大黄素溶液,每个样品5个浓度,常温下氮气吹干,流动相复溶,涡旋1min,超声10s后离心(12000r/min,4℃, 10min),取上清液进行分析,得到药物和内标的峰面积之比,记为A2;回收率=A1/A2×100%(表2)。
2.4.5 基质效应
于空白Ep管中,分别加入浓度为83.16、4620和23100ng/mL浓度的PPCl的工作溶液和30800ng/mL的大黄素内标溶液,每个浓度5个样本,常温下氮气吹干,流动相复溶,涡旋1min,超声10s后离心(12000r/min, 4℃, 10min),取上清液按照“2.1”项色谱质谱条件测定PPCl与内标的峰面积之比,记为A3;基质效应=A2/A3×100%,结果表明基质对样品的测定无明显影响(表2)。
2.4.6 稳定性考察
按“2.3”项方法操作,分别考察83.16、4620和23100ng/mL 3个浓度的血浆样本于室温下放置12h、经处理后的血浆样本在自动进样器中放置24h(室温)、经3次冻存复溶的稳定性以及在-20℃环境下冰冻放置30d后的稳定性,每个浓度5个样本,结果如表3。

表2 PPCl大鼠血浆样品回收率和基质效应(n=5)Tab.2 Extraction recovery and matrix effect of PPCl in rat plasma (n=5)
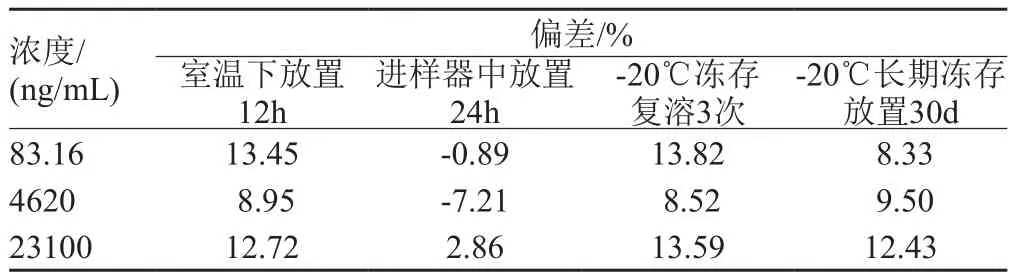
表3 PPCl大鼠血浆样品的稳定性(n=5)Tab.3 The stability of PPCl in rat plasma (n=5)
2.5 方法应用和结果
2.5.1 实验动物和样品处理
选取8只SD大鼠(雌雄各半)单剂量灌胃给予10mg/kg的PPCl,于给药前及给药后0.5、1、3、5、8、10、12 、17、24、36、48和72h眼眶取血0.3mL,置于肝素化离心管中,离心(3500 r/min, 4℃,15min),取上清液血浆,贮藏于-20℃待用。
2.5.2 药动学参数的计算
按“2.3”项方法处理后,以“2.1”项色谱质谱条件检测PPCl的浓度,应用软件:Phoenix WinNonlin 6.3,以非房室模型处理所得数据,得出相关的药动学参数。结果如表4,平均药-时曲线如图3。
3 实验讨论
本研究采用HPLC-MS法对PPCl在SD大鼠血浆中的浓度进行了测定,以与PPCl结构相似的大黄素作为内标,利用乙酸乙酯萃取的方法处理血浆样品,方法专属性高,无内源性杂质影响。其次,在流动相中加入醋酸铵盐,增强药物的离子响应,改善待测物的峰型,提高灵敏度,最低可测浓度达到3ng/mL。本实验采用梯度洗脱程序,提高水相比例,让极性大的内源性物质先出峰,避免杂质影响药物的响应,降低基质效应[8],提高方法的稳定性。
本实验通过对PPCl在大鼠体内药动学研究,首次获得了相应的药动学参数。该药物的半衰期为(14.57±1.93)h,半衰期较长,在体内的滞留时间长,消除缓慢,可能与药物的吸收或者血浆蛋白结合率有关。本实验建立的测定大鼠血浆中PPCl的HPLCMS法,能够满足PPCl药动学的研究,得到的药动学数据为PPCl进一步的研究与开发提供科学依据。
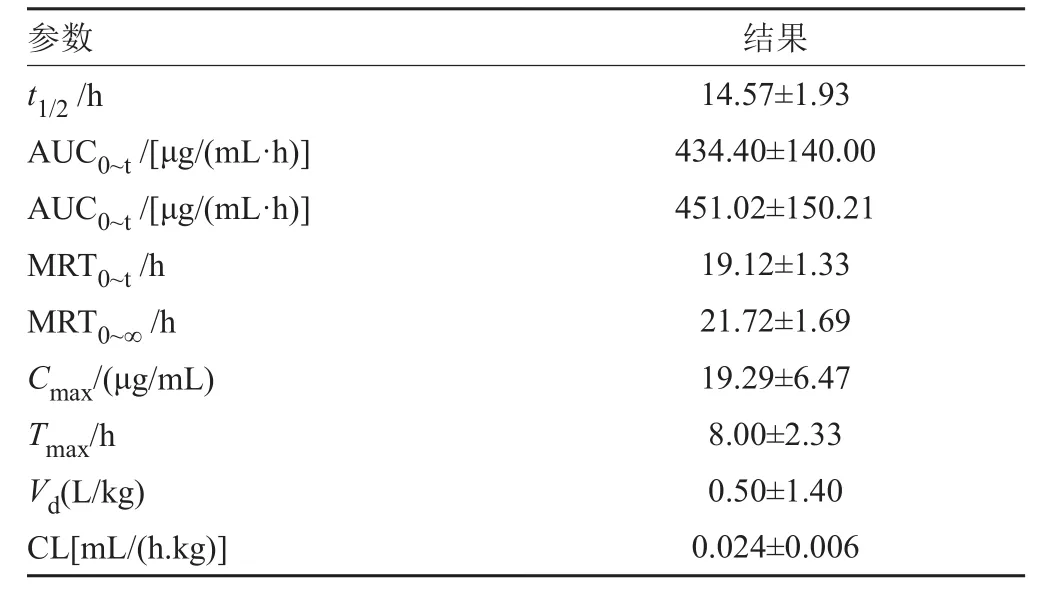
表4 大鼠灌胃给予PPCl的主要药动学参数(x±s , n=8)Tab.4 Pharmacokinetic parameters of PPCl in rats plasma after intragastric administration of 10mg/kg PPCl (x±s , n=8)
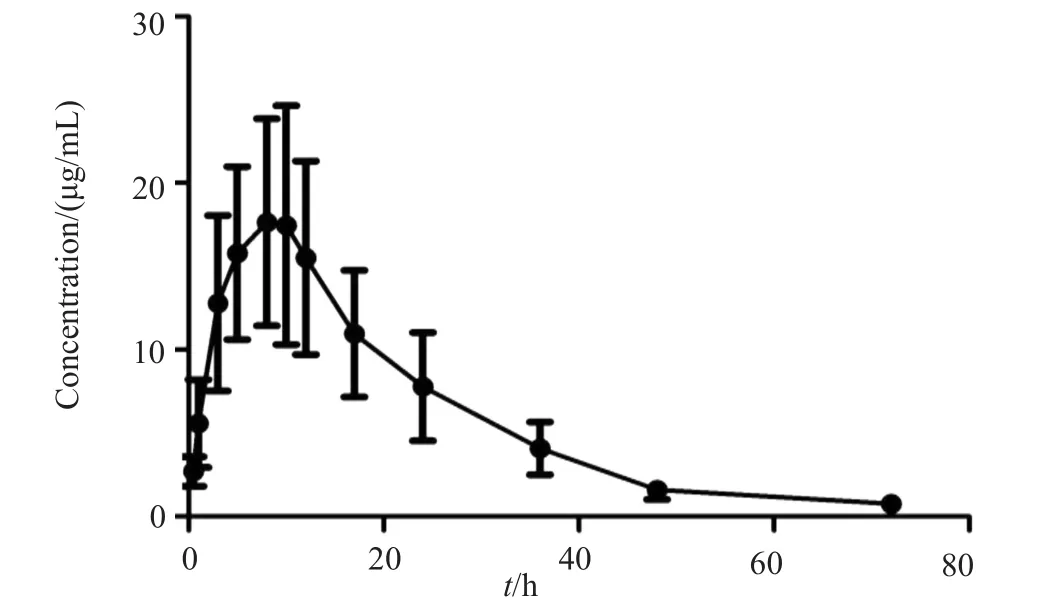
图3 PPCl按10mg/kg灌胃给药后大鼠平均药-时曲线(n=8)Fig.3 Mean plasma concentration-time profiles of PPCl in rats plasma after intragastric administration of 10mg/kg PPCl(n=8)
