氨基功能化金属有机框架的染料吸附研究
2019-05-31辛亮亮孙琪杨琳燕李存马吉飞
辛亮亮 孙琪 杨琳燕 李存 马吉飞

摘 要:金属有机框架(Metal Organic Frameworks,MOFs)因其比表面积较高在染料吸附方面有巨大潜力,试验通过溶剂热法分别合成了MOFs(Gd-BDC)和氨基化MOFs(Gd-NH2BDC)两种单晶材料,二者之间的差异在于辅助配体分别为对苯二甲酸和2-氨基对苯二甲酸;通过单因素试验设计,分析Gd-BDC和Gd-NH2BDC在20 min,40 min,1 h,2 h,3 h,4 h吸附时间序列,以及Gd-NH2BDC在不同pH条件(3.0,7.0,9.0,11.0)下对甲基橙和甲苯胺蓝染料的吸附情況。结果表明,Gd-NH2BDC和Gd-BDC对甲基橙染料的吸附量和吸附百分含量均随着吸附时间的延长波动增加,均于4 h时达到本试验的最大值,其吸附能力后者优于前者,而对甲苯胺蓝染料的吸附量和吸附百分含量分别在吸附40 min和3 h时达到最大值,其吸附能力前者优于后者;Gd-NH2BDC对甲基橙和甲苯胺蓝的吸附能力分别在pH值为5.0和11.0时最高,其吸附百分含量分别为0.977%和70.666%。综合而言,Gd-NH2BDC单晶材料更适宜应用于对甲苯胺蓝染料的吸附,其最佳吸附时间为40 min,最佳pH值为11.0,而Gd-BDC单晶材料在甲基橙染料的吸附中较Gd-NH2BDC有优势,但其吸附时间和pH有待于进一步优化。
关键词:氨基功能化金属有机框架;染料;吸附
中图分类号:X703;O647.33 文献标识码:A DOI 编码:10.3969/j.issn.1006-6500.2019.04.018
Studies on Dye Adsorption of Amino-Functionalized Metal-Organic Frameworks
XIN Liangliang1, SUN Qi2, YANG Linyan2,3, LI Cun2, MA Jifei2
(1. Domestic Discovery Service Unit, Wuxi App Tec Company Limited, Tianjin 300457, China; 2.College of Animal Science and Veterinary Medicine, Tianjin Agricultural University, Tianjin 300384, China; 3.State Key Laboratory for Chemistry and Molecular Engineering of Medicinal Resources, Guangxi Normal University Tianjin, Guilin, Guangxi 541004, China )
Abstract: Metal-Organic Frameworks(MOFs) have great potential for dye adsorption due to their high specific surface area. In this paper, MOFs(Gd-BDC) and MOFs(Gd-NH2BDC) were synthesized by solvo-thermal method, which the ancillary ligands were terephthalic acid and 2-aminoterephthalic acid, respectively. The absorption indices against methyl orange and toluidine blue under different adsorption time series(20 min, 40 min, 1 h, 2 h, 3 h, 4 h) of Gd-BDC and Gd-NH2BDC,and different pH conditions (3.0, 7.0, 9.0, 11.0) of Gd-NH2BDC were analyzed by single factor experimental design. The results showed that with the increase of adsorption time, the adsorption amount and the adsorption percentage of methyl orange by Gd-NH2BDC and Gd-BDC fluctuated increasing, which the maximum value were both appeared at 4 h, the adsorption capacity of Gd-BDC was better than Gd-NH2BDC. However, the adsorption amount and the adsorption percentage of toluidine blue reached the maximum at 40 min and 3 h, respectively, and the adsorption capacity of Gd-NH2BDC was better than Gd-BDC. The adsorption capacity of Gd-NH2BDC against methyl orange and toluidine blue was highest at pH 5.0 and pH 11.0, respectively, and the percent adsorption was 0.977% and 70.666%, respectively. In summary, Gd-NH2BDC was more suitable for the adsorption of toluidine blue, and its optimal adsorption time was 40 min and pH was 11.0, while Gd-BDC was superior to Gd-NH2BDC in the adsorption of methyl orange, but its adsorption time and pH need to be further optimized.
Key words: amino-functionalized metal-organic frameworks; dyes; adsorption
染料是一种能使纤维或其他材料染色的物质,广泛使用的同时产生了大量染料废水,一方面造成染料资源浪费,另一方面由于染料在光照、加热和氧化等日常条件下难以降解,进一步影响水生物光合作用和水生生态系统[1]。目前,处理染料废水的常见方法有吸附法、混凝法、膜分离法、生化法和氧化法等,其中,常用吸附剂有海藻酸钙[2]、炭基材料[3]、沸石[4]、聚合物、金属有机框架(Metal-Organic Frameworks,MOFs)[5]等。MOFs通常具有较高的比表面积,在染料吸附[6]、分离[7]、催化分解[8]等方面具有极大潜力。目前已经制备出了包含有特定官能团(-OH,-NH2和-Br)的一系列MOFs,其中,-NH2修饰的MOFs 凭借对酸性气体的强吸附作用,活性的催化位点以及为进一步的后合成修饰(PSM)提供位点等优势,获得了普遍的关注。
笔者拟用氨基化稀土金属有机框架作为吸附剂,分析其在不同吸附时间和不同pH条件下对2种阴离子型染料甲基橙和甲苯胺蓝的吸附情况,旨在为氨基化MOFs的染料吸附应用提供参考。
1 材料和方法
1.1 试剂和仪器
2种阴离子型染料甲基橙和甲苯胺蓝购自天津市福晨化学试剂厂;2-氨基对苯二甲酸购自济南恒化科技有限公司;4-(3-甲基-5-(吡啶-4-基)-4H-1,2,4-三唑-4-基)苯甲酸(HL)根据文献[9]合成。所用试剂均为分析纯。JASCO-UV-570 UV-vis分光光度计用于记录染料的UV-vis吸收光谱。
试验材料:溶剂热法制备的单晶材料[Gd(L)(NH2BDC)(H2O)2]n·1.5nH2O (即Gd-NH2BDC)和Gd-BDC。
1.2 Gd-NH2BDC和Gd-BDC的制备
Gd-NH2BDC制备:0.135 4 g[Gd(NO3)3·6H2O],0.084 1 g HL,0.108 1 g 2-氨基对苯二甲酸(H2BDC-NH2),7.5 mL水和7.5 mL乙腈混合,加入25 mL水热反应釜中,程控式烘箱1 h内升温至140 ℃,保持5 h,60 h内缓慢降温到25 ℃,产物用10 mL蒸馏水洗涤3次。
Gd-BDC的制备:以0.099 7 g对苯二甲酸(H2BDC)代替0.108 1 g H2BDC-NH2,其余条件与Gd-NH2BDC制备相同。
1.3 染料吸附研究
使用Gd-NH2BDC、Gd-BDC兩种MOFs分别与甲基橙和甲苯胺蓝2种阴离子型染料发生吸附作用,根据剩余染料的紫外吸收值分析2种材料对两种染料的吸附性。
1.3.1 时间对甲基橙/甲苯胺蓝吸附的影响 称取0.2 g Gd-NH2BDC或Gd-BDC于圆底烧瓶中,加入20 mg·L-1甲基橙或甲苯胺蓝溶液100 mL,调节溶液pH值为5.0,预热水浴锅,加热至35 ℃,将圆底烧瓶放入水浴锅。分别在20 min,40 min,1 h,2 h,3 h,4 h时,精确量取5 mL溶液,10 000 rpm离心5 min。离心完毕后,取上清液4 mL,置于另一离心管中,冷藏保存。剩下的1 mL加4 mL 20 mg·L-1的甲基橙或甲苯胺蓝溶液,混匀,倒回圆底烧瓶中,继续加热[10-13]。每个试验设置3个重复。
1.3.2 pH值对甲基橙/甲苯胺蓝吸附的影响 试验分为3组作为3个重复,每组有4瓶同样配置的溶液和吸附剂,包括0.2 g Gd-NH2BDC和20 mg·L-1的甲基橙或甲苯胺蓝溶液100 mL,但每瓶溶液pH值不同,分别为3.0,7.0,9.0,11.0。预热水浴锅,加热至35 ℃。将圆底烧瓶放入水浴锅。加热1 h后,精确量取5 mL溶液,放入离心管中,10 000 rpm离心5 min。取上层清液4 mL置于离心管中,留样冷藏保存。
1.4 样品检测
1.4.1 晶体结构 在BRUKER SMART 1000 型单晶衍射仪上测定单晶结构:选取大小合适的晶体,在-160.15 ℃的低温下,以石墨单色器单色化的Mo-Kα射线(λ = 0.710 73 ?)作为入射光源,采用ω-2θ扫描方式收集衍射点。
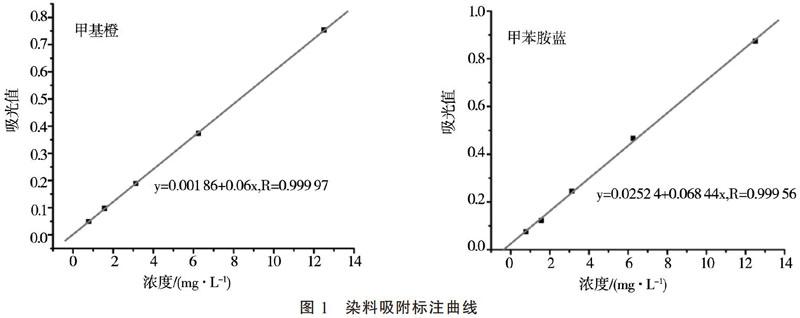
1.4.2 染料吸附 染料吸附标准曲线绘制:甲基橙和甲苯胺蓝浓度均为0.781 25,1.562 5,3.125,6.25,12.5 mg·L-1,染料吸附数据标准曲线(图1)。将试验中的冷藏样品,使用紫外分光光度计测定MOFs材料吸附染料后剩余溶液的最大吸收峰所在的波长,从而可看出2种MOFs吸附2种染料的情况,并记录相应波长下的吸光度,根据标准曲线计算剩余溶液中的染料浓度(Ct),并根据如下公式计算染料吸附量(m)和吸附百分含量(n):
吸附量m=(C0-Ct×t)×V0(1)
吸附百分含量n=100×m/(C0×V0)(2)
式中,C0为溶液初始染料浓度(mg·L-1);Ct为剩余溶液染料浓度(mg·L-1);t为稀释倍数,本试验中t=2;V0为试验用染料的量(L)。
1.5 数据处理与分析
运用SHELXS-97和SHELXL-97程序包对晶体结构进行数据计算,采用Olex2对单晶衍射数据进行解析,并用Diamond软件画图。通过直接法解出晶体结构,并对其坐标及各向异性热参数用全矩阵最小二乘法修正,并用理论加氢法得到氢原子位置。
染料吸附UV-vis光谱图采用Origin8.1软件绘制,吸附量和吸附率采用Microsoft Excel 2010进行计算。
2 结果与分析
2.1 Gd-NH2BDC和Gd-BDC的晶体结构
由于Gd-NH2BDC单晶与Gd-BDC单晶制备过程仅辅助配体上存在细微差别,前者为2-氨基对苯二甲酸,而后者为对苯二甲酸,晶体结构以Gd-NH2BDC为例说明。经X射线单晶衍射仪测定晶体结构,Gd-NH2BDC配合物属于三斜晶系,其主要配体与金属离子形成的单元见图2,辅助配体与金属离子形成的一维结构见图3。NH2BDC2-辅助配体和Gd3+离子连成链,一维链通过双核单元连接成二维结构;或者说双核单元通过相邻的4个NH2BDC2-辅助配体连接成二维结构,Gd-NH2BDC的二维结构见图4。所用辅助配体2-氨基对苯二甲酸为单氨基结构,解析后画出的图上为双氨基结构,原因为N发生了裂分,2个N原子各占1/2权重,见图5。
2.2 Gd-NH2BDC和Gd-BDC吸附甲基橙的研究
由图6可知,Gd-NH2BDC和Gd-BDC对甲基橙的吸收波峰均为469 nm。监测不同吸附时间甲基橙469 nm吸光度,并计算其吸附量(表1)。由表1可以看出,随着吸附时间的延长,Gd-NH2BDC和Gd-BDC对甲基橙染料的吸附量和吸附百分含量均呈波动增加的趋势,均以吸附4 h时达到最大值,其中Gd-BDC对甲基橙染料的吸附量和吸附百分含量在各吸附时间均高于Gd-NH2BDC,说明其对甲基橙染料的吸附能力优于Gd-NH2BDC。
2.3 Gd-NH2BDC和Gd-BDC吸附甲苯胺蓝的研究
由图7可知,Gd-NH2BDC和Gd-BDC对甲苯胺蓝的吸收波峰均为633 nm。监测不同吸附时间甲苯胺蓝633 nm吸光度,并计算其吸附量(表2)。由表2可以看出,随着吸附时间的延长,Gd-NH2BDC和Gd-BDC对甲苯胺蓝染料的吸附量和吸附百分含量均呈波动幅度较大,分别在吸附40 min和3 h时达到最大值,其中Gd-NH2BDC对甲苯胺蓝染料的吸附量和吸附百分含量在各吸附时间均高于Gd-BDC,说明其对甲苯胺蓝染料的吸附能力优于Gd-BDC。
2.4 Gd-NH2BDC在不同pH情况下对甲基橙的吸附研究
由图8可以看出,Gd-NH2BDC在pH值为3时,甲基橙有2个UV吸收峰,与其他pH处理相比较,吸收峰红移;pH值为5时,甲基橙在波长为469nm吸光度最小,为0.596,说明pH值为5为Gd-NH2BDC吸附甲基橙染料的最佳pH值,计算甲基橙吸附量为0.020 mg,吸附百分含量为0.977%。
2.5 Gd-NH2BDC在不同pH情况下对甲苯胺蓝的吸附研究
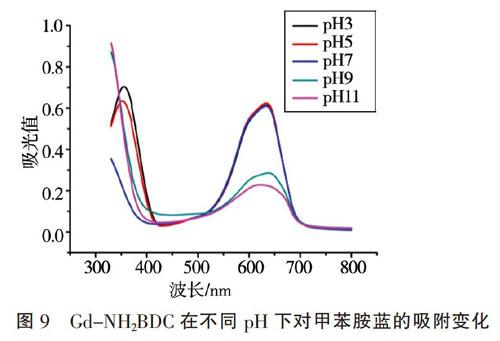
由图9可以看出,Gd-NH2BDC在pH值为3和pH值为5时,甲苯胺蓝有2个UV吸收峰;pH值为11时,甲苯胺蓝在633 nm吸光度最小,为0.226,说明11为Gd-NH2BDC吸附甲苯胺蓝染料的最佳pH值,甲苯胺蓝的吸附量为1.413 mg,吸附百分含量为70.666%。基于文献报道带正电荷的MOFs对阴离子型染料吸附有促进作用[11],Gd-NH2BDC带有未配位氨基,甲基橙为单磺酸根,甲苯胺蓝为二磺酸根,同时,甲苯胺蓝有较大的共轭结构,以及甲苯胺蓝结构式上的羟基,可能有氢键的影响,故其对甲苯胺蓝的吸附能力优于甲基橙。
3 结 论
MOFs因其比表面积较高,可被应用于染料吸附方面[6],本试验根据溶剂热法制备了Gd-NH2BDC和Gd-BDC两种金属有机框架,二者辅助配体分别为2-氨基对苯二甲酸和对苯二甲酸。
甲基橙和甲苯胺蓝均为阴离子型染料,其紫外可见光谱最大吸收波长分别为469 nm和633 nm。本试验中,Gd-NH2BDC和Gd-BDC对甲基橙染料的吸附量和吸附百分含量均随着吸附时间的延长呈波动增加趋势(表1),其吸附能力后者优于前者,吸附4 h时二者均达到本试验的最大值,但其吸附潜力是否仍会随着时间的进一步延长而提高有待于进一步开展研究;Gd-NH2BDC和Gd-BDC对甲苯胺蓝染料的吸附量和吸附百分含量分别在吸附40 min和3 h时达到最大值,其吸附能力前者优于后者。
MOFs对染料的吸附能力受pH影响较大[5],本试验中Gd-NH2BDC对甲基橙的吸附能力在pH值为5时最高,但吸附百分含量较低,仅为0.977%,一方面可能是因为Gd-NH2BDC不适合用于甲基橙染料的吸附,另一方面应该与吸附时间有关;Gd-NH2BDC对甲苯胺蓝的吸附能力在pH值为11时最高,吸附百分含量为70.666%。综合说明Gd-NH2BDC材料更适宜应用于对甲苯胺蓝染料的吸附,而Gd-BDC在甲基橙染料的吸附中优于Gd-NH2BDC,但其吸附时间和吸附pH有待于进一步优化。
参考文献:
[1]QIANG T T, LUO M, BU Q Q, et al. Adsorption of an acid dye on hyperbranched aminated collagen fibers[J]. Chemical engineering journal,2012,197:343-349.
[2]孫亮,郭英杰,夏延致,等. 多胺型染料用于海藻酸钙纤维染色研究[J].染整技术,2017(6):29-32.
[3]DINESH M, KUNWAR P S, VINOD K S. Wastewater treatment using low cost activated carbons derived from agricultural by products——a case study[J]. Journal of hazardous materials, 2008, 3(152): 1045-1053.
[4]MESHKO V, MARKOVSKA L, MINCHEVA M, et al. Adsorption of basic dyes on granular activated carbon and natural zeolite[J]. Water research, 2001, 35(14): 3357-3366.
[5]ABD E H, ZAKI T. Removal of hazardous cationic organic dyes from water using nickel-based metal-organic frameworks[J]. Inorganic chimica acta, 2018, 471: 203-210.
[6]HUANG L J, HE M, CHEN B B,et al. Magnetic Zr-MOFs nanocomposites for rapid removal of heavy metal ions and dyes from water[J]. Chemosphere, 2018, 199: 435-444.
[7]YANG Q X, REN S S, ZHAO Q Q, et al. Selective separation of methyl orange from water using magnetic ZIF-67 composites[J]. Chemical engineering journal, 2018, 333: 49-57.
[8]WEN G, GUO Z G. Facile modification of NH2-MIL-125(Ti) to enhance water stability for efficient adsorptive removal of crystal violet from aqueous solution[J].Colloids and surfaces a: physicochemical and engineering aspects, 2018, 541: 58-67.
[9]YANG L Y, GU W, TIAN J L, et al. 2D lanthanide-based pyridine-substituted triazole benzoate coordination polymers: Structure, optical and magnetic properties[J].Inorganic chemistry communications, 2013, 35: 195-199.
[10]羅敏.氨基化胶原纤维的制备及其对染料的吸附性能研究[D].西安: 陕西科技大学, 2012.
[11]沈婷婷.功能化MIL-101类、UIO-66类MOFs的制备及其对水体中染料、汞和砷的吸附性能研究[D].南昌: 南昌航空大学, 2015.
[12]杜晶晶.纳米孔洞金属-有机骨架的选择性吸附与催化性能研究[D].合肥:安徽大学, 2011.
[13]钟莉,许艳玲,杨雪莲,等.氨基官能化介孔二氧化硅的制备和表征[J].天津农学院学报,2016,23(2):11-14.
[14]GUESH K, CAIUBY C A D, MAYORAL A, et al. Sustainable preparation of MIL-100(Fe) and its photocatalytic behavior in the degradation of methyl orange in water[J]. Crystal growth & design, 2017,17:1806-1813.
[15]HUANG X X, Qiu L G, ZHANG W, et al. Hierarchically mesostructured MIL-101 metalorganic frameworks: supramolecular
template-directed synthesis and accelerated adsorption kinetics for dye removal[J]. Crystengcomm, 2012, 14: 1613-1617.
[16]JI W J, HAO R Q, PEI W W, et al. Design of two isoreticular Cd-biphenyltetra-carboxylate frameworks for dye adsorption, separation and photocatalytic degradation[J]. Dalton transactions, 2018, 47: 700-707.
