水热合成Cs0.32WO3纳米粒子的结构特点及其近红外吸收特性
2018-10-09林树莹张晓强周忠华
林树莹,张晓强,黄 悦,2,周忠华,2*
(1.厦门大学材料学院,2.福建省特种先进材料重点实验室(厦门大学),福建 厦门 361005)
可见光区(380~780 nm)和近红外光区(780~2 500 nm)集中了太阳光的大部分能量,其中,近红外光因其具有明显的热效应,不仅会使人体皮肤产生灼热感,且易造成室内或车内温度升高,导致空调耗能,因此,车窗玻璃和建筑玻璃在保持可见光高透过的同时,应尽可能地屏蔽近红外光.近年来,探究新型的环保热屏蔽材料始终是研究者追求的目标,具有可见光高透过性,同时能有效地吸收或反射近红外光的纳米粉体及功能薄膜材料,在绿色建筑节能和汽车玻璃隔热领域具有十分广阔的应用前景[1].
透明导电薄膜如铟锡氧化物(ITOs)和锑掺杂氧化锡(ATOs)薄膜已应用于透明隔热材料,但它只能隔绝波长大于1 500 nm的近红外光[2].铯钨青铜(CsxWO3, 0 探索环境友好的制备方法和提高隔热性能是铯钨青铜的研究热点.铯钨青铜中W的价态低于+6价,需要在还原气氛下合成.在制备方法方面,Takeda等[4]将铯盐和钨酸铵混合水溶液烘干,然后在H2气氛下经800 ℃高温热处理得到Cs0.32WO3纳米粉体,但该制备工艺繁琐且原材料利用率低;Guo等[5]以氯化钨和氢氧化铯为原料,以乙酸为还原剂,用溶剂热法制备了Cs0.32WO3粉体,然而,原材料氯化钨既昂贵又具有毒性,限制了该制备工艺的发展;Liu等[6]以钨酸钠和碳酸铯为原料,以柠檬酸为还原剂,通过水热法制备了Cs0.32WO3粉体,但是得到的Cs0.32WO3粉体形貌为不规则团聚粒子,其隔热性能有待提高.在提高隔热性能方面,Mattox等[7]指出载流子表面等离子体共振是铯钨青铜具有近红外吸收功能的主要原因,其形貌对局域表面等离子共振(local surface plasmon resonance,LSPR)有重要影响;Liu等[8]进一步通过添加HF,水热合成了F掺杂CsxWO3(0 苹果酸具有两个羧基和一个羟基基团,结构上与柠檬酸相似,但目前尚无以苹果酸为还原剂通过水热法制备Cs0.32WO3粉体的报道.本研究中以钨酸钠和碳酸铯为原料,以D-苹果酸为还原剂,采用水热法成功合成了棒状Cs0.32WO3纳米粒子,并通过共混法将其与SiO2溶胶混合,在玻璃基板上制备了透明隔热涂层,采用X射线衍射(XRD)、扫描电镜(SEM)及紫外-可见-近红外漫反射吸收光谱对其进行表征,考察了粉体结晶度和微观形貌等结构特点对其近红外吸收性能的影响. 先将钨酸钠充分溶于20 mL蒸馏水中,用强酸型苯乙烯阳离子交换树脂进行离子交换,用30 mL蒸馏水冲洗树脂柱获得浓度为0.53 mol/L的黄色钨酸溶液;按照Cs/W比(摩尔比,下同)0.5往溶液中加入碳酸铯,然后添加D-苹果酸调节pH值至1;将所得溶液倒入聚四氟乙烯高压釜中,在175 ℃下水热反应72 h;离心后用去离子水和无水乙醇洗涤沉淀数次,再于80 ℃下干燥2 h;最后使用玛瑙研钵进行研磨得到粉体样品. 在上述实验条件的基础上,分别考察了Cs/W比(0.1,0.2,0.3,0.4,0.5,0.6)和反应时间(24,48,72 h)对合成样品的影响. 为了评估上述样品的近红外屏蔽性能,将2 mL样品的乙醇分散液(固体质量分数为30.8%)和 8 mLSiO2溶胶成膜剂搅拌30 min得到涂料,以商用的、浮法制备的、含铁的钠钙硅酸盐汽车绿玻原片(3.2 mm Solar Green Glass,3.2SG玻璃,福耀集团提供)为玻璃基板,将涂料旋涂(转速为250 r/min,时间为30 s)在基板上,200 ℃下烘干30 min,制得透明隔热玻璃.同时,以不含样品的SiO2溶胶为涂料制备了SiO2溶胶涂层玻璃进行比较.SiO2溶胶成膜剂参照文献[9]的方法制备,由正硅酸乙酯在硝酸的水-乙醇溶液中水解而得,其中添加了3%(质量分数)偶联剂KH560作为黏结剂. 采用Bruker AXS(D8 advance)XRD仪分析样品的晶体结构:Cu Kα(λ=0.154 nm),管电压40 kV,管电流40 mA,使用步进扫描方式,步长0.016 7°,每步停留0.1 s,2θ扫描范围10°~80°.采用日立SU-70 SEM表征样品的形貌,加速电压10 kV.采用Cary 5000可见-近红外分光光度计表征样品的吸光度,测试范围380~2 500 nm,速率600 nm/min.用Perkin Elmer Lambda 950紫外-可见分光光度计检测透明隔热玻璃的紫外-可见-近红外吸收光谱,测试范围250~2 500 nm.采用Quantum 2000型X射线光电子能谱(XPS)仪检测样品的光电子能谱,使用Al阳极靶、扫描式单色器,操作功率23.2 W,样品室真空度<1.33×10-6Pa.利用白光干涉膜厚仪(FTM-Lite UVNIR)检测透明隔热玻璃表面的涂层膜厚. 图1(a)为按照不同Cs/W比制备的粉体样品的XRD谱图.可以看出:Cs/W比为0.1和0.2时,存在六方晶型的Cs0.32WO3(JCPDS No.83-1334)和WO3(JCPDS No.72-2141)两个混合相,这是由于反应体系中Cs浓度较低,未掺杂完全,铯钨青铜结构中自由载流子浓度较低;Cs/W比为0.3~0.6时,样品的衍射峰则与Cs0.32WO3(JCPDS No.83-1334)完全对应,没有多余杂峰,证实其为Cs0.32WO3结构.理论上,Cs0.32WO3粉体的晶粒尺寸、形貌以及结晶度对其吸光性能影响很大.为了更好地对比结晶度,本研究采用衍射峰较少且不与样品衍射峰重合的SiC作为校正标准物,将样品与商用纳米SiC(纯度99.9%)粉体按照1∶2 的质量比混合,再在玛瑙研钵中充分研磨均匀,定量取出混合粉体进行XRD表征,对样品的结晶度进行校正.通过将Cs0.32WO3的主衍射峰(2θ= 27.77°)与校正标准物SiC主衍射峰(2θ=35.7°)对比可以更直观地显示其结晶度的变化.根据校正结果(图1(b))可知,Cs/W比为0.1~0.5时,目标产物Cs0.32WO3的主衍射峰随原料中Cs浓度的增大而增强,说明制备的Cs0.32WO3结晶度随Cs浓度增大而增强,当Cs/W比为0.5时,主衍射峰最为尖锐且强度最高,表明该条件下合成的Cs0.32WO3结晶度最高;当Cs/W比为0.6时,主衍射峰强度开始下降,表明结晶度开始下降. (a) 未经SiC校正;(b) 经SiC校正.图1 不同Cs/W比下合成样品的XRD谱图Fig.1 XRD patterns of the samples synthesized with different Cs/W ratios 图2 不同Cs/W比下合成样品的紫外-可见-近红外漫反射吸收光谱Fig.2 Diffuse reflectance UV-Vis-NIR absorption spectra of the samples synthesized with different Cs/W ratios 图2为原料Cs/W比为0.1~0.6时得到的粉体的紫外-可见-近红外漫反射吸收光谱,可以看出,Cs/W比在0.1~0.5范围内,样品的近红外吸光度(即近红外屏蔽性能)随Cs浓度的增大而增强,Cs/W比为0.5时达到极大值,为1.85,Cs/W比为0.6时则有所下降.近红外屏蔽性能随原料Cs/W比的变化趋势与结晶度的变化趋势一致.随着Cs掺杂量的增加,铯钨青铜结构中的自由载流子含量也逐渐增加,所得Cs0.32WO3的结晶度越高,晶体结构越完整.Cs0.32WO3的近红外吸光度与自由载流子的等离子体共振密切相关[8],随自由载流子浓度增加,其表面等离子体共振效果增强,因此Cs0.32WO3的近红外屏蔽性能增强.Cs/W比为0.5时得到的Cs0.32WO3样品具有高浓度自由载流子,结晶度最高,近红外屏蔽性能最佳;而当Cs/W比为0.6时,其近红外屏蔽性能略低,这可能是由于结晶度较低且过量添加Cs2CO3导致反应活性降低,产生W缺陷所致[10].此外,由于Cs+的离子半径为0.17 nm,钨青铜六方隧道的尺寸为0.163 nm,两者尺寸相近,Cs+可以稳定嵌入六方钨青铜隧道,在形成的铯钨青铜结构中不会轻易流失,所以制得的Cs0.32WO3纳米粉体的化学性能及物理性能均较为稳定[11]. 图3(a)和(b)分别为原料Cs/W比为0.5,以D-苹果酸为还原剂,在175 ℃下,分别反应24,48和72 h合成样品校正前和校正后的XRD谱图.由图3(a)可知,所有样品的衍射峰均与Cs0.32WO3(JCPDS No.83-1334)对应,没有杂峰;利用SiC校正产物结晶度,结果如图3(b)所示,随水热反应时间延长,Cs0.32WO3样品的主衍射峰(2θ=27.77°)逐渐增强,结晶度提高.观察Cs0.32WO3的SEM图发现,反应24 h时出现不规则团聚颗粒(图3(c));反应48 h时不规则颗粒和棒状结构共存(图3(d));进一步延长反应时间至72 h时,不规则颗粒逐渐消失,出现直径约50 nm、长度约1 μm的长棒状结构(图3(e)).结合XRD表征结果证实了具有较大纵横比的Cs0.32WO3的衍射峰强度更高[12]. (a) 产物未经SiC校正的XRD谱图;(b) 产物经SiC校正后的XRD谱图;(c),(d)和(e) 水热反应时间分别为24,48和72 h的SEM图.图3 不同反应时间下合成样品的XRD谱图和SEM图Fig.3 XRD patterns and SEM images of the samples synthesized at different reaction time 图4 不同反应时间下合成样品的紫外-可见-近红外漫反射吸收光谱Fig.4 Diffuse reflectance UV-Vis-NIR absorption spectra of the samples synthesized at different reaction time 图4是原料Cs/W比为0.5,以D-苹果酸为还原剂,在175 ℃下反应24,48和72 h合成的Cs0.32WO3纳米粉体的紫外-可见-近红外漫反射吸收光谱.可以看出:合成的Cs0.32WO3纳米粉体在1 000~2 500 nm波段处具有较强的吸收能力,且随着反应时间的延长,其吸收能力明显增强;另外,水热反应72 h合成的Cs0.32WO3纳米粉体在1 314 nm处具有强烈的吸收,其吸光度接近1.9,而水热反应24 h合成的无定型Cs0.32WO3纳米粉体在此波长的吸光度为1.06,表明棒状结构的生成使Cs0.32WO3的近红外吸光度大幅提高.本研究通过添加D-苹果酸促进棒状结构Cs0.32WO3的生成.苹果酸中的羧基和羟基基团可以与钨酸形成钨氧配合物,从而强烈地与平行于c轴的晶面连结,这种选择性覆盖将驱使晶核添加到其他晶面[13],因此,晶体优先沿着六方晶相生长,产生纳米棒状结构,这也是本研究选择苹果酸作为还原剂的主要原因.因为表面等离子体共振除了受自由载流子浓度的影响,还与纳米结构的微观形貌密切相关[14],表面等离子沿着纳米棒晶体的长度和宽度分别产生纵向和横向共振,棒状结构所产生的等离子体共振效果更强,所以纵横比越大,粉体的吸光度越大[15].综上所述,制备的Cs0.32WO3纳米粉体的吸光度与其结晶度和微观结构等因素密切相关,Cs0.32WO3的近红外屏蔽性能随自由载流子浓度及结晶度提高而增强,并且随纳米棒状形貌的形成而大幅增强. (a) Cs0.32WO3的宽程XPS谱图;(b) 高分辨Cs3d XPS谱图;(c) 高分辨W4f XPS谱图.图5 Cs0.32WO3的XPS谱图Fig.5 XPS spectra of Cs0.32WO3 为了探索合成的Cs0.32WO3棒状纳米粉体(Cs/W比为0.5,以D-苹果酸为还原剂,在175 ℃下水热反应72 h)中元素的化学状态,对其进行XPS分析.图5(a)为Cs0.32WO3的宽程XPS谱图,其中结合能36 eV附近对应W4f能级,284 eV附近对应C1s能级,530 eV附近对应O1s能级,724和738 eV附近对应Cs3d能级[9],说明合成样品中存在W、C、O和Cs 4种元素,而其中C主要来源于测量时仪器和环境等的影响.除上述4种元素特征峰外,并未出现其他元素的特征峰,结合XRD谱图进一步说明合成的样品纯度较高.图5(b)为Cs0.32WO3的高分辨Cs3dXPS谱图,在724和738 eV处的特征峰对应Cs+的3d能级信号,证明Cs+已稳定地掺杂进入钨青铜结构.图5(c)为Cs0.32WO3的高分辨W4fXPS谱图,通过对W4f轨道进行分峰拟合处理,可以看出合成样品中W以W5+和W6+两种状态存在,其中W5+两个峰对应的结合能为34.5和36.7 eV,W6+两个峰对应的结合能为35.8和37.9 eV,与文献[16]一致.通过计算W5+对应的两个拟合峰峰面积与W4f拟合峰峰面积之比,求得产物中W5+/W的原子比为0.36,即CsxWO3中x的取值为0.36,虽然与理论值0.32不完全一致,但这是由仪器误差造成的,属于允许的误差范围. 采用共混法将上述水热合成得到的Cs0.32WO3棒状纳米粉体分散之后与SiO2溶胶混合,旋涂于3.2 mm SG玻璃基底上制备Cs0.32WO3透明隔热玻璃,采用白光干涉膜厚仪测得涂层厚度为4.80 μm.从图6和表1可以看出:未添加Cs0.32WO3的空白SiO2溶胶涂层对玻璃基底的透光性并未产生影响,而Cs0.32WO3透明隔热玻璃不仅保持了较高的可见光透过率(71.6%),并且近红外光透过率大幅降低,仅10.2%,说明添加Cs0.32WO3可以有效改善玻璃基底对光的选择透过性,制备的Cs0.32WO3薄膜具有高透明和高近红外屏蔽性能;此外,Cs0.32WO3透明隔热玻璃在250~2 500 nm波段内的光反射率很低,表明Cs0.32WO3粉体的近红外屏蔽能力是基于吸收而非反射. 图6 空白玻璃(a),SiO2溶胶涂层玻璃(b)和Cs0.32WO3透明隔热玻璃(c)的透过光谱及Cs0.32WO3透明隔热玻璃的反射光谱(d)Fig.6 Transmittance spectra of blank glass(a),glass with SiO2 sol coating(b),Cs0.32WO3 transparent insulated glass(c)and reflectance spectra of Cs0.32WO3 transparent insulated glass(d) 样品TUVTLTNIR空白玻璃26.175.127.5SiO2溶胶涂层玻璃22.475.027.0Cs0.32WO3透明隔热玻璃14.271.610.2 注:T表示透过率,下标UV表示紫外光波段(250~380 nm),L表示可见光波段(380~780 nm),NIR表示近红外光波段(780~2 500 nm). 图7为Cs0.32WO3透明隔热玻璃断面的SEM图,可知涂层厚度约为4.8 μm,与白光干涉膜厚仪测量数据基本一致.由图7可看出:涂层均匀且致密地附着于玻璃基底上,观察区域的涂层厚度均匀;膜层与玻璃之间界面清晰、平整,界面处无明显裂纹、空洞或空隙等缺陷,表明玻璃与膜层之间结合力优异.透明隔热涂层与玻璃基板界面的结合力,根据JIS K 5600-5-6规定方法,采用(1.00±0.01) mm百格刀进行测试,结果如图8所示,100个格子中无一脱落,表明界面结合牢固,与图7结果一致.这是由于Cs0.32WO3透明隔热涂层选用的成膜物的主要成分与玻璃基底的主要成分相同,均为SiO2,SiO2溶胶与玻璃表面之间形成—Si—O—Si— 化学键,在化学键的作用下紧密结合. 图7 Cs0.32WO3透明隔热玻璃断面的SEM图Fig.7 SEM image of the cross section of Cs0.32WO3 transparent insulated glass 图8 Cs0.32WO3透明隔热玻璃涂层的百格刀试验Fig.8 Cross-cut test of the coating of Cs0.32WO3 transparent insulated glass 采用钨酸钠和碳酸铯为原料,以D-苹果酸为还原剂,原料Cs/W比为0.5,在175 ℃下水热反应72 h,成功合成了具有优异的近红外吸收性能的Cs0.32WO3棒状纳米粒子,其近红外吸收能力的提高与结晶度的提高、棒状结构的生成以及自由载流子浓度提高有关.采用合成的Cs0.32WO3棒状纳米粉体制备的透明隔热玻璃保持了较高的可见光透过率,为71.6%,近红外光透过率降低至10.2%,展现出优异的光学选择透过性及近红外屏蔽性能,有望在汽车车窗玻璃及建筑玻璃上得以应用.1 实 验
1.1 纳米粒子的水热法合成
1.2 透明薄膜涂层及隔热玻璃的制备
1.3 测试与表征
2 结果与讨论
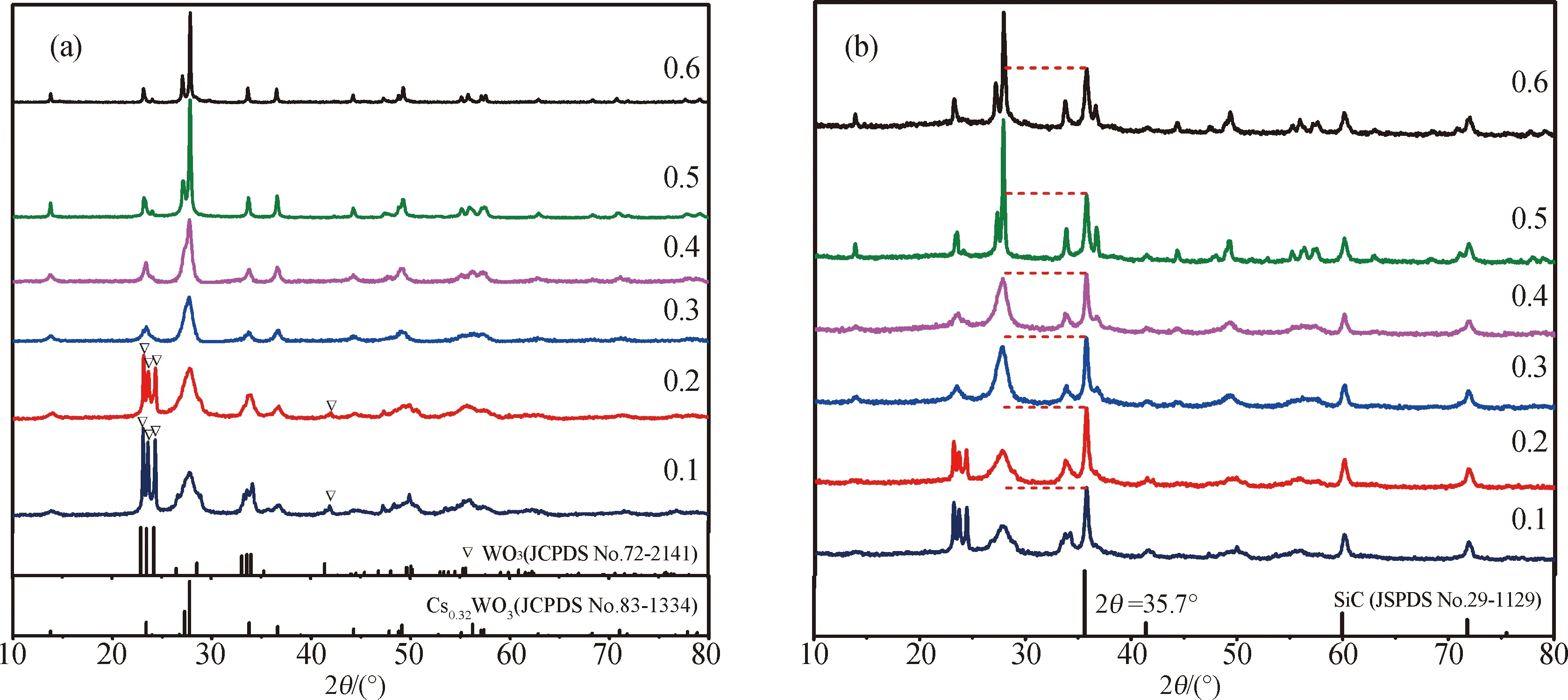
2.1 原料Cs/W比对结晶度和吸光性能的影响
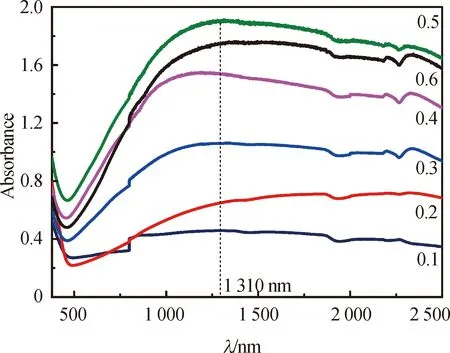
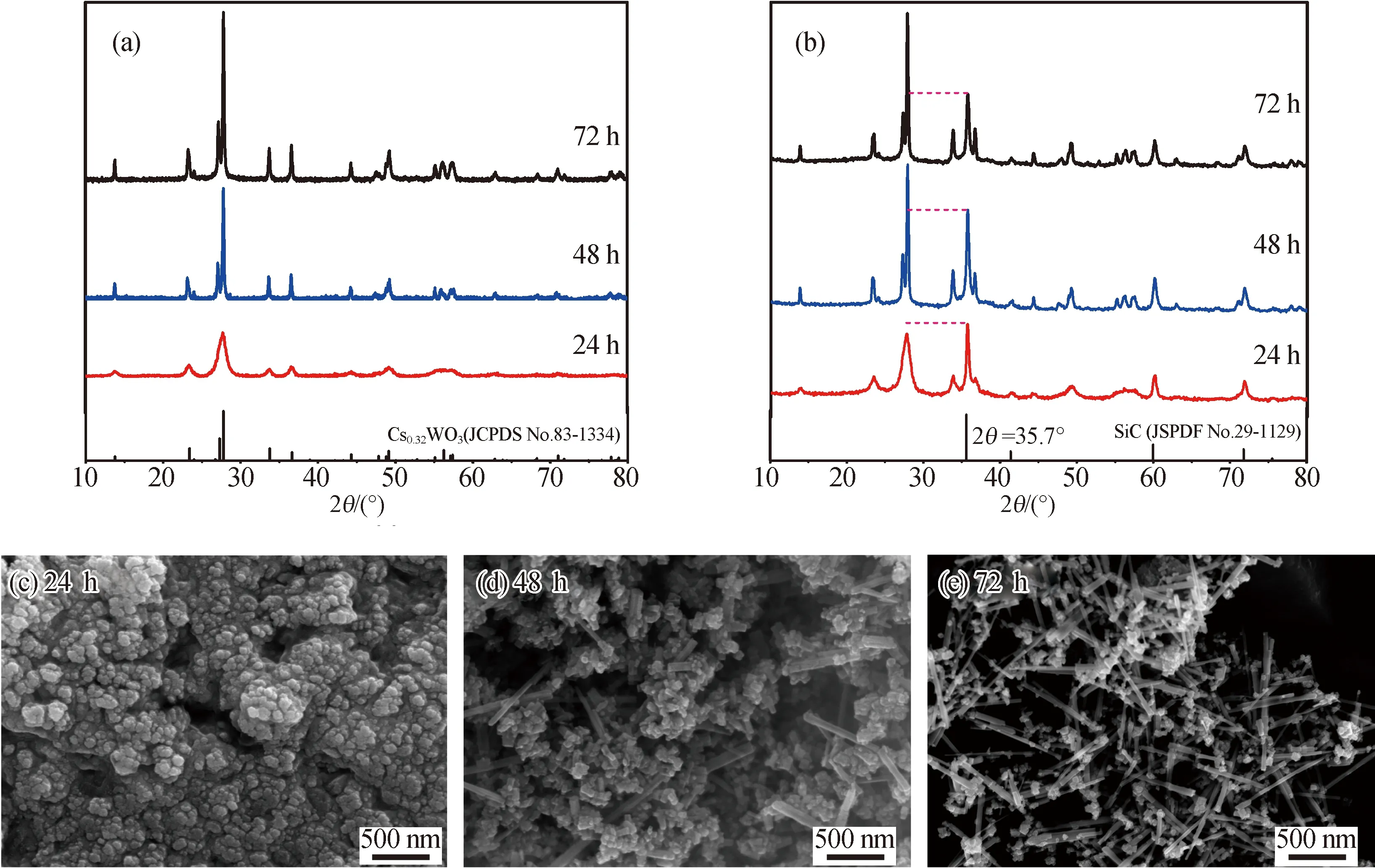
2.2 水热反应时间对微观结构和吸光性能的影响
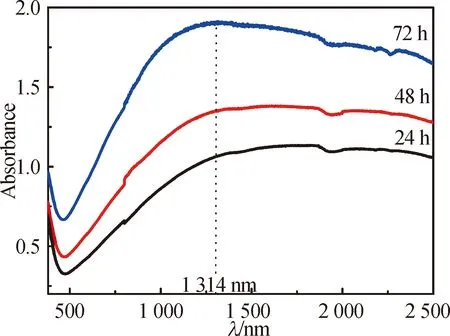
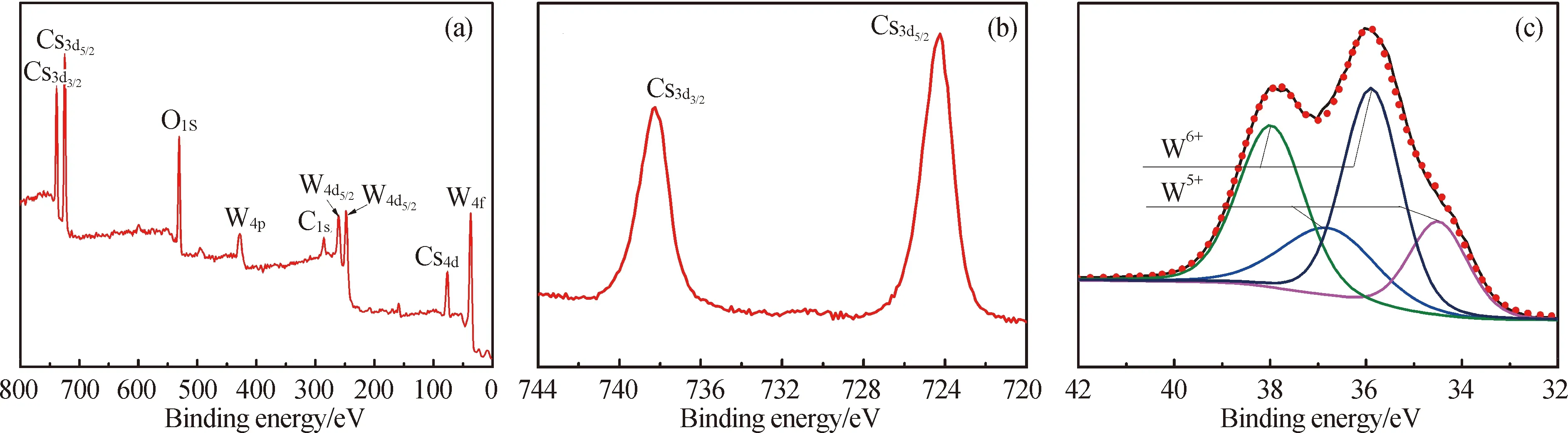
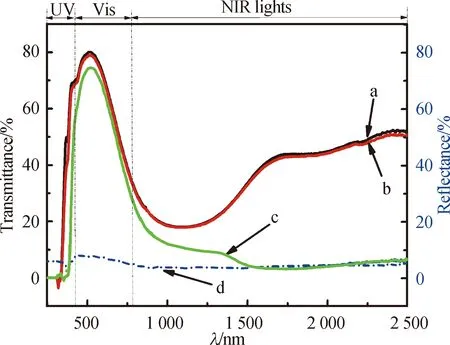
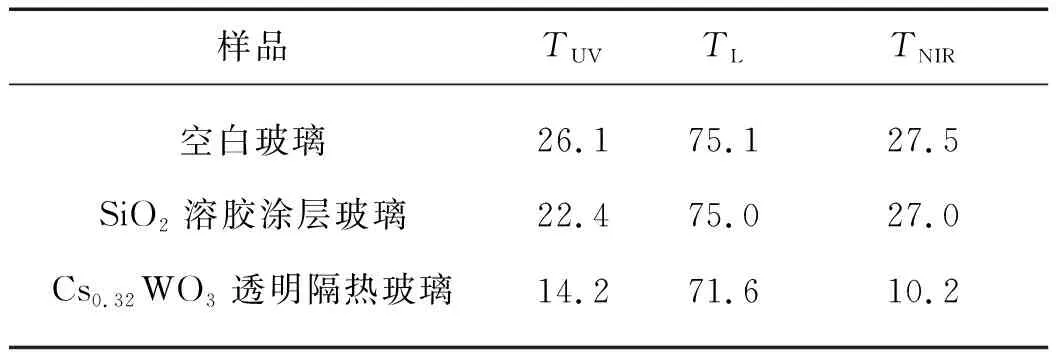
2.3 Cs0.32WO3透明涂层及隔热玻璃的近红外屏蔽性能


3 结 论
