3组常用一线抗HIV药物疗效观察
2018-01-11罗晓璐磨立达魏振满苏国生黄金萍吴景瑜
罗晓璐,磨立达,魏振满,苏国生,黄金萍,吴景瑜
3组常用一线抗HIV药物疗效观察
罗晓璐,磨立达,魏振满,苏国生,黄金萍,吴景瑜
目的通过动态临床试验分析,对广西地区目前常用的AZT、d4T及TDF为主的3组抗反转录病毒治疗方案进行临床疗效比较。方法收治HIV/AIDS患者76例,分为3组,AZT组接受AZT+3TC+EFV治疗,d4T组接受d4T+3TC+EFV治疗,TDF组接受TDF+3TC+EFV治疗。对3组30个月内新发机会性感染率、免疫重建效果、病毒学应答效果、主要生化指标变化、换药及耐药情况进行动态分析比较。结果3组患者经治疗满6个月时HIV RNA载量显著下降(P均<0.05),CD4+T淋巴细胞计数显著上升(P均<0.05),但是3组间差异无统计学意义;6个月以后各组CD4+T淋巴细胞计数上升缓慢,12个月和18个月时,d4T组CD4+T淋巴细胞计数上升幅度均大于AZT组和TDF组(P均<0.05);3组患者治疗满6个月ALB显著升高(P均<0.05),而后各阶段变化不大;AZT组、d4T组、TDF组随访期间新发机会性感染发生率分别为15.62%、11.53%、27.77%,不良反应换药率分别为12.50%、30.80%、16.67%,但差异均无统计学意义。结论广西地区3组常用一线抗HIV药物方案的治疗效果显著且相似,但d4T方案因药物不良反应和耐药而换药的发生率较高,应考虑停用。
HIV/AIDS患者;齐多夫定;司他夫定;替诺福韦;疗效
目前,抗反转录病毒治疗(antiretroviral theraphy,ART)是惟一能够持续、有效抑制HIV复制的治疗方法。但HIV感染者ART后普遍存在免疫重建炎性综合征[1],对药物难以耐受而出现不良反应,影响服药依从性,进而影响对HIV的抑制效果[2]。因此,保证ART理想而持久的疗效成为当前迫切须要解决的问题。目前,国内较常用的一线ART方案包括:齐多夫定(zidovudine,AZT)+拉米夫定(lamivudine,3TC)+依非韦伦(efavirenz,EFV),司他夫定(stavudine,d4T)+3TC+EFV,替诺福韦(tenofovir,TDF)+3TC+EFV。近年来,d4T+3TC+EFV方案不良反应多、耐药率高时有报道,部分地区已停用,然而广西省属于我国发展落后地区,又是我国HIV-1高流行地区,国家提供的免费ART药物较有限,d4T+3TC+EFV仍为本地区十二五国家规划项目的ART方案。本文就3组方案的疗效、安全性、耐药性等进行分析,旨在探讨广西地区AIDS临床治疗的优化方案。
1 资料与方法
1.1 对象 选择2013年4月—2013年6月未曾接受ART且在南宁市第四人民医院就诊的HIV/AIDS患者76例,随访期至2015年12月。其中男57例,女19例,年龄为20~70岁。纳入标准参照《艾滋病诊疗指南(第三版)》[3]。排除标准:①急性感染期患者;②现症机会性感染或相关恶性肿瘤未控制者;③常酗酒者,现吸毒者,或严重胰腺、心、脑、肝、肾等疾病患者;④妊娠期或哺乳期妇女。患者按治疗方案,分为AZT组(n=32)、d4T组(n=26)、TDF组(n=18)。3组患者年龄、性别、民族、婚姻、职业、传播途径、病毒学、免疫学以及生化指标在基线水平差异均无统计学意义。见表1。
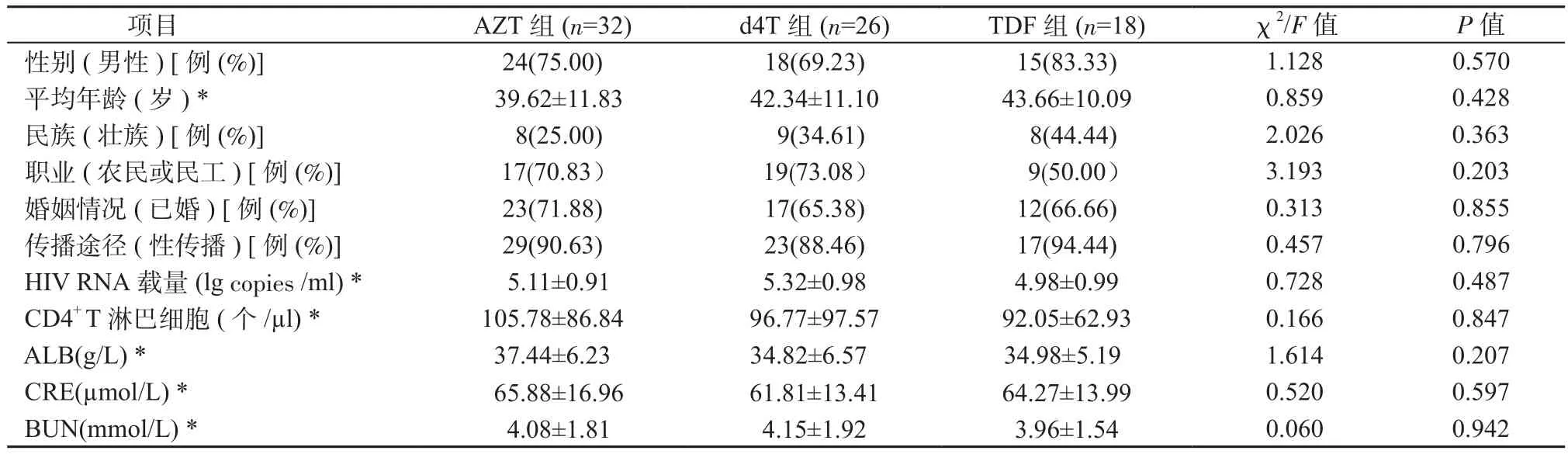
表1 3组患者基线情况Table 1 Baseline information of 3 groups of patients
1.2 仪器与试剂 全自动生化仪(Roche公司,Roche Modular PPE),流式细胞仪(美国BD公司,FACSCalibur),病毒载量仪(Roche公司,COBAS Taqman 48);试剂均由对应仪器公司配套提供,均在有效期内使用。
1.3 方法
1.3.1 治疗方案 将纳入对象分成3组,AZT组:AZT 300 mg,2次 /d;3TC 300 mg,1次 /d;EFV 600 mg,1次 /d。d4T组:d4T 30 mg,2次 /d;3TC 300 mg,1次/d;EFV 600 mg,1次/d。TDF组:TDF 300 mg,3TC 300 mg,EFV 600 mg,各1次/d。其他治疗药物如抗痨、抗真菌感染、降脂、护肝、护肾等药物,用药剂量按照医嘱进行。
1.3.2 观察时间位点及检测方法 对入选患者按基线治疗每满6、12、18、24、30个月进行随访,随访当天上午8时(过夜空腹)抽静脉血标本。采用全自动生化仪测定患者肝、肾功能及电解质等生化指标;利用流式细胞仪检测CD4+T淋巴细胞计数,采用病毒载量仪检测血HIV RNA载量。如血浆HIV RNA载量高于1000 copies /ml,提取RNA,通过反转录及巢式PCR扩增HIV-1pol区基因,用ContigExpress软件将核苷酸序列拼接、校对后,得到pol基因区序列,提交美国斯坦福大学HIV耐药数据库进行比对,确定耐药突变位点和对各种抗病毒药物的耐受程度。
1.3.3 疗效评价 通过CD4+T淋巴细胞计数、HIV RNA载量、主要生化指标等评价疗效。①免疫学有效的标准:ART 3个月后,CD4+T淋巴细胞计数与治疗前相比增加了30%或在治疗第1年后CD4+T淋巴细胞计数增长100个/μl,提示治疗有效。②病毒学治疗成功的标准:ART后3~6个月,HIV RNA载量即可降到小于1.3l lg copies/ml。③病情恢复的依据(生化指标):治疗后ALB较基线有显著升高。④不良反应的依据(CK、BUN及CRE、ALT的改变情况):治疗后CK、BUN及CRE较基线有显著升高。
1.3.4 伦理审查结果 经伦理审查委员会审核,本项目设计方案科学,受试者风险/受益合理,知情同意书符合要求。
1.4 统计学处理 用SASS 9.4进行统计分析。计量资料呈正态分布或近似正态分布,用±s表示。3组间基线比较用单因素F检验(组间方差齐)。3组间计数资料比较用R×Cχ2检验。P<0.05表示差异具有统计学意义。6个月~30个月相关重复计量的指标则应用混合效应线性模型进行重复测量统计分析,共引入简单结构(VC)、复合对称结构(CS)、一阶自回归结构(AR1)、无结构(UN)及空间幂相关结构[SP(POW)]5种协方差结构。5种协方差结构的筛选按如下原则:首先比较各协方差结构模型拟合的AIC值和BIC值,以AIC值或BIC值小者为佳,如果2个或2个以上协方差结构模型拟合的AIC值及BIC值均较小且相接近,则以-2LogL较小的值为最佳模型。当3组整体有统计学差异时(P<0.05),则继续应用混合效应线性模型进行两两比较,α´=α/3,依据P<0.0167的检验水准,差异有统计学意义。
2 结 果
2.1 随访情况 3组治疗满30个月的随访率分别为84.37%、61.53%、77.78%,差异无统计学意义(χ2=4.087,P=0.130)。
在AZT组,1例治疗满6个月出现细菌性肺炎和肠炎,3例治疗满12个月分别出现口腔念珠菌感染、肺部结核感染、重型细菌性肺炎;在d4T组,1例治疗满6个月出现革兰阴性杆菌感染引起的败血症,1例治疗满12个月出现口腔念珠菌感染,1例治疗满30个月出现新型隐球菌血症和卡氏肺孢子菌肺炎;在TDF组,2例治疗满6个月分别出现卡氏肺孢子菌肺炎和重型细菌性肺炎,2例治疗满12个月分别出现马尔尼菲青霉菌引起的皮损和肺部结核感染,1例治疗满18个月出现卡氏肺孢子菌肺炎,其余患者无新发机会性感染。AZT组、d4T组、TDF组随访期间新发机会性感染发生率分别为15.62%、11.53%、27.77%,差异无统计学意义(χ2=2.064,P=0.356)。
AZT组、d4T组、TDF组不良反应换药率分别为12.50%、30.80%、16.67%,差异无统计学意义(χ2=3.163,P=0.208);耐药换药率分别为3.13%、3.84%、0,差异无统计学意义(χ2=0.667,P=0.717)。
d4T组于随访第30个月有1例死亡,死亡原因为继发新型隐球菌血症和卡氏肺孢子菌肺炎;TDF组于随访第30个月有1例死亡,死亡原因为继发弥漫性大B细胞淋巴瘤。见表2。
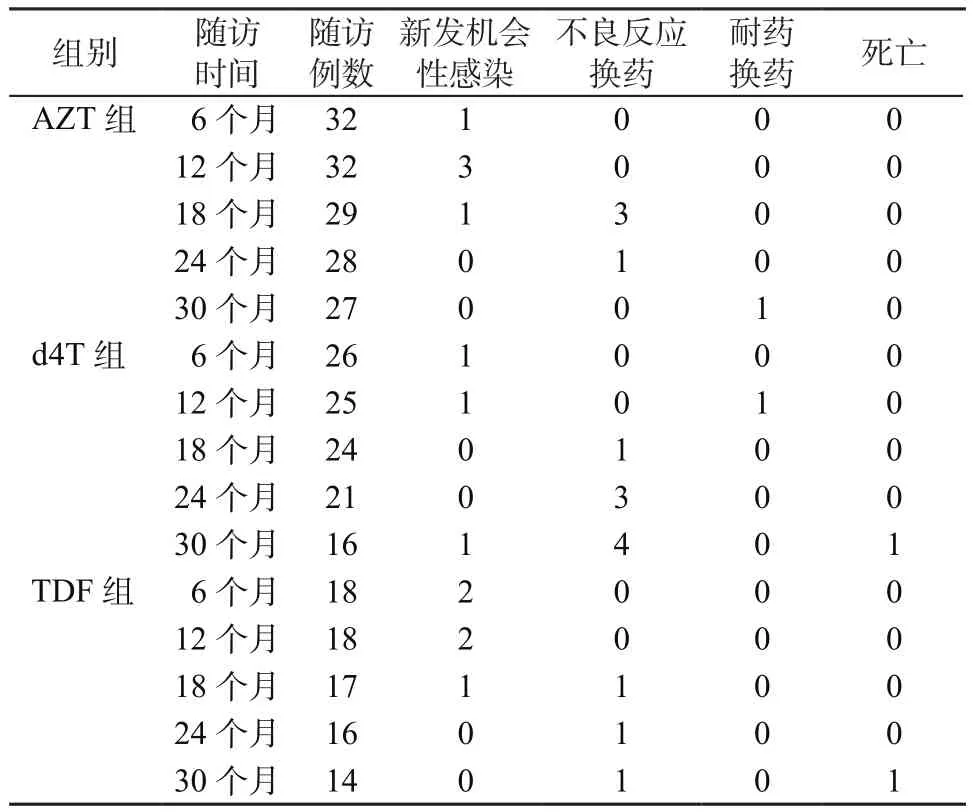
表2 3组治疗后各随访时间新发机会性感染、不良反应换药、耐药换药以及死亡情况(例)Table 2 Number of new opportunistic infections,adverse drug reactions-induced dressing change,drug resistanceinduced dressing changes and deaths at different followup times after treatment in 3 groups(cases)
2.2 治疗效果
2.2.1 病毒学应答 3组患者治疗满6个月时HIV RNA载量较基线显著下降(P均<0.05),但3组差异无统计学意义;6个月后各时间点HIV RNA载量比较稳定,差异无统计学意义,且3组各随访时间点HIV RNA载量差异也均无统计学意义。见表3。
表3 3组各时间点HIV RNA载量(±s,lg copies/ml)Table 3 HIV/RNA loading level in 3 groups at each time points(±s,lg copies/ml)
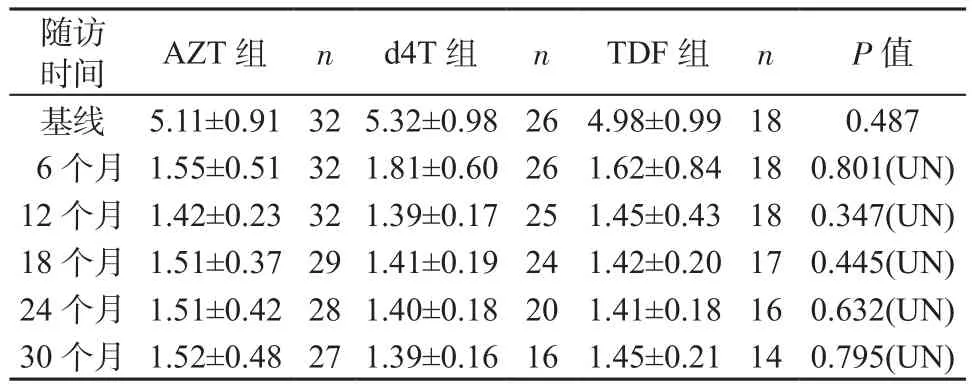
表3 3组各时间点HIV RNA载量(±s,lg copies/ml)Table 3 HIV/RNA loading level in 3 groups at each time points(±s,lg copies/ml)
随访时间 AZT组 n d4T组 n TDF组 n P值基线 5.11±0.91 325.32±0.98 26 4.98±0.99 18 0.487 6 个月 1.55±0.51 321.81±0.60 26 1.62±0.84 18 0.801(UN)12 个月 1.42±0.23 321.39±0.17 25 1.45±0.43 18 0.347(UN)18 个月 1.51±0.37 291.41±0.19 24 1.42±0.20 17 0.445(UN)24 个月 1.51±0.42 281.40±0.18 20 1.41±0.18 16 0.632(UN)30 个月 1.52±0.48 271.39±0.16 16 1.45±0.21 14 0.795(UN)
2.2.2 免疫学应答 3组经治疗后CD4+T淋巴细胞计数显著上升,满6个月时较基线上升最明显(P均<0.05),但3组差异无统计学意义。6个月以后各组CD4+T淋巴细胞计数上升缓慢,12个月和18个月时,d4T组CD4+T淋巴细胞计数上升幅度均大于AZT组和TDF组(P均<0.05)。见表4。
2.2.3 生化指标变化 3组患者治疗满6个月,ALB水平较基线显著升高(P<0.05),但3组间差异无统计学意义,而后各时间点变化不大,差异均无统计学意义。3组CK、CRE、BUN、ALT的平均值均在正常范围,且差异无统计学意义。见表5。但AZT组随访期间CK、CRE、BUN、ALT水平高于正常范围的患者分别为4例(12.50%)、3例(9.38%)、2例(6.25%)、9例(28.13%),d4T组分别为13例(50.00%)、5例(19.23%)、3例(11.54%)、7例(26.92%),TDF组分别为4例(22.22%)、8例(44.44%)、5例(27.78%)、1例(5.55%)。
2.2.4 耐药位点 在治疗满30个月时发现AZT组有1例患者的耐药突变位点为V90IV、V179D、V106M。在治疗满6个月时发现d4T组有1例耐药突变位点为K103KN、V106IMV、G190AG。
2.2.5 药物更换情况 在AZT组,有4例出现无法耐受不良反应,2例为骨髓抑制,1例发生中度肝功能损害,1例出现严重皮疹,均更换为TDF+3TC+EFV。在d4T组,有8例出现无法耐受不良反应,其中2例为外周神经损害,2例为脂肪萎缩,2例血脂严重异常,1例发生严重胃肠道反应,1例出现严重皮疹,均更换为TDF+3TC+EFV。TDF组中3例患者因肾损害、低磷、低钙不良反应被更换为AZT+3TC+EFV。换药后患者病情稳定,服药依从性高,各项生化指标基本正常。
3 讨 论
目前,AIDS的治疗方案以抗病毒药物、免疫调节剂和抗机会性感染药物为主。抗病毒治疗基本上采用核苷(酸)类反转录酶抑制剂(nucleoside reverse transcriptase inhibitors,NRTIs)、非核苷(酸)类反转录酶抑制剂(nonnucleoside reverse transcriptase inhibitors,NNRTIs)及蛋白酶抑制剂(protease inhibitor,PIs)3类药物来控制HIV的复制和预防耐药的产生[4]。临床上通常采用联合疗法 ,包括2种NRTIs和1种NNRTIs或者 PIs。
表4 3组各时间点CD4+ T淋巴细胞计数(±s,个/μl)Table 4 CD4+ T lymphocyte counts in 3 groups at each time point (±s,cells/μl)
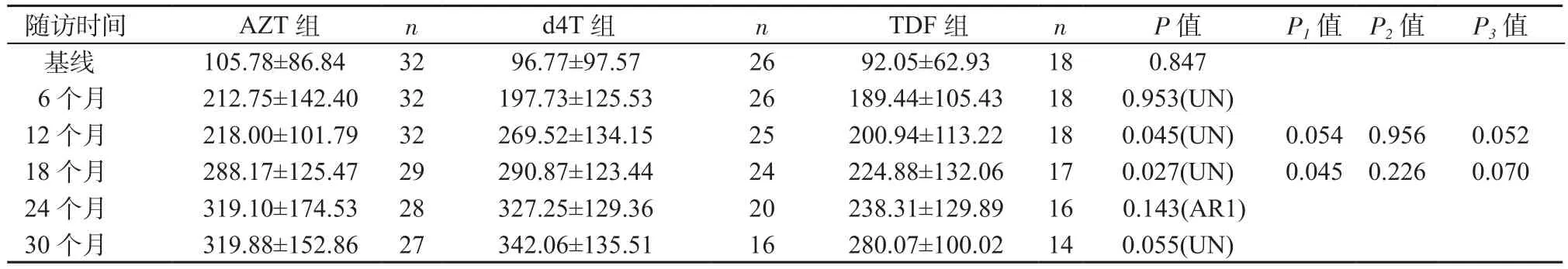
表4 3组各时间点CD4+ T淋巴细胞计数(±s,个/μl)Table 4 CD4+ T lymphocyte counts in 3 groups at each time point (±s,cells/μl)
注:P1、P2、P3分别是AZT组与d4T组、AZT组与TDF组、d4T组与TDF组间比较的差异值
随访时间 AZT组 n d4T组 n TDF组 n P值 P1值 P2值 P3值基线 105.78±86.84 32 96.77±97.57 26 92.05±62.93 18 0.847 6 个月 212.75±142.40 32 197.73±125.53 26 189.44±105.43 18 0.953(UN)12 个月 218.00±101.79 32 269.52±134.15 25 200.94±113.22 18 0.045(UN) 0.054 0.956 0.052 18 个月 288.17±125.47 29 290.87±123.44 24 224.88±132.06 17 0.027(UN) 0.045 0.226 0.070 24 个月 319.10±174.53 28 327.25±129.36 20 238.31±129.89 16 0.143(AR1)30 个月 319.88±152.86 27 342.06±135.51 16 280.07±100.02 14 0.055(UN)
表5 3组各时间点生化指标(±s)Table 5 Biochemical indices in 3 groups at each time point (±s)
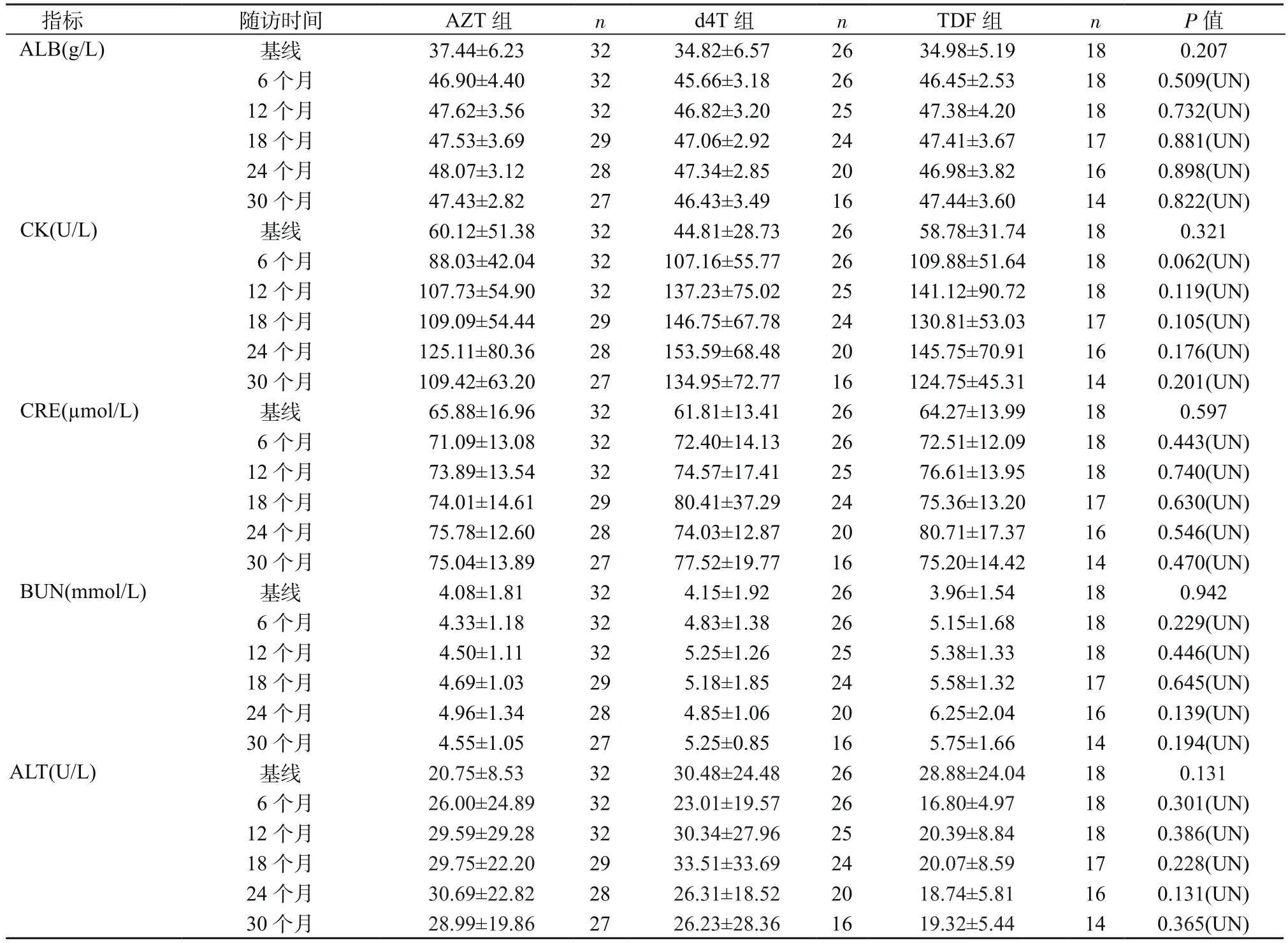
表5 3组各时间点生化指标(±s)Table 5 Biochemical indices in 3 groups at each time point (±s)
?
本研究显示,3组HIV/AIDS患者经过ART后,血浆中病毒载量呈下降趋势,治疗满6个月下降最明显,超过85%的病例在随后的治疗中已检测不出病毒,提示6个月后已进入平台期。由此表明ART能有效地控制HIV在体内的复制 ,使之几乎达到检测不出的水平,其传播风险大大降低。从免疫学应答来看,3组患者治疗满6个月和12个月时CD4+T淋巴细胞计数的增幅明显,提示ART后1年效果良好,与有关报道相符[5]。此后CD4+T淋巴细胞计数增幅不大,虽然病毒载量控制在较低水平,但是没有获得理想的免疫重建,其机制可能与胸腺T淋巴细胞生成减少和持续免疫激活,CD4+T淋巴细胞破坏增加有关[6]。
本研究还显示,3组治疗满6个月的ALB水平较基线明显升高(ALB在治疗前和治疗期间均在正常值范围),以后保持在正常值范围。提示3组患者经ART 6个月后病情恢复快,且病情较稳定,实施个体化精确治疗收到成效。另外,给予患者抗真菌、细菌药物,患者机会性感染能得到有效控制,肝功能逐渐恢复至正常,腹泻、恶病质等并发症得到控制,营养状况得到改善。本研究经耐药基因分析发现,在治疗满30个月发现AZT组有1例耐药突变位点为V90IV、V179D、V106M,在治疗满6个月发现d4T组有1例耐药突变位点为K103KN、V106IMV、G190AG,可能与患者携带原发耐药株有关[7]。但总体上,3组患者耐药率不高,说明定期病毒载量检测、个体化关爱服务等措施落实到位。
另外,3组不良反应换药率差异虽然无统计学意义,但d4T组换药率较高,达30.80%,主要不良反应为骨髓抑制、胃肠道反应、外周神经损害、血脂异常严重、严重皮疹等。2015年《艾滋病诊疗指南(第三版)》[3]已计划将一线抗病毒治疗方案中的d4T更换为AZT,对于不能耐受AZT的患者可选用TDF。
综上,广西地区3种常用一线抗HIV药物方案均能获得有效的病毒学应答和免疫学应答,但是d4T方案因药物不良反应换药率较高,应考虑停用。HIV RNA、CD4+T淋巴细胞、主要生化指标及耐药基因分析是进行ART中非常重要的考核指标,通过对接受不同治疗方案的HIV/AIDS患者进行动态监测,能及时判断HIV RNA的抑制率、机体免疫系统的改变、生理调控系统的变化、不良反应的严重性、耐药率,可为广西地区建立规范AIDS精确化诊断方法和优化临床治疗方案提供参考。
[1]史继静,张昕,徐若男,等.细胞治疗与AIDS功能性治愈[J].传染病信息,2015,28(6):265-270.
[2]杨文杰,樊盼英,梁妍,等.2008—2013年河南省艾滋病患者抗病毒治疗对HIV的抑制效果及其影响因素分析[J].中华预防医学杂志,2015,49(1):13-20.
[3]中华医学会感染病学分会艾滋病学组.艾滋病诊疗指南(第三版)[J].中华传染病杂志,2015,33(10):577-593.
[4]孙永涛,王临旭.AIDS的高效抗反转录病毒治疗指南解读[J].传染病信息,2010,23 (6):329-332.
[5]姜明东,夏永惠,曲文才,等.德州市2005—2015年艾滋病免费抗病毒治疗效果及影响因素评价[J].中国艾滋病性病,2016,22(11):856-859.
[6]Li T,Wu N,Dai Y,et al.Reduced thymic output is a major mechanism of immune reconstitution failure in HIV-infected patients after long-term antiretroviral therapy[J].Clinical Infectious Diseases,2011,53(9):944-951.
[7]宋映雪,辛若雷,叶军,等.北京地区未经抗病毒治疗的HIV感染者HIV-1毒株耐药基因变异研究[J].中国艾滋病性病,2015,21(10):836-838.
Study of curative effect accuracy among 3 groups of commonly used anti-HIV drugs
LUO Xiao-lu,MO Li-da*,WEI Zhen-man,SU Guo-sheng,HUANG Jin-ping,WU Jing-yu
Clinical Laboratory,the Fourth People's Hospital of Nanning,530023,China
*Corresponding author,E-mail:1773398578@qq.com
ObjectiveTo compare clinical curative effect of 3 ART regimens in Guangxi region through a dynamic clinical trial analysis.MethodsSeventy-six HIV/AIDS patients were included in this study and randomly divided into 3 groups.AZT group was treated with AZT+3TC+EFV.The d4T group
d4T+3TC+EFV treatment.TDF group received TDF+3TC+EFV treatment.The incidence of opportunistic infections,immune reconstitution,virological response,changes of major biochemical indexes,dressing change and drug resistance were dynamically analyzed and compared in 3 groups within 30 months.ResultsThe HIV-RNA loading was significantly decreased in 3 groups at 6 months of treatment (P<0.05),while the levels of CD4+T lymphocytes increased significantly (P<0.05),but there was no significant difference among 3 groups.After 6 months of treatment,CD4+T lymphocytes increased gradually in 3 groups.At 12 and 18 months,the increment of CD4+T lymphocytes in d4T group was more significant than that in AZT group and TDF group (P<0.05).The ALB level in 3 groups increased significantly at 6 months of treatment (P<0.05),and then the change was not obvious at subsequent time points.The incidence of opportunistic infections was 15.62% in AZT group,11.53%in d4T group,27.77% in TDF group.The dressing change rate was 12.50% in AZT group,30.80% in d4T group and 16.67% in TDF group,respectively,however no significant difference was observed.ConclusionsThree first-line anti-HIV drug regimens commonly used in Guangxi area have significant and similar effects,but the rate of dressing change for d4T regimen is higher due to adverse drug reactions and drug resistance,so this regimen is recommended to withdraw.
HIV/AIDS patients; zidovudine; stavudine; tenofovir; curative effect
R512.91
A
1007-8134(2017)06-0342-05
10.3969/j.issn.1007-8134.2017.06.007
南宁市兴宁区科学研究与技术开发项目(2015A15);十三五国家重大新药创制课题(2017ZX09009070-001-008)
530023,南宁市第四人民医院检验科(罗晓璐、磨立达、苏国生),艾滋病科(黄金萍);100039 北京,解放军第三〇二医院药学部(魏振满);530002,南宁市兴宁区疾病预防控制中心艾滋病科(吴景瑜)
磨立达,E-mail:1773398578@qq.com
(2017-08-23收稿 2017-10-16修回)
(本文编辑 闫晶晶)
