Fe3O4@碳/氧化石墨烯复合材料制备及染料吸附性能
2017-01-19吴日良刘云芳石向辉迟伟东黄启谷喻长远田小军北京化工大学化工资源有效利用国家重点实验室北京00029北京化工大学碳纤维及功能高分子教育部重点实验室北京00029北京化工大学生命科学与技术学院北京00029
吴日良,刘云芳,2*,任 森,石向辉,2,迟伟东,黄启谷,2,喻长远,田小军(.北京化工大学,化工资源有效利用国家重点实验室,北京 00029;2.北京化工大学,碳纤维及功能高分子教育部重点实验室,北京 00029;.北京化工大学生命科学与技术学院,北京 00029)
Fe3O4@碳/氧化石墨烯复合材料制备及染料吸附性能
吴日良1,刘云芳1,2*,任 森1,石向辉1,2,迟伟东1,黄启谷1,2,喻长远3,田小军3(1.北京化工大学,化工资源有效利用国家重点实验室,北京 100029;2.北京化工大学,碳纤维及功能高分子教育部重点实验室,北京 100029;3.北京化工大学生命科学与技术学院,北京 100029)
采用水热法合成了四氧化三铁@碳/氧化石墨烯(Fe3O4@C/GO)复合材料,并利用XRD、TEM、VSM等对其结构与性质进行了表征,进一步研究了其对水中染料的吸附性能.研究结果表明,Fe3O4比较均匀地分散在GO上;在实验范围内,随着GO用量、罗丹明B初始浓度或吸附温度的提高,Fe3O4@C/GO复合材料对罗丹明B染料的饱和吸附量均相应地增加;而且高GO用量条件下所制备的复合材料的吸附速率更快;随着pH值在2~11范围内增加,复合材料的饱和吸附量先增大后降低,pH值为7时达到最大值.对于GO和Fe3O4质量比为0.8的条件下所制备的Fe3O4@C/GO复合材料,当罗丹明B初始浓度为1000mg/L,其饱和吸附量可达到303.4mg/g.
四氧化三铁;碳;氧化石墨烯;染料;吸附
染料污染带来的水体安全问题已引起广泛关注[1].染料废水的处理方法很多,如生物法、离子交换法、光降解法、化学絮凝法和吸附法等[2-4].其中,吸附法常用于处理难生物降解的污染物,而且也是废水深度处理的重要技术.吸附剂的优良决定了吸附处理效果.研究报道的吸附剂有碳纳米管[5]、粘土矿物[6]、粉煤灰[7]、聚合树脂[8]、生物炭[9]等.如何获得优良的吸附剂仍然是相关领域的研究重点和热点.磁性吸附材料由于既具有良好的吸附能力,又具有从污染物中快速分离的特性,引起了人们的广泛关注[10-12].研究者通过各种方法制备Fe3O4@碳(Fe3O4@C)复合材料,并进行了水中污染物的吸附研究.研究结果表明,Fe3O4@C复合材料的吸附性能与其表面积、孔径和Fe3O4的结构与用量有关[12-13]. Fe3O4@C复合材料具有合成原材料易得、无毒、合成方法简单的特点,而且吸附过程中不引入对水体有害的物质,因此有望成为重要的吸附材料.
石墨烯作为一种新型碳材料因其巨大的比表面积和良好的表面可修饰性使其可以成为优良的吸附材料[14-16],但面临着难以回收、重复利用率低的问题,而其与Fe3O4复合后,则赋予其良好的磁性分离和回收再生特性,可以充分发挥两者的优势. 研究者采用溶剂热法和水热法等方法制备出氧化石墨烯/Fe3O4复合材料(GO/Fe3O4),并进行染料吸附研究,其结果表明复合材料对染料具有很好的吸附能力[17-19].
本文以GO、共沉淀法Fe3O4和可溶性淀粉为原料,通过水热法制备出Fe3O4@C/GO复合材料.淀粉基生物质碳将Fe3O4包覆并固定于GO平面.这样既可以保持了GO和生物质碳的大比表面积和多孔结构特性,又可以稳定Fe3O4,使其不容易脱落,而且不被氧化而失去磁性,从而扩大了复合材料的应用范围.本文对所制备复合材料的结构和RhB吸附性能进行了研究.
1 材料与方法
1.1 实验材料
氯化铁AR级、氢氧化钠AR级、可溶性淀粉AR级,北京现代东方精细化学品有限公司;硫酸亚铁AR级,罗丹明B(AR级),天津市光复精细化工研究所;GO(自制)[20].
1.2 Fe3O4@C/GO材料的制备
Fe3O4纳米颗粒通过共沉淀法制备:1)称取FeCl3·6H2O(40mmol)和FeSO4·7H2O(20mmol)溶于300mL去离子水中,称取NaOH(160mmol)也溶于300mL去离子水中(Fe3+:Fe2+:OH-=2:1:8),配好的溶液通氮气30min以除氧;2)用恒流泵将Fe离子溶液加入NaOH溶液中,流速为5mL/min,混合后立即发生反应,整个过程持续通氮气保护;3)反应结束后,所得产物用水和乙醇洗涤数次,直至pH为中性,然后60℃真空干燥24h,得到Fe3O4纳米颗粒.
采用水热法制备Fe3O4@C/GO材料:1)称取制备的0.65g Fe3O4、3g可溶性淀粉和一定量的GO,加入50mL去离子水中,超声处理10min,并充氮气除氧15min;2)所得混合物转移至水热反应釜中,加热到180℃反应20h;3)待反应结束后,所得产物水洗和乙醇洗若干次,真空干燥后待用.
1.3 Fe3O4@C/GO材料吸附罗丹明B实验
0.05 g吸附剂分散在100mL不同浓度的RhB溶液中,定时取样,磁场分离后取上清液,采用紫外可见分光光度计(TU1810,北京普析通用仪器有限责任公司)在RhB最大吸收波长552nm测定其浓度.不同时间的吸附量qt(mg/g)通过下式计算:
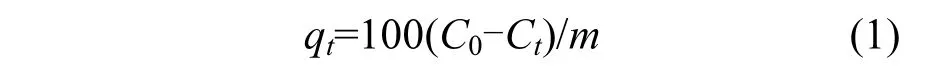
式中:C0为染料起始浓度,mg/L;Ct为吸附后剩余浓度,mg/L;m为吸附剂质量,g.饱和吸附量同理计算[15].实验流程图如图1所示.

图1 实验流程示意Fig.1 Experimental schematic illustration
1.4 材料表征
采用日本理学X射线衍射仪(Riguka D/max-2400型,激发源为CuKa靶,λ =0.15418nm,40kV,200mA,石墨单色器,X-射线计数为闪烁计数器)对材料进行物相分析;采用透射电子显微镜(TEM,日立H-800型)表征吸附剂的微观结构与形貌;采用振动样品磁强计(美国LakeshOre 7307vsM)测试样品的室温磁滞曲线;采用BK100C型比表面积及孔隙度分析仪(北京精微高博科学技术有限公司)进行N2吸附-脱附实验,通过BET(Brunauer-Emmet-Teller)模型计算样品的比表面积,通过DFT(density functional theory)理论来计算孔径分布;采用ESCALAB 250型X射线光电子能谱仪(美国THERMO VG公司)对材料元素及表面含氧基团含量进行分析;采用ZetaPALS型Zeta电位仪(美国布鲁克海文仪器公司)对材料的等电点进行测试并确定.
2 结果与讨论
2.1 吸附剂结构
图2为样品的XRD衍射曲线.Fe3O4的衍射图在30.0°(220),35.2°(311),42.9°(400),56.9°(511)和62.5°(440)有衍射峰,与反尖晶石结构的Fe3O4(JCPDS卡片序号03-0863)数据相一致,没有杂峰,峰强且尖锐.GO在24.8°左右有一个宽的衍射峰.Fe3O4@C复合材料的衍射曲线只能看到明显的Fe3O4衍射峰,说明所含碳组分为无定形结构,Fe3O4@C/GO复合材料在24.8°左右出现GO的衍射峰,而且衍射峰强度随着GO添加量的增大而增强.

图2 材料的XRD衍射图Fig.2 X-ray diffraction patterns of samples
图3为样品的TEM照片.共沉淀法合成的Fe3O4纳米颗粒的平均粒径为12nm,碳包覆后Fe3O4颗粒分散均匀.图3(b)-(d) 为不同GO/ Fe3O4配比条件下所制备Fe3O4@C/GO复合材料的TEM照片.结果显示,Fe3O4纳米颗粒负载于片状结构的GO上,而且随着GO用量的增大,单片GO上的Fe3O4纳米颗粒减少.样品在清洗过程中经过了长时间的超声处理,但是Fe3O4颗粒仍然良好地负载于GO而没有脱落.结果清楚地表明,通过淀粉基碳的包覆及其与GO的良好结合将Fe3O4颗粒牢固地固定在GO上.

图3 样品的TEM照片Fig.3 TEM images of samples
图4是样品室温下的磁滞曲线.所制备的材料均具有超顺磁特性,Fe3O4纳米颗粒、Fe3O4@C和Fe3O4@C/GO(GO与Fe3O4质量比为0.8)的磁饱和强度Ms分别为56.1、15.1和11.9emu/g. Fe3O4与生物质碳和GO复合后,其相对含量降低,因此复合材料的磁饱和强度降低.如果Fe3O4纳米颗粒含量过低,复合材料的Ms会过小,从而其磁分离能力会减弱.图4中的插图清楚地显示,所制备的Fe3O4@C/GO(同上)在外磁场作用下能快速容易地从水中分离出来.
Fe3O4@C/GO(GO与Fe3O4质量比为0.8)的氮气吸附-脱附曲线如图5所示,有明显滞后环.这表明材料具有中孔结构.孔径分布图结果显示,材料主要为中孔和大孔结构.材料的比表面积和总孔容分别为62.5m2/g和0.343cm3/g,微孔孔容为0.024cm3/g.另外,Fe3O4@C的比表面积和总孔容分别为15.6m2/g和0.069cm3/g,微孔孔容为0.0045cm3/g.通过比较得出,GO的加入使复合材料的比表面积和孔容增大,性能显著提高.

图4 样品室温下的磁滞曲线Fig.4 Magnetization curves of samples at room temperature
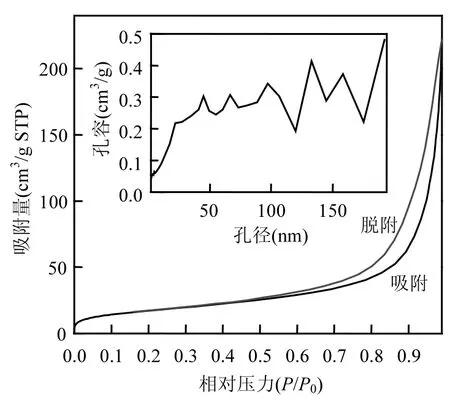
图5 样品的氮气等温吸脱附曲线及孔径分布Fig.5 Nitrogen adsorption/desorption isotherms and pore size distribution (inset) of sample
图6为样品Fe3O4@C/GO(O与Fe3O4质量比为0.8)的XPS图.结果表明,复合材料表面,Fe含量为0.54wt.%,O含量为24.66wt.%,C含量为74.8wt.%,结果分析表明,复合材料表面有丰富的含氧官能团,如表1所示.
图7中Fe3O4@C/GO复合材料的Zeta电位图.Fe3O4@C/GO复合材料的等电点约为pH=2. Fe3O4@C/GO复合材料的表面电性是由其表面H+、OH-荷电离子决定的.当pH值小于等电点时,材料表面带正电;当pH值大于等电点时,材料表面带负电.
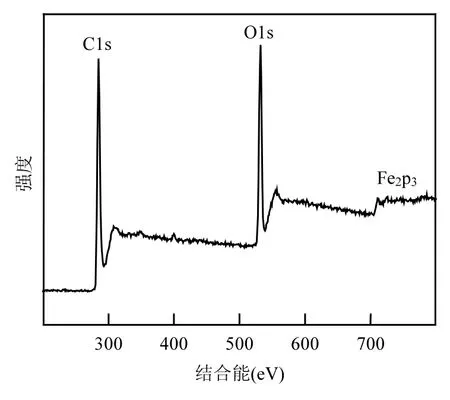
图6 Fe3O4@C/GO复合材料的XPS图Fig.6 XPS curve of Fe3O4@C/GO composite
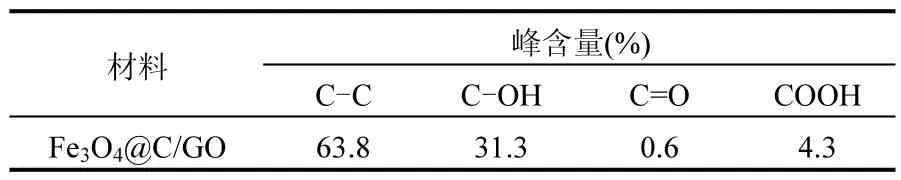
表1 Fe3O4@C/GO复合材料C元素的XPS分析结果Table 1 C1s XPS spectrum analysis of Fe3O4@C/GO
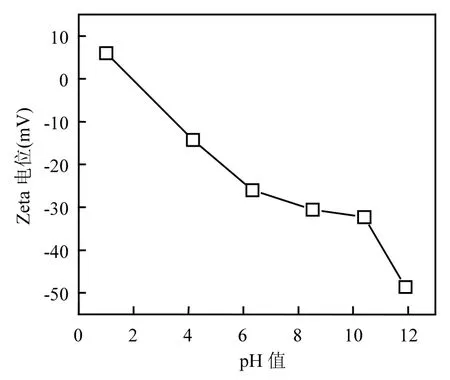
图7 样品的Zeta电位与pH值的关系Fig.7 Relationship between Zeta potential and pH value of sample
2.2 GO与Fe3O4的配比对吸附性能的影响
图8为材料的RhB等温吸附曲线.结果清楚地显示,复合材料的RhB饱和吸附量随着GO用量的增大而增大,当w(GO)/w(Fe3O4)超过0.8后,饱和吸附量变化不大,但是吸附速率增大.纯Fe3O4基本没有吸附能力,Fe3O4@C复合材料的饱和吸附量只有15mg/g,但是w(GO)/w(Fe3O4)为0.8和1.2条件下所制备Fe3O4@C/GO复合材料的饱和吸附值分别为48.5mg/g和48.7mg/g.结果清楚地表明,GO的引入显著提高了材料对RhB的吸附能力.从成本和磁回收效率角度考虑,选用合适的w(GO)/w(Fe3O4)比值即可.后续实验均采用w(GO)/w(Fe3O4)为0.8条件下所制备产物.

图8 样品的RhB等温吸附曲线Fig.8 RhB adsorbing isotherms of samples
2.3 染料初始浓度对材料吸附性能的影响
图9显示了染料初始浓度对材料吸附性能的影响.随着RhB初始浓度的增大,Fe3O4@C/GO的饱和吸附量增大.RhB初始浓度从25mg/L提高到1000mg/L时,Fe3O4@C/GO的饱和吸附值从33.7mg/g增大到303mg/g.复合材料初始吸附速率快,在30min内基本达到饱和吸附.吸附初期,Fe3O4@C/GO材料表面的吸附位点较多,因此吸附速率快,随着吸附位点减少,材料内外RhB浓度差减小,吸附阻力逐渐增大,RhB与吸附剂接触机会减小,因此吸附速率降低[21].复合材料能够吸附RhB的原因可能是:1)RhB为阳离子型碱性染料,能与材料产生静电作用;2)RhB的结构中存在羧基,可与Fe3O4@C/GO表面的羟基和羧基产生氢键作用;3)二者的共轭π键结构使彼此产生π-π堆积作用[22].
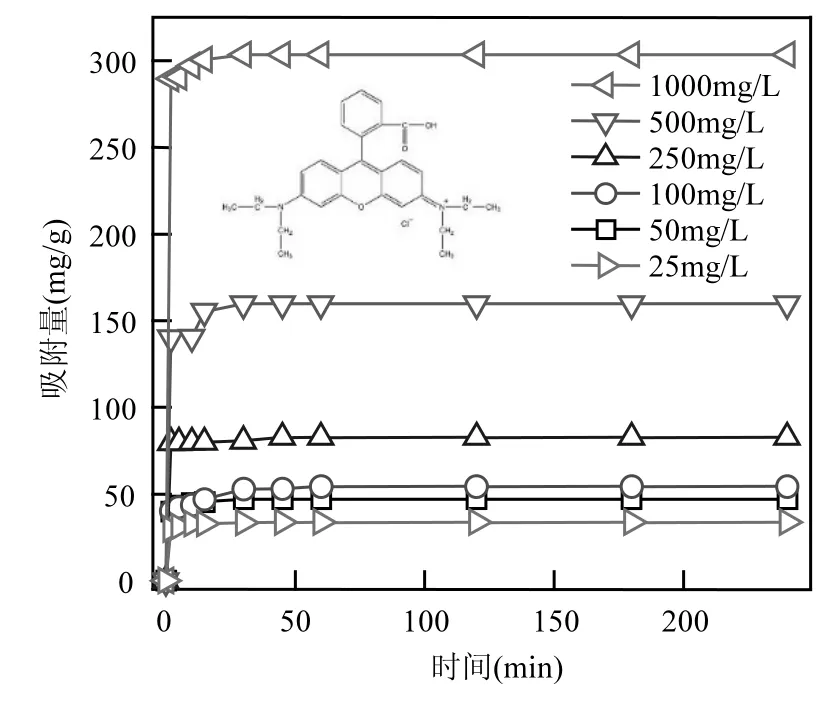
图9 RhB初始浓度对材料吸附的影响(24℃,pH 3.64)Fig.9 Effect of RhB initial concentration on adsorption of sample (24℃, pH 3.64)
2.4 温度对材料吸附性能的影响

图10 温度对Fe3O4@C/GO吸附RhB的影响Fig.10 Effect of temperature on RhB adsorption of Fe3O4@C/GO
温度是影响吸附的重要因素.图10为不同温度下复合材料的饱和吸附量.Fe3O4@C/GO对染料的吸附有物理吸附和化学吸附.物理吸附过程较快,吸附力不强,为可逆性吸附,温度升高容易导致脱附.化学吸附是由吸附剂与吸附质间的化学键作用力而引起的,吸附热较大,吸附需要活化能,温度升高有利于吸附[23].此外,温度对溶液粘度和染料分子活性也有影响,在一定范围内,随着温度的升高,溶液的粘度减小,分子运动加剧,与吸附剂的碰撞机会增多,进而有利于吸附,使吸附量增加.实验结果显示,在30~70℃范围内,随吸附温度的升高,吸附剂的饱和吸附量增大,在70℃达到了97.9mg/g,吸附作用应以化学吸附为主[24].
2.5 pH值对材料吸附性能的影响
图11为不同pH值条件下复合材料的RhB饱和吸附量.饱和吸附量随pH值的提高先增大后降低,在pH值为6.94时达到最大值(67.4mg/g). pH值在2.01~6.94范围内,Fe3O4@C/GO表面含氧官能团去质子化程度逐渐加大,使得吸附剂与RhB分子的作用力更强;而在6.94~11范围内,pH值继续增大时,RhB会发生团聚作用,即由单分子向二分子结合体过渡,增大了吸附阻力,因此饱和吸附量有所下降.以上结果也表明,若在更低的pH值下吸附剂可被重生回收[25].pH值对吸附过程的影响可能主要是吸附剂表面的含氧官能团和染料分子的结构[26].XPS测试得出, Fe3O4@C/ GO材料表面存在大量的含氧基团,使其表面带负电荷.同时通过对材料在不同pH值条件下的Zeta电位测试得出其等电点为2,当染料溶液pH值大于2时,吸附剂表面带负电,有利于吸附过程.
综上所述,吸附剂与RhB分子间的主要作用是静电吸附.
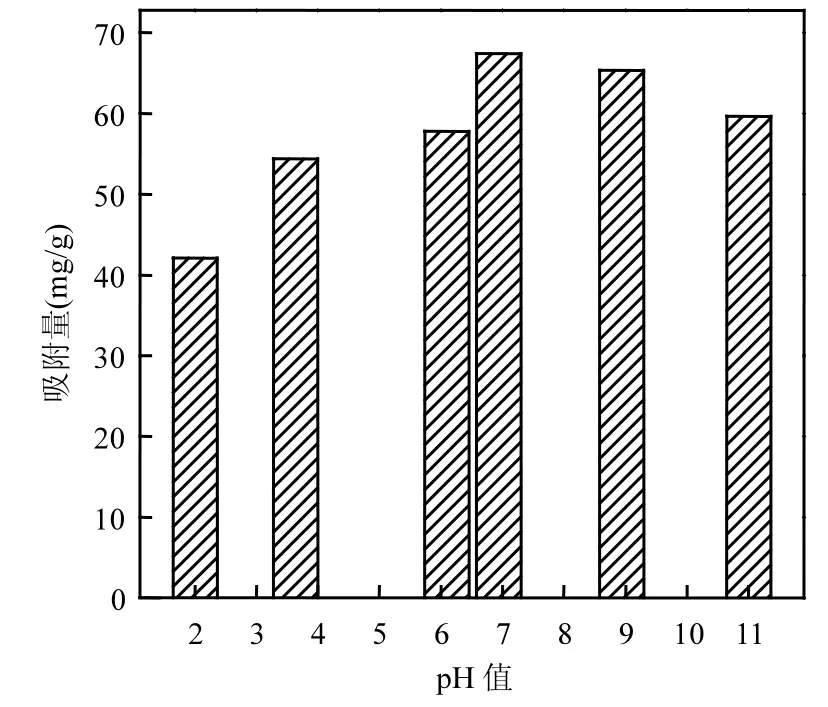
图11 pH对Fe3O4@C/GO吸附RhB的影响Fig.11 Effect of pH on RhB adsorption of Fe3O4@C/GO
3 结论
3.1 采用水热法制备了Fe3O4@C/GO复合材料,Fe3O4被淀粉基生物质包覆,并固定在GO片层上,复合材料通过外加磁场能快速从水中分离出来.
3.2 Fe3O4@C/GO复合材料对染料(RhB)具有良好的吸附能力,随着GO用量增大,复合材料的吸附速率和饱和吸附量呈增大趋势.
3.3 在实验范围内,Fe3O4@C/GO对RhB的饱和吸附量随温度和RhB初始浓度的升高而增大,随pH值升高而先增大后降低,在pH值为6.94时达到最大值.
3.4 Fe3O4@C/GO表面含有丰富的含氧官能团,其等电点pH值为2,与RhB分子的作用主要是静电吸附,以及氢键作用.
[1] Martínez-Huitle C A, Brillas E. Decontamination of wastewaters containing synthetic organic dyes by electrochemical methods: a general review [J]. Applied Catalysis B: Environmental, 2009,87(3):105-145.
[2] 佟雪娇,李九玉,袁金华,等.稻草炭对溶液中Cu (Ⅱ)的吸附作用[J]. 环境化学, 2012,31(1):64-68.
[3] 丁绍兰,李郑坤,王 睿.染料废水处理技术综述 [J]. 水资源保护, 2010,26(3):73-78.
[4] 陈文华,李 刚,许方程,等.染料废水污染现状及处理方法研究进展 [J]. 浙江农业科学, 2014,1(2):264-269.
[5] 王 彬,龚继来,杨春平,等.磁性多壁碳纳米管吸附去除水中罗丹明B的研究 [J]. 中国环境科学, 2008,28(11):1009-1013.
[6] Shen D, Fan J, Zhou W, et al. Adsorption kinetics and isotherm of anionic dyes onto organo-bentonite from single and multisolute systems [J]. Journal of hazardous materials, 2009,172(1):99-107.
[7] Wei L, Wang K, Zhao Q, et al. Kinetics and equilibrium of adsorption of dissolved organic matter fractions from secondary effluent by fly ash [J]. Journal of Environmental Sciences,2011,23(7):1057-1065.
[8] Yavuz E, Bayramoğlu G, Arica M Y, et al. Preparation of poly(acrylic acid) containing core-shell type resin for removal of basic dyes [J]. Journal of Chemical Technology and Biotechnology, 2011,86(5):699-705.
[9] 郎印海,刘 伟,王 慧.生物炭对水中五氯酚的吸附性能研究[J]. 中国环境科学, 2014,34(8):2017-2023.
[10] Wang Z, Guo H, Yu Y, et al. Synthesis and characterization of a novel magnetic carrier with its composition of Fe3O4/carbon using hydrothermal reaction [J]. Journal of Magnetism and Magnetic Materials, 2006,302(2):397-404.
[11] 刘云芳,任 森,吴日良,等.双层SiO2包覆Fe3O4复合材料的制备及其染料吸附性能 [J]. 无机化学学报, 2015,31(12):2373-2378.
[12] Zhang S, Niu H, Hu Z, et al. Preparation of carbon coated Fe3O4nanoparticles and their application for solid-phase extraction of polycyclic aromatic hydrocarbons from environmental water samples [J]. Journal of Chromatography A, 2010,1217(29):4757-4764.
[13] Han C, Ma Q, Dong X, et al. Ⅰn situ synthesis of porous Fe3O4/C composite nanobelts with tunable magnetism, electrical conduction and highly efficient adsorption characteristics [J]. Journal of Materials Science: Materials in Electronics, 2015,26(4): 2457-2465.
[14] Novoselov K S, Geim A K, Morozov S V, et al. Science,2004,306:666-669.
[15] Lazar P, č Karlický F, Jureka P, et al. Adsorption of small organic molecules on grapheme [J]. Journal of the American Chemical Society, 2013,135(16):6372-6377.
[16] 庄 媛,于 飞,马 杰,等.石墨烯去除水中重金属和抗生素的研究进展 [J]. 功能材料, 2014,45(23):23001-23009.
[17] Santhosh C, Kollu P, Doshi S, et al. Adsorption, photodegradation and antibacterial study of graphene—Fe3O4nanocomposite for multipurpose water purification application [J]. RSC Advances,2014,4(54):28300-28308.
[18] Qin Y, Long M, Tan B, et al. RhB Adsorption Performance of Magnetic Adsorbent Fe3O4/RGO Composite and Ⅰts Regeneration through A Fenton-like Reaction [J]. Nano-Micro Letters, 2014,6(2):125-135.
[19] Geng Z, Lin Y, Yu X, et al. Highly efficient dye adsorption and removal: a functional hybrid of reduced graphene oxide—Fe3O4nanoparticles as an easily regenerative adsorbent [J]. Journal of Materials Chemistry, 2012,22(8):3527-3535.
[20] Zhou H, Liu Y, Chi W, et al. Preparation and antibacterial properties of Ag@polydopamine/graphene oxide sheet nanocomposite [J]. Applied Surface Science, 2013,282(10):181-185.
[21] 张春荣,闫李霞,申大忠,等.Fe3O4/C纳米粒子的制备及其对水中罗丹明B的去除 [J]. 环境化学, 2012,31(11):1670-1675.
[22] Pereira M F R, Soares S F, Órfão J J M, et al. Adsorption of dyes on activated carbons: influence of surface chemical groups [J]. Carbon, 2003,41(4):811-821.
[23] 陈 荣.化学吸附中的几个问题 [J]. 化学通报, 1963,16:18-25.
[24] Ⅰram M, Guo C, Guan Y, et al. Adsorption and magnetic removal of neutral red dye from aqueous solution using Fe3O4hollow nanospheres [J]. Journal of hazardous materials, 2010,181(1): 1039-1050.
[25] Qu L, Han T, Luo Z, et al. One-step fabricated Fe3O4@C core—shell composites for dye removal: Kinetics, equilibrium and thermodynamics [J]. Journal of Physics and Chemistry of Solids,2015,78:20-27.
[26] Wu R, Liu J H, Zhao L, et al. Hydrothermal preparation of magnetic Fe3O4@C nanoparticles for dye adsorption [J]. Journal of Environmental Chemical Engineering, 2014,2(2):907-913.
Preparation and dye adsorbing properties of Fe3O4@carbon/graphene oxide composites.
WU Ri-liang1, LIU Yun-fang1,2*, REN Sen1, SHI Xiang-hui1,2, CHI Wei-dong1, HUANG Qi-gu1,2, YU Chang-yuan3, TIAN Xiao-jun3(1.State Key Laboratory of Chemical Resource Engineering, Beijing University of Chemical Technology, Beijing 100029, China;2.Key Laboratory of Carbon Fiber and Functional Polymers, Ministry of Education, Beijing University of Chemical Technology, Beijing 100029, China;3.College of Life Science and Technology, Beijing University of Chemical Technology, Beijing 100029, China). China Environmental Science, 2016,36(10):2981~2987
Fe3O4@carbon/graphene oxide (Fe3O4@C/GO)composites were synthesized by hydrothermal method and characterized by X-ray diffraction, transmission electron microscopy, vibrating sample magnetometer. And their dye adsorbing properties were investigated. The results indicated that the Fe3O4nanoparticles were uniformly anchored on GO sheets. The saturated adsorption capacities towards Rhodamine B (RhB) of the composites increased with the increase of GO content, initial RhB concentration and adsorbing temperature. And the higher GO content in the composite was, the quicker the absorbing rate was. The saturated adsorption capacity of the composite reached a maximum value when the pH value was 7. For the composite prepared at 0.8 of the mass ratio of GO to Fe3O4, the saturated adsorption capacity reached 303.4mg/g at 1000mg/L of initial RhB concentration.
Fe3O4;carbon;graphene oxide;dye;adsorption
X703.5
A
1000-6923(2016)10-2981-07
吴日良(1990-),男,江西上饶人,北京化工大学硕士研究生,主要从事炭材料的制备及其性能研究.
2016-02-29
国家自然科学基金(21174011,U1462102);中央高校基本科研业务费项目(JD1406)
* 责任作者, 副教授, liuyunfang@mail.buct.edu.cn
