邻菲罗啉法测定低聚异麦芽糖铁Ⅲ配合物铁含量及条件优化
2016-12-05江昌照潘红春
胡 莉 江昌照 张 静 潘红春 刘 红
(1. 西南大学药学院,重庆 400715;2. 重庆药物过程与质量控制工程技术研究中心,重庆 400715)
邻菲罗啉法测定低聚异麦芽糖铁Ⅲ配合物铁含量及条件优化
胡 莉1,2江昌照1,2张 静1,2潘红春1,2刘 红1,2
(1. 西南大学药学院,重庆 400715;2. 重庆药物过程与质量控制工程技术研究中心,重庆 400715)
建立邻菲罗啉法测定低聚异麦芽糖铁Ⅲ配合物铁含量,并对该方法的试验过程逐一进行条件优化,以确定最佳检测条件。消解因素试验显示酸的种类对消解没有选择性,但随着酸体积分数的增加,加热温度和时间的增大,消解越趋于完全。2 mL以上的邻菲罗啉显色剂才能完全络合亚铁离子,且络合物可在pH 3~8条件下放置240 min。铁浓度在1~5 mg/L 时线性相关性良好,R2=0.999 9;低聚异麦芽糖铁Ⅲ配合物铁含量分别为42.04%,40.43%,39.45%;平均回收率以及精密度试验结果均显示了该试验方法的精确性。
低聚异麦芽糖铁Ⅲ配合物;分光光度法;邻菲罗啉;铁含量
低聚异麦芽糖铁Ⅲ配合物是以低聚异麦芽糖为糖基,三价铁(Fe3+)为配糖基,通过络合作用而生成的一种稳定多糖铁复合物[1]。低聚异麦芽糖铁Ⅲ配合物集中了两单体功能,具有其独特的优势,被广泛应用于各行业,特别是作为食品添加剂,可以显著增加食品的营养价值。稳定络合的三价铁,不以游离状态存在,减少了对胃肠道的刺激作用,当进入生物体后,低聚异麦芽糖铁Ⅲ配合物被破坏,一方面Fe3+被还原成二价铁(Fe2+)而快速吸收,另一方面释放的低聚异麦芽糖是胃肠道微生物生长不易利用的糖[2-3],但可以被肠道益生菌吸收利用,从而可以调节消化道微生物区系[4-5],提高免疫力[6],保护肝脏[7],降低血脂和胆固醇[8],预防锯齿[9]等等。
铁元素是这种复合物的活性成分,铁含量为其重要的表征指标之一。目前,2015年版中国药典采用碘量法测定右旋糖酐铁配合物的铁含量,但是此碘量法并不适用于低聚异麦芽糖铁Ⅲ配合物,铁含量测定结果明显偏小。而测定多糖铁复合物铁含量的其他方法(如邻菲罗啉法、原子吸收光谱法、磺基水杨酸分光光度法、高效液相色谱法、等离子发射光谱法等)中,邻菲罗啉法具有简便、准确和灵敏度高等优点,已经被广泛应用。如邻菲罗啉法被李玉贤等[10]用来测定百合多糖铁复合物的铁含量;被李明静等[11]用来表征怀山药多糖铁Ⅲ复合物的铁含量;被何丹鸿等[12]应用于多糖铁复合物微丸中铁离子的含量测定;以及邓芬等[13]的厚朴叶多糖铁复合物和赵文阳等[14]的刺梨多糖铁Ⅲ配合物的铁含量测定。但是针对不同的物质,特别是复合物,一方面铁与其它成分的作用方式和空间位阻的差异导致铁离子释放难易程度不同;另一方面微环境的差异对邻菲罗啉有色络合物的稳定性有一定影响。以往的研究[15]也对波长、缓冲溶液的用量、显色时间、显色剂的用量,以及还原剂等进行选择的,但是对影响因素进行全面系统分析却不是很多,并且不同的物质介绍的操作方法也不尽相同。值得重视的是针对此方法测具体物质铁含量时,最佳适用条件也是有差异的,所以本试验建立邻菲罗啉法测低聚异麦芽糖铁Ⅲ配合物这种新复合物的铁含量,开展消解单因素试验,显色单因素试验等,探究邻菲罗啉法对低聚异麦芽糖铁Ⅲ配合物的最佳适用条件,不仅有利于准确测定低聚异麦芽糖铁Ⅲ配合物的铁含量,还可以为邻菲罗啉法测定其他多糖铁配合物方法学优化提供一定的指导。
1 材料与方法
1.1 仪器与试剂
1.1.1 材料与试剂
低聚异麦芽糖铁Ⅲ配合物:参照文献[1]制备;
试验用水:超纯水,用LH75G-4型超纯水机制备;
六水硫酸亚铁铵、三水乙酸钠、抗坏血酸、1,10-菲罗啉、氢氧化钠、碳酸钠、碘化钾、硫代硫酸钠、可溶性淀粉:分析纯,成都市科龙试剂化工厂;
硫酸、盐酸、硝酸、高锰酸钾:分析纯,重庆川东化工(集团)有限公司。
1.1.2 主要仪器设备
紫外分光光度计:UV-1800型,上海美谱达仪器有限公司;
电子天平:EL104型,梅特勒—托利多(上海)有限公司;
pH计:FE-20K型,梅特勒—托利多(上海)有限公司;
水浴箱:XMTD-6000型,余姚市金电仪表有限公司。
1.2 试验方法
1.2.1 硫酸亚铁铵标准溶液的配制 精密称取六水硫酸亚铁胺0.070 23 g于烧杯中, 加入20 mL超纯水和1 mL盐酸搅拌至完全溶解,移入100 mL容量瓶中,蒸馏水定容摇匀,得Fe2+质量分数为0.1 g/L 的亚铁标准溶液。
1.2.2 最大吸收波长选择 精密吸取2.0 mL硫酸亚铁铵标准溶液于50 mL容量瓶中,再按照邻菲罗啉法步骤分别加入抗坏血酸溶液5 mL,乙酸钠溶液5 mL和邻菲罗啉显色液3 mL,蒸馏水定容,放置15 min,在分光光度计上,波长420~570 nm内每隔10 nm扫描,最大吸收波长处每隔0.5 nm扫描得出吸收光谱。
1.2.3 消解因素试验 采用邻菲罗啉法。精密称取0.01 g低聚异麦芽糖铁Ⅲ配合物粉末,用酸消解法破坏,使铁离子(Fe3+)游离,蒸馏水定容于100 mL容量瓶,得样品供试液。然后吸取适量样品供试液于50 mL容量瓶中,加入抗坏血酸(10 g/L)5 mL,Fe3+还原成亚铁离子(Fe2+),再用乙酸钠(1 mol/L)、盐酸(1 mol/L)或者氢氧化钠(1 mol/L)调节pH,然后加入适量邻菲罗啉显色液(1 g/L)与Fe2+反应得橙红色络合物,蒸馏水定容摇匀,在一定的温度下放置一定时间,最后在最大波长处以不加样品供试液为参比溶液测定吸光度值。
首先,分别用浓盐酸、浓硫酸和浓硝酸5.0 mL消解样品,其他条件不变,考察酸种类对消解的影响。然后,分别用浓盐酸、50 mL/100 mL盐酸和10 mL/100 mL盐酸5.0 mL消解样品,其他条件不变,考察酸体积分数对消解的影响,并将上述样品于70 ℃加热10 min,其他条件不变,考察加热对消解的影响。其次,加5.0 mL 10 mL/100 mL盐酸到样品中,其他条件不变,分别于 50,55,60,65,70,75 ℃加热10 min进行消解温度试验;分别于 70 ℃加热2,3,4,5,6 min进行消解时间试验。最后得各样品供试液,吸取2.0 mL,按照邻菲罗啉法步骤测定吸光度值,平行3次。
1.2.4 显色单因素试验
(1) 显色剂用量对显色的影响:将试验条件固定为显色pH 6.0,显色温度35 ℃,显色时间20 min,分别调整显色剂用量为1.0,2.0,3.0,4.0,5.0 mL,测定其最大吸收波长处吸光度值。
(2) pH对显色的影响:将试验条件固定为显色剂用量3.0 mL,显色温度35 ℃,显色时间20 min,分别调整显色pH为1.0,2.0,3.0,4.0,6.0,8.0,11.0,测定其最大吸收波长处吸光度值。
(3) 温度对显色的影响:将试验条件固定为显色pH 6.0,显色剂用量3.0 mL,显色时间20 min,分别调整显色温度为5,20,35,50,65 ℃,测定其最大吸收波长处吸光度值。
(4) 时间对显色的影响:将试验条件固定为显色pH 6.0,显色温度35 ℃,显色剂用量3.0 mL,分别调整显色时间为0,20,40,60,120,240 min,测定其最大吸收波长处吸光度值。1.2.5 方法验证
(1) 加样回收率:分别定量吸取Fe2+标准供试液和样品供试液(见表1)于 50 mL容量瓶中,按邻菲罗啉法测定吸光度值,计算样品回收率,RSD值。
(2) 精密度试验:甲精密吸取2.0 mL样品供试液,邻菲罗啉法平行试验6次,进行重复性试验;乙用同一批样品各平行试验6次,进行中间精密度试验;甲乙丙分别在实验室A、B、C用同一批样品分别平行试验3次,进行重现性试验。
(3) 标准曲线绘制:分别精密取Fe2+标准溶液0.5,1.0,1.5,2.0,2.5 mL于50 mL容量瓶中,按照邻菲罗啉法步骤测定吸光度值,以Fe2+的质量浓度为横坐标,吸光度为纵坐标制作标准曲线图。然后分别精密取Fe2+标准溶液0.1,0.2,0.5,1.0,1.5,2.0,2.5,3.0,3.5,4.0,5.0 mL测定吸光度值,用标准曲线测定铁含量与理论铁含量进行对比。
1.2.6 铁含量测定
(1) 与中国药典法测定结果的比较:参照2015版《中国药典》中右旋糖酐铁配合物的铁含量测定方法[16]和本试验建立的邻菲罗啉法,以及先用后者邻菲罗啉法配合物消解方法处理样品,然后用前者《中国药典》法分别测定批号为20160101、20160315的样品铁含量。
(2) 样品铁含量测定:取批号分别为20140712、20150320和20150511的低聚异麦芽糖铁Ⅲ配合物样品,按照邻菲罗啉法测定吸光度值,根据标准曲线计算铁的含量。
(3) 铁含量的计算:按式(1)进行。
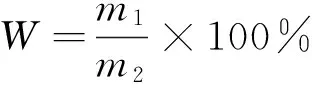
(1)
式中:
W——样品铁含量,%;
m1——样品中铁的质量,g;
m2——样品的质量,g。
2 结果与分析
2.1 最大吸收波长选择
如图1所示,在 510 nm 时有最大吸光度,因此后面试验采用的波长均为510 nm。
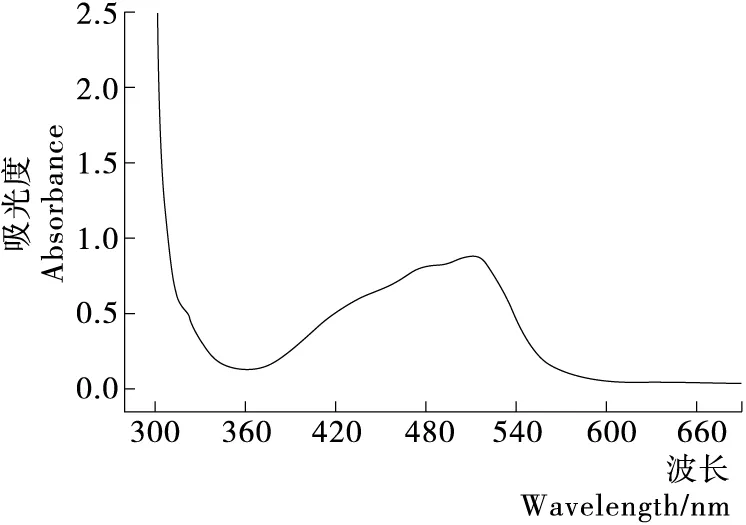
图1 低聚异麦芽糖铁Ⅲ配合物的吸收光谱
Figure 1 The absorption spectrum isomaltooligosaccharide-iron (Ⅲ) complex
2.2 消解因素试验
酸消解是铁含量测定的第一步,也是最重要的一步,低聚异麦芽糖铁Ⅲ配合物消解的难易程度和完全程度间接影响结果的准确性。由图2可知,HCl、H2SO4和HNO3对低聚异麦芽糖铁Ⅲ配合物的消解结果相同,为方便后续试验均选用盐酸消解;随着盐酸的体积分数增大,消解越完全,但是相同程度地辅助加热后,吸光度都有所增加并且最大值基本一致,表明加热促进消解,长时间高温加热利于消解。
由于浓盐酸具有腐蚀性,为了安全高效,所以试验均选择用10 mL/100 mL盐酸70 ℃辅助加热消解5 min。
2.3 显色单因素试验
2.3.1 显色剂用量对显色的影响 邻菲罗啉显色剂用量是影响铁含量测定的另一重要因素。由图3(a)可知,当铁离子处于完全游离状态后,与大于2 mL的邻菲罗啉显色剂(1 g/L)完全生成橙红色络合物,才能准确测定铁含量。根据节约原则试验选择每次加入3 mL邻菲罗啉显色剂。
2.3.2 pH对显色的影响 生成的橙红色络合物保持其稳定性,是准确测定铁含量的关键。试验考察了常见的3个因素对其稳定性的影响。由图3(a)可知,pH为3~11时,吸光度值基本一致;pH为11时吸光度值略微有下降趋势,表明络合物在更碱性的环境下开始不稳定;而pH为1,2时吸光度值明显偏小,邻菲罗啉络合物极不稳定。而本试验选择每次加入乙酸钠(1 mol/L)5 mL调节的pH为5.6~5.8,可以确保邻菲罗啉和Fe2+稳定络合。

图2 各因素对低聚异麦芽糖铁Ⅲ配合物消解的影响
Figure 2 Effect of factors on digestion of isomaltooligosaccharide-iron (Ⅲ) complex
2.3.3 温度对显色的影响 由图3(b)可知,随着温度的升高,吸光度值下降,表明试验受温度影响很大且低温利于显色。但低温的试验条件难控制,为了兼顾操作和试验准确性,控制在25 ℃环境中显色。
2.3.4 时间对显色的影响 由图3(b)可知,0~240 min时吸光度值没有明显差异,表明邻菲罗啉络合物放置240 min也能保持良好的稳定性,为了试验方便,本试验选择放置10 min 后测定吸光度值。
2.4 方法验证
2.4.1 加样回收率 由表1可知,平均加样回收率为99.55%,RSD为0.57%,小于2%,说明方法的准确度良好。
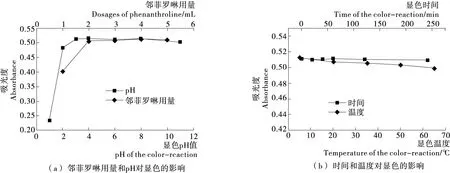
图3 各因素对邻菲罗啉显色的影响

编号Fe2+标准供试液/mL样品供试液/mLFe2+标准加入量/(mg·L-1)Fe2+实际回收量/(mg·L-1)样品回收率/%平均回收率/%RSD/%10.51.01.00.997599.7520.51.51.01.0024100.2430.52.01.00.992699.2641.00.52.01.995299.7651.01.02.01.985299.2661.01.52.01.995099.7571.50.53.02.992599.7581.51.03.02.948498.2891.51.53.02.997699.9299.550.57
2.4.2 精密度试验 由表2可知,操作人员甲的RSD为0.54%,操作人员乙的RSD为0.40%,表明方法的重复性好;甲乙12组数据的RSD为0.58%,表明中间精密度高,符合分析要求。表3显示RSD为1.36%,重现性好,符合分析要求。

表2 重复性和中间精密度试验结果

表3 重现性试验结果
2.4.3 标准曲线绘制 由图4可知,铁含量在6 mg/L以下的低聚异麦芽糖铁Ⅲ配合物可以直接准确测定,根据试验所测数据得到线性回归方程:Y=0.203 5X-0.003 7,R2=0.999 9。表明铁浓度在1~5 mg/L时线性相关性良好。
2.5 铁含量测定
2.5.1 与中国药典法测定结果的比较 由表4可知,邻菲罗啉法所测铁含量明显高于2015版《中国药典》规定的碘量法,且与两种方法的组合法的试验结果相当。说明本试验所建立的方法对低聚异麦芽糖铁Ⅲ配合物的铁含量测定结果可靠。
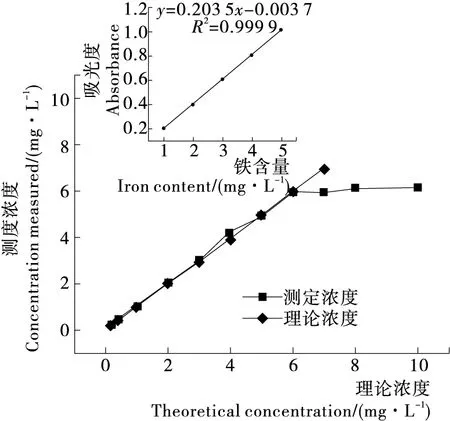
图4 标准曲线

样品批号铁含量/%药典法本试验建立的方法邻菲罗啉法RSD36.5640.2340.342016010136.9840.9841.220.89~1.1837.2141.0241.1235.1439.7739.652016031534.3438.5338.771.46~1.9134.1138.4438.58
2.5.2 样品铁含量测定 由表5可知,3批不同的样品铁含量分别为42.04%,40.43%,39.45%,RSD分别为 0.49%,0.61%,0.55%,说明此方法的试验数据准确可靠。
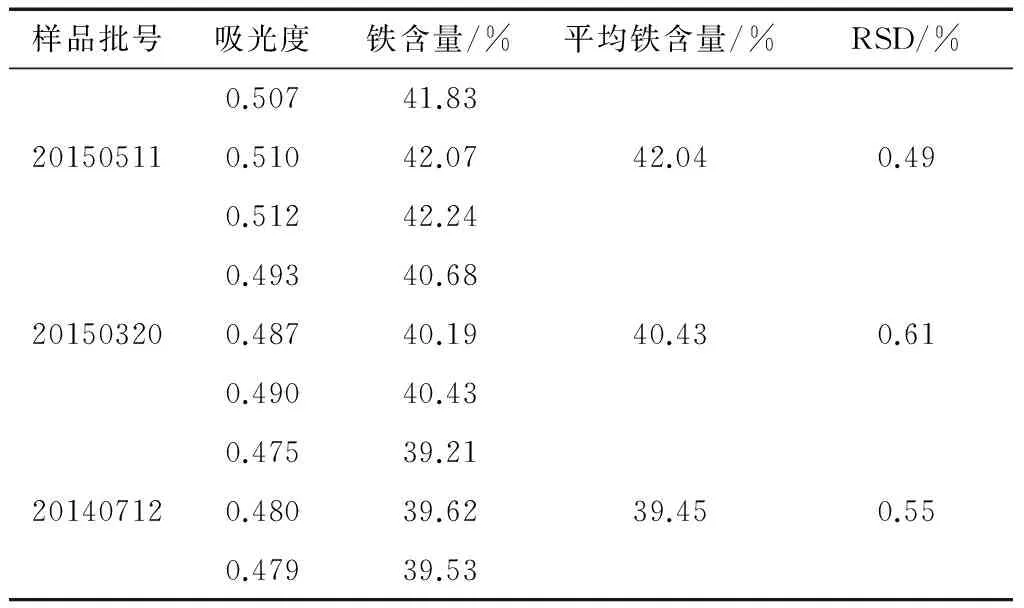
表5 样品铁含量测定结果
3 结论
本试验建立的邻菲罗啉法测定低聚异麦芽糖铁Ⅲ配合物铁含量的方法较药典规定的碘量法操作简单、快速、准确,并且通过一系列的优化试验,确立了最佳适应条件,使其铁含量测定结果更加准确、可靠。本试验的研究方法还为其他类似的多糖铁配合物的含量测定提供了一定的参考价值;也为市场上的含铁食品、保健品、药品等的铁含量测定提供了一种简便有效的方法;也可为邻菲罗啉法应用于其他化合物的方法学优化提供指导。试验的不足之处在于建立的邻菲罗啉法并不能适用于所有多糖铁复合物;进一步研究可以从增加消解多糖铁复合的强度和增强邻菲罗啉络合物的稳定性两方面着手。
[1] MAO Kai, LIU Li, MO Ting, et al. Preparation, characterization, and antioxidant activity of an isomaltooligosaccharide-iron complex (IIC)[J]. Journal of Carbohydrate Chemistry, 2015, 34(7): 430-443.
[2] 郑建仙, 耿立萍. 功能性低聚糖析论[J]. 食品与发酵工业, 1997, 23(1): 39-46.
[3] KANEKO T, KOHMOTO T, KIKUCHI H, et al. Effects of Isomaltooligosaccharides with Different Degrees of Polymeri-zation on Human Fecal Bifidobactcria[J]. Bioscience, biotechnology, and biochemistry, 1994, 58(12): 2 288-2 290.
[4] BI Jin-feng, LIU Chang-jiang. Properties and application of isomaltooligosaccharide[J]. Science and Technology of Cereals, oils and Foods, 2002, 10(5): 42-44.
[5] HAN Xu, GUO Yue-hong, LAI Xiao-ying, et al. Functional Isomaltooligosaccharide and its application on food[J]. China Food Additives, 2005, 12(3): 96-100.
[6] LI Mao-ling. Study on the biological function of isomaltooligosaccharide [J]. China Food Additives, 2002, 9(2): 37-39.
[7] ZHAO Jin, WANG Jiao, KAN Jian-quan. The study of isomaltooligosaccharide’s physiological function and the application[J]. Food Research and Development, 2007, 28(2): 166-170.
[8] ROBERFROID M B. Health benefits of non-digestible oligosaccharides [M]. Springer US: Dietary Fiber in Health and Disease, 1997: 211-219.
[9] GOFFIN D, DELZENNE N, BLECKER C, et al. Will isomalto-oligosaccharides, a well-established functional food in Asia, break through the European and American market? The status of knowledge on these prebiotics[J]. Critical Reviews in Food Science and Nutrition, 2011, 51(5): 394-409.
[10] 李玉贤, 刘艳菊. 大枣多糖铁的合成及其铁含量测定[J]. 安徽农业科学, 2011, 39(15): 9 112-9 114.
[11] 李明静, 杨静, 王宁, 等. 怀山药多糖铁 (Ⅲ) 的组成及性能表征[J]. 中国中药杂志, 2008, 33(16): 2 002-2 005.
[12] 何丹鸿, 袁曦, 林功舟, 等. 多糖铁复合物微丸中铁离子的含量测定[J]. 中国医院药学杂志, 2006, 26(1): 107-108.
[13] 邓芬, 张芳芹, 穆琳, 等. 厚朴叶多糖铁复合物中铁的含量测定[J]. 安徽农业科学, 2012, 40(2): 791-791.
[14] 赵文阳, 孙丙政, 陈穆彦, 等. 刺梨多糖铁 (Ⅲ) 配合物的合成及其铁含量的测定[J]. 辽宁中医杂志, 2012, 39(11): 2 256-2 257.
[15] 姚雪霞, 戴存礼, 李晓林, 等. 邻菲罗啉分光光度法测定微量铁实验条件的探讨[J]. 实验室研究与探索, 2015, 34(3): 16-19.
[16] 国家药典委员会. 中华人民共和国药典: 二部[M]. 2015版. 北京: 中国医药科技出版社, 2015: 172.
Spectrophotometric iron (Ⅲ) determination and optimizing of isomaltooligosaccharide-iron complex using phenanthroline
HULi1,2JIANGChang-zhao1,2ZHANGJing1,2PANHong-chun1,2LIUHong1,2
(1.CollegeofPharmaceuticalSciences,SouthwestUniversity,Chongqing400715,China;2.ChongqingEngineeringResearchCenterforPharmaceuticalProcessandQualityControl,Chongqing400715,China)
In this study,the detection approach was established for spectrophotometric determination of iron (Ⅲ), existing in the form of isomaltooligosaccharide-iron (Ⅲ) complex. The method was optimized by operating experiments considering the factors of the process. Several factors effected on isomaltooligosaccharide-iron (Ⅲ) complex digestion, including the volume fraction of acid, the heating temperature and time, and this approach yielded to accurate results except the kinds of acid. The digestion was positively correlated with the acid volume fraction, heating temperature and time. It was found that over 2 mL phenanthroline solution was demanded and that the complexation could maintain stability within pH 3-8 at 240 min. Good linear correlation personated in 1-5 mg/L of iron concentration,R2=0.999 9. Iron contents of isomaltooligosaccharide-iron (Ⅲ) complex were 42.04%, 40.43% and 39.45% respectively. Therefore, a simple, rapid, sensitive and selective assay for iron (III) determination was proposed successfully by the results of average recovery and precision of the experiments.
isomaltooligosaccharide-iron (Ⅲ) complex; spectrophotometry; phenanthroline; content of iron (III)
重庆市制药过程与质量控制工程技术研究中心能力提升项目(编号:CSTC2012gg-yyjsb10002-33);西南大学博士基金项目(编号:SWU110056);西南大学博士基金项目(编号:SWU110057)
胡莉,女,西南大学在读硕士研究生。
刘红(1965—),男,西南大学教授。
E-mail:lhphch@126.com
2016—07—05
10.13652/j.issn.1003-5788.2016.10.011
