Si-FeOOH催化臭氧氧化法降解苯胺
2015-04-24纪荣昌
纪荣昌
(1. 福州大学 环境与资源学院,福建 福州 350116;2. 漳州开发区招商置业有限公司,福建 漳州 363122)
Si-FeOOH催化臭氧氧化法降解苯胺
纪荣昌1,2
(1. 福州大学 环境与资源学院,福建 福州 350116;2. 漳州开发区招商置业有限公司,福建 漳州 363122)
通过掺杂Si提高FeOOH的机械强度,制备无定型Si-FeOOH,并用于催化臭氧氧化降解苯胺。考察了n(Si)∶n(Fe)、Si-FeOOH加入量、溶液pH、初始苯胺质量浓度等因素对苯胺去除率的影响,并研究了Si-FeOOH的重复利用效果与铁离子的溶出情况。实验结果表明:Si-FeOOH对臭氧氧化降解苯胺具有明显的催化作用,Si-FeOOH催化臭氧氧化对苯胺的降解效果明显高于单独臭氧氧化和FeOOH催化臭氧氧化;在溶液pH为11、Si-FeOOH加入量为1.0 g/L、n(Si)∶n(Fe)=0.55的最佳降解条件下处理初始苯胺质量浓度为300 mg/L的苯胺溶液,降解10 min后,苯胺去除率可达100%;Si-FeOOH催化剂经5次重复使用后,苯胺的去除率仍高达97.8%,且铁离子的溶出量明显低于FeOOH。
硅-羟基氧化铁;催化臭氧氧化;羟基自由基;苯胺;降解
苯胺是一种严重污染环境和危害人体健康的有毒有害物质[1],进入人肌体后会导致神经系统损害与三致效应[2],因此在工业废水排放中受到严格控制[3]。目前,处理苯胺废水的方法主要有物理法(吸附法、萃取法)、化学法(光催化氧化法、Fenton试剂氧化法、臭氧氧化法、电化学降解法)和生物法[3]。物理法作为一种预处理方法,处理后的废水仍难以达到国家排放标准;生物法因苯胺废水的毒性强、生物降解性差等特点难于满足日益提高的废水处理要求;化学法具有操作简便、反应条件温和、处理效率高等优点,受到广泛的应用。
臭氧是一种强氧化剂,直接氧化有机物虽具有选择性,但难以彻底去除COD和TOC。因此,在水处理过程中需与其他方法联合,以提高臭氧的氧化效率[4-6]。FeOOH是一种表面富含羟基、高活性的催化剂,且来源丰富、价格低廉,在水处理中具有广阔的应用前景[7-10]。但FeOOH物理强度不高,易破碎,铁离子易溶出,难以回收利用。因此,亟需采取一定措施提高FeOOH的机械强度,减少铁离子的溶出。
本工作利用Si与Fe的配位作用提高FeOOH的物理强度,同时减少铁离子的溶出,制备得到Si-FeOOH催化剂,并用于催化臭氧氧化降解苯胺。
1 实验部分
1.1 试剂和仪器
苯胺、硅酸钠、氢氧化钠、硝酸铁、亚硫酸钠:分析纯。
FeOOH:按文献[11]中所述方法制得。
UV-2000型紫外-可见分光光度计:上海尤尼柯分析仪器厂;PHS-3C型精密pH计:上海雷磁仪器厂;DHX-SS-1G型实验室用臭氧发生器:哈尔滨久久电化学工程技术有限公司;CL-1A型磁力搅拌器:郑州长城工贸有限公司;DHG-9140A型电热恒温鼓风干燥箱:上海一恒科技有限公司。
1.2 Si-FeOOH催化剂的制备
取硅酸钠溶液250 mL加入到250 mL 1 mol/L的氢氧化钠溶液中,充分搅拌混合。向混合液中缓慢滴加入0.25 mol/L的硝酸铁溶液,强烈搅拌后产生胶状的Si-Fe复合物。将所得中间产物置于50℃的恒温水浴锅中活化24 h后,离心分离,充分洗涤至洗出液保持恒定的pH和电导率。将所得沉淀物置于70 ℃烘箱中烘干,研磨过筛,取粒径为0.075~0.300 mm的无定型Si-FeOOH备用[12]。
1.3 实验方法
在温度为25 ℃的条件下,向装有苯胺溶液的1 L反应器中加入催化剂Si-FeOOH并通入臭氧,开动搅拌,使催化剂在液相中分布均匀。控制臭氧的进气流量为30 L/h。每间隔2 min取样,用过量的亚硫酸钠溶液终止反应,经0.45 μm滤膜过滤后,采用萘乙二胺偶氮分光光度法[13]测定苯胺质量浓度,计算苯胺去除率。采用邻菲啰啉分光光度法[13]测定铁离子的质量浓度,即铁离子溶出量。
2 结果与讨论
2.1 不同体系催化氧化降解苯胺的效果比较
在溶液pH为7、初始苯胺质量浓度为300 mg/ L、催化剂加入量为1.0 g/L、n(Si)∶n(Fe)=0.33的条件下,不同体系催化臭氧氧化降解苯胺的效果比较见图1。由图1可见:随降解时间的延长,单独臭氧氧化、FeOOH催化臭氧氧化和Si-FeOOH催化臭氧氧化的苯胺去除率均逐渐增加;相比单独臭氧氧化,催化剂FeOOH和Si-FeOOH的加入均不同程度地提高了苯胺的去除效果,与FeOOH相比,Si-FeOOH对苯胺的催化去除效果更好,这可能是由于Si的掺入生成无定型的Si-Fe二元配合物,使FeOOH表面颗粒的粒径变小,比表面积和球形度增大[10],有利于催化臭氧分解产生·OH;反应2 min后,单独臭氧氧化对苯胺的去除率为39.6%,FeOOH催化臭氧氧化体系和Si-FeOOH催化臭氧氧化体系对苯胺的去除率分别为44.8%和58.8%,分别较单独臭氧氧化体系提高了5.2百分点和19.2百分点;随降解时间的延长,3种体系对苯胺去除率的差别逐渐缩小,反应10 min后,3种体系对苯胺的去除率均接近100%。这主要是因为,在反应的前半阶段,液相中臭氧的浓度较低,催化剂FeOOH和Si-FeOOH均可加快臭氧分子的分解,增加单位时间内·OH自由基的产生量,从而加速苯胺的降解;随着反应的进行,臭氧通入量不断增加,臭氧分子对苯胺的氧化作用也不断增加,3种体系对苯胺的去除率逐渐接近。

图1 不同体系催化臭氧氧化降解苯胺的效果比较
2.2 n(Si)∶n(Fe)对苯胺去除率的影响
在溶液pH为7、初始苯胺质量浓度为300 mg/ L、Si-FeOOH加入量为1.0 g/L的条件下,n(Si)∶n(Fe)对苯胺去除率的影响见图2。由图2可见:苯胺去除率随n(Si)∶n(Fe)的增加先升高而后降低;当n(Si)∶n(Fe)=0.55时,苯胺去除效果最好。这可能是由于,随催化剂中Si含量的增加,Fe原子的空间分布更为分散,FeOOH表面的羟基分布更多,更多的羟基促进了臭氧分解生成·OH;但当Si掺杂过多时,覆盖了FeOOH的活性位点,减少了FeOOH与臭氧接触的机会,导致生成·OH自由基的机会减少,从而降低了催化剂Si-FeOOH的催化效果。因此,选择n(Si)∶n(Fe)= 0.55较适宜。

图2n(Si)∶n(Fe)对苯胺去除率的影响
2.3 Si-FeOOH加入量对苯胺去除率的影响
在溶液pH为7、初始苯胺质量浓度为300 mg/ L、n(Si)∶n(Fe)=0.33的条件下,Si-FeOOH加入量对苯胺去除率的影响见图3。由图3可见:随Si-FeOOH加入量的增加,苯胺去除率先逐渐增加,这主要是由于随Si-FeOOH加入量的增加,催化剂比表面积随之增加,有机会产生更多的·OH自由基;当Si-FeOOH加入量为3.0 g/L时,苯胺的催化氧化去除效果最好;继续增加Si-FeOOH的加入量,苯胺去除率降低,这可能是由于随催化剂表面的增加,臭氧分解产生·OH自由基的速率增加过快,过量的·OH自由基来不及与苯胺反应,而发生了自淬灭。由于Si-FeOOH加入量为1.0 g/L时的苯胺去除效果与Si-FeOOH加入量为3.0 g/L时的去除效果接近,考虑运行成本,选择Si-FeOOH加入量为1.0 g/L为宜。
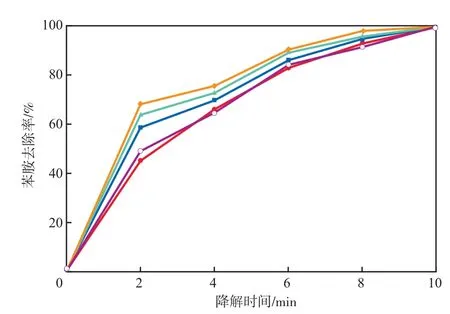
图3 Si-FeOOH加入量对苯胺去除率的影响
2.4 溶液pH对苯胺去除率的影响
在Si-FeOOH加入量为1.0 g/L、初始苯胺质量浓度为300 mg/L、n(Si)∶n(Fe)=0.33的条件下,溶液pH对苯胺去除率的影响见图4。由图4可见:随溶液pH的增加,Si-FeOOH催化臭氧氧化对苯胺的去除率逐渐增大。OH-是臭氧分解链反应的引发剂[14]。随溶液pH的升高,OH-浓度逐渐增加,有利于臭氧分解链反应的发生,生成更多的·OH自由基,从而提高苯胺的去除率。此外,溶液pH的改变影响了Si-FeOOH表面的电性,进而影响Si-FeOOH催化臭氧的活性。Si-FeOOH的等电点约为中性。当溶液pH大于Si-FeOOH的等电点时,催化剂表面带负电荷;当溶液pH小于Si-FeOOH的等电点时,催化剂表面带正电荷。臭氧作为一种亲电试剂[15],易于吸附在带负电荷的催化剂表面。因此,pH的增加有利于·OH自由基的形成,促进苯胺的降解。

图4 溶液pH对苯胺去除率的影响
2.5 初始苯胺质量浓度对苯胺去除率的影响
在Si-FeOOH加入量为1.0 g/L、溶液pH为7、n(Si)∶n(Fe)=0.33的条件下,初始苯胺质量浓度对苯胺去除率的影响见图5。由图5可见:在相同实验条件下,处理不同初始苯胺质量浓度的苯胺溶液,降解速率不同;当初始苯胺质量浓度为100 mg/L时,6 min内即可完全降解;当苯胺初始质量浓度大于200 mg/L时,10 min以上才可降解完全。这是因为当苯胺质量浓度较高时,反应生成的中间产物较多,消耗了一部分臭氧和·OH自由基;并且,在臭氧流量恒定时,产生的臭氧量有限,臭氧分解产生的·OH自由基的数量一定,随着苯胺质量浓度的增大,与苯胺分子碰撞的·OH自由基的数量减少,导致其催化降解的速率下降[9]。

图5 初始苯胺质量浓度对苯胺去除率的影响
2.6 小结
在溶液pH为11、Si-FeOOH加入量为1.0 g/L、n(Si)∶n(Fe)=0.55的最佳降解条件下,处理初始苯胺质量浓度为300 mg/L的苯胺溶液,降解10 min后,苯胺去除率可达100%。
2.7 Si-FeOOH的重复使用效果及铁离子的溶出情况
高效的催化剂除需具备高的催化能力,同时还应具备可重复利用性和较高的稳定性。在溶液pH为7、Si-FeOOH加入量为1.0 g/L、n(Si)∶n(Fe)=0.33、初始苯胺质量浓度为300 mg/L、降解时间为10 min的条件下,Si-FeOOH的重复使用效果及铁离子溶出量见表1。由表1可见,Si-FeOOH催化剂重复使用5次后,对苯胺的催化降解性能没有明显影响,对苯胺的去除率仍高达97.8%;Si-FeOOH铁离子的溶出量明显低于FeOOH,这是由于Si的掺杂不仅提高了FeOOH的比表面积,同时又对FeOOH起到固化作用,使其不易溶解流失。由此可见,Si-FeOOH是一种高效、稳定且易于回收、重复使用的催化剂。
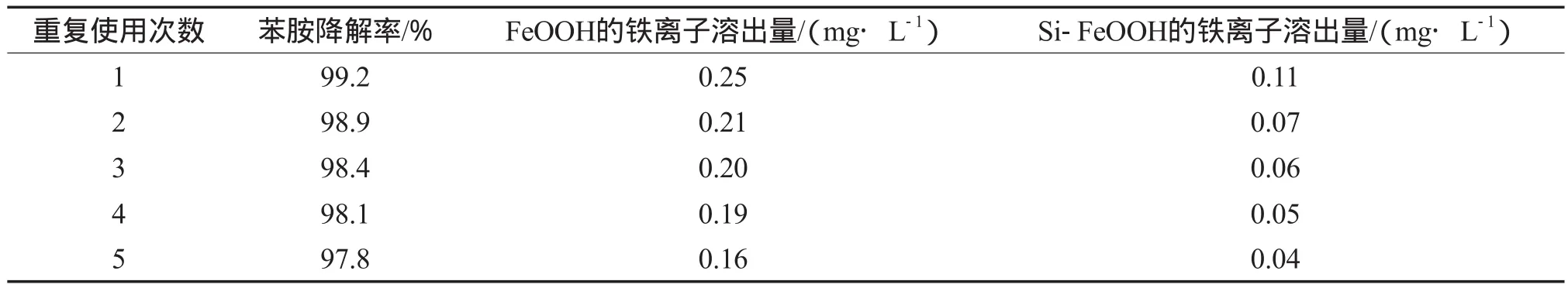
表1 Si-FeOOH的重复使用效果及铁离子溶出量
3 结论
a) Si-FeOOH对臭氧氧化降解苯胺具有明显的催化作用,Si-FeOOH催化臭氧氧化降解苯胺的效率明显高于单独臭氧氧化和FeOOH催化臭氧氧化。
b)Si-FeOOH的催化效果随n(Si)∶n(Fe)和Si-FeOOH加入量的增加而先增大后减小;溶液pH的升高和初始苯胺质量浓度的降低加速了苯胺的降解。
c)在溶液pH为11、Si-FeOOH加入量为1.0 g/ L、n(Si)∶n(Fe)=0.55的最佳降解条件下,处理初始苯胺质量浓度为300 mg/L的苯胺溶液,降解10 min后,苯胺去除率可达100%。
d) Si-FeOOH催化剂经5次重复使用后,苯胺的去除率仍高达97.8%,且铁离子的溶出量明显低于FeOOH。
[1] 叶招莲,郑晓,郑璐,等. 高铁酸盐降解苯胺废水的机制研究[J]. 环境污染与防治,2009,31(4):1 - 4.
[2] 郑金来,李君文,晃福寰.苯胺、硝基苯和三硝基甲苯生物降解研究进展[J]. 微生物学通报,2001,28(5):85 - 88.
[3] 聂永平,邓正栋,袁进. 苯胺废水处理技术研究进展[J]. 环境污染治理技术与设备,2003,4(3):77 -81.
[4] Kasprzyk-Hordern B,Ziolek M,Nawrocki J. Catalytic Ozonation and Methods of Enhancing Molecular Ozone Reactions in Water Treatment[J]. Appl Catal,B,2003,46(4):639 - 669.
[5] Zhang Tao,Ma Jun.Catalytic Ozonation of Trace Nitrobenzene in Water with Synthetic Goethite[J].J Mol Catal A,2008,279:82 - 89.
[6] 马军,刘正乾,虞启义,等. 臭氧多相催化氧化除污染技术研究动态[J]. 黑龙江大学自然科学学报,2009,26(1):1 - 15.
[7] 鲁金凤,马军,何如,等. 负载型FeOOH催化臭氧氧化对THMFP的控制效果[J]. 中国给水排水,2008,24(15):32 - 39.
[8] 张涛,陈忠林,马军,等. 水合氧化铁催化臭氧氧化去除水中痕量硝基苯[J]. 环境科学,2004,25(4):43 - 47.
[9] 熊慧欣,周立祥. 不同晶形羟基氧化铁(FeOOH)的形成及其在吸附去除Cr(Ⅵ)上的作用[J]. 岩石矿物杂志,2008,27(6):559 - 565.
[10] 李坤林,陈武强,李小婷,等. UV/Si-FeOOH/H2O2氧化降解水中邻苯二甲酸二甲酯[J]. 环境科学,2010,31(9):2075 - 2080.
[11] 黄先锋,姜成春,苑宝玲. 羟基氧化铁催化臭氧氧化去除水中阿特拉津[J]. 环境工程学报,2010,4(9):2042 - 2046.
[12] Zeng Le. A Method for Preparing Silica-Containing Iron(Ⅲ) Oxide Adsorbent for Arsenic Removal[J]. Water Res,2003,37:4351 - 4358.
[13] 国家环境保护总局《水和废水监测分析方法》编委会. 水与废水监测分析方法[M]. 4版. 北京:中国环境科学出版社,2002:241 - 387.
[14] Staehelin J,Hoigné J. Decomposition of Ozone in Water:Rate of Initiation by Hydroxide Ions and Hydrogen Peroxide[J]. Environ Sci Technol,1982,16:676 - 681.
[15] von Gunten U. Ozonation of Drinking Water:I. Oxidation Kinetics and Product Formation[J]. Water Res,2003,37(7):1443 - 1467.
(编辑 王 馨)
Degradation of Aniline by Catalytic Ozonation with Si-FeOOH
Ji Rongchang1,2
(1. School of Environment and Resources,Fuzhou University,Fuzhou Fujian 350108,China;2. Zhangzhou Development Zone Merchants Co. Ltd.,Zhangzhou Fujian 363122,China)
The Si-FeOOH for catalytic ozonation of aniline was prepared by Si doping in order to enhance the mechanical strength. The factors affecting the aniline removal rate were studied. The stability of the reused catalyst and the condition of Fe dissolution were also researched. The experimental results show that:The catalytic effect of Si-FeOOH on aniline degradation by ozonation is signif cant,since the aniline degradation rate by Si-FeOOH catalytic ozonation is much higher than that by ozonation and that by FeOOH catalytic ozonation;Under the optimum conditions of solution pH 11,Si-FeOOH dosage 1.0 g/L,n(Si)∶n(Fe)=0.55,initial aniline mass concentration 300 mg/L and degradation time 10 min,the aniline degradation rate can reach 100%; After Si-FeOOH has reused for 5 times,the aniline degradation rate is still up to 97.8%,and the Fe dissolved quantity of Si-FeOOH is obviously lower than that of FeOOH.
silicon-hydroxyl ferric oxide;catalytic ozonation;hydroxyl radical;aniline;degradation
X703
A
1006-1878(2015)06-0588-05
2015 - 08 - 07;
2015 - 09 - 16。
纪荣昌(1982—),男,福建省厦门市人,硕士,工程师,电话 18050751760,电邮 rongchang_ji@163.com。
