硫酸浸出硼泥制备片状氢氧化镁实验研究
2013-10-17侯会丽郑水林
孙 青,侯会丽,郑水林,叶 鹏
[中国矿业大学(北京)化学与环境工程学院,北京 100083]
硼泥是制取硼化工产品时产生的大宗废弃物,目前已在辽宁、吉林、四川和青海等地造成大量堆积,并且在中国正以每年100万t以上的排放量增加。由于硼泥呈碱性,大量硼泥露天堆积,易造成碱液渗漏,污染周围水体、生态环境,并影响人体健康[1-4]。 硼泥主要化学成分是 MgO、SiO2、Fe2O3、Na2O和CaO等,其中MgO含量最为丰富。目前,已对硼泥利用开展了相关研究,制成镁盐产品、耐火材料和建筑材料等,取得了节省资源和保护环境的良好效果[5-6]。
氢氧化镁是重要的镁化工制品,作为无机阻燃填料在塑料、橡胶材料应用广泛,具有无卤、无毒、无烟、热稳定性好和分解温度高的优点[7-9]。将硼泥中的镁回收利用,可制得氢氧化镁产品,现有工艺主要包括碳化法、焙烧法、中性盐浸出法、相转移法及直接酸浸法[10-11]。笔者针对废弃硼泥成分和物相组成特点,采用硫酸直接浸出、梯度碱析和水热反应方法,制备出纯度高、形貌均一和分散性好氢氧化镁产品。
1 实验
1.1 实验原料与试剂
实验用硼泥来自吉林集安,其主要化学成分见表1。由表1可以看出,硼泥中主要化学成分为MgO、SiO2和 Fe2O3, 还有少量的 B2O3、Al2O3、Na2O、CaO和MnO等。硼泥中MgO含量丰富,高达40%(质量分数,下同)以上,为制取 Mg(OH)2提供了高品位原矿,但同时易浸出杂质成分Fe2O3、Al2O3的含量也较高。

表1 硼泥化学成分分析 %
由X射线衍射分析得出,该硼泥主要矿物组成有含铁橄榄石[(Mg,Fe)2SiO4]、 菱镁矿(MgCO3)、变质 蛇 纹 石 (Mg,Al)3[(Si,Fe)2O5] (OH)4、 磁 铁 矿(Fe3O4)、石英(SiO2)等。 依据 X 光衍射 ASTM 数据卡片对硼泥矿物组成进行分析,各矿物组成见表2。由表2可知,硼泥中的镁橄榄石物相含量最高,占硼泥成分的50%(质量分数,下同)以上,镁元素在硼泥中主要以镁橄榄石物相存在;菱镁矿物相有24.10%,还有少量的镁以蛇纹石的形式存在(2.00%)。当硼泥中镁以菱镁矿(MgCO3)物相存在时,可以通过煅烧处理,使镁以MgO的形式释放出来。提镁工艺较为简单,而对于镁橄榄石和蛇纹石,需采用强酸破坏其矿物结构,使镁以Mg2+形式进入溶液。对浸出液进一步净化处理,可以制得相应的MgSO4、MgCl2及 Mg(OH)2等产品。
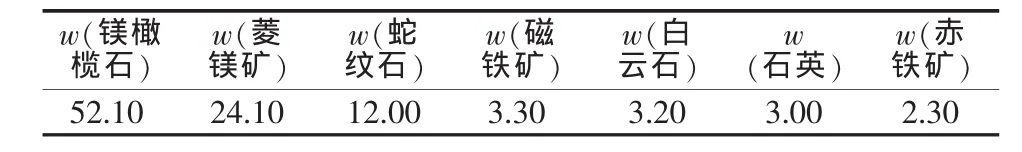
表2 硼泥物相组成分析 %
实验所用浓硫酸、过氧化氢、氨水、氢氧化钠均为分析纯,实验用水为自制蒸馏水。
1.2 实验方法与仪器
1.2.1 实验方法
取一定量硼泥置于三口烧瓶中,加入适量的硫酸,开启加热及搅拌,浸出反应一段时间后,经过过滤、洗渣、烘干、称重后,采用电感耦合等离子体发射光谱仪(ICP-OES)分析滤渣中未浸出的镁含量,计算镁浸出率,并对反应渣进行XRD物相分析。滤液经氧化除杂后,过滤、沉淀、干燥得富含Fe(OH)3的渣;滤液加入适量的氢氧化钠溶液,得到氢氧化镁沉淀,将沉淀物洗涤、过滤后,对氢氧化镁沉淀进一步水热反应,得到水热氢氧化镁。实验流程见图1。

图1 硫酸浸出硼泥制取片状氢氧化镁实验流程示意图
1.2.2 仪器设备
CDE-300E型打散机、DZKW-4型恒温水浴锅、JJ-2型机械搅拌器、HL-2型恒流泵、真空泵、水热反应釜、DGB/20-002A型台式干燥箱、D/max 2500型X射线衍射仪、EVO 18 Special Edition型扫描电子显微镜、iCAP 6000 Series型等离子体发射光谱仪。
2 结果与讨论
2.1 正交实验
为分析硼泥在硫酸溶液中的浸出行为,采用正交实验确定影响硼泥中镁浸出率的主要因素。影响硼泥中镁浸出率因素有反应温度、反应时间、硫酸用量、硫酸初始浓度(酸用量和初始浓度共同影响反应体系的固液比)、固体颗粒物的粒度等。因此,为了寻求硼泥酸浸优化工艺条件,选择反应温度(℃)、反应时间(h)、硫酸用量(实际用量与理论用量的物质的量比)、硫酸初始浓度(%),设计 4 因素 3 水平 L9(34)正交实验,结果见表3。正交实验及极差分析结果见表4。正交实验方差分析见表5。
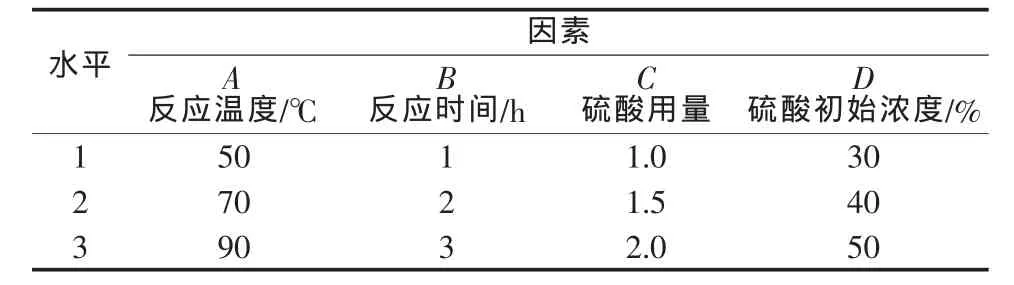
表3 正交实验因素及水平
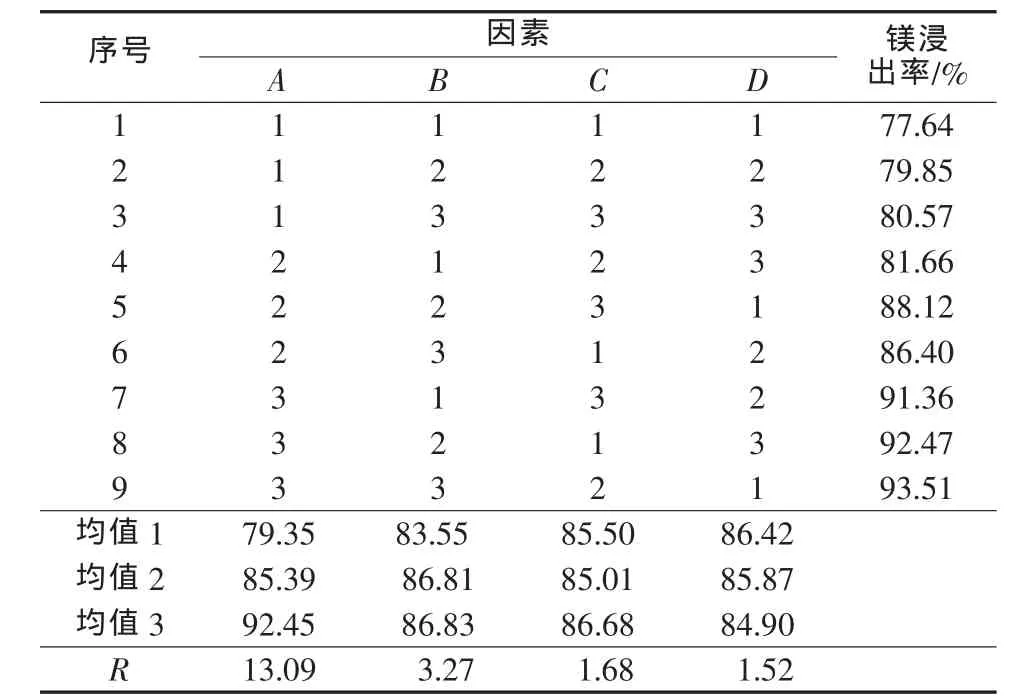
表4 正交实验结果
由表4、5可知,各因素对镁浸出率影响大小顺序:反应温度>反应时间>硫酸用量>硫酸初始浓度。说明在浸出硫酸用量足够的条件下,反应温度对Mg的浸出率影响最大。最优水平A3B3C2D1,即反应温度为90℃、反应时间为3 h、硫酸用量为1.5倍、硫酸初始浓度为30%(质量分数,下同)时,镁的浸出率最大。
2.2 因素实验
通过正交实验得知,对Mg的浸出率影响最大的因素为反应温度。在实验过程中,浓硫酸经稀释后会有大量稀释热放出,在不进行外加热的情况下,就能使反应温度升到50℃以上。结合工业实际及成本考虑,硼泥浸出反应温度的提高较易实现,而硫酸用量会影响浸出液除铁及沉淀 Mg(OH)2过程碱量消耗,在保证硼泥中Mg能有较好浸出率的前提下,应尽量减小硫酸用量。因此,在固定条件下,通过因素实验考察了不同反应温度、硫酸用量对Mg浸出率的影响。
1)反应温度。在反应时间为3 h、硫酸用量为理论量1倍、硫酸初始浓度为40%的条件下,考察了反应温度对Mg浸出率的影响,结果见图2。由图2可知,在反应温度为50~90℃时,Mg浸除率随反应温度的升高迅速升高,继续升至95℃,Mg浸出率增幅变小。因此,实验选择硫酸浸出硼泥的反应温度为95℃。
2)硫酸用量。在反应时间为3 h、反应温度为95℃、硫酸初始浓度为40%的条件下,考察了硫酸用量对Mg浸出率的影响,结果见图3。由图3可知,Mg的浸出率随着硫酸用量的增加而增大。当硫酸用量为理论量的0.8倍时,Mg浸出率仅为82.19%,当硫酸用量为理论量的1.2倍时,Mg浸出率为95.62%。当硫酸加入量大于1.1倍时,Mg的浸出率增幅不大。为节省沉淀氢氧化镁时碱的用量,实验选择硫酸用量为理论量的1.2倍。
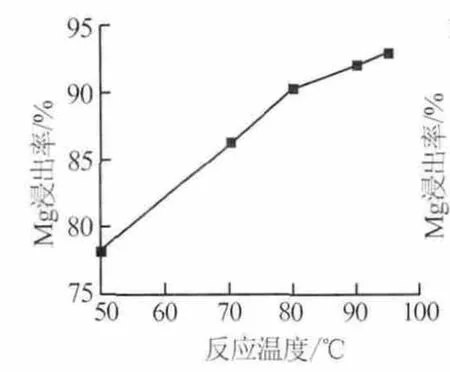
图2 反应温度对Mg浸出率的影响
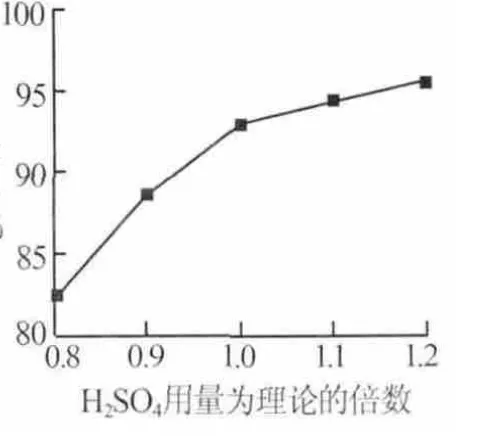
图3 H2SO4用量对Mg浸出率的影响
通过因素实验,确定优化酸浸条件:反应温度为95℃、反应时间为3 h、硫酸初始浓度为40%、硫酸用量为理论量的1.2倍。反应完成后,浆洗一次、淋洗一次反应渣,经过滤得到初级硫酸镁浸出液。图4为浸出反应渣的XRD谱图。从图4可以看出,酸浸过后的渣中只含少量未浸出的硅酸镁、石英及氧化铁物相,大量 Mg2+、Fe2+、Al3+等被浸出,在 2θ为 10~30°时形成无定形的SiO2衍射鼓包。

图4 硼泥浸出渣的XRD谱图
2.3 氢氧化镁制备实验
2.3.1 氧化除杂
取初级硫酸镁浸出液于三口烧瓶中,反应温度为90℃,开启搅拌,加入少量质量分数为30%的双氧水氧化30 min,使溶液中的Fe2+氧化成Fe3+。以质量分数为25%的氨水为沉淀剂,用蠕动泵缓慢滴加至pH为5~6,沉化30 min后过滤得到氢氧化铁沉淀物。
2.3.2 沉淀氢氧化镁
反应温度为70℃,配制质量分数为20%的氢氧化钠溶液作为氢氧化镁沉淀剂,用蠕动泵缓慢滴加至pH为12~13,沉化30 min。过滤沉淀物并对滤饼加水洗涤3次,制得氢氧化镁滤饼。
2.3.3 氢氧化镁的提质水热反应
水热反应是在加压反应釜中进行的,采用沉淀氢氧化镁滤饼,加水调浆至150~200 g/L,氢氧化镁的水热条件:水热温度为150℃,水热时间为2 h。
2.3.4 氢氧化镁产品的表征
硫酸浸出硼泥制得氢氧化镁经水热反应后,采用SEM、XRD及建筑材料行业标准 JC/T 1021.9—2007《水镁石化学分析方法》等分别对样品形貌、物相、化学成分等进行了分析。
图5 为未水热 Mg(OH)2和水热 Mg(OH)2的SEM照片。由图5可见,水热反应前,沉淀反应生成的氢氧化镁呈团聚状;在高温、高压条件下,经水热反应后,氢氧化镁沉淀可以进一步结晶,除去沉淀时包聚的水分、Na+、SO4-等杂质,形成晶粒发育完整、粒度分布均匀、颗粒分散性好的片状氢氧化镁粉体。

图5 未水热 Mg(OH)2和水热 Mg(OH)2的 SEM 照片
图6 为水热 Mg(OH)2的 XRD 谱图(a)和标准Mg(OH)2衍射卡片(b)的对比。 由图 6 可见,水热Mg(OH)2结晶性较好,与标准 Mg(OH)2衍射卡片(JCPDS 76-0667)对比可以看出,实验所得 Mg(OH)2无其他杂质物相峰出现,其Mg(OH)2质量分数为99.35%。
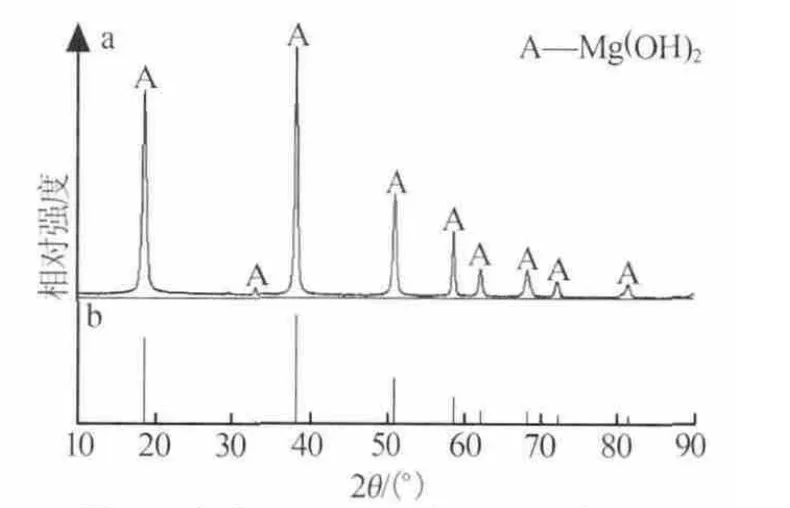
图6 水热 Mg(OH)2的 XRD谱图
3 结论
1)硼泥中含有丰富的镁资源,通过硫酸浸出、梯度碱析和水热反应,可以有效回收硼泥中镁元素,制得片状高纯 Mg(OH)2产品。
2)用硫酸浸出硼泥优化工艺条件:浸出温度为95℃、浸出时间为3 h、硫酸初始浓度为40%(质量分数)、硫酸用量为理论量的1.2倍。
3)硼泥中氧化镁组分经硫酸浸出后可制得形貌均一、颗粒分散性好、晶粒发育完整的Mg(OH)2粉体,其 Mg(OH)2质量分数高达 99.35%。
[1]孙彤.硼泥综合利用概况与展望[J].辽宁工学院学报.2004,24(4):45-48.
[2]单松高,阎加强,陈文,等.硼泥的性质及综合利用[J].山东建材,1998(2):37-39.
[3]徐华琴.硼泥的综合利用[J].矿产保护与利用,1993(5):38-40.
[4]刘见芬,蒋引珊,方送生.硼泥的综合回收利用试验研究[J].非金属矿,2001,24(3):27-29.
[5]刘宝树,胡庆福,胡永琪,等.硼泥综合利用研究进展[C]∥2010年全国镁盐行业年会暨节能减排与发展研讨会论文集.德州:中国无机盐工业协会钙镁盐分会,2010:78-84.
[6]钱洪伟,薛向欣,刘然,等.硼泥资源化利用的重要途径[J].化工矿物与加工,2007,36(9):33-36.
[7]胡庆福,宋丽英,刘宝树.中国工业镁化合物生产现状与展望[J].无机盐工业,2009,41(4):8-10,34.
[8]Mordike B L,Ebert T.Magnesium:Properties-applications-potential[J].MaterialsScienceandEngineeringA,2001,302(1):37-45.
[9]高善民,王善华,孙树声,等.市场前景广阔的无机阻燃剂——氢氧化镁[J].化工进展,2001(08):56-59.
[10]向兰,吴会军,金永成,等.阻燃型氢氧化镁制备技术评述[J].海湖盐与化工,2001,30(5):1-4.
[11]孙青,侯会丽,郑水林,等.硼泥中镁、硅回收及综合利用研究进展[J].中国粉体技术,2012(增刊):20-23.
[12]Lebedev V N.Specific features of disposal of sulfuric acid solutions resulted from magnesium silicate decomposition[J].Russian Journal of Applied Chemistry,2010,83(4):607-610.
