重铬酸钾电合成过程阳极液折光率变化规律研究
2012-12-25李成未支娟娟李珂张颂平
李成未,支娟娟,李珂,张颂平
(1.河南教育学院应用化学重点学科组,河南郑州450046; 2.郑州华信学院药学系,河南郑州 451100)
重铬酸钾电合成过程阳极液折光率变化规律研究
李成未1,支娟娟2,李珂2,张颂平1
(1.河南教育学院应用化学重点学科组,河南郑州450046; 2.郑州华信学院药学系,河南郑州 451100)
在重铬酸钾电合成过程中,实验测得阳极液在不同反应条件下不同反应时间的折光率,建立了阳极液折光率随反应条件变化的数学模型,分析了折光率的影响因素及其变化规律,模型很好地表征了折光率的变化规律,表明折光率变化速率平稳,电解过程中电流效率基本不变.
重铬酸钾;阳极液;电合成;折光率;数学模型
铬盐是无机化工的主要系列产品之一,广泛应用于冶金、制革、材料、颜料、电镀、印染、木材防腐、橡胶等工业部门,在国民经济中占有重要地位,在国际上被列为最具竞争力的8种资源性原料之一[1].重铬酸钾是铬化合物生产中产生污染最严重、三废最多的产品,也是生产其他铬化合物的基础产品之一.其传统生产技术有碳酸钾碳化法、复分解法、霞石焙烧法、碳酸钾硫酸法、铬酸钾碳化法和苛性钾碳化法等,但这些方法技术落后、资源利用率低、能耗高,排放大量铬渣和有毒废水、废气及含铬芒硝等副产物[2],铬渣经雨水冲淋后,其中的大量六价铬离子随雨水溶渗、流失、渗入地表从而污染水源、危害农田、水产品和人体健康.其对环境造成的危害,已越来越引起广泛注意,我国和世界发达国家一样,将其列入危险固体废物名录[3-4].所以开发重铬酸钾清洁生产新技术具有急切的社会需求,技术改造刻不容缓.国内外进行了大量的研究工作[1-2,5-8],其中具有广泛发展前景的被称为绿色生产技术的电合成法是最近的研究热点之一[9-10].电合成法与传统的生产方法相比,副产品O2、H2和KOH可循环使用,可在温和条件下最大程度地实现含铬副产品的零排放和目标反应的原子经济性,其基础研究亟待进行.为了更多地提供基础数据和生产过程的有效监控,本文根据测定的重铬酸钾电合成过程铬酸钾阳极液折光率,由数学模型表征了折光率随反应时间的变化规律.
1 实验
1.1 主要试剂及材料
铬酸钾和氢氧化钾均为分析纯试剂.实验用水为Master-Q型超纯水机制备的超纯水.阳离子交换膜为Aciplex®-F4603型全氟磺酸/羧酸复合膜.
1.2 主要仪器
自制两室复极式电解槽,TPR-3010D型直流稳压、稳流电源;WAY(2WAJ)型阿贝折射仪.
1.3 实验过程
实验在自制金属两室电解槽中进行,两室内各装电动搅拌器以消除温度差和传质的影响,两室出口各装有冷凝管.两室中间是固定的Aciplex®-F4603型阳离子交换膜,膜两边分置钛基多元金属氧化物复合阳极和不锈钢阴极.反应温度由超级恒温水浴控制,控温精度±0.1 K.
实验开始时,在阴、阳极室分别加入350 mL给定浓度的KOH和K2CrO4水溶液,在搅拌下并控制一定反应温度,开始恒电流反应,用阿贝折射仪测量不同反应时间的阳极液折光率.
1.4 电合成反应原理
在直流电的作用下,阳极液的水失去电子产生O2而不断析出,同时产生的H+酸化CrO而转变为Cr2O,水合K+离子通过阳离子交换膜进入阴极室;在阴极区,水得到电子产生H2而析出,同时产生的OH-与从阳极室迁移来的K+形成KOH溶液,OH-由于受阳离子交换膜羧酸层的排斥而不会反渗透至阳极室.当阳极液中Cr2O达到一定浓度时,电解结束.这时阳极液为以Cr2O为主并含有少量未转化的CrO的溶液.其反应方程式[1]为
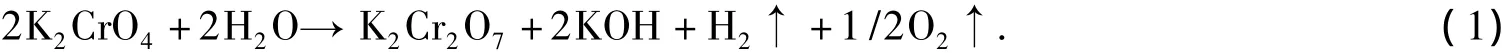
2 结果与讨论
根据电合成反应原理,在电解液与电极相界面处存在着扩散、吸附、表面反应、解吸等基元过程.水合钾离子由阳极室向阴极室的迁移过程亦存在众多物理化学过程,即吸附、溶解、穿透、解吸、扩散、反应等基元过程[9].显然,电合成过程是集物理过程和化学过程为一体的非均相反应体系,随着电合成反应的进行,阳极液浓度、黏度、组成、酸度等反应参数和物理性质都在发生变化,从而引起阳极液折光率发生改变.
根据上述实验方法,控制电流密度为3 kA/m2,分别测定阳极液初始铬酸钾浓度c0为1.016 mol/L、1.576 mol/L和2.005 mol/L,反应温度T为333.15 K、343.15 K和353.15 K时,不同反应时间t下的阳极液折光率,如图1、2所示.

图1 重铬酸钾电合成反应进程中阳极液不同初始浓度时折光率的变化Fig.1Plot of refractive index against reaction time at different initial concentrations of anolyte in electrosynthesis process of potassium dichromate
由图1、2看出,在重铬酸钾电合成反应过程中,不同温度、阳极液不同铬酸钾初始浓度时的折光率随反应时间的变化关系相当类似.反应温度一定时,阳极液的折光率随反应进程而减小,随阳极液初始浓度增大而增大;当阳极液初始浓度一定时,阳极液的折光率随反应进程亦减小,随温度升高而增大.
不同反应条件下阳极液折光率的变化规律相似,并呈线性关系,显然,重铬酸钾的电合成过程稳定,电流效率稳定[11].因此,阳极液折光率n随反应时间t的变化关系即可用线性方程表征,

式中A和B为参数.
用最小二乘法按式(2)拟合实验数据,可得参数A、B和复相关系数R2的值,如表1所示.由表1看出,参数A随c0增大而减小,随T变化不明显;参数B随c0和T的增大而增大.经对数据拟合,参数A和B可用下式计算

显然,阳极液铬酸钾初始浓度c0和反应温度T一定,A和B即可按式(3)、(4)确定,进而按式(2)计算不同反应时间下的折光率n,部分结果见图1、2(图中直线为模型计算值).计算值与实验数据相比较,64个实验点的总标准误差和总平均相对误差分别为0.008 8和1.48%.因此,所建模型很好地表征了阳极液折光率随反应时间、铬酸钾初始浓度和温度的变化规律,为重铬酸钾电合成工艺的理论研究提供了基础数据.
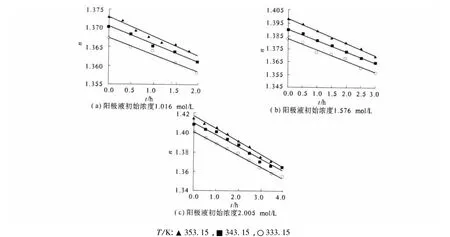
图2 重铬酸钾电合成反应进程中不同反应温度时折光率的变化Fig.2Plot of refractive index against reaction time at different temperatures in electrosynthesis process of potassium dichromate
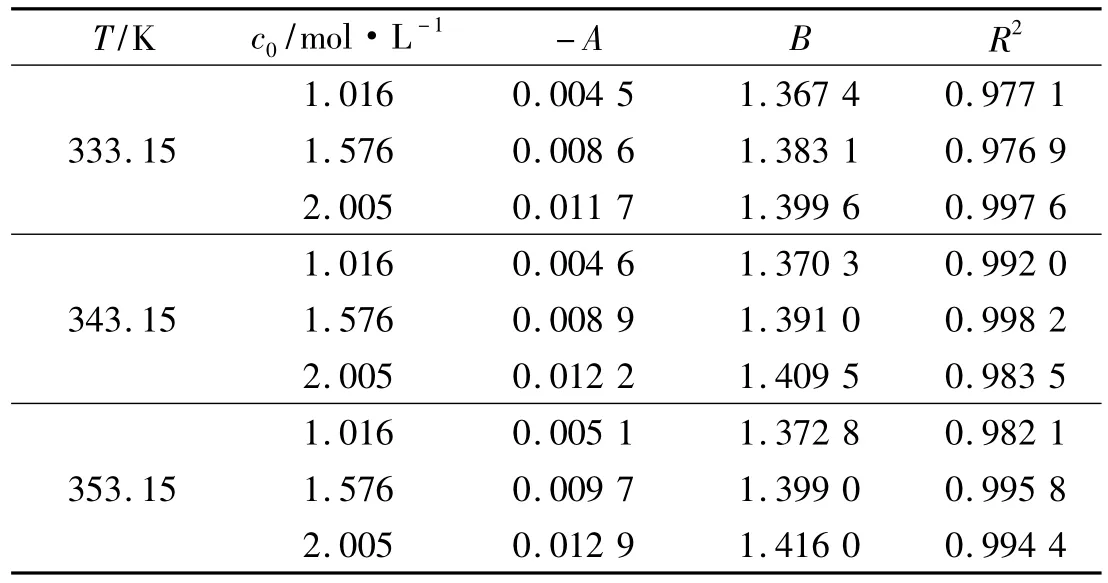
表1 不同反应条件下方程(2)参数A、B的值及复相关系数R2Tab.1Parameter A,B of Equition(2)and correlation coefficient R2at different reaction conditions
3 结论
在重铬酸钾电合成过程中,测得不同铬酸钾初始浓度、不同温度下阳极液折光率,建立了阳极液折光率随反应时间变化的数学模型,表征了折光率的变化规律.指出反应温度一定时,阳极液的折光率随反应进程而减小,随阳极液初始浓度增大而增大;当阳极液初始浓度一定时,阳极液的折光率随反应进程亦减小,随温度升高而增大.重铬酸钾的电合成过程稳定,电流效率稳定.
[1]李成未,李珂,张颂平,等.重铬酸钾电催化合成进程表征研究[J].河南教育学院学报:自然科学版,2010,19(4):25-28.
[2]李成未,齐涛,陈根生,等.重铬酸钾电化学合成反应表观动力学[J].化学通报,2011,74(5):444-449.
[3]WENG C H,HUANG C P,ALLEN H E,et al.Cr(VI)adsorption onto hydrous concrete particles from groundwater[J].Journal of Environmental Engineering,2001,127(12):1124-1131.
[4]CHEW I,OBBARD J P,STANFORTH R R.Microbial cellulose decomposition in soils from a rifle range contaminated with heavy metals[J].Environmental Pollution,2001,111(3),367-375.
[5]AHMED M I,HOLSEN T M,SELMAN J R.Electrochemical chromic acid generation process with fuel-cell electrode assistance,Part I:Removal of contaminants[J].Journal of Applied Electrochemistry,2001,31(12):1381-1387.
[6]王少娜,郑诗礼,张懿.铬盐清洁生产工艺中铝硅的脱除[J].中国有色金属学报,2007,17(7):1188-1194.
[7]杜春华.铬盐清洁工艺亚熔盐介质脱除铝酸钾、碳酸钾研究Ⅰ——溶解度[J].化工科技,2008,16(4):5-8.
[8]FRENZEL I,HOLDIK H,STAMATIALIS D F,et al.Chromic acid recovery by electro-electrodialysis:I.Evaluation of anion-exchange membrane[J].Journal of Membrane Science,2005,261(1-2):49-57.
[9]LI CHENGWEI,QI TAO,WANG FUAN,et al.Macrokinetic study of the electrochemical synthesis process of sodium dichromate[J].Chemical Engineering and Technology,2007,30(4):467-473.
[10]LI CHENGWEI,WANG FUAN,QI TAO,et al.Apparent kinetics for electrosynthesis process of chromic acid[J].Chemical Research in Chinese Universities,2009,25(4),532-536.
[11]WANG FUAN,WANG JIYAN,ZHANG PENG,et al.Measurement and model of refractive index for multicomponent chromium compounds solution[J].Chemical Engineering and Technology,2008,31(3):426-432.
Study on Rules of Refractive Index Changing of Anolyte in Electrosynthesis Process of Potassium Dichromate
LI Cheng-wei1,ZHI Juan-juan2,LI Ke2,ZHANG Song-ping1
(1.Group of Applied Chemistry Key Discipline,Henan Institute of Education,Zhengzhou 450046,China; 2.Department of Pharmacy,Zhengzhou Huaxin College,Zhengzhou 451100,China)
Refractive index of anolyte was experimentally determined at different reaction times under different reaction conditions in the electrosynthesis process of potassium dichromate.A mathematical model of the dependence of refractive index on reaction condition was upbuilt.Factors affected refractive index of anolyte and its law were analyzed.The model proves to be well in reflecting the rules of refractive index changes.The results show that the change rate of refractive index was stable,and the current efficiency of electrolytic process of potassium chromate was substantially unchanged.
potassium dichromate;anolyte;electrosynthesis;refractive index;mathematical model
TQ131.13
A
1007-0834(2012)02-0001-04
10.3969/j.issn.1007-0834.2012.02.001
2012-03-16
河南省科技攻关项目(112102310424)
李成未(1966—),男,河南兰考人,河南教育学院应用化学重点学科组教授,工学博士,研究方向:绿色化学与清洁生产.
