卷柏属植物化学成分及药理活性研究进展
2012-12-23徐康平谭桂山
邹 辉,徐康平,谭桂山,2*
1中南大学药学院,长沙410013;2 中南大学湘雅医院,长沙410008
卷柏属(Selaginella)为蕨类植物门卷柏科(Selaginellaceae)植物,约有700 种,广泛分布于全世界,我国约有60-70 种[1],分布于全国各地。《中国药典》2010年版[2]收载了卷柏(S. tamariscina(Beauv.)Spring)和垫状卷柏(S.pulvinata (Hook.et Grev.)Maxim)。民间作为药用的有鳞叶卷柏(S.lepidophylla),江南卷柏(S.moelledndorfii Hieron),兖州卷柏(S.involvens spring),深绿卷柏(S.doederleinii Hieron),薄叶卷柏(S. delicatula),中华卷柏(S.sinensis),翠云草(S.uncinata (Desv.)Spring)等20多个品种[3]。
近年来卷柏属植物因其独特的生物学特征受到人们的关注,引起了国内外众多学者的研究兴趣。为进一步深入研究和开发利用卷柏属植物,作者对国内外学者多年来对该属植物的化学成分、药理活性等方面的研究进行系统综述,以期为相关研究者提供参考。
1 化学成分
1.1 黄酮类
卷柏属植物黄酮类成分丰富,结构复杂多样,自1971 年日本学者Okigawa Masayoshi 等[4]首次从S.tamariscina 中分离得到穗花杉双黄酮等5 种黄酮类化合物以来,国内外学者先后从卷柏属植物中分离得到近百种黄酮类化合物,其中包括双黄酮类、黄酮及色原酮类。
1.1.1 双黄酮类
目前从卷柏属植物中分离得到的双黄酮类化合物共有68 种,其结构复杂,连接方式多样,主要有C-C 和C-O-C 两种连接方式。根据连接方式的不同可以把它们分为五类:
1)3',8''-双芹菜素型,即amentoflavone 型(I);
2)3',6''-双芹菜素型,即robustaflavone 型(II);
3)4'-O-6''-双苯醚型,即hinokiflavone 型(III);
4)3-O-4'''-双苯醚型,即delicaflavone 型(Ⅳ);
5)3'-O-4'''双苯醚型(Ⅴ)。
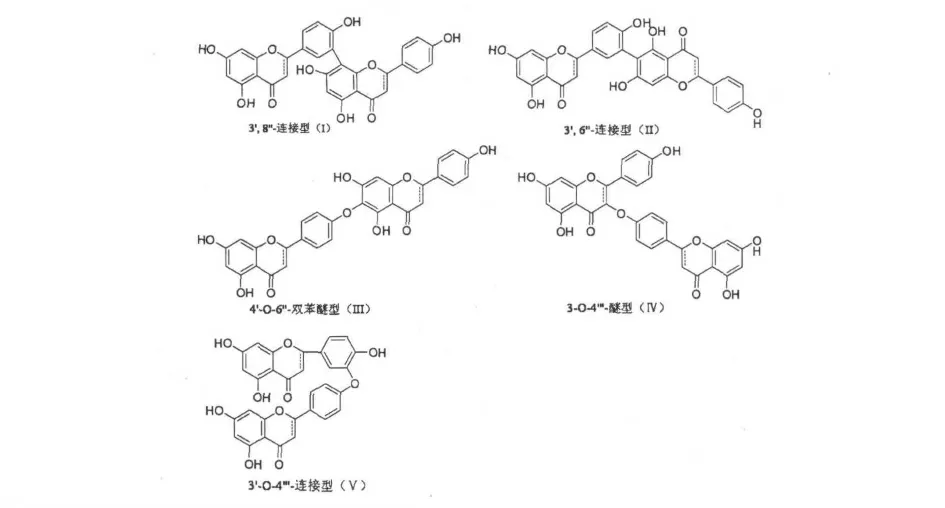

表1 卷柏属植物中分离得到的双黄酮类化合物Table 1 Biflavones from genus Selaginella

15 Sequoiaflavone S.bryopteris[11]、S.tamariscina[32]16 2,3-Dihydroamentoflavone S. bryopteris[11]、S. stautoniana[22]、S. tamariscina[29]、S. uncinata[31]、S.moellendorfi[33]17 Sumaflavone S.tamariscina[5]18 4'-O-methyl-2'',3''-dihydroamentoflavone S.uncinata[12,31]19 Isoginkgetin S.moellendorfii[15]、S.pulvinata[19]20 (2S)-4'-O-methyl-2,3-dihydroamentoflavone S.uncinata[31]21 (2S,2''S)-2,3,2'',3''-4'-O-methyl-tetrahydroamentoflavone S.uncinata[31]22 7''-Hydroxy-2,3-dihydroamentoflavone S.moellendorfii[33]II 23 Robustaflavone S. tamariscina[5]、S. willdenowii[10]、S. uncinata[12]、S. moellendorfii[16]、S.delicatula[17]、S. labordei[21]S. lepidophylla[25]、S. uncinata[34,35]、S. lepidophylla[36]、24 7''-O-methylrobustaflavone S.willdenowii[10]25 4'-O-methylrobustaflavone S.moellendorf?i[15,16]、S.delicatula[17]、S.labordei[21]、S.uncinata[34,35]26 7,4'-Di-O-methylrobustaflavone S.delicatula[17,30]27 7,4'-Di-O-methyl-2'',3''-dihydrorobustaflavone S.delicatula[17]28 7,4',7''-Tri-O-methyl-2'',3''-dihydrorobustaflavone S.delicatula[17]29 7,4',7"-Tri-O-methyl-2,3-dihydrorobustaflavone S.delicatula[37]30 7,4',4'''-Tri-O-methylrobustaflavone S.delicatula[30]31 4',4'''-Di-O-methylrobustaflavone S.delicatula[30]32 4'-O-methyl-2'',3''-dihydrorobustaflavone S.uncinata[12,34]33 2,3,2'',3''-tetrahydrorobustaflavone S.uncinata[34,35]34 4'''-O-methyl-(2S,2''S)-2,3,2'',3''-tetrahydrorobustaflavone S.uncinata[35]35 4'-O-methyl-(2S,2'' S)-2,3,2'',3''-tetrahydrorobustaflavone S.uncinata[35]36 7''-O-methyl-(2S,2'' S)-2,3,2'',3''-tetrahydrorobustaflavone S.uncinata[35]37 4'-O-methyl-(2S)-2,3-dihydrorobustaflavone S.uncinata[35]38 5-O-methyl-2,3-dihydrorobustaflavone S.lepidophylla[36]39 2,3-Dihydrorobustaflavone S.lepidophylla[36]40 7,4',7''-Tri-O-methylrobustaflavone S.moellendorfii[16]、S.doederleinii[38]41 7,7''-Di-O-methylrobustaflavone S.moellendorfii[16]42 7,4',7''-O-trimethyl-2,2'',3,3''-tetrahydrorobustaflavone S.doederleinii[38]

III 43 Hinokiflavone S.tamariscina[4,7,8]、S. bryopteris[11]、S. uncinata[14]、S. moellendorfii[16,39]、S.pulvinata[19]、S.stautoniana[23]44 Isocryptomerin S.tamariscina[4,7,29]、S.willdenowii[10]、S.moellendorffli[15]、S.pulvinata[19]45 Cryptomerin B S.denticulata[26]46 2'',3''-Dihydroisocryptomerin S.willdenowii[10]47 2,3-Dihydroisocryptomerin S.delicatula[37]48 Chamaecyparin/Pulvinatabiflavone S.pulvinata[18]、S.tamariscina[32]、S.delicatula[37]49 7-O-methyl-2'',3''-dihydroisocryptomerin S.delicatula[30]50 2,3-Dihydrohinokiflavone S.bryopteris[11]51 2,3,2'',3''-Tetrahydrohinokiflavone S.bryopteris[11]、S.rupestris[20]52 Neocryptomerin S.bryopteris[11]53 2'',3''-Dihydrohinokiflavone S.bryopteris[11]54 7,4'''-Di-O-methyl-2,3,2'',3''-ltetrahydrohinokiflavone S.rupestris[20]55 7"-O-methyl-2,3,2'',3''-tetrahydrohinokiflavone S.uncinata[12]Ⅳ 56 Delicaflavone S.delicatula[37]57 Chrysocauloflavone I S.chrysocaulos[11]58 Chrysocauloflavone II S.chrysocaulos[11]59 5,7,4',5''-Tetrahydroxy-7''-metroxy-[3-O-4''']biflavone S.uncinata[13]V 60 2,3-Dihydro-5,5'',7,7'',4'-pentahydroxy-6,6''-dimethyl-[3'-O-4''']-biflavone S.labordei[40]61 5,5'',7,7'',4'-Pentahydroxy-6,6''-dimethyl-[3'-O-4''']-biflavone S.moellendorffii[33]62 Ochnaflavone S.moellendorffii[33]63 2'',3''-Dihydroochnaflavone S.moellendorffii[33]、S.labordei[40]其它连接 64 Chrysocauloflavone III S.chrysocaulos[11]65 Isochamaejasmin S.chrysocaulos[11]66 2',8''-Biapigenin S.tamariscina[5]67 Taiwaniaflavone S.tamariscina[5]68 2,3-Dihydro-3',3'''-biapigenin S.labordei[40]
1.1.2 黄酮及色原酮类化合物
卷柏属植物中分离得到的黄酮类化合物主要为芹菜素及其衍生物,近年来从卷柏属植物中分离得到的一些新型的黄酮类化合物引起了研究者的关注。郑俊霞[44]及刘建峰[6,45]等分别从翠云草和卷柏中分离得到3 个6 位连苯基的新型芹菜素的衍生物(76,77,82);我国学者先后从江南卷柏中分离得到了6 个新的5 位连羧基或酯基的芹菜素衍生物[15,43,48](75,84-86,89,90)。杨帆等[47]首次在薄叶卷柏中发现查尔酮(88)。
迄今为止,色原酮类化合物在卷柏属植物中较为少见,马玲云等[14,49]从翠云草中分离得到三个具有抗病毒活性的色原酮类化合物(97~99)。

表2 卷柏属植物中的黄酮及色原酮类化合物Table 2 Flavones and chromogens from genus Selaginella

91 Quercetin-3-O-α-L-rhamnopyranoside S.stautoniana[22]92 Kaempferol-3-O-α-L-rhamnopyranoside S.stautoniana[22]93 7-O-(β-glucopyranosyl(1→2)-[β-glucopyranosyl(1→6)]-β-glucopyranosyl)flavone-3',4',5,7-tetraol S.moellendorffii[33]94 7-O-(β-glucopyranosyl(1→2)-[β-glucopyranosyl(1→6)]-β-glucopyranosyl)flavone-4',5,7-triol S.moellendorffii[33]95 Apigenin-7-O-β-neohesperidoside S.moellendorffii[39]96 Apigenin-8-C-β-D-glucopyranoside S.moellendorffii[39]97 Uncinoside A S.uncinata[14,49]98 Uncinoside B S.uncinata[14,49]99 8-Methyl eugenitol S.uncinata[14,49]
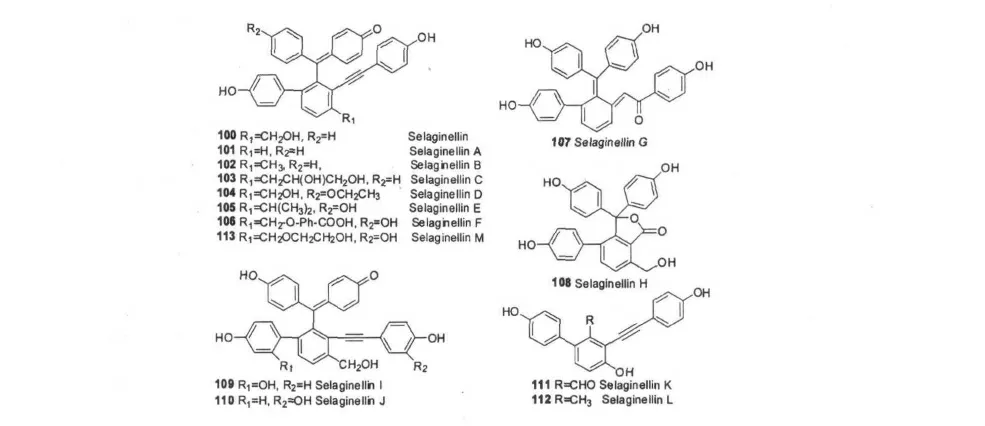
1.2 炔酚类化合物
2007 年,张丽平等[50]首次从中华卷柏(S.sinensis (Desv.)Spring)中分离得到一类具有全新碳骨架的炔酚类化合物(Alkynyl phenols),并通过X-ray确证了其结构和空间构象。这类化合物具有较大的共轭体系,具有特征的紫外吸收,这一研究吸引了国内外学者的高度关注,此后,研究者又从卷柏属植物中分离出了13 个炔酚类化合物(表3)。值得注意的是Cao Y 等[19]从垫状卷柏中分离得到两个炔键断裂的化合物(107 和108),尽管其分子中并无炔键,但仍具有较大的共轭体系,本文将其归属为炔酚类化合物。目前,这一类化合物仅在卷柏属植物中发现,在其它植物中未见相关文献报道。而我国学者对此类化合物的化学及生物学等方面的研究正方兴未艾。

表3 卷柏属植物中的炔酚类化合物Table 3 Alkynyl phenols from genus Selaginlla
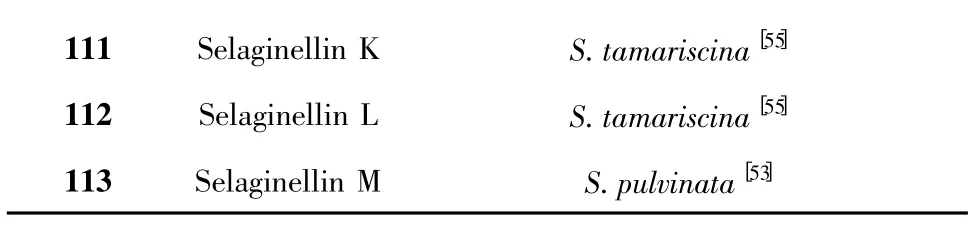
111 Selaginellin K S.tamariscina[55]112 Selaginellin L S.tamariscina[55]113 Selaginellin M S.pulvinata[53]
1.3 苯丙素类化合物
卷柏属植物中分离得到的苯丙素类化合物以简单苯丙素和木脂素类居多,香豆素类化合物报道较少。
1.3.1 简单苯丙素类
卷柏属植物中的简单苯丙素类以咖啡酸衍生物较为常见,并且研究者从中分离得到多个新的咖啡酸衍生物。如王跃虎等[56]从江南卷柏中分离得到6 个苯丙素类化合物(114~119),其中包括4 个新的咖啡酸衍生物。毕跃峰等[57]从卷柏中分离得到卷柏酯A,1-(4'-Hydroxyl-3'-methoxyphenyl)glycerol,阿魏酸,咖啡酸(120~123)。
此外,林瑞超等[9]从深绿卷柏中分离得到两个苯丙酮类化合物:3-羟基-1-(3-甲氧基-4-羟基苯基)-1-丙酮(124)和3 -羟基-1-(3,5-二甲氧基-4-羟基苯基)-1-丙酮(125)。冯卫生等[58]从中华卷柏中分离得到丁香苷(126)。Wu B 等[33]从江南卷柏中分离得到127。
1.3.2 香豆素类
卷柏属植物中香豆素类成分的报道较少,刘建峰等[6]从卷柏中分离得到4-羟基苯基-6,7-二羟基香豆素(128)。毕跃峰等[57]从卷柏中分离得到7-羟基香豆素(129)。
1.3.3 木脂素类
卷柏属植物中的木脂素类化合物的结构类型多样,其中以苯骈呋喃类、四氢呋喃及双四氢呋喃类型较为多见。
王跃虎等[56]从江南卷柏中分离得到8 个木脂素(130~137),其中包括6 个新的木脂素,130~136 均属苯骈呋喃类。郑晓珂等[59-61]分别从卷柏和江南卷柏中分离得到卷柏苷B(138)、卷柏苷C(139)和Moellenoside A(140),其中139 和140 为两个新的苯骈二氢呋喃型木脂素。Wang YZ 等[62]从中华卷柏中分离得到1 个新的倍半木脂素:Sinensiol A(141)。冯卫生等[58,63]从中华卷柏中分离得到两个新的裂木脂素(142,143)以及丁香脂素(144)、丁香脂素-4,4'-O-二-β-D-葡萄糖苷(145)、(7S,8R)-4,9,9'-三羟基-3,3'-二甲氧基-7,8-二氢苯并呋喃-1'-丙基新木脂素(146)、(–)-松脂素(147)、松脂酚-4-O-β-D-葡萄糖苷(148)、落叶松树酯醇(149)、落叶松树酯醇-4-O-β-D-葡萄糖苷(150)、Styraxlignolide D(151)、罗汉松脂素-4,4'-O-双-β-D-葡萄糖苷(152)。冯卫生等[39]从江南卷柏中分离得到一个新的去甲木脂素苷(Moellenoside B,153)。
此外,林瑞超等[9]从深绿卷柏中分离得到五个木脂素类化合物:(–)-Lirioresinol A(154),(–)-Lirioresinol B(155),(+)-Wikstromol(156),(+)-Nortracheloside(157),(+)-Matrairesinol(158),它们均属于木脂内酯类化合物。戴忠等[28]从中华卷柏中分离得到松脂醇二葡萄糖苷(159)。Lin LC等[17]从薄叶卷柏中得到三个咖啡酰奎宁酸类化合物(160~162)。毕跃峰等[57]从卷柏中分离得到163 和144。张红伟等[42]从垫状卷柏中分离得到的卷柏苷A 即为卷柏苷B,并无卷柏苷A 这一化合物,此外还分得丁香脂素-4,4'-O-二-β-D-葡萄糖苷(145);Wu B 等[33]从江南卷柏中分离得到6 个木脂素类化合物(164~169),其中包括2 个新的木脂素(164,165)。

表4 卷柏属植物中的苯丙素类化合物Table 4 Phenylpropanoids from genus Selaginlla

147 (–)-Pinoresinol S.sinensis[63]148 Pinoresinol-4-O-β-D-glucopyranoside S.sinensis[63]149 Lariciresinol S.sinensis[58]、S.moellendorffii[39]150 Lariciresinol-4-O-β-D-glu-copyranoside S.sinensis[58]151 Styraxlignolide D S.sinensis[58]152 Matairesinol-4,4'-di-O-β-D-glucopyranoside S.sinensis[58]153 Moellenoside B S.moellendorffii[39]154 (–)-Lirioresinol A S.doederleinii[9]155 (–)-Lirioresinol B S.doederleinii[9]156 (+)-Wikstromol S.doederleinii[9]157 (+)-Nortracheloside S.doederleinii[9]158 (+)-Matrairesinol S.doederleinii[9]159 Pinoresinol digucoside S.sinensis[28]160 3,5-Di-O-caffeoylquinic acid S.delicatula[17]161 3,4-Di-O-caffeoylquinic acid S.delicatula[17]162 4,5-Di-O-caffeoylquinic acid S.delicatula[17]163 (2R,3S)-dihydro-2-(3',5'-dimethoxy-4'-hydroxyphenyl)-7-methoxy-5-acetyl-benzofuran S.tamariscina[57]164 (7'E)-3,5,3',5'-tetramethoxy-8:4'-oxyneolign-7'-ene-4,9,9'-triol S.moellendorffii[33]165 3,3'-Dimethoxylign-8'-ene-4,4',9-triol S.moellendorffii[33]166 (7'E)-3,3',5'-Trimethoxy-8 :4'-oxyneolign-7'-ene-4,7,9,9'1-tetraol S.moellendorffii[33]167 Picraquassioside C S.moellendorffii[33]168 (7'E)-3,5,3',5'-Tetramethoxy-8 :4'-oxyneolign-7'-ene-4,7,9,9'-tetraol S.moellendorffi[33]169 Secoisolariciresinol S.moellendorffii[33]
1.4 生物碱类
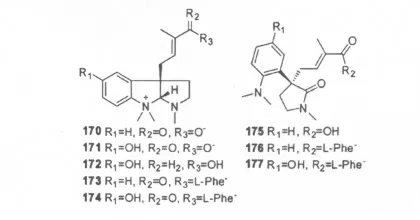
王跃虎等[64]从江南卷柏中分离得到8 个吡咯烷吲哚类(Pyrrolidinoindoline)生物碱(170~177),并用化学合成修饰模拟了这些生物碱之间的生源转化途径。王跃虎等[56]从江南卷柏中分离得到Paucine 3'-β-D-glucopyranoside (117 )、 Paucine(118)、N-cis-p-coumaroylagmatine(119),此三个化合物亦被归属为苯丙素类化合物。
1.5 甾体类
卷柏属植物中的甾体类化合物以甾醇类为主。谭桂山等[18]从垫状卷柏中分离得到一个新的胆甾酮类化合物:垫状卷柏胆甾酮(179)。郑兴等[41,65]从垫状卷柏中分离得到β-谷甾醇(180)和一个新的甾体(3β,16α-Dihydroxy-(5α)-cholestan-21-oic acid,181)。高亮亮等[66]从卷柏中分离得到181,此外还发现两个新的甾体(182~183)。王雪等[46]从卷柏中分离得到3β-羟基-7α-甲氧基-24β-乙基-胆甾-5-烯、胆甾醇、胡萝卜苷(184~186)。鲁曼霞等[24]从兖州卷柏中分离得到豆甾醇和β-D-glucopyranoside,(3β)-cholest-5-en-3yl(187~188)。Roh EM 等[67]从卷柏中分离得到6 个甾醇(189~194),其中191 的结构中5,8 位连有双氧桥。此外,刘海青等[68]在旱生卷柏中发现化合物179 和191。
1.6 萜类
目前卷柏属植物中分离得到的萜类较少,并且主要为五环三萜类。王雪等[46]从卷柏中分离得到海棠果酸(195)、白桦脂酸(196)。鲁曼霞等[24]从兖州卷柏中分离得到β-香树脂醇(197)。杨帆等[47]从薄叶卷柏中分离得到甘草次酸(198)、木栓烷酮(199)。此外Wang HS 等[48]从江南卷柏中分离得到一个单萜((4Z,6E)-2,7-dimethyl-8-hydroxyocta-4,6-dienoic acid 8-O-β-D-glucopyranoside,200)。
1.7 蒽醌类
刘海青等[23,68-69]从旱生卷柏中分离得到了5 个蒽醌:大黄酚、大黄素、大黄酸、大黄素甲醚、芦荟大黄素(201~205)。王雪等[46]从卷柏中分离得到3-甲氧基-1,8-二羟基蒽醌(206)。刘建锋等[6]从卷柏中分离得到1-甲氧基-3-甲基蒽醌(207)。杨帆等[70]从薄叶卷柏中分离得到三个蒽醌苷:大黄素甲醚-8-O-β-D-葡萄糖苷,大黄酚-8-O-β-D-葡萄糖苷,大黄素-8-O-β-D-葡萄糖苷(208~210)。
1.8 有机酸类
郑兴等[14]从垫状卷柏中分离得到对羟基苯甲酸。毕跃峰等[57]从卷柏中分离得到香荚兰酸和丁香酸。刘海青等[69]从旱生卷柏中分离得到棕榈酸(十六烷酸)、三十烷醇、三十烷酸。郑俊霞[71]等从翠云草中分离得到阿魏酸棕榈酸-16-醇酯、对羟基桂皮酸、对羟基苯乙酮、香草醛。
1.9 其他成分
郑晓珂等[59,60]从卷柏中得到D-甘露醇、酪氨酸、腺苷、熊果苷、鸟苷。戴忠等[72]从中华卷柏中分离得到一个新的糖苷(Selaginoside,211)。此外,卷柏属植物还含有丰富的微量元素,以S、P、Si、Fe、Mg、Al、Ca、K 为主[73]。
2 药理活性
卷柏属药用植物在我国民间被广泛应用,现代药理研究表明该属植物具有抗肿瘤、抗炎、抗菌抗病毒、免疫调节、降血糖及扩张血管等药理活性。近年来,对卷柏属植物药理活性的研究引起了研究人员的高度重视。双黄酮类成分是卷柏属的主要活性成分之一,国内外学者对卷柏属植物药理活性的研究多集中在双黄酮类成分,对穗花杉双黄酮(Amentoflavone,AME)的药理活性研究较为深入。此外,卷柏属特征性炔酚类成分的药理活性研究也受到了研究者的关注。
2.1 抗肿瘤作用
卷柏抗肿瘤活性成分及其作用的研究已成为卷柏属植物药理活性研究的重要方面,从目前的研究来看,双黄酮是其主要的活性成分,作用机制主要为:(1)细胞毒作用;(2)诱导细胞凋亡,包括上调p53 基因表达,激活caspase 系统,抑制COX-2 等炎症因子等。
2.1.1 卷柏提取物
卷柏不同萃取部位对人髓性白血病细胞株(U937)均具有较强的杀伤作用,对正常的人淋巴细胞没有影响,其中水萃取部位能有效提高抑癌基因p53 基因表达,并诱导细胞周期阻滞于G1 期,饲喂含1%卷柏的饲料可引起前胃上皮中增生细胞核抗原(PCNA)明显减少[74]。卷柏水提物(ST)对人白血病细胞(HL-60)具有细胞毒作用,这种作用能被超氧化物歧化酶(SOD)和过氧化氢酶等活性氧清除剂所抑制;此外,ST 还能通过激活caspase-3 诱导肿瘤细胞凋亡,此过程中伴随着PARP 的裂解,还能引起促细胞凋亡基因Bax 水平的升高以及Bcl-2 表达的下调,而这一作用亦能被超氧化物歧化酶和过氧化氢酶减弱,这表明ST 诱导细胞凋亡是通过caspase-3 激活所介导的,而其细胞毒性可能与氧化应激有关[75]。Yang SF 等[76]对卷柏50%乙醇提取物(STE)抗肺癌作用进行了研究,它通过对人肺癌A549 和LLC 细胞以及LLC 肿瘤小鼠实验证实STE能显著抑制A549 和LLC 的侵袭,能下调肿瘤迁移相关蛋白MMP-2,-3 和u-PA 的水平。高浓度的深绿卷柏提取物对人鼻咽癌细胞TW03 具有较好的抑制作用,其作用机制可能是下调Bcl-2 和上调Bax表达,使Bcl-2/Bax 表达比例降低,诱导TW03 细胞周期阻滞于S 期,从而导致TW03 细胞凋亡[77]。S.bryopteris 水提物经硅胶柱后的苯洗脱部位(主含双黄酮类成分)对由甲基异氰酸酯(致癌物)诱导的人肾上皮细胞(HEK-293)、人克隆上皮细胞FHC、人肺成纤维细胞(HLF)、鼠卵巢上皮细胞、鼠肾上皮细胞(MM55.K)和鼠精原上皮细胞(GC-1)凋亡具有明显的保护作用,能抑制白细胞介素-8(IL-8)、白细胞介素1β(IL-1β)以及肿瘤坏死因子(TNF)的表达;能降低3,4-苯并芘(BP)诱导的肺腺瘤的发生率,能显著降低甲基苯丙蒽(DMBA)和巴豆油诱导的皮肤癌小鼠的比例以及小鼠肿瘤的数目,结果表明S.bryopteris 具有抗癌作用[78]。
2.1.2 黄酮类化合物
从江南卷柏中分离得到的银杏双黄酮(8)对人卵巢腺癌OVCAR-3 具有细胞毒作用,且高浓度的GIN 能引起OVCAR-3 细胞凋亡,其作用机制是经体内产生过氧化氢而激活caspase-3 而发挥药效[79]。Cao Y 等[15]发现双黄酮类化合物8、19、25 和44 对人肿瘤细胞株A549、BGC-823 和BEL-7402 具有选择性细胞毒性。孙颖祯等[80-82]研究发现细叶卷柏中的双黄酮类化合物对肝癌细胞Bel-7402 具有抑制作用,并且能诱导肿瘤细胞凋亡,而翠云草总黄酮和江南卷柏总黄酮能在mRNA 水平上抑制COX-2,抑制COX-2 蛋白的表达,降低PGE2 的含量,从而抑制肿瘤细胞的增殖,这可能是翠云草和江南卷柏抗肿瘤作用的机制。薄叶卷柏中的7,4'-二甲基罗伯斯塔双黄酮(26)和7,4'-二甲基-2'',3''-二氢罗伯斯塔双黄酮(27)能有效抑制淋巴瘤Raji 及呼吸道上皮Galu-1 肿瘤细胞的生长[18];4',4'''-二甲基罗伯斯塔双黄酮(31)、7,4'-二甲基-2,3-二氢穗花杉双黄酮(12)对小鼠白血病细胞P-388 及人结肠癌细胞HT-29 均有杀伤作用[10]。
2.2 抗炎作用
2.2.1 卷柏提取物
卷柏70%醇提物能抑制药物诱发的过敏性休克,能浓度依赖性地阻滞被动皮肤过敏反应以及皮肤不良反应;能抑制肥大细胞脱颗粒和胞吐,升高肥大细胞内的cAMP 水平从而阻止肥大细胞激活并降低组胺的释放,最终抑制炎症反应[83]。
2.2.2 黄酮类化合物
Banerjee T 等[84]发现AME 的抗炎机制主要是通过强烈的抑制核转录因子-κB(NF-κB)与DNA 的结合,抑制IκBα 的水解及NF-κB 的核转位,进而抑制COX-2 的表达。Woo ER 等[85]研究表明AME 是通过抑制IκBα 的水解及NF-κB 的激活,进而抑制LPS 诱导的NO 的产生,发挥抗炎作用;2',8''-双芹菜素(66)也通过这一途径发挥抗炎作用[86]。Sumaflavone(17)能强烈抑制NO 的生产,其作用机制是通过抑制AP-1 的活性,从而抑制诱生型一氧化氮合酶(iNOS)的基因表达,但其对NF-κB 的活性没有影响,这与AME 的作用机制明显不同,而Robustaflavone(23)对iNOS 基因表达以及NO 的生成没有影响,这可能与两分子黄酮单元的连接方式不同有关[87]。
2.3 抗菌、抗病毒作用
2.3.1 卷柏提取物
翠云草醇提物的乙酸乙酯萃取部位具有较好的抗单纯疱疹病毒(HSV-1)和柯萨奇病毒(Cox B3)的作用[88]。江南卷柏不同部位提取物对柯萨奇病毒CVB3 均具有一定的抑制作用,包括抑制CVB3 病毒生物合成和直接杀死病毒的作用,且脂溶性双黄酮部位与水溶性的双黄酮部位的活性均比单体穗花杉双黄酮的活性要强[89];而其对单纯疱疹病毒I 型(HSV-1)的实验则表明江南卷柏脂溶性双黄酮部位与水溶性的双黄酮部位的活性均要低于单体穗花杉双黄酮的活性[90]。兖州卷柏和S. inaequalifolia 的石油醚、苯、甲醇和水萃取部位对大肠杆菌(E.coli)和假单胞菌(Pseudomonas)均具有一定的抑制作用[91]。
2.3.2 黄酮类化合物
Ma SC 等[92]研究表明AME 具有较好的抗呼吸道合胞病毒(RSV)的活性。Jung HJ 等[93]发现AME 对白色念珠菌、酿酒酵母及白色毛孢子菌等真菌具有较强的抑制作用,并且无溶血作用。Lee JY等[94-95]研究发现卷柏中的异柳杉双黄酮(ISO,44)具有抗真菌的作用,并且不会导致溶血,其作用机制可能是破坏细菌的细胞膜;ISO 对多种革兰氏阴性、阳性菌有较强的抗菌作用,包括对甲氧西林耐药的金黄色葡萄球菌,并且ISO 与头孢噻肟酸(cefotaxime)有协同作用。兖州卷柏中的AME、β-D-glucopyranoside,(3β)-cholest-5-en-3yl(188)和β-香树脂醇(197)具有较强的抗肺炎链球菌的作用[24]。从江南卷柏中分离得到的两个新的黄酮类化合物(85~86)能抑制人肝癌细胞株HepG2.2.15 的乙型肝炎病毒表面抗原(HbsAg)的分泌,从而发挥抗HBV的作用[15]。
2.3.3 新型炔酚类化合物
垫状卷柏中的炔酚类成分100、104 和107 具有较好的抗白色念珠菌的活性;100~102 显示了较好的抗金黄色葡萄球菌的活性[19,52]。
2.4 抗氧化及抗衰老作用
2.4.1 卷柏提取物
细叶卷柏对黄嘌呤氧化酶(XOD)有很强的抑制活性,对脂氧化酶(LOX)也有一定的抑制作用,能显著清除ABTS+自由基,并能抑制COX-2 的表达[96]。
2.4.2 黄酮类化合物
徐智等[97]发现AME 与垫状卷柏双黄酮(48)均能浓度依赖性地清除DPPH 自由基,并能显著减轻LPC 所致的ECV304 细胞损伤。垫状卷柏中的双黄酮具有抑制黄嘌呤氧化酶的活性,并且三个双黄酮的混合物的活性比单体双黄酮的活性强[98]。从中华卷柏中分离得到的多个双黄酮具有清除DPPH 自由基的活性,其中槲皮素(79)的活性最强,IC50为3.2 μM[99]。
2.4.3 新型炔酚类化合物
Wang CJ 等[100,101]首次报道了卷柏属植物中特征性炔酚类成分的药理活性,其研究表明Selaginellin 能抑制同型半光氨酸(Hcy)诱导的内皮细胞衰老,其机制可能与抑制氧化应激和上调与衰老密切相关的SIRT1 基因的表达有关;Selaginellin 能降低氧化应激反应而抑制谷氨酸诱导的PC12 细胞损伤和凋亡,其抗凋亡作用可能与上调抗衰老基因(klotho 基因)的表达有关。
2.5 免疫调节作用
卷柏能降低小鼠血清IgG、IgM、IgA 的含量,但对小鼠胸腺、脾脏及T 淋巴细胞α-醋酸萘酯酶活性没有影响[102]。从兖州卷柏中得到的有效部位能显著逆转小鼠胸腺退化,能抑制脂质过氧化,并提高小鼠免疫功能,可能成为缓解老年疾病、延长老年人寿命的抗衰老药物[103]。
2.6 降血糖作用
2.6.1 卷柏提取物
李方莲等[104]研究了卷柏水煎剂对四氧嘧啶诱导的高血糖老龄鼠模型的降血糖作用,显示卷柏水煎剂能显著降低大鼠的血糖,可较好恢复其体质,而对正常鼠的降血糖作用不明显。吴奕富等[105]研究表明卷柏能显著降低链脲佐菌(STZ)诱发的糖尿病大鼠的血糖,升高胰岛素浓度,降低MDA 的含量,而对正常大鼠血糖无影响。郑晓珂等[106]通过Ⅱ型糖尿病大鼠模型评价了卷柏不同溶剂提取部位对降糖活性的影响,证实卷柏醇提物比水提物具有更好的降糖活性,卷柏醇提物经聚酰胺柱洗脱的80%乙醇部位具有很强的降血糖作用。
2.6.2 黄酮类等化合物
韩国学者Na MK 等[107]应用蛋白酪氨酸磷酸酶1B(PTP1B)抑制活性导向的分离从卷柏甲醇提取物分离得到AME,证明AME 是PTP1B 的非竞争性抑制剂,并且AME 还能引起胰岛素受体(IR)中酪氨酸磷酸化水平增加,结果说明AME 可能通过抑制PTP1B 的活性,增强胰岛素诱导的细胞内的信号传导,从而治疗Ⅱ型糖尿病。Lee JY 等[108]报道了AME 对PTP1B 有很强的抑制作用,并采用对接模型对40 个天然双黄酮进行了活性筛选,得到了两个活性化合物:Tetrahydroamentoflavone(14)和Sumaflavone(17)。Wang HS 等[48]研究表明从江南卷柏中分离得到的一个新黄酮类化合物(90)能增强胰岛素抵抗细胞对胰岛素的敏感性,并降低细胞对胰岛素的抵抗。
2.7 扩张血管作用
体外实验表明,卷柏提取物及AME 均具有舒张血管的作用,对去氧肾上腺素引起的动脉收缩具有拮抗作用,其作用机制是通过内皮细胞依赖的NOcGMP 信号通路,并可能伴随非特异性的K+和Ca2+通道的参与,与毒蕈碱样乙酰胆碱受体和β-肾上腺素受体无关[109]。许兰等[110]对卷柏的正己烷、乙酸乙酯和正丁醇的提取物进行了扩张血管的研究,结果显示此3 种提取物均由明显的舒张血管的作用,其中乙酸乙酯提取物的作用最强,并且证明其有效成分为AME,AME 舒张血管作用存在内皮依赖性,且有NO 参与。
此外,卷柏属植物还有止血[111]、护肝[112]、心肌保护[113]、防辐射[114]等作用。
3 结语
卷柏属植物化学成分丰富,结构类型复杂,药理活性广泛,目前发现双黄酮类成分为其主要活性成分之一,随着研究的不断深入,人们发现卷柏属植物中的炔酚、生物碱、苯丙素等多类成分具有良好药理活性。从天然药物中开发高效、低毒的新药系新药开发的重要途径,对卷柏属植物的化学及生物学等进行广泛深入的研究仍然具有较大的空间和开发价值。
1 The Flora of China Editorial Committee.Flora of China.Beijing:Science Press,2004.87.
2 Chinese Pharmacopoeia Commission. Chinese Pharmacopoeia.Beijing:China Medica Science Press,2010.210.
3 Bi YF(毕跃峰),et al. The chemical constituents and phamocologicala ctivities of genus Selaginella. World Phytomed(国外医药 植物药分册),2002,17:97-99.
4 Okigawa M,et al. Biflavones in Selaginella species. Phytochemistry,1971,10:3286-3287.
5 Lee CW,et al.Biflavonoids isolated from Selaginella tamariscina regulate the expression of matrix metalloproteinase in human skin fibroblasts. Bioorg Med Chem,2008,16:732-738.
6 Liu JF,et al. A new flavonoid from Selaginella tamariscina(Beauv.)Spring.Chem Pharm Bull,2010,58:549-551.
7 Zheng XK(郑晓珂),et al.Flavnoids from Selaginella tamariscina.Chin Tradit Herb Drugs(中草药),2004,35:742-743.
8 Cheng XL,et al.Selaginellin A and B,two novel natural pigments isolated from Selaginella tamariscina. Chem Pharm Bull,2008,56:982-984.
9 Lin RC,et al.Phenolic constituents of Selaginella doederleinii.Plant Med,1994,60:168-170.
10 Silva GL,et al.Cytotoxic biflavonoids from Selaginella willdenowii.Phytochemistry,1995,40:129-134.
11 Swamy RC,et al.Structurally unique biflavonoids from Selaginella chrysocaulos and Selaginella bryopteris. Chem Biodivers,2006,3:405-414.
12 Fan XL(范晓磊),et al. Biflavonoids from Selaginella uncinata(Desv.)spring.Chin Pharm J(中国药学杂志),2009,44:15-19.
13 Lei T,et al. A new biflavonoid from Selaginella uncinata(Desv.)Spring.Chem J Int,2010,12:6.
14 Ma LY,et al. Uncinoside A and B,two new antiviral chromone glycosides from Selaginella uncinata.Chem Pharm Bull,2003,51:1264-1267.
15 Cao Y,et al. Bioactive flavones and biflavones from Selaginella moellendorffii Hieron.Fitoterapia,2010,81:253-258.
16 Jiang XP(江雪平),Chen KL(陈科力). Study on biflavonoids from Selaginella moellendorffii Hieron.Chin Pharm J(中国药学杂志),2009,44:96-98.
17 Lin LC,et al.Cytotoxic biflavonoids from Selaginella delicatula.J Nat Prod,2000,63:627-630.
18 Tan GS(谭桂山),et al. Study on chemical constituents of Selaginella pulvinata Maxim.Chin J Org Chem(有机化学),2004,24:1082-1085.
19 Cao Y,et al.Structure determination of selaginellins G and H from Selaginella pulvinata by NMR spectroscopy. Magn Reson Chem,2010,48:656-659.
20 Reddy NP,et al. New biflavonoid from Selaginella rupestris.Nat Prod Commun,2007,2:659-662.
21 Tan WJ,et al.Bioactive compounds of inhibiting xanthine oxidase from Selaginella labordei.Nat Prod Res,2009,23:393-398.
22 Feng WS,et al.Chemical constituents of Selaginella stautoniana.Chin J Nat Med,2011,9:108-111.
23 Liu HQ(刘海青),et al. Study on chemical constituents of Selaginella stautoniana(Ⅰ). Chin Tradit Herb Drugs(中草药),2003,34:298-299.
24 Lu MY(鲁曼霞),et al. Study on chemical constituents of Selaginella invovens spring and antibacterial activity. Nat Prod Res Dev(天然产物研究与开发),2009,21:973-975.
25 Qasim MA,et al.Phenolic constituents of Selaginellaceae.Indian J Chem B,1985,24B:220.
26 Lopez-Saez JA,et al. Biflavonoids of Selaginella denticulata growing in Spain.J Biosci,1994,49:267-270.
27 Sun CM,et al.Selective cytotoxicity of ginkgetin from Selaginella moellendorffii.J Nat Prod,1997,60:382-384.
28 Dai Z(戴忠),et al.Study on chemical constituentsof Selaginella sinensis(Desv.)Spring.Chin Tradit Herb Drugs(中草药),2001,32:784-785.
29 Zheng XK(郑晓珂),et al. Chemical constituents of hypolipemic parts in Selaginella tamariscina. Chin Tradit Herb Drugs(中草药),2009,40:1712-1715.
30 Chen JJ,et al. New cytotoxic biflavonoids from Selaginella delicatula.Planta Med,2005,71:659-665.
31 Zheng JX,et al.New 3',8''-linked biflavonoids from Selaginella uncinata displaying protective effect against anoxia.Molecules,2011,16:6206-6214.
32 Zhang HM(张红梅),et al. Biflavonoids from Selaginella tamariscina and NMR characteristics.Centr South Pharm(中南药学),2011,9:419-423.
33 Wu B,Wang J. Phenolic compounds from Selaginella moellendorffii.Chem Biodivers,2011,8:1735-1747.
34 Zheng JX,et al.A new biflavonoid from Selaginella uncinata.Asian J Trad Med,2007,2:92-97.
35 Zheng JX,et al.Four new biflavonoids from Selaginella uncinata and their anti-anoxic effect. J Asian Nat Prod Res,2008,10:945-952.
36 Aguilar MI,et al.Biflavonoids isolated from Selaginella lepidophylla inhibit photosynthesis in spinach chloroplasts.J Agric Food Chem,2008,56:6994-7000.
37 Lin LC,Chou CJ. Three new biflavonoids from Selaginella delicatula.Chin Pharm J(Taipei),2000,52:211-218.
38 Lee NY,et al. Identification of a new cytotoxic biflavanone from Selaginella doederleinii. Chem Pharm Bull,2009,40:1360-1361.
39 Feng WS,et al.A new norlignan lignanoside from Selaginella moellendorffii Hieron.Acta Pharm Sin,2011,1:36-39.
40 Xu JC,et al.A new biflavonoid from Selaginella labordei Hieron.ex Christ.Chin Chem Lett,2009,20:939-941.
41 Zheng X(郑兴),et al.Study on chemical constituents of selaginella pulvinata. Chin Tradit Herb Drugs(中草药),2001,32:17-18.
42 Zhang HW(张红伟),et al.Study on chemical constituents of Selaginella pulvinata. Asia Pacific Tradit Med,2008,4:36-37.
43 Zhu TM,et al. A new flavone glycoside from Selaginella moellendorffii Hieron.Chin Chem Lett,2008,19:1456-1458.
44 Zheng JX,et al.A new flavonoid with a benzoic acid substituent from Selaginella uncinata. Chin Chem Lett,2008,19:1093-1095.
45 Liu JF,et al.A new flavonoid from Selaginella tamariscina.Chin Chem Lett,2009,20:595-597.
46 Wang X(王雪),et al. Chemical constituents of Selaginella tamaricina(Beauv.)Spring.J Shenyang Pharm Univ(沈阳药科大学学报),2009,126:623-625.
47 Yang F(杨帆),et al. Chemical constituents of Selaginella delicatula.Centr South Pharm(中南药学),2010,8:496-499.
48 Wang HS,et al.Carboxymethyl flavonoids and a monoterpene glucoside from Selaginella moellendorffii. Arch Pharm Res,2011,34:1283-1288.
49 Ma LY,et al.Two new chromone glycosides from Selaginella uncinata.Chin Chem Lett,2002,13:748-751.
50 Zhang LP,et al.A new unusual natural pigment from Selaginella sinensis and its noticeable physicochemical properties.J Org Chem,2007,72:3921-3924.
51 Tan GS,et al.Selaginellin C,a new natural pigment from Selaginella pulvinata Maxim(Hook et Grev.). J Asian Nat Products Res,2009,11:1001-1004.
52 Cao Y,et al.Antimicrobial selaginellin derivatives from Selaginella pulvinata. Bioorg Med Chem Lett,2010,20:2456-2460.
53 Xu KP,et al. Selaginellin M,a new selaginellin derivative from Selaginella pulvinata. J Asian Nat Prod Res,2011,13:1051-1055.
54 Xu KP,et al.Selaginellins I and J,two new alkynyl phenols from Selaginella tamariscina(Beauv.)Spring. J Asian Nat Prod Res,2011,13:93-96.
55 Xu KP,et al.Two new selaginellin derivatives from Selaginella tamariscina(Beauv.)Spring.J Asian Nat Prod Res,2011,13:356-360.
56 Wang YH,et al.Neolignans and caffeoyl derivatives from Selaginella moellendorffii. Helv Chim Acta,2010,93:2467-2477.
57 Bi YF(毕跃峰),et al.Isolation and structural identification of chemical constituents from Selaginella tamariscina(Beauv.)Spring. Acta Pharm Sin(药学学报),2004,39:41-45.
58 Feng WS,et al.Two new secolignans from Selaginella sinensis(Desv.)Spring.J Asian Nat Prod Res,2009,11:658-662.
59 Zheng XK(郑晓珂),et al. Study on the chemical constituents of Selaginella tamariscina. Acta Pharm Sin(药 学 学报),2004,39:266-268.
60 Zheng XK(郑晓珂),et al.. The isolation and identification of a new lignanoside from Selaginella tamariscina(Beauv.)Spring.Acta Pharm Sin(药学学报),2004,39:719-721.
61 Zheng XK,et al. A new dihydrobenzofuran lignanoside from Selaginella moellendorffii Hieron.Chin Chem Lett,2008,19:79-81.
62 Wang YZ,et al.A new sesquilignan from Selaginella sinensis(Desv.)Spring.Chin Chem Lett,2007,18:1224-1226.
63 Feng WS(冯卫生),et al.Study on chemical constituents of Selaginella sinensis(Desv.)Spring. Chin Tradit Herb Drugs(中草药),2008,39:654-656.
64 Wang YH,et al.Pyrrolidinoindoline alkaloids from Selaginella moellendorffii.J Nat Prod,2009,72:1151-1154.
65 Zheng X,et al.A new steroid from Selaginella pulvinata.Fitoterapia,2007,78:598-599.
66 Gao LL,et al. Three novel sterols isolated from Selaginella tamariscina with antiproliferative activity in leukemia cells.Planta Med,2007,73:1112-1115.
67 Roh EM,et al. Structural implication in cytotoxic effects of sterols from Sellaginella tamariscina.Arch Pharm Res,2010,33:1347-1353.
68 Liu HQ(刘海青),et al. Study on chemical constituents of Selaginella stautoniana(Ⅲ). Chin Tradit Herb Drugs(中草药),2006,37:1152-1153.
69 Liu HQ(刘海青),et al. Study on chemical constituents of Selaginella stautoniana(Ⅱ). Chin Tradit Herb Drugs(中草药)2004,35:14-15.
70 Yang F,et al. Anthraquinones and biflavonoids from Selaginella delicatula.Chem Nat Comp,2011,47:627-629.
71 Zheng JX(郑俊霞),et al.Isolation and identification of phenolic constituents from Selaginella uncinata(Desv.)Spring.Chin J Med Chem(中国药物化学杂志),2007,17:302-305.
72 Dai Z,Lin RC. A new glucoside from Selaginella sinensis. J Asian Nat Products Res,2006,8:529-533.
73 Dai Z(戴忠),et al.Study on the trace elements of Selaginella.Chin Pharm Affairs(中国药事),2001,15:390-391.
74 Lee IS,et al. Effects of Selaginella tamariscina on in vitro tumor cell growth,p53 expression,G1 arrest and in vivo gastric cell proliferation.Cancer Lett,1999,144:93-99.
75 Ahn SH,et al.Selaginella tamariscina induces apoptosis via a Caspase-3-Mediated mechanism in human promyelocytic leukemia cells.J Med Food,2006,9:138-144.
76 Yang SF,et al.Antimetastatic activities of Selaginella tamariscina(Beauv.)on lung cancer cells in vitro and in vivo. J Ethnopharm,2007,110:483-489.
77 Jing Y(景艳),et al. Effects of Selaginella doederleinii on human nasopharyngeal carcinoma TW03 cells in vitro and its mechanism.J Chin Med Mater(中药材),2009,32:1864-1867.
78 Mishra1 PK,et al.In vitro and in vivo evaluation of the anticarcinogenic and cancer chemopreventive potential of a flavonoid-rich fraction from a traditional Indian herb Selaginella bryopteris.Br J Nutr,2011,106:1-15.
79 Su Y,et al.Studies on the cytotoxic mechanisms of ginkgetin in a human ovarian adenocarcinoma cell line. Naunyn-Schmiedeberg's Arch Pharmacol,2000,362:82-90.
80 Sun YZ(孙颖桢),et al.Inhibiting action of bisflavones from Selaginella labordei on Bel-7402 cells. Chin Hosp Pharm J(中国医院药学杂志),2009,29:1156-1158.
81 Sun YZ(孙颖桢),et al.Inhibition Action of Total Flavones from Selaginella unicinata on COX-2 mRNA Expression in HT-29 Cells.China Pharmacist(中国药师),2010,13:163-164.
82 Sun YZ(孙颖桢),et al. Inhibition action of total flavones from Selaginella unicinata on proliferation of HT-29 cells and COX-2 mRNA expression in HT-29 cells.Chin Tradit Patent Med(中成药),2010,32:1590-1591.
83 Dai Y,et al. Inhibitory effects of Selaginella tamariscina on immediate allergic reactions.Am J Chin Med,2005,33:957-966.
84 Banerjee T,et al. Inhibition of TNFα-induced cyclooxygenase-2 expression by amentoflavone through suppression of NF-κB activation in A549 cells. Mol Cell Biochem,2002,238:105-110.
85 Woo ER,et al.Amentoflavone inhibits the induction of nitric oxide synthase by inhibiting NF-kappa B activation in macrophages.Pharmacol Res,2005,51:539-546.
86 Woo ER,et al.Inhibition of nuclear factor-kappa B activation by 2',8''-biapigenin.Biol Pharm Bull,2006,29:976-980.
87 Yang JW,Pokharel YR,Kim M,et al.Inhibition of inducible nitric oxide synthase by sumaflavone isolated from Selaginella tamariscina.J Ethnopharmacol,2006,105:107-113.
88 Jiang HY(江海燕),et al.Several Yao drug in vitro antiviral activity preliminary study. J Jinan Univ(暨南大学学报),2008,29:500-504.
89 Yin D(殷丹),Chen KL(陈科力). Study on the inhibitory action on CVB3 replication in vitro by the extracts from Selaginella moelledorfii Hieron.Chin Hosp Pharm J(中国医院药学杂志),2009,29:262-264.
90 Yin D(殷丹),Chen KL(陈科力). Study on the inhibitory action on HSV-Ⅰreplication in vitro by the extracts from Selaginella moelledorfii.Chin Hosp Pharm J(中国医院药学杂志),2009,29:349-352.
91 Duraiswamy H,et al.The effect of extracts of Selaginella involvens and Selaginella inaequalifolia leaves on poultry pathogens.Asian Pac J Trop Med,2010,3:678-681.
92 Ma SC,et al.Antiviral amentoflavone from Selaginella sinensis.Biol Pharm Bull,2001,24:311-312.
93 Jung HJ,et al. Antifungal effect of amentoflavone derived from Selaginella tamariscina.Arch Pharm Res,2006,29:746-751.
94 Lee JY,et al.Antibacterial and synergistic activity of isocryptomerin isolated from Selaginella tamariscina. J Microbiol Biotechnol,2009,19:204-207.
95 Lee JY,et al. Isocryptomerin,a novel membrane-active antifungal compound from Selaginella tamariscina.Biochem Biophys Res Commun,2009,379:676-680.
96 Chen KL,et al.Antioxidant activities of extracts from five anti-viral medicinal plants. J Ethnopharmacol,2005,96:201-205.
97 Xu Z(徐智),et al.Study on pharmacological activity of biflavones from Selaginella pulvinata(Hook. Et Grev.)Maxim.Chin J Mod Med(中国现代医学杂志),2004,14:88-89.
98 Zhu TM(朱田密),et al.Study on xanthine oxidase inhabitor acitivities in vitro of biflavonids from Selaginella pulvinata.Pharm Clin Chin Mater Med(中国药理与临床),2007,23:33-34.
99 Zhang YP,et al.Target-guided isolation and purification of antioxidants from Selaginella sinensis by offline coupling of DPPH-HPLC and HSCCC experiments. J Chromatogr B,2011,879:191-196.
100 Wang CJ,et al. Effects of selaginellin on homocysteine-induced senescence in human umbilical vein endothelial cells.J Cardiovasc Pharmacol,2010,55:560-566.
101 Wang CJ,et al. Protective effect of selaginellin on glutamate-induced cytotoxicity and apoptosis in differentiated PC12 cells.Naunyn-Schmiedeberg's Arch Pharmacol,2010,381:73-81.
102 Li JM(林久茂),et al. Influence of tamariskoid spikemoss herb on immuological functions in mice.J Fujian Coll TCM(福建中医学院学报),2003,13:36-37.
103 Gayathri V,et al. Protection of immunocompromised mice from fungal infection with a thymus growth-stimulatory component from Selaginella involvens,a fern.Immunopharm Immunotoxicol,2011,33:351-359.
104 Li FL(李方莲),et al. Hypoglycemic action of Selaginella tamariscina on the aging diabetic rats model.Chin J Geront(中国老年学杂志),1999,19:301-302.
105 Wu YF(吴奕富),et al. Study on the hypoglycemic action of Selaginella tamariscina on the diabetic rats by STZ. Fujian J TCM(福建中医药),2001,32:42-43.
106 Zheng XK(郑晓珂),et al.Eeperimental study of Selaginella tamariscina(Beauv.)Spring on glucose metabolism among type 2 diabetic rats.Mod Prev Med(现代预防医学),2009,36:1918-1922.
107 Na MK,et al.Protein tyrosine phosphatase 1B inhibitory activity of amentoflavoneand its cellular effect on tyrosine phosphorylation of insulin receptors and its cellular effect on tyrosine phosphorylation of insulin receptors. Biol Pharm Bull,2007,30:379-381.
108 Lee JY,et al.Docking study of biflavonoids,allosteric inhibitors of protein tyrosine phosphatase 1B. Bull Korean Chem Soc,2008,29:1479-1484.
109 Kang DG,et al. Vasorelaxation by amentoflavone isolated from Selaginella tamariscina. Planta Med,2004,70:718-722.
110 Xu L(许兰),Yi MH(尹明浩).Experiment study on vasorelaxation effects of amentoflavone ethyl acetate extract of Selaginella tamariscina.J Med Sci Yanbian Univ(延边大学医学学报),2009,32:246-248.
111 Peng ZC(彭智聪),et al.Effects of Selaginella tamariscina on hemostatic action after being carbonized. Chin J Chin Mater Med(中国中药杂志),2000,25:89-90.
112 Lin JM(林久茂),Wang RG(王瑞国).Protective effect of herba Selaginellae on experimental liver injury in mice. J Fujian Coll Tradit Chin Med(福建中医学院学报),2006,16:28-30.
113 Li YF(李远发),et al.Effects of Selaginella tamariscina on mouse myocadial ischemic-reperfusion injury.Med J Wuhan Univ(武汉大学学报(医学版)),2011,32:429-431.
114 Zheng XK(郑晓珂),et al.Radioprotective effect of the water part of Selaginella tamariscina on hematopoietic system in irradiated mice.Chin J Radiol Med Prot(中华放射医学与防护杂志),2008,28:35-38.
