中药注射剂对细胞色素P450酶亚型的调控作用*
2011-12-08刘蕊刘高峰赵宇光
刘蕊,刘高峰,赵宇光
(哈尔滨医科大学附属第二医院药学部,哈尔滨 150086)
近年来,随着中药注射剂的快速发展和在临床上的广泛应用,与其他药物联合应用的机会也越来越多。目前关于中药注射剂应用的安全性问题,多侧重于质量及体外配伍方面的考虑,对于中药注射剂与其他药物联合应用是否会产生体内代谢性相互作用,从而导致疗效降低或不良反应增加,尚未引起足够的重视。虽然已上市的中药注射剂已有上百种,但在药品说明书中,均未有药物代谢方面的信息,因而无法预测与其他药物联用可能导致的药物相互作用及可能产生的后果,给临床安全合理用药带来隐患。中药注射剂对于药物代谢酶细胞色素P450(cytochrome P450,CYP)的影响研究,是近年来新的研究领域,对于预测中药注射剂和西药,或中药之间的相互作用,提高中药注射剂在临床应用的安全性和有效性具有重要意义。现将近年来国内外报道的中药注射剂对CYP酶亚型调控作用的研究进行总结和分析,以了解该领域的研究现状并指导临床合理用药。
1 CYP酶的简介
CYP酶又称肝药酶,主要存在于肝微粒体中,参与生物体内源性和外源性物质的生物转化[1-2]。CYP酶系中涉及药物代谢的主要有CYP1、CYP2、CYP3基因家族的 7种同工酶(CYP1A2、CYP2A6、CYP2C9、CYP2C19、CYP2D6、CYP2E1、CYP3A4)[3-4],临床有 >90%的药物经 CYP1A2、CYP2C9、CYP2D6、CYP3A4 代谢[5-6]。CYP的活性受多种因素影响,特别是药物可对其产生诱导或抑制[7-8]。酶的诱导可增加生物转化率,降低药物浓度,使药物作用降低;某种CYP亚型抑制则增加了该亚型代谢的药物浓度,延长药理作用时间,增加药物不良反应[9]。CYP的诱导和抑制是药物相互作用最常见的原因[10-13],使得≥2种药物同时或前后序贯使用时,相互干扰代谢环节,使药物疗效增强或减弱[14]。因此,CYP酶系统在药物相互作用方面发挥重要作用,对中西药联合应用有着重要的指导意义。
2 中药注射剂概况
中药注射剂是指在中医药理论指导下,采用现代科学技术与方法,从中药、天然药物的单方或复方中提取有效物质制成的可供注入体内的灭菌制剂以及供临床前配制溶液的无菌粉末或浓缩液[15]。中药注射剂是传统中医药理论与现代生产工艺相结合的产物,突破了中药传统给药方式。目前,全国生产中药注射剂的企业近400家,生产经国家批准的中药注射剂120多种,主要应用领域为心脑血管疾病、肿瘤、细菌和病毒感染等。据统计,1999~2010年我国中药注射剂市场份额呈连续增长趋势,其中脑血管疾病和肿瘤疾病市场份额前10位的中成药品种中,中药注射剂的产品占 7 种[16]。
3 中药注射剂对CYP酶亚型调控作用的研究
中药注射剂对CYP酶系作用的相关研究仍很少,其中主要涉及到一些较常用的中药注射剂,见表1。
3.1 抗菌和抗病毒药物 研究柴胡注射液对大鼠CYP各亚型活性的影响时,用高效液相色谱(high performance liquid chromatography,HPLC)法观察探针药物代谢率的变化来反映柴胡注射液对大鼠CYP1A2活性的影响;用Western blot法测定了大鼠肝微粒体CYP1A2、3A4、4A1蛋白的相对含量。实验柴胡注射液对CYP1A2亚型无影响,但在蛋白质水平,可抑制大鼠肝CYP4A1表达。高剂量柴胡注射液可诱导大鼠CYP3A4 蛋白质表达[17]。
穿琥宁注射液对CYP1A2亚型影响的研究,用HPLC法测定对照组和各实验组全血中咖啡因的代谢率,利用Western blot技术测定穿琥宁注射液对大鼠CYP1A2亚型蛋白表达的影响;在肝微粒体温孵体系中,加入探针药物非那西丁,通过HPLC法测定不同组大鼠肝微粒体中非那西丁的代谢物对乙酰氨基酚的生成速率的变化。体内外实验结果均表明,穿琥宁注射液对大鼠CYP1A2亚型无诱导或抑制作用[18]。
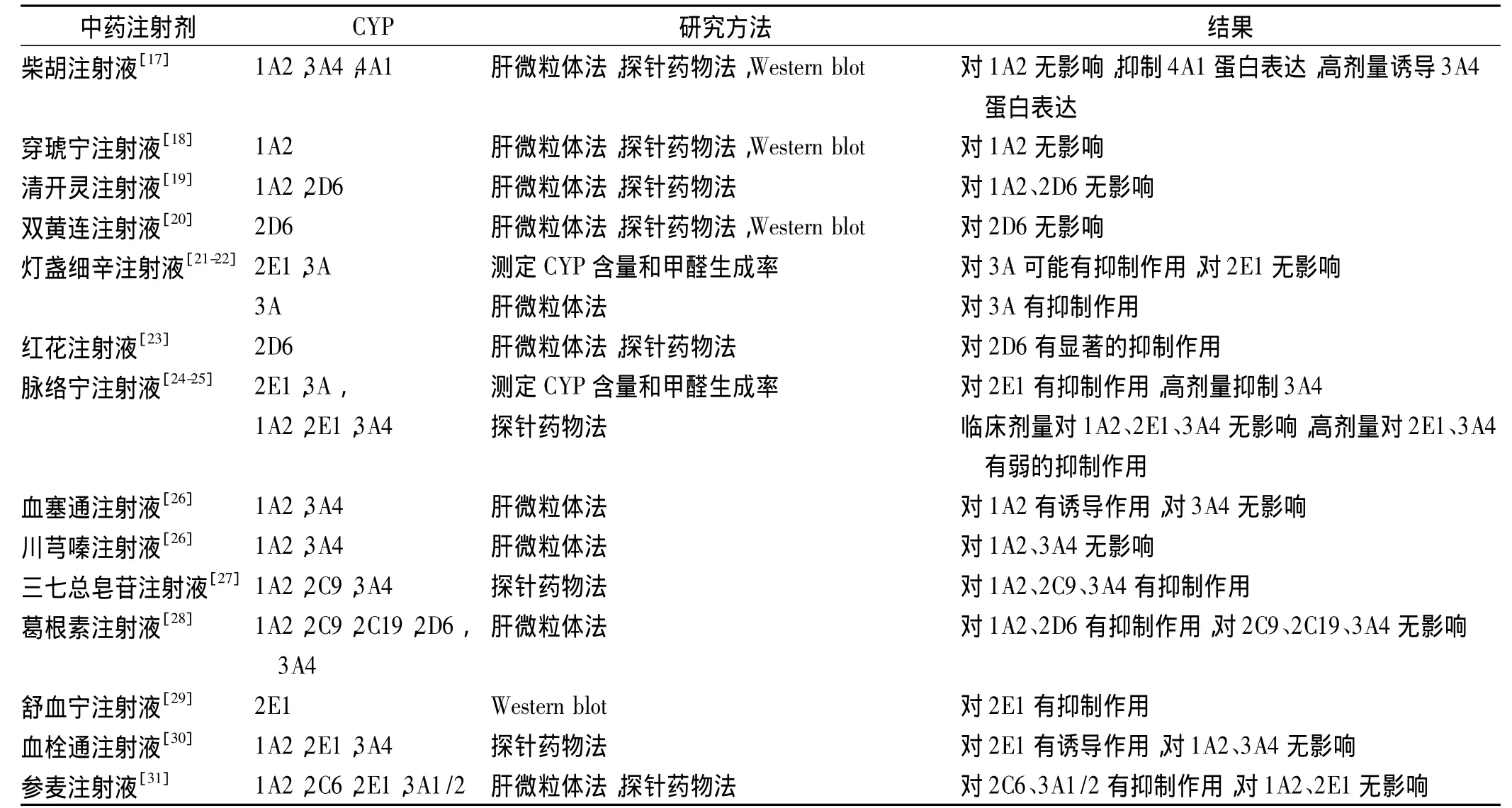
表1 中药注射剂对CYP酶亚型的调控作用
刘艳等[19]通过HPLC法测定大鼠全血中及肝微粒体重组系统咖啡因的代谢率,确定清开灵注射液对CYP1A2无影响,通过测定右美沙芬的代谢率,确定清开灵注射液对CYP2D6无影响。
王欢等[20]在双黄连注射液对大鼠CYP2D6亚型影响的研究中,用HPLC法测定大鼠尿样及肝微粒体中CYP2D6探针药物右美沙芬的代谢率,观察氨苄西林、双黄连注射液分别单用及合用时对大鼠CYP2D6活性的影响。通过Western blot法测定其对大鼠肝微粒体CYP2D6蛋白表达的调控。结果显示,双黄连注射液与氨苄西林单用和两药配伍使用,对CYP2D6没有抑制或诱导作用。
3.2 心脑血管疾病用药 据报道,通过大、小鼠肝微粒体体外实验,表明灯盏细辛注射液对CYP3A有抑制作用[21-22]。
考察红花注射液对大鼠CYP2D6活性的影响,用HPLC法测定各实验组大鼠体内尿液中与体外肝微粒体温孵系统中右美沙芬的代谢率,结果红花注射液对大鼠CYP2D6有显著的抑制作用[23],其半数抑制浓度(IC50)=10.64 mg·mL-1。
通过测定CYP含量和甲醛生成率,考察脉络宁注射液对小鼠总CYP以及CYP3A和CYP2E1活性的影响。采用紫外分光光度法和体外温孵反应,结果表明脉络宁注射液对CYP2E1有抑制作用,高剂量时可能抑制CYP3A的活性[24]。另有研究脉络宁注射液对大鼠CYP1A2、CYP2E1和CYP3A4活性的影响,用HPLC法同时测定大鼠体内各探针药物的血药浓度,并进行药动学参数比较,表明脉络宁注射液对大鼠CYP1A2、CYP2E1和CYP3A4活性均无显著影响,高剂量脉络宁注射液对大鼠CYP2E1和CYP3A4均有弱的抑制作用[25]。
通过研究CYP1A2、CYP3A4的专属探针药物咖啡因、氨苯砜的体外代谢变化,表明血塞通注射液对CYP1A2有诱导作用,而对CYP3A4无影响;而川芎嗪注射液对CYP1A2和CYP3A4均无影响[26]。
用探针药物法研究三七总苷注射液对大鼠肝CYP酶的影响,显示长时间给予三七总苷注射液对CYP1A2、CYP2C9 和 CYP3A4 有抑制作用[27]。
分别以咖啡因、甲苯磺丁脲、美芬妥因、美托洛尔、咪达唑仑为探针药,利用HPLC法测定探针药与相应代谢产物的浓度,结果表明,在体外重组酶反应体系中,葛根素注射液对CYP2C9、CYP2C19及CYP3A4酶活性无明显影响,但对CYP1A2和CYP2D6酶活性有较明显的抑制作用,且随葛根素浓度增高,抑制作用增强[28]。
银杏叶提取物(舒血宁注射液)对CYP2E1表达的抑制作用,通过细胞免疫染色和Western blot法观察CYP2E1的蛋白表达,以对硝基苯酚为探针测定全细胞CYP2E1的活性变化,结果银杏叶提取物可显著抑制E47细胞的CYP2E1表达,降低CYP2E1的活性[29]。
以茶碱、氯唑沙宗和咪达唑仑作为 CYP1A2,CYP2E1及CYP3A4的探针药物,采用HPLC法测定连续使用血栓通注射液前后,大鼠血浆中相应的探针药物的浓度及其药动学参数,结果显示血栓通注射液对CYP2E1酶活性有显著的诱导作用,而对 CYP3A4、CYP1A2 酶活性无影响[30]。
参麦注射液对 CYP3A1/2、CYP2C6、CYP1A2和CYP2E1的影响:分别采用咪达唑仑、双氯芬酸、茶碱和氯唑沙宗作为 CYP3A1/2、CYP2C6、CYP1A2和CYP2E1的探针药物,利用液相色谱-质谱联用(LCMS)法测定探针药物的药动学参数。在体外实验中,采用肝微粒体法,利用LC-MS法或HPLC法测定探针药物与相应代谢产物的浓度。结果表明,参麦注射液对CYP3A1/2和CYP2C6具有抑制作用,对CYP1A2和CYP2E1 酶活性无影响[31]。
4 中药注射剂对CYP酶亚型影响的研究方法
中药注射剂对CYP酶亚型调控作用的研究方法目前主要采用探针药物法、肝微粒体法和Western blot技术。
4.1 探针药物法 探针药物法是指某些经CYP酶代谢的药物,以其代谢物和原型药的比例或速率衡量酶代谢能力变化的方法,如分别用咖啡因、右美沙芬、氯唑沙宗、咪达唑仑来评价 CYP1A2、CYP2D6、CYP2E1、CYP3A4的活性[32]。将实验动物分为对照组、中药注射液不同给药剂量组,连续给药一段时间,然后取血样或尿样进行测定,通过比较对照组和实验组探针药物的代谢率,来考察中药注射液对CYP酶各亚型活性的影响。探针药物及其代谢物的测定方法一般采用HPLC 或 LC-MS/MS技术[33-34]。
4.2 肝微粒体法 肝微粒体体外温孵实验是采用从肝脏中提取的肝微粒体,加入还原型辅酶Ⅱ再生系统,在体外模拟生理环境下进行代谢反应,采用HPLC、HPLC-MS等测定方法对原型药及代谢产物进行测定的一种体外代谢的实验方法[35]。肝微粒体法制备简单,代谢快,易大量操作,近年来在药物代谢研究中用于酶活性及体外代谢等方面的研究,应用较广。
4.3 Western blot技术 利用Western blot技术可研究中药注射剂对大鼠肝微粒体中CYP蛋白表达的影响。该技术是将通过聚丙烯酰胺凝胶电泳分离的蛋白质样品,转移到固相载体(例如硝酸纤维素薄膜)上,固相载体以非共价键形式吸附蛋白质,且能保持电泳分离的多肽类型及其生物学活性不变。以固相载体上的蛋白质或多肽作为抗原,与对应的抗体起免疫反应,再与酶或同位素标记的第二抗体起反应,经过底物显色或放射自显影以检测电泳分离的特异性目的基因表达的蛋白成分。该技术可应用于检测CYP酶各亚型蛋白水平的表达[18]。
5 结束语
随着现代技术在中药开发上的广泛应用,国内中药注射剂的品种越来越多,为临床治疗疾病提供了更多的选择。目前国家对于中药注射剂在临床应用的安全性问题,给予高度的关注,但其安全性研究多侧重于工艺研究以及与其他药物配伍对于中药注射剂质量和稳定性的影响,对于中药注射剂的代谢研究及由此导致的体内相互作用研究极少有报道。国家食品药品监督管理局2007年颁布的《中药、天然药物注射剂基本技术要求》中指出,中药、天然药物注射剂的处方及临床使用方法的确定,要求有药动学研究结果的支持;由有效成分制成的注射剂,应全面研究其药动学参数;由多成分制成的注射剂,应对其药动学特征进行探索性研究;在药品说明书中应包括药物相互作用的内容。因此,对于中药注射剂的代谢研究及研究方法的建立具有必要性和重要性。
已有的研究结果显示,不同的中药注射剂对CYP酶亚型可能会产生抑制或诱导作用。抑制或诱导药物代谢酶是产生药物相互作用的主要机制。药物代谢相互作用中,酶抑制引起的相互作用占全部相互作用的70%,酶诱导引起的相互作用约占23%。药物间的相互抑制作用通常被视为一种潜在的危险或至少是所不期望的,由CYP酶抑制所产生的药物间相互作用是药物的潜在毒性,这种毒性有时十分危险。CYP酶诱导是药物相互作用导致疗效降低的重要原因。诱导某一CYP酶亚型后,可使该药物的亚型活性增高,导致由该亚型催化的药物代谢增强,加快该药物的消除,使之难以达到有效的血药浓度。但目前关于中药注射剂对CYP酶亚型调控作用的研究结果仍太少,急需对其他中药注射剂进行广泛深入的研究。中药注射剂通常由多种成分组成,如果再与其他药物联合应用,就可能发生难以预测的药物相互作用。因此,探讨中药注射剂对CYP酶亚型的调控作用及中药-西药或中药-中药联用是否会产生药物相互作用及机制,对促进临床合理用药并最大限度地避免盲目联合用药导致不良后果,保证临床用药的安全性和有效性无疑有重要意义和紧迫性。
[1] NEBERT DW,RUSSELL DW.Clinical importance of the cytochromes P450[J].Lancet,2002,360:1155-1162.
[2] COON M J.Cytochrome P450:nature’smost versatile biological catalyst[J].Ann Rev Pharmacol Toxicol,2005,45:1-25.
[3] SLAUGHTER R L,EDWARDSD J.Recent advances:the cytochrome P450enzymes[J].Ann Pharmacother,1995,29(6):619-624.
[4] BROSEN K,SKJELBO E,NIELSEN K K.Imipramine:a model drug for P450research [J].Methods Enzymol,1996,272:177-186.
[5] 王宇光,高月,柴彪新,等.人参、藜芦合用对大鼠肝P450酶活性及mRNA表达的调控作用[J].中国中药杂志,2004,29(4):366-370.
[6] RENDIC S,DICARLO F J.Human cytochrome P450enzyme:a status report summarizing their reactions,substrates,induction,and inhibitors[J].Drug Metab Rev,1997,29(1-2):413-580.
[7] IDANIA R,MARIA TD,NURIA J,et al.Inhibiton of human P450enzeymes by natural extracts used in traditional medicine[J].Phytother Res,2009,23(2):279-282.
[8] RENDIC S,GUENGERICH F P.Update information on drug metabolism systems-2009,partⅡ:summary of information on the effects of diseases and environment factors on human cytochrome P450(CYP)enzymes and transports[J].Curr Drug Matab,2010,11(1):4-84.
[9] 朱大岭,韩维娜,张荣.细胞色素P450酶系在药物代谢中的作用[J].医药导报,2004,23(7):440-443.
[10] FOTIR S,WIENKERS L C,WAHLSTROM J L.Application of cytochrome P450drug interaction screening in drug discovery [J].Comb Chem High Throughput Screen,2010,13(2):145-158.
[11] HISAKA A,OHNOY,YAMAMOTO T.Prediction of pharmacokinetic drug-drug interaction caused by changes in cytochrome P450activity using in vivo information [J].Pharmacol Ther,2010,125(2):230-248.
[12] DOBORAH A K,DUGALD S.Clinically based evidence of drug-herb interactions:a systematic review[J].Expert Opin Drug Saf,2010,9(1):79-124.
[13] HUANG SM,STRONG JM,ZHANG L,etal.New era in drug interaction evaluation: US Food and Drug Administration update on CYP enzymes,transporters,and the guidance process [J].J Clin Pharmacol,2008,48(6):662-670.
[14] LEUCUTA S E,VLASE L V.Pharmacokinetics and metabolic drug interactions[J].Curr Clin Pharmacol,2006,1(1):5-20.
[15] 杜冠华.中药注射剂的评价与研究方向[J].医药导报,2009,28(11):1387-1393.
[16] 吴俊杰.中药注射剂医院市场走势上扬[J].中国处方药,2010,96:52-53.
[17] 王晶,余辉艳,郭蕾,等.柴胡注射液对大鼠细胞色素P450各亚型活性的影响[J].中国临床药理学与治疗学,2007,12(9):1037-1041.
[18] 吴东媛,杨振宇,王欢,等.穿琥宁注射液对大鼠CYP1A2亚型的影响[J].哈尔滨医科大学学报,2008,42(5):443-445.
[19] 刘艳,王晶,鲍岩岩,等.清开灵注射液对大鼠CYP1A2和2D6的影响[J].中国中药杂志,2007,32(19):2044-2047.
[20] 王欢,吴东媛,杜智敏.氨苄西林与双黄连注射液单用及配伍对大鼠 CYP2D6的影响[J].医药导报,2008,27(5):491-494.
[21] 许黎君,居文政,陈为烤,等.灯盏细辛注射液对小鼠肝微粒体细胞色素P450含量的影响[J].中国临床药理学与治疗学,2008,13(10):1122-1126.
[22] 韩永龙,余奇,孟祥乐,等.灯盏细辛注射液对大鼠肝微粒体CYP3A的抑制作用[J].中国临床药理学与治疗学,2009,14(8):891-895.
[23] 刘高峰,郭兴蕾,黄丽军.红花注射液对大鼠细胞色素P4502D6亚型的抑制作用[J].中草药,2008,39(12):1829-1833.
[24] 陈为烤,居文政,许黎君,等.脉络宁注射液对小鼠肝药酶活性的影响[J].药学与临床研究,2008,16(5):351-354.
[25] 陈为烤,居文政,徐黎君,等.Cocktail法研究脉络宁注射液对大鼠CYP1A2、CYP2E1和CYP3A4活性的影响[J].中国临床药理学与治疗学,2009,14(4):386-390.
[26] 石杰,陈安进,张芳,等.血塞通及川芎嗪对细胞色素P450不同亚型代谢酶影响的研究[J].中国中西医结合急救杂志,2008,15(6):342-345.
[27] 李晓宇,刘皋林,周佳纯,等.三七总苷注射液对大鼠肝CYP酶的影响[J].中国临床药理学与治疗学,2009,14(8):849-854.
[28] 王启斌,狄伟,程晓莉,等.葛根素对细胞色素P450酶活性的影响[J].医药导报,2008,27(5):500-504.
[29] 陈宏超.银杏叶提取物对细胞色素P4502E1表达的抑制作用[D].郑州:郑州大学,2007.
[30] 刘史佳,居文政,陈为烤,等.血栓通注射液对大鼠体内细胞色素P450酶活性的影响[J].中国药学杂志,2010,45(2):115-118.
[31] XIA C H,SUN JG,WANG G J,et al.Herb-drug interactions:in vivo and in vitro effect of shenmai injection,a herbal preparation,on the metabolic activities of hepatic cytochrome P4503A1/2,2C6,1A2,and 2E1 in rats[J].Planta Med,2010,76(3):245-250.
[32] 朱立勤,娄建石.细胞色素P450与药物代谢的研究现状[J].中国临床药理学与治疗学,2004,9(10):1081-1086.
[33] 李彧,赵春杰.药物代谢在中药研究中的应用概况与展望[J].海峡药学,2009,21(1):10-12.
[34] FUHR U,JETTER A,KIRCHHEINER J.Appropriate phenotyping procedures for drug metabolizing enzymes and transporters in humans and their simultaneous use in the“cocktail”approach [J].Clin Pharmacol Ther,2007,81(2):270-283.
[35] 李文东,马辰.药物体外肝代谢研究进展[J].中国药学杂志,2003,38(10):737-740.
[36] MORIK,HASHIMOTO H,TAKATSU H,et al.Cocktailsubstrate assay system for mechanism-based inhibition of CYP2C9, CYP2D6, and CYP3A using human liver microsomes at an early stage of drug development[J].Xenobiotica,2009,39(6):415-422.
