15 种医院口腔抑菌制剂微生物限度检查方法的建立*
2024-05-07赵慧雯
赵慧雯,冯 斌
(军事口腔医学国家重点实验室·国家口腔疾病临床医学研究中心·陕西省口腔生物工程技术研究中心·中国人民解放军空军军医大学第三附属医院药剂科,陕西 西安 710032)
医院制剂是指医院制剂室按药品标准或协定处方制成的一类适应本院临床需要而市场未能供应的制剂,具有制备数量少、周期短、品种多、供应及时等优点[1]。医院制剂应保证质量稳定,微生物是衡量制剂安全性的重要指标,故需建立科学可靠的微生物限度检查方法[2]。口腔类制剂因临床主要用于抑菌消炎、控制感染、促进修复等,多含有抑菌成分,因此对该类制剂进行微生物限度检查时,应先消除自身的抑菌活性,以保证方法的适用性,从而真实准确地反映制剂被微生物污染的情况[3]。本研究中基于2020年版《中国药典(四部)》通则1105,1106,1107 项下要求,拟采用平皿法、薄膜过滤法和培养基稀释法对15 种口腔抑菌制剂进行微生物限度适用性检查[4],从而保障临床用药的质量可控和安全有效。现报道如下。
1 仪器、试药与菌株
1.1 仪器
LDZX - 30KBS 型压力蒸汽灭菌器(上海申安医疗器械厂);XY500JC 型电子天平(常州市幸运电子设备有限公司,精度为0.01 g);HFsafe-1800TE型生物安全柜(上海力申科学仪器有限公司);BSD-TX345型台式恒温振荡器(上海博讯实业有限公司);HH 系列电热恒温水浴锅(北京科伟永兴仪器有限公司);LRH - 250F 型生化培养箱,M250FI型霉菌培养箱(上海一恒科学仪器有限公司);VORTEX-5 型涡旋混合器(海门市其林贝尔仪器制造有限公司);EX30 系列生物显微镜(宁波舜宇仪器有限公司);PHS - 4C + 型酸度计(成都世纪方舟科技有限公司);API 型微生物鉴定系统(法国Bio-Mérieux 公司);HTY - 602 型集菌仪(杭州泰林生物技术设备有限公司)。
1.2 试药
醋酸氯己定口崩片(成分为醋酸氯己定等,批号为220908),醋酸氯己定洗剂(成分为醋酸氯己定等,批号为211008),复方替硝唑溶液(成分为替硝唑、醋酸氯己定等,批号为211014),碘甘油(成分为碘等,批号为210927),甲醛甲酚涂剂(成分为甲醛、甲酚等,批号为211013),硼酸甘油涂剂(成分为硼酸等,批号为220629),人工唾液(成分为氯化钠、羟苯乙酯等,批号为211021),脱敏糊剂(成分为多聚甲醛、乙醇等,批号为210919),干髓糊剂(成分为多聚甲醛等,批号为211010),锌麝酚醛糊剂(成分为氧化锌、麝香草酚等,批号为211006),牙周塞糊剂(成分为氧化锌、鞣酸等,批号为211007),甲硝唑膜(成分为甲硝唑等,批号为210922),复方克林霉素膜(成分为克林霉素磷酸酯等,批号为211010),多聚甲醛新失活剂(成分为多聚甲醛、盐酸可卡因等,批号为211020),多聚甲醛牙髓失活剂(成分为多聚甲醛、盐酸可卡因等,批号为211005),分别为制剂1-15,均为空军军医大学第三附属医院的医院制剂;胰酪大豆胨琼脂及液体培养基(TSA,TSB,批号分别为2009032,2103015),沙氏葡萄糖琼脂及液体培养基(SDA,SDB,批号分别为2010302,2009202),麦康凯琼脂及液体培养基(批号分别为2008272,2008202),溴化十六烷基三甲铵琼脂培养基(USP,批号为2009212),甘露醇氯化钠琼脂培养基(MSA,批号为2003262),pH 7.0 无菌氯化钠-蛋白胨缓冲液(批号为2108202),均购自北京三药科技有限公司;0.9%无菌氯化钠溶液(四川科伦药业股份有限公司,批号为M21030902C)。
1.3 菌株
金黄色葡萄球菌Staphylococcus aureus[CMCC(B)26003],铜绿假单胞菌Pseudomonas aeruginosa[CMCC(B)10104],枯草芽孢杆菌Bacillus subtilis[CMCC(B)63501],白色念珠菌Candida albicans[CMCC(F)98001],黑曲霉Aspergillus niger[CMCC(F)98003],大肠埃希菌Escherichia coli[CMCC(F)44102],均购自中国医学细菌保藏管理中心,试验菌株均为第2代。
2 方法与结果
2.1 溶液制备
菌液:将金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌分别接种于TSB 中,35 ℃培养24 h;将白色念珠菌接种于SDB 中,25 ℃条件下培养3 d。均用0.9%无菌氯化钠溶液(稀释液1)制成适宜浓度的菌悬液。将黑曲霉接种于SDA 中,25 ℃条件下培养7 d,加入5 mL 含0.05%聚山梨酯80 的0.9%无菌氯化钠溶液,洗脱孢子,收集孢子悬液,并制成适宜浓度的孢子悬液。
供试品溶液:取样品10 g/10 mL/100 cm2,各2份,置250 mL 玻璃瓶中,加入pH 7.0 无菌氯化钠-蛋白胨缓冲液(稀释液2)稀释至100 mL,45 ℃条件下恒温振荡15 min,制成1∶10(m/V)的供试品溶液Ⅰ。取10 mL,加稀释液2适量,混匀,分别制成1∶20(m/V)、1∶50(m/V)的供试品溶液Ⅱ、Ⅲ。
2.2 需氧菌总数、霉菌和酵母菌总数计数方法适用性试验
2.2.1 平皿法
试验组:取2.1 项下供试品溶液9.9 mL,置无菌试管中,加入含菌量不大于10 000 cfu / mL 的试验菌液0.1 mL,混匀。分别取适量,注入2 个平皿,各1 mL。分别注TSA(需氧菌计数)、SDA(霉菌和酵母菌计数)各20 mL,温度均不超过45 ℃。前者35 ℃条件下倒置培养2~3 d,后者25 ℃条件下倒置培养2~5 d。
供试品对照组:取2.1 项下供试品溶液适量,以稀释液2替代菌液,同试验组方法操作。
菌液对照组:取稀释液2 适量替代供试品溶液,加入试验菌,同试验组方法操作。
2.2.2 薄膜过滤法
试验组:取2.1 项下供试品溶液Ⅰ1 mL,加入含100 mL 稀释液2 的滤器中,滤过,用稀释液2 冲洗滤膜3~8 次,每次100 mL,最后1 次冲洗液中加入含菌量不大于100 cfu的试验菌液1 mL,取出滤膜,贴于相应平板培养基,按规定条件倒置培养、计数。
供试品对照组:取2.1 项下供试品溶液Ⅰ适量,以稀释液2替代菌液,同试验组方法操作。
菌液对照组:取稀释液2 适量替代供试品溶液,加入试验菌,同试验组方法操作。
2.2.3 回收比计算
菌株回收比(%)=(试验组菌落数-供试品对照组菌落数)/菌液对照组菌落数×100%。
2.2.4 验证试验
制剂1-5、9-11、14-15 需氧菌总数检查均采用薄膜过滤法,其余制剂均采用平皿法;制剂1-3、6-8、12 - 13 霉菌和酵母菌检查均采用平皿法,其余制剂均采用薄膜过滤法,试验菌回收比均在0.5~2.0 范围内。详见表1和表2(仅列出了最优检查方法)。
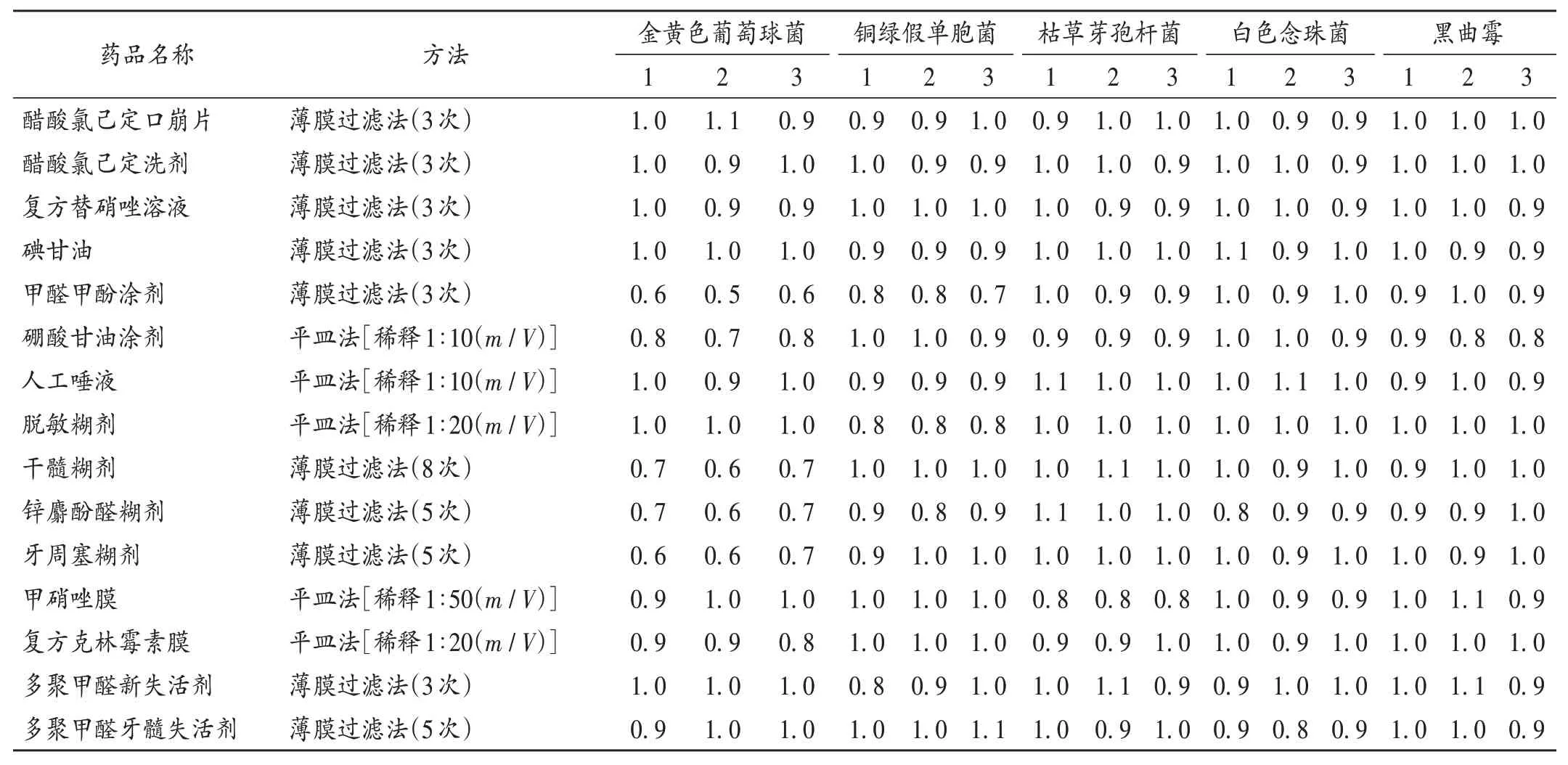
表1 需氧菌回收试验结果(n=3)Tab.1 Results of the recovery test of aerobic bacteria(n = 3)
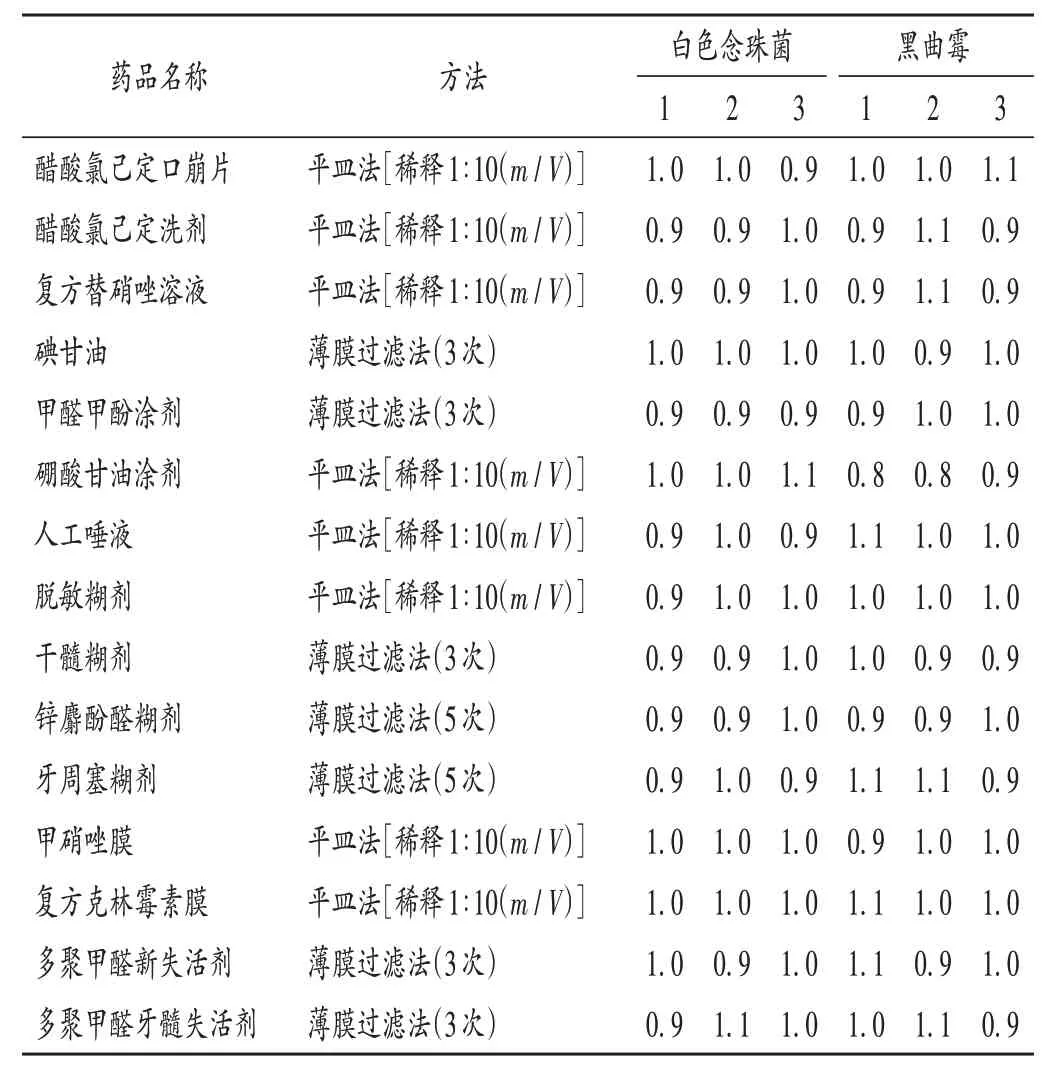
表2 霉菌及酵母菌回收试验结果(n=3)Tab.2 Results of the recovery test of molds and yeasts(n = 3)
2.3 控制菌检查法适用性试验
2.3.1 金黄色葡萄球菌
培养基稀释法:取2.1 项下供试品溶液Ⅰ10 mL,加入不少于100 mL的TSB中,加入不大于100 cfu 的相应试验菌液1 mL,混匀,35 ℃条件下培养18 h;取TSB 划线接种于MSA,35 ℃条件下培养18 h,观察结果。以此作为试验组。
薄膜过滤法:取2.1项下供试品溶液Ⅰ10 mL,加入含100 mL 稀释液2 的滤器中,滤过,用稀释液2 冲洗滤膜3~8 次,每次100 mL,取出滤膜,接种至100 mL TSB中,同时加入不大于100 cfu 的试验菌液1 mL,35 ℃条件下培养18 h。将上述培养物接种于MSA,35 ℃条件下培养18 h,观察结果。以此作为试验组。
2.3.2 铜绿假单孢菌
采用培养基稀释法和薄膜过滤法,按2.3.1项下方法操作,以TSB 35 ℃条件下培养18 h后,将其划线接种于USP,35 ℃条件下培养18 h,观察结果。以此作为试验组。
2.3.3 大肠埃希菌
采用培养基稀释法和薄膜过滤法,按2.3.1项下方法操作,以TSB 35 ℃条件下培养18 h 后,取1 mL 接种至100 mL麦康凯液体培养基中,42 ℃条件下培养24 h,取培养物划线接种于麦康凯琼脂培养基上,35 ℃条件下培养18 h,观察结果。以此作为试验组。
以上3种控制菌检查均另设阳性对照组(以稀释液2替代供试品溶液,加入试验菌,同试验组方法操作)、阴性对照组(以稀释液2替代供试品溶液,不加试验菌,同试验组方法操作)。
2.3.4 验证试验
控制菌检查,制剂1-3、5、9-11、14-15采用薄膜过滤法,其余采用培养基稀释法,试验组相应阳性菌均能正常检出。详见表3(仅列出最优检查方法)。
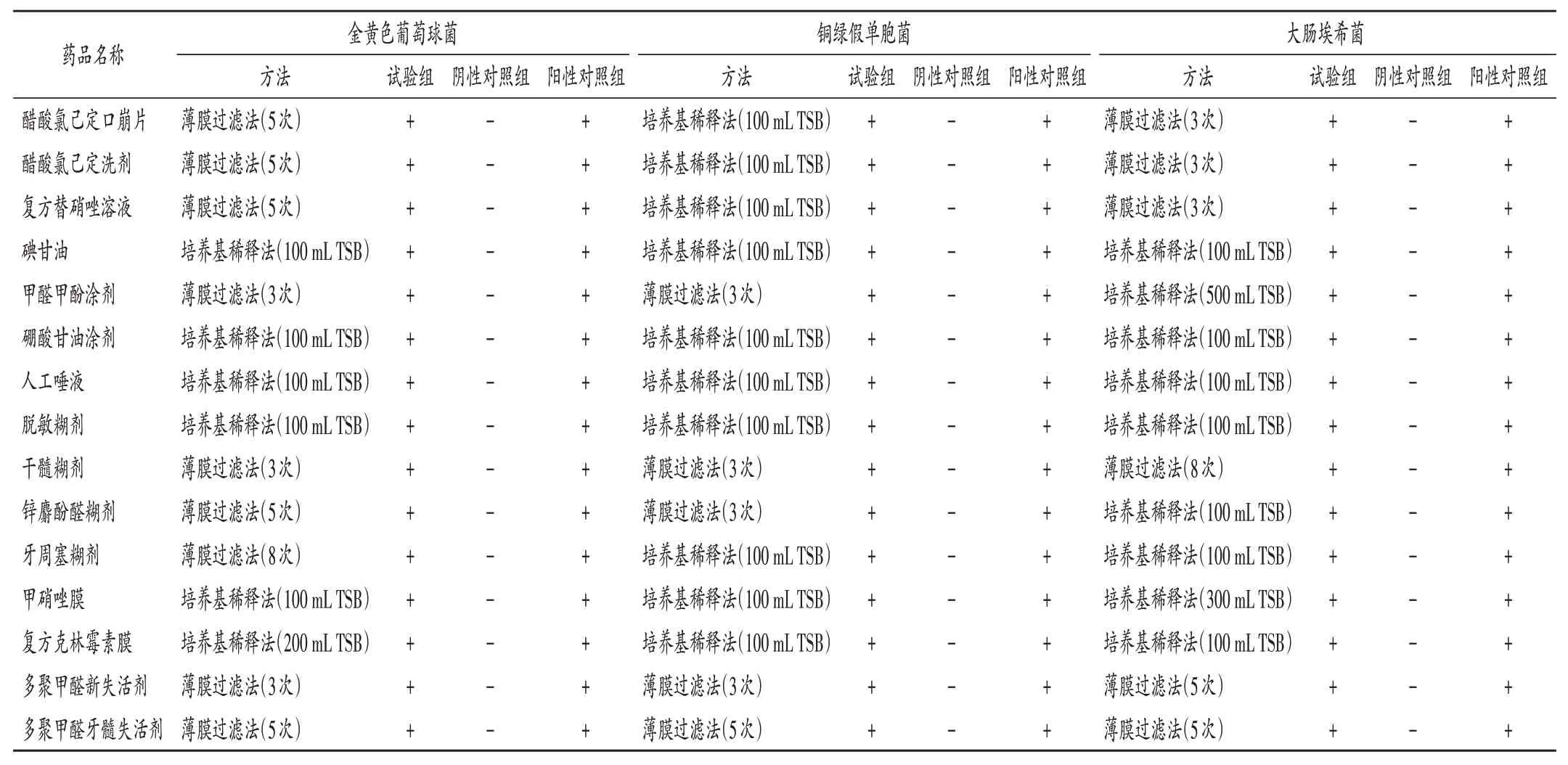
表3 控制菌检查法适用性试验结果Tab.3 Results of applicability test of control bacteria detection
3 讨论
常见的口腔疾病包括牙龈炎、牙周炎、牙髓炎、复发性口腔溃疡等,临床用药多采用局部治疗方式以消除口腔炎症,控制术后感染,故医院口腔制剂多含有抑菌成分。不同单位生产的制剂,即使所含主要成分相同,由于采用的制备工艺和辅料不同,制剂仍可能表现出不同的抑菌特性,故微生物限度检查方法应具有针对性和适用性[1]。
本研究中建立了15种含抗菌药物及消毒防腐剂的医院口腔制剂的微生物限度检查方法。抗菌药物中替硝唑和甲硝唑均属硝咪唑类,能抑制细菌DNA 的合成,从而干扰其生长、繁殖,对厌氧菌的活性较高[5-6];克林霉素磷酸酯为克林霉素衍生物,主要通过作用于细菌核糖体的50 S 亚基,从而抑制细菌合成蛋白质,对革兰阳性菌的抑制作用较强[7],对于含上述成分的制剂可采用平皿法和培养基稀释法进行检查。消毒防腐剂中醋酸氯己定为季铵盐类阳离子表面活性剂,通过破坏细胞膜而产生抑制活性[8];碘、氧化锌具有化学活性,可与细菌内的多种有机物发生氧化反应,从而把大部分细菌杀灭[9-10];甲醛、甲酚、羟苯乙酯可使菌体蛋白变性从而发挥杀菌作用[11-13];硼酸通过与氨基结合,鞣酸和麝香草酚通过与氢键或疏水键结合,从而使菌体蛋白变性,还可通过抑制细菌代谢所需酶的活性发挥抑菌作用[14-16],上述成分组成复方制剂后抑菌作用更强,故需联合采用培养基稀释法、薄膜过滤法等方法进行检查。
本研究针对制剂剂型和所含抑菌成分采用了不同的试验方法,对于抑菌活性较强的制剂,采用平皿法若在最低稀释级无法进行方法适用性试验时,可增加稀释液或培养基体积或采用薄膜过滤法进行检查,以消除抑菌活性。
综上所述,本研究中建立的方法操作便捷,结果准确,为医院制剂微生物限度质量控制提供了可靠的检测手段,对于保障制剂质量具有重要意义,同时也为类似抑菌制剂的检查提供了研究思路。
