参麦颗粒中红参掺伪研究*
2024-05-07刘亚茹王晓蕾刘永利
雷 蓉,刘亚茹,2,王晓蕾,刘永利△
(1. 河北省药品医疗器械检验研究院·河北省中药质量评价与标准研究重点实验室,河北 石家庄 050227;2. 河北医科大学,河北 石家庄 050017)
参麦颗粒由红参、南沙参、麦冬、黄精、山药、枸杞子等中药组方,具有养阴生津功效,主要用于治疗面黄肌瘦、津少口渴、腰膝酸软、食欲不振、头晕眼花、心悸气短、神经衰弱等症[1]。方中红参为五加科植物人参Panax ginsengC. A. Mey. 的栽培品经蒸制后的干燥根和根茎,具有大补元气、复脉固脱、益气摄血等功效。西洋参为五加科植物西洋参Panax quinquefoliumL. 的干燥根,具有补气养阴、清热生津等功效,原产于加拿大、美国等北美地区,现主要栽培于我国山东、东北等地[1-2]。人参、西洋参主要含皂苷类成分,但两者所含皂苷种类与含量及比例有一定差异,特别是拟人参皂苷F11,其在西洋参中含量较高,而人参中基本不含,因此以其作为判断非法添加的依据[3-9]。近年来,西洋参冒充人参或西洋参掺入人参进行含人参制剂投料生产屡有发生,而乌鸡白凤丸、消糜栓、人参养荣丸(大蜜丸、小蜜丸、水蜜丸)中拟人参皂苷F11检查项补充检验方法也相继颁布,用于西洋参掺伪人参投料的监督检验。考虑到红参是由人参经蒸制所得,为进一步筛查红参中是否也存在西洋参掺伪的投料情况,本研究中结合参麦颗粒中红参用量少(仅0.2%)、辅料蔗糖用量大(占92%)、基质效应复杂的处方特点,建立了固相萃取(SPE)[10-19]-超高效液相色谱串联质谱(UPLC - MS/MS)法检查制剂中是否含有拟人参皂苷F11,为其中红参的质量控制提供参考。现报道如下。
1 仪器与试药
1.1 仪器
AB SCIEX Triple Quad 6500+高效液相色谱- 质谱联用仪(配置SCIEX OS 软件、电喷雾离子源,美国AB SCIEX公司);XPE26型电子天平、XS105DU型电子天平(瑞士Mettler Toledo 公司,精度分别为0.001 mg 和0.01 mg);KQ - 500DE 型数控超声波清洗器(昆山市超声仪器有限公司);Milli - Q 超纯水制备系统(美国Millipore公司)。
1.2 试药
参麦颗粒(厂家A,B,C,编号分别为S1-S28,S29-S51,S52- S85;为2022年国家药品抽检样品);拟人参皂苷F11对照品(中国食品药品检定研究院,批号为110841 - 201406,含量测定用);甲醇、乙腈、甲酸均为色谱纯,水为超纯水。红参、西洋参药材均购自河北安国中药材市场,经河北省医疗器械检验研究院段吉平主任药师鉴定为正品。
2 方法与结果
2.1 试验条件
色谱条件:色谱柱为Shimadzu Shim-pack GIST C18柱(100 mm×2.1 mm,2 μm);流动相为乙腈(A)-水(B),梯度洗脱(0~2 min 时20%A →50%A,2~4.5 min 时50%A →80%A);流速为0.35 mL/ min;柱温为40 ℃;进样量为5 μL。
质谱条件:电喷雾离子源、负离子模式(ESI-),多反应监测(MRM)模式;电喷雾电压5 500 V;离子源温度500 ℃;气帘气(CUR)压15.0 psi;碰撞气(CAD)压10.0 psi;雾化气(氮气)压50.0 psi;辅助气压50.0 psi;射入电压(EP)10 V;射出电压(CXP)15 V。拟人参皂苷F11的母离子m/z799.6,子离子m/z653.7(定量离子),m/z491.6(定性离子),去簇电压(V)-20 V,碰撞能量-50 V。
2.2 溶液制备
对照品溶液:取拟人参皂苷F11对照品适量,精密称定,加甲醇制成每1 mL 含拟人参皂苷F1110 ng 的溶液,即得。
供试品溶液:取样品细粉约2.0 g,精密称定,置具塞锥形瓶中,精密加入20 mL 水,密塞,超声(功率700 W,频率80 kHz)处理30 min,取出,冷却至室温,滤过,取续滤液10 mL,经C18固相萃取小柱(500 mg,容量为6 mL,预先用甲醇、水各6 mL 洗脱)层析,用水15 mL洗脱,放置5 min,继续用甲醇15 mL 洗脱;收集洗脱液,置蒸发皿中蒸干,残渣加甲醇溶解,置5 mL容量瓶中,加甲醇稀释并定容,经0.22 μm滤膜滤过,取续滤液,即得。
参比溶液、阴性对照品溶液和阳性对照品溶液:按参麦颗粒处方工艺及比例制得参比样品,缺红参的阴性样品,以及将红参换为西洋参的阳性样品,按供试品溶液制备方法分别制备参比溶液、阴性对照品溶液和阳性对照品溶液。
2.3 方法学考察
专属性考察:分别取2.2 项下对照品溶液、参比溶液、阴性对照品溶液、阳性对照品溶液各适量,按2.1项下试验条件进样测定,记录图谱。结果显示,除阳性对照品溶液外,阴性对照品溶液和参比溶液均未检出拟人参皂苷F11,说明参麦颗粒中其他药味对测定无干扰,表明方法的专属性良好。详见图1。

1. 拟人参皂苷F11A1 - D1.m / z 799.6 →653.7 A2 - D2.m / z 799.6 →491.6A1、A2. 对照品溶液 B1、B2. 阴性对照品溶液 C1,C2. 参比溶液 D1,D2. 阳性对照品溶液图1 MRM图1.Pseudoginsenoside F11A1 - D1.m / z 799.6 →653.7A2 - D2.m / z 799.6 →491.6A1,A2.Reference solution of pseudoginsenoside F11 B1,B2.Negative reference solution of Shenmai Granules C1,C2.Reference solution Negative reference solution of Shenmai Granules D1,D2.Positive reference solution of Shenmai GranulesFig.1 MRM diagrams
线性关系考察:取拟人参皂苷F11对照品适量,加甲醇制成质量浓度分别为344.0,103.2,51.60,25.80,9.030 ng/mL 系列对照品溶液,按2.1 项下试验条件进样测定,记录离子强度,以待测成分质量浓度(X,ng/mL)为横坐标、离子强度(Y)为纵坐标进行线性回归,得回归方程Y1=916.18X1+6 193.91(r=0.999 2,n=5)。结果表明,拟人参皂苷F11质量浓度在9.030~344.0 ng/mL范围内与峰面积线性关系良好。
基质效应考察:取2.2 项下参比溶液(为基质),配制质量浓度为68.80 ng/mL 的对照品溶液,并取2.2项下对照品溶液,按2.1 项下试验条件进样测定,记录峰面积。结果表明,以参比溶液为基质对照品溶液的峰面积(14 346.9 →3 090.4)较以甲醇为基质的峰面积(75 026.3 →12 035.1)明显降低,基质效应明显,故以参比溶液为基质制备系列对照品溶液(待测成分质量浓度分别为344.0,103.2,51.60,25.80,9.030 ng/mL),按2.1 项下试验条件进样测定,记录离子强度,以待测成分质量浓度(X,ng/mL)为横坐标、离子强度(Y)为纵坐标进行线性回归,得回归方程Y2= 160.91X2+1 354.05(r=0.999 3,n=5)。结果表明,拟人参皂苷F11质量浓度在9.030~344.0 ng/mL范围内与峰面积线性关系良好。
检测限和定量限考察:取“基质效应”项下以参比溶液为基质的对照品溶液适量,逐步稀释,并按2.1 项下试验条件进样测定,对离子强度相对较低的定性离子对进行检测,以信噪比(S/N)为3 和10 时待测成分质量浓度分别作为检测限和定量限,结果分别为1.128 8 ng/mL和22.8 ng/mL。
精密度试验:取2.2项下对照品溶液适量,按2.1项下试验条件连续进样测定6 次,记录离子强度。结果拟人参皂苷F11峰面积的RSD为1.94%(n=6),表明仪器精密度良好。
稳定性试验:取同一供试品溶液(编号S55)适量,分别于室温下放置0,4,8,12,24 h时按2.1项下试验条件进样测定,记录离子强度。结果拟人参皂苷F11峰面积的RSD为1.32%(n= 5),表明供试品溶液在室温下放置24 h内基本稳定。
重复性试验:取同一样品(编号S55)适量,按2.2项下方法平行制备6 份供试品溶液,按2.1 项下试验条件进样测定,记录离子强度,带入上述基质效应线性方程,计算含量。结果拟人参皂苷F11含量为312.05 ng/g,RSD为3.61%(n=6),表明方法重复性良好。
加样回收试验:取同一供试品溶液(编号S55)约1.0 g,共6 份,精密称定,分别加入一定量的对照品溶液,按2.2 项下方法制备供试品溶液,按2.1 项下试验条件进样测定,记录离子强度,带入上述基质效应线性方程计算加样回收率。结果见表1。
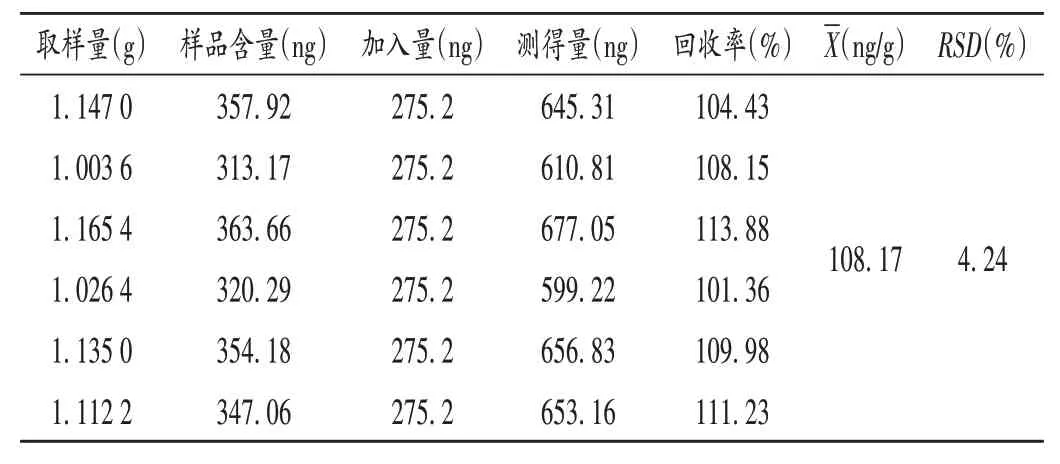
表1 加样回收试验结果(n=6)Tab.1 Results of the recovery test(n = 6)
2.4 样品含量测定
取各批样品适量,均平行3 份,按2.2 项下方法制备供试品溶液,按2.1 项下试验条件进样测定,记录离子强度,并计算样品含量,结果见表2(其中,-为低于检测限)。

表2 样品含量测定结果(μg/g,n=3)Tab.2 Results of the content determination of pseudoginsenoside F11 in samples(μg / g,n = 3)
掺伪比例及转移率考察:取已知含量的红参、西洋参,按样品处方工艺和比例分别制成5%西洋参阳性样品、10%西洋参阳性样品、西洋参阳性样品各3 份,按2.2 项下方法制备供试品溶液,按2.1 项下试验条件进样测定。结果各样品中拟人参皂苷F11的转移率分别为33.21%,33.70%,28.22%,平均转移率为31.71%。
限度确定:结合掺伪比例及转移率考察结果,且5%掺伪样品溶液中拟人参皂苷F11的S/N=239,满足定量限要求,以红参中添加有5%以上的西洋参作为非法添加的判定依据,拟人参皂苷F11的质量浓度为10 ng/mL,折合参麦颗粒中的量为0.051 μg/g。故9 批样品(S54,S55,S57,S60,S65,S67,S72,S80,S83)超出拟订限度,检出率为10.59%,均来自厂家C。
3 讨论
3.1 供试品溶液制备方法考察
样品处方中,红参仅占0.2%,蔗糖占92%,且各成分含量较低,基质复杂,易造成色谱系统污染。SPE小柱目前常用于样品前处理,是一项结合了选择性保留、选择性洗脱等过程的分离技术,可实现从复杂样品中提取净化或富集微量目标化合物,降低样品基质干扰,提高检测灵敏度的目的,且操作简便、回收率和重复性好。预试验中考察了C18柱、硅胶柱、C8柱、反相亲水亲脂平衡柱HLB、氨基SPE 小柱,结果显示,C18柱固相萃取柱可有效除去处方中的蔗糖,且回收率最高,操作简便,可有效减少有机试剂的使用和废物产生,故选择C18固相萃取柱用于供试品溶液提取。
3.2 试验条件考察
预试验中流动相考察了乙腈-水、甲醇-水、乙腈-0.1%甲酸水溶液、甲醇-0.1%甲酸水溶液,并进行梯度洗脱,分别监测m/z799.6 →653.6,491.6 和m/z845.5 →653.6,491.6 离子对,后者总体响应相对较低,而前者在4种体系中差异不大,但乙腈-水的流动相柱压较低,配制简单,故选择乙腈- 水为流动相,选择m/z799.6 →653.6,491.6为监测离子对。
3.3 拟人参皂苷F11 检出判定原则
以拟人参皂苷F11的质量浓度10 ng/mL 为西洋参非法添加判定依据,即供试品溶液的提取离子流色谱中,同时出现与对照品溶液色谱相应的色谱峰,且供试品溶液色谱中m/z799.6 →653.6 的色谱峰面积值大于对照品溶液中相应的峰面积值,视为检出。
3.4 结果分析
85批参麦颗粒中有9批样品拟人参皂苷F11含量超出拟订限度,掺伪比例在5.41%~7.23%,推断投料用红参可能存在西洋参掺伪现象,须引起企业重视。在市场上收集红参药材时发现一些不法商贩将采收加工中产生的“下脚料”、个小的西洋参掺入人参药材或饮片中加工成“红参”,不易区分,借此提高利润。部分企业贪图便宜,选用价格较低的掺杂部分伪品的红参。故企业需提高药材鉴定人员的技术水平,从源头上控制饮片质量。
3.5 方法评价
本研究中建立了UPLC-MS/MS 法对参麦颗粒中红参中拟人参皂苷F11的检查方法,前处理中采用的SPE 技术能有效从复杂基质样品中富集、净化特征成分,提高检测灵敏度、节省溶剂。该方法专属性强、准确度高、简单快速,可对制剂的质量控制和监督提供有力的技术支持。
