金纳米立方体的制备及其对水体污染物的SERS检测
2024-01-03马玉琪李磊施浩洋张仲鑫李沛然王聪秦苗
马玉琪,李磊,施浩洋,张仲鑫,李沛然,王聪,秦苗
(宿州学院 化学化工学院,安徽 宿州 254000)
随着人类工业文明的发展进步,水资源污染问题每况愈下,研发出可以快速检测水质、及时掌握水体动态变化的检测新方法具有十分深远的意义。孔雀石绿(Malachite Green,MG)作为一种人工合成的有机染料,常用于陶瓷、纺织、细胞化学染色等,但更为人们所熟知的用途是其具有杀灭霉菌的药效,长期用于水产品养殖的驱虫、杀菌以及防腐等方面[1-3]。随着研究的不断深入,孔雀石绿的安全性遭到质疑,科学家们发现其具有高毒性、高致癌、致突变和致畸的毒副作用,已被多个国家明令禁止使用,是水体污染和水产品安全中重点监控的污染物[4]。水产养殖禁止使用孔雀石绿几乎家喻户晓,但水产品中孔雀石绿的残留却时有发生。
现如今主要通过高效液相色谱法(HPLC)[5]和高效液相色谱串联质谱法(LC-MS)[6]等方法来进行孔雀石绿的检测,虽然这些方法具有分离效率高、检测灵敏度高的优势,但对于水体动态环境的实时检测分析却存在着检测时间长、成本高、预处理复杂等劣势[7]。因此,研究出能快速检测动态水体中孔雀石绿残留的新方法对保护水体环境有着积极的意义。
表面增强拉曼光谱法是一种新兴的快速检测方法,近年来得到了广泛的研究与应用[8]。由于拉曼信号较弱,需通过将被测物吸附在某些粗糙的表面或金属纳米颗粒表面时(Ag、Au、Cu等),这样可使得被测物质的拉曼散射产生极大的增强效应[9-11]。同时,与红外光谱不同,水分子的拉曼信号可忽略不计,更适合对含水物质进行分析检测[12]。因此,SERS分析技术由于前处理简单、灵敏性高、检测快速[13],为水体中孔雀石绿的检测带来了新的机遇。本研究建立了测定模拟真实水体中孔雀石绿污染的SERS检测方法,简单、高效、低损耗,在实际生活中有良好的应用前景。
本实验利用种子生长法制备金纳米立方体,使用扫描电子显微镜(SEM)、紫外-可见分光光度(UV-Vis)等方法对金纳米立方体的形貌结构进行表征。并选用CV作为拉曼探针分子测定金纳米立方体基底的SERS增强性能。进一步将MG粉末添加至湖水中,模拟真实水体中MG污染,以金纳米立方体为SERS基底,利用拉曼光谱仪测其SERS光谱。研究建立了测定真实水体中MG的SERS分析方法,检测效率高、成本低,具有实际应用前景。
1 实验部分
1.1 试剂
浓盐酸,分析纯,上海苏懿化学试剂有限公司;浓硝酸,分析纯,国药集团化学试剂有限公司;双氧水,分析纯,国药集团化学试剂有限公司;结晶紫(CV),分析纯,国药集团化学试剂有限公司;L-抗坏血酸(AA),分析纯,国药集团化学试剂有限公司;氯金酸(HAuCl4),分析纯,国药集团化学试剂有限公司;孔雀石绿(MG),分析纯,国药集团化学试剂有限公司;十六烷基三甲基溴化铵(CTAB),分析纯,国药集团化学试剂有限公司;硼氢化钠(NaBH4),分析纯,国药集团化学试剂有限公司。实验用水均为宿州学院自制Milli-Q的超纯水。
1.2 仪器
表面拉曼光谱仪,XPLORA PLUS型,法国HORIBA Jobin Yvon;超级恒温水浴锅,HK-2A型,南京南大万和科技有限公司;台式高速离心机,JW-3021H型,安徽嘉文仪器装备有限公司;数显恒温磁力搅拌器,HJ-3型,金坛市杰瑞尔电器有限公司;紫外分光光度计,UV-5700型,日立科学仪器(北京)有限公司;数控超声波清洗器,KQ5200DB型,昆山市超声仪器有限公司;聚焦离子束显微镜(FIB-SEM),Zeiss Auriga Compact型,德国ZEISS公司;电子天平,FA1004N型,上海菁海仪器有限公司;多用途混匀仪,MTX2000型,杭州瑞城仪器有限公司。
1.3 实验步骤
1.3.1 金纳米立方体的合成
首先,配制种子液,将103 μL氯金酸(HAuCl4)水溶液(质量分数1%)和897 μL十六烷基三甲基溴化铵(CTAB)水溶液(75 mmol/L)混合均匀。然后快速加入用冰水现配的0.6 mL硼氢化钠(NaBH4)水溶液(10 mmol/L),溶液立刻变为茶褐色,并用磁力搅拌器搅拌5 min。温度为25 ℃,静置2 h,备用。
接着,配制生长液,向21.33 μL十六烷基三甲基溴化铵(CTAB)水溶液(75 mmol/L)中加入790 μL氯金酸(HAuCl4)水溶液(质量分数1%)轻轻振动混匀,再加入99.19 mL抗坏血酸(AA)水溶液(0.645 mmol/L)轻轻摇晃数秒后,溶液立刻变成红色。
最后,边搅拌边向25 mL的生长液中加入12.5 μL稀释10倍的金种子溶液,静置8 h。
1.3.2 金纳米立方体SERS基底的制备
吸取适量上述溶液于1.5 mL的离心管中,进行离心(离心机参数设置为10 000 r/min,12 min)。离心结束后除去上层清液,其目的是除去金纳米立方体的表面活性剂,再加入适量的超纯水,放置于混匀仪中震荡摇匀。重复上述离心操作,除去上层清液后,吸取2~3 μL上述离心产物滴在洗净的硅片上,待自然晾干备用。
1.3.3 金纳米立方体基底的SERS性能表征
称取0.004 1 g的结晶紫(crystal violet,CV)于15 mL离心管中,加入超纯水定容至10 mL,配置成1×10-3mol·L-1的CV待测溶液,然后依次稀释到10-6,10-7,10-8,10-9mol·L-1。取2 μL不同浓度的CV溶液滴在上述制备好的基底上,等待自然风干,留一个空白基底作为对照。进行SERS检测,拉曼光谱仪的检测参数设置:激发波长为633 nm,积分时间为1 s,激发功率为500 mW,光谱范围为400~1 800 cm-1。
1.3.4 孔雀石绿标准溶液的制备及SERS检测
称取0.004 64 g孔雀石绿粉末,溶解于约5 mL超纯水中,并定容至10 mL容量瓶中,配得1×10-3mol·L-1的MG标准溶液。然后依次用超纯水稀释到浓度为10-6,10-7,10-8,10-9,10-10mol·L-1,备用。用移液枪依次取2 μL不同浓度的孔雀石绿待测溶液滴至基底上,并留一个空白基底作为对照。自然晾干后,进行SERS检测。
1.3.5 真实水体中孔雀石绿的配置及SERS检测
从学校珍珠湖取水100 mL,按上述操作步骤配得1×10-3mol·L-1的真实水体MG储备液。然后依次用湖水稀释,分别配制成浓度为10-6,10-7,10-8,10-9mol·L-1的真实水体MG待测溶液,备用。取上述不同浓度的孔雀石绿待测溶液2 μL滴在基底上,留一个空白基底加湖水作为对照。等待自然风干,利用拉曼光谱仪测得样品图谱。
2 实验结果与讨论
2.1 金纳米立方体的形貌表征
利用紫外分光光度计对样品进行紫外表征,吸取适量合成好的金纳米立方体溶胶置于石英比色皿中进行吸光度测试,波长范围设定为300~900 nm。紫外-可见吸收光谱测试结果表明该金纳米立方体约在574 nm处有一个较为尖锐的表面等离子体共振吸收峰,表明制备出了金纳米立方体,且金纳米立方体具有一定的分散性,如图1所示。
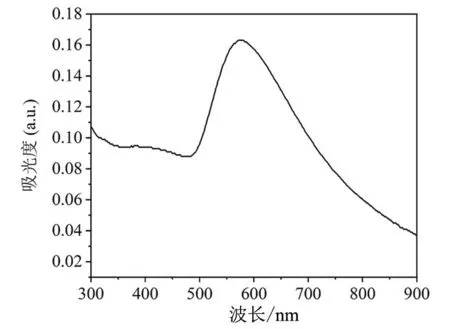
图1 金纳米立方体的紫外-可见光谱图
利用扫描电子显微镜对样品进行形貌观测,取上述合成好的金纳米立方体溶胶1 200 μL放入1.5 mL的离心管中,进行离心。离心后用移液枪吸去上层清液,目的是除去表面活性剂。接着进行第二次离心,同样去除上层清液。然后加入少量纯水,振荡摇匀。取少量溶液滴于硅片上,等待其自然干燥。并进行扫描电镜检测,如图2所示,金纳米立方体很大程度上被合成出来,但是也有少量其他形貌的纳米颗粒,这在种子生长法制备纳米材料时有发生,文献报道,使用种子生长法制备粒径约为100 nm左右的金纳米立方体的产率大概为70 %[14]。图2a右上角中插入了单个金纳米立方体的SEM图像,颗粒大小约为100 nm。图2b为金纳米立方体的尺寸分布直方图,显示颗粒的平均粒径约为102 nm。
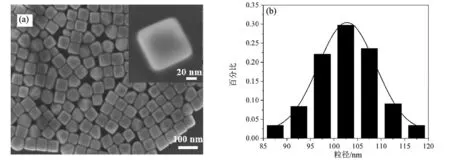
(a)金纳米立方体SEM表征图(右上角插图为单个纳米立方体的SERS图像);(b)金纳米立方体的粒径分布图
2.2 金纳米立方体基底的SERS检测灵敏性与重现性表征
为了考察金纳米立方体基底的SERS检测灵敏度和重现性,使用新制的SERS基底对不同浓度的CV溶液进行测试。如图3所示,使用金纳米立方体作为SERS基底检测10-6mol/L CV,随机采集50条光谱,SERS光谱表现出较好的重现性和稳定性。如图4所示,在10-6mol/L CV的五十条光谱图中1 619 cm-1处峰强度的相对标准偏差(RSD)= 15.33% <20%,说明金纳米立方体基底的SERS检测信号均匀性良好。如图5所示,是金纳米立方体吸附不同浓度CV的SERS谱图,从图中可以很明显看出,在439,797,938,1 171,1 615 cm-1处[15]存在着很明显的特征峰。如图6所示,随着CV浓度的降低,SERS信号也不断降低,检测最低浓度达到10-9mol/L。因此,基于上述SERS谱图,可以初步说明金纳米立方体基底可以有效放大目标物的信号。

图3 10-6 mol/L CV的50条SERS光谱图
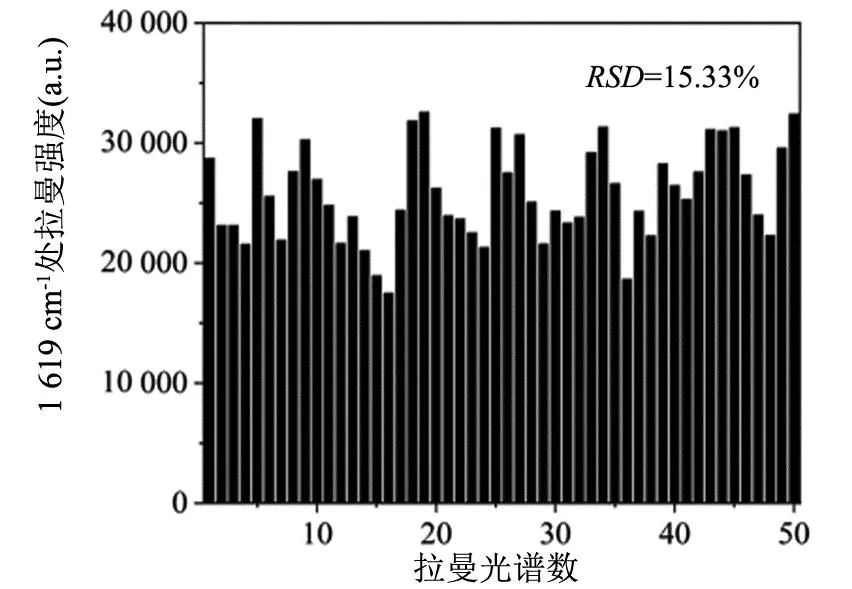
图4 金纳米立方体吸附10-6 mol/L CV 1 619 cm-1处的特征峰点的50条柱状图

图5 金纳米立方体作为基底检测不同浓度(10-6~10-9 mol/L)CV的SERS光谱图

图6 金纳米立方体吸附不同浓度(10-6~10-9 mol/L)的CV 1 619 cm-1处特征峰的点线图
2.3 孔雀石绿标准溶液的SERS检测
利用拉曼光谱仪测定不同浓度的MG标准溶液。如图7a所示,图中436,916,1 174,1 367,1 616 cm-1处均是MG的特征峰[16],SERS信号的强度随着MG浓度的降低而逐渐降低,检测限可低至10-10mol/L。为探究SERS峰强度与浓度之间的关系,在图7b中建立了MG在1 616 cm-1处SERS峰强度与浓度对数的点线图。实验结果表明,制备的金纳米立方体基底可用于对MG标准溶液的高灵敏度SERS检测,说明SERS技术应用在MG标准溶液检测方面具有巨大应用潜力。
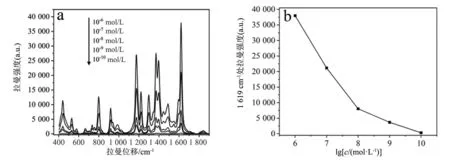
(a)SERS光谱图;(b)在1 619 cm-1处特征峰的点线图
2.4 真实水体中孔雀石绿的SERS检测
为探究金纳米立方体基底在实际样品中的测试性能,以学校珍珠湖湖水为溶剂制备MG溶液,并利用拉曼光谱仪测定其检测极限以及重现性。如图8所示,分别是滴加10-6,10-7,10-8,10-9mol/L四个浓度的MG实际水样以及湖水的SERS谱图。图中可以清晰看到436,916,1 174,1 367,1 616 cm-1处MG的特征峰,检测限可低至10-9mol/L。由于10-8,10-9mol/L浓度在图8的SERS谱线并不明显,特将10-7,10-8,10-9mol/L时的MG实际水样SERS谱线进一步作图,如图9,可以看出真实水样中10-9mol/L的MG特征峰仍能清晰辨别。同时为探究金纳米立方体基底对MG实际水样的重复性,使用金纳米立方体作为SERS基底检测10-7mol/L MG,随机采集30条光谱,如图10所示。如图11所示,对MG 1 616 cm-1处的特征峰的30个点SERS强度进行相对标准偏差计算,得到RSD= 17.96% <20%,SERS光谱表现出较好的重现性和稳定性。所得结果表明,在实际应用中,可用制备的金纳米立方体基底检测真实水体中MG溶液,为SERS技术应用在真实水体中MG溶液检测提供了可能性。
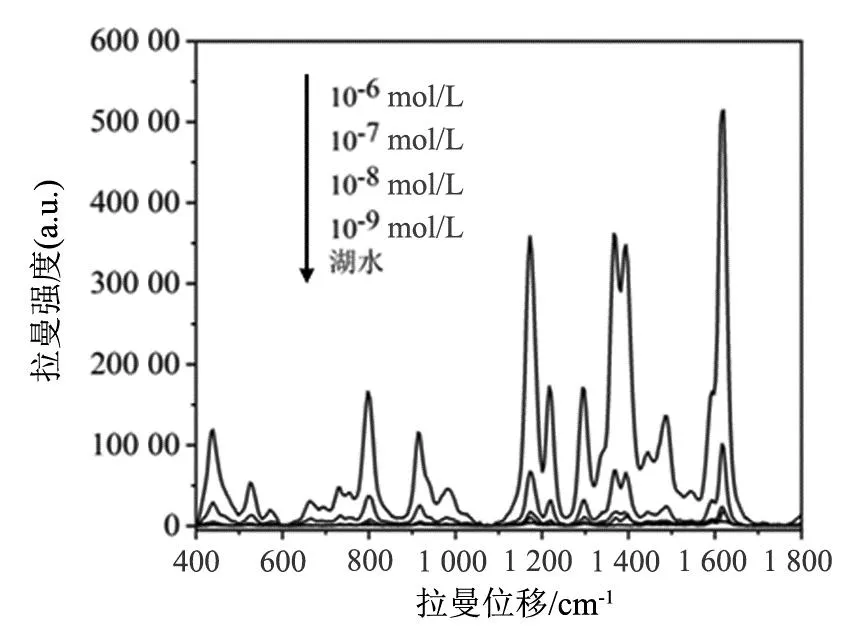
图8 金纳米立方体作为基底检测不同浓度(10-6~10-9 mol/L)MG真实水样以及湖水的SERS光谱图
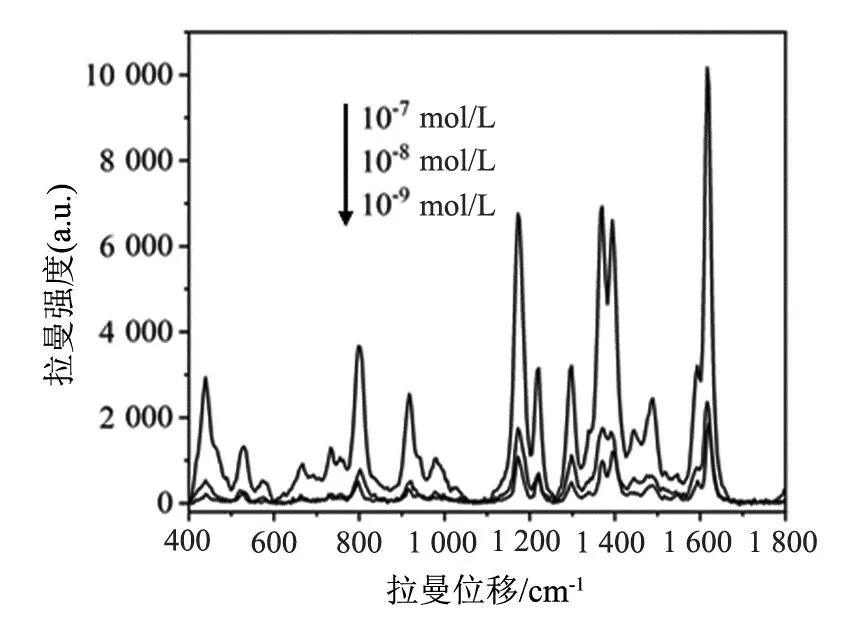
图9 金纳米立方体作为基底检测不同浓度(10-7~10-9 mol/L)的MG真实水样的SERS光谱图

图10 金纳米立方体作为基底检测10-7 mol/L MG真实水样的30条SERS光谱图

图11 金纳米立方体作为基底检测10-7 mol/L MG真实水样在1 619 cm-1处特征峰点的30条柱状图
3 结论
以种子生长法制备金纳米立方体,利用SEM和UV-Vis方法对合成的金纳米立方体进行表征,表明制备出形貌均一的金纳米立方体。并选用CV作为拉曼探针分子测定金纳米立方体基底的SERS增强性能。结果表明,金纳米立方体对CV的检出限为10-9mol/L,1 619 cm-1处的RSD为15.33%,表现出良好的检测灵敏性和重现性。使用金纳米立方体作为SERS基底测定水体污染物孔雀石绿标准溶液,检测极限可达10-10mol/L。最后,将MG标准添加至真实湖水中模拟真实水样,无需任何前处理,可以检测到浓度低于10-9mol/L的MG。实验结果表明使用SERS方法对真实水体孔雀石绿进行检测准确可靠、选择性强、灵敏性高,表明该技术有望应用到实际生活中真实水体中孔雀石绿的检测。
