凝胶电解质软包钠离子电池的研究
2023-12-19黄华文范珊珊唐伟超郭盼龙邱亚明
黄华文,范珊珊,赵 伟,唐伟超,郭盼龙,邱亚明
(1.华南理工大学化学与化工学院,广州 510641;2.珠海冠宇电池股份有限公司,珠海 519600)
在“双碳”政策驱动、前期研究技术积累和市场需求等多重刺激下,钠离子电池由于具有成本低、低温性能出色、循环稳定和倍率优异等优势,在2022年以来被推到了科研和工业的开发前端[1~4].现阶段,在钠离子电池的正极材料中,层状氧化物由于与锂三元正极材料的工艺路线相近,且能量密度高,是目前产业界主要的推进路线[5~11].以镍基层状氧化物为例,其工作电压上限越高,比容量越高,体系的能量密度也越高,如3.9 V 的比容量是120 mA·h/g,4.2 V 时具有160 mA·h/g 比容量[12,13].目前,高能量密度氧化物体系钠离子电池工业化推进遇到了以下挑战:(1)钠的标准电位较低(Li:-3.04 V;Na:-2.71 V),电解液承受的实际电压较高[14,15];(2)正极脱钠态的产物具有强氧化性,工作电压越高,氧化性越强;上述因素会导致钠离子电池在充放电过程中易出现电解液分解、产气,使电池容量迅速恶化[16~18];(3)常用的有机液态电解质存在易燃、易泄露的特性,当电池出现热失控后易发生爆炸而引起安全隐患[19~22].上述问题严重阻碍了软包钠离子电池的开发进度.
针对上述问题,借鉴锂离子电池的研究经验,将电解质固态化以提高电解质的稳定性是科学家们的主要切入点,其中,聚合物凝胶电解质由于具有高的安全性和室温离子电导率而备受青睐[23~27].而相对于常规的凝胶电解质制备的复杂工艺流程,原位固化凝胶电解质与现有的电池制备工艺兼容性高、且有利于实现稳定的电解质-电极的固-固界面,实现界面融合,有效降低界面阻抗,有利于提高电池的循环寿命,具有很好的应用前景[28~30].Sun等[31]利用原位固态化技术制造了丙烯酸酯基聚合物电解质准固态软包锂离子电池,该电池显示出优异的循环稳定性;稳定的电化学性能归因于原位固化技术在电解质/电极之间构建了稳健、均匀的界面,从而成功抑制了界面副反应并防止电极界面结构退化.此外,Guo 等[32]采用类似的思路,将凝胶电解质应用到钠离子电池中,并展示了出色的电化学性能.然而,目前,对于凝胶电解质钠离子电池的研究大多停留在纽扣电池层面,关于凝胶电解质应用到工业化的软包钠离子电池的研究仍鲜有报道[33~37].
本文以层状氧化物作为正极材料,通过原位固化1,5-戊二醇二丙烯酸酯基聚合物电解质制备准固态凝胶电解质软包钠离子电池;原位固化的凝胶电解质可以提高材料的界面稳定性,同时具有良好的离子传输效果,所制备的凝胶电解质软包钠离子电池具有出色的循环稳定性(1C倍率下循环300次的容量保持率高达97.7%),同时可以很好地抑制了电池在循环过程中产气(1C倍率下循环300次的膨胀为1.15%),而且在提高电芯安全性方面有很好的效果.
1 实验部分
1.1 试剂与仪器
1,5-戊二醇二丙烯酸酯(C11H16O4,分析纯)和偶氮二异丁腈(C8H12N4,AIBN,分析纯),Aladdin试剂公司;镍基层状氧化物(NaNi1/3Fe1/3Mn1/3O2)正极材料,江苏翔鹰新能源科技有限公司;硬碳负极材料,日本可乐丽株式会社;基础电解液[1 mol/L 六氟磷酸钠(NaPF6)+碳酸乙烯酯(EC)/碳酸二乙酯(DEC)/碳酸二甲酯(DMC)(体积比1∶1∶1)+氟代碳酸乙烯酯(FEC)(体积分数3%)+碳酸亚乙烯酯(VC)(体积分数1%)],珠海市赛纬电子材料股份有限公司;导电碳黑(Super P,电池级),天津亿博瑞化工有限公司;聚偏二氟乙烯(PVDF,电池级),山东联创产业发展集团股份有限公司;N-甲基吡咯烷酮(NMP,电池级),迈奇化学股份有限公司;羧甲基纤维素钠(CMC,电池级)和丁苯橡胶乳液(SBR,电池级),深圳一特科技有限公司.
Discovery550型热重分析仪(TGA),美国TA公司;VMP3型电化学工作站,法国Biologic公司;iN10型红外光谱仪(IR),美国Nicolet 公司;SU5000型扫描电子显微镜(SEM),日本Hitachi 公司;7820A型气相色谱仪,美国Agilent公司.
1.2 实验过程
1.2.1 软包钠离子电池的制备 将镍基层状氧化物、导电炭黑和PVDF(质量比95∶3∶2)溶于NMP配制成浆料,并涂覆在铝箔两面,单面的材料面密度为15 mg/cm2;将硬碳、导电炭黑、CMC和SBR按质量比90∶4∶3∶3 混合,用去离子水作为溶剂配制成浆料,并涂覆在铝箔两面,单面的材料面密度为8 mg/cm2.制备好正负极片后,与隔离膜一起按照Z字方案叠片,电芯容量设计为1.0 A·h.将电芯装配极耳后封装到铝塑袋中,留一侧不封边,然后置于烘箱于90 ℃烘烤.将烘烤合格的电芯注入适量的基础电解液,然后封口静置24 h.随后化成、二封、分选后制备得到软包钠离子电池.
1.2.2 凝胶电解质的制备 将5%(质量分数)的1,5-戊二醇二丙烯酸酯单体溶解在基础电解液中制备前驱体,在单体完全溶解后,向混合物中加入0.1%(质量分数)的AIBN,将混合溶液搅拌30 min后,转移到模具中,然后在80 ℃下热处理12 h引发单体聚合成凝胶态.
1.2.3 凝胶电解质软包钠离子电池的制备 将5%的1,5-戊二醇二丙烯酸酯单体溶解在基础电解液中制备前驱体,在单体完全溶解后,向混合物中加入0.1%的AIBN,混合溶液搅拌30 min后,取适量混合电解液直接注入预干燥的全电池中,然后在真空密封器中完全密封铝袋,静置24 h让前驱体溶液充分浸润到电极和隔膜中.通过在80 ℃下热处理12 h引发单体聚合成凝胶态.随后化成、二封、分选后制备得到凝胶电解质软包钠离子电池.
1.2.4 循环膨胀率测试 测试第一次充电状态电池的厚度(记为H1),随后在循环50,100,150,200和300次时在充满电的状态下停止充放电测试,将电池取下测试位置,用厚度测量仪测试电池的厚度(记为Hx),通过公式循环膨胀率=Hx/H1×100%计算指定循环次数的循环膨胀率.
2 结果与讨论
2.1 凝胶电解质的电导率、力学性能和热力学稳定性
通过定制的模具将凝胶电解质制备成直径12 mm、高度20 mm 的凝胶圆柱(图1),用于电导率测试.利用电化学工作站对凝胶块测试交流阻抗谱(EIS),同时测试了基础电解质的交流阻抗谱作为对比[图2(A)].通过拟合电路[图2(A)插图:Rs(Ω)为界面电阻;Rct(Ω)为表面电荷转移过程电阻;Cd(F)为电双层电容;Zw(Ω)为Warburg阻抗,即离子在电极材料中的扩散阻抗],可以计算出电解质的界面电阻Rs.基础电解液的内阻为281 Ω,凝胶电解质的内阻为387 Ω.通过σ=L/RS[其中,σ(mS/cm)为电导率,R(Ω)为电阻,S(cm2)为导体的横截面面积,L(cm)为导体的长度][33],可算出基础电解质的电导率为6.78 mS/cm,凝胶电解质的电导率为4.41 mS/cm,约为基础电解质电导率的65.0%[图2(B)].凝胶电解质电导率下降,是由于聚合物形成凝胶后对离子传输存在阻碍作用[31,32].

Fig.1 Schematic diagram of gel-electrolyte sodiumion battery(left),and the prepared gel electrolyte(right)
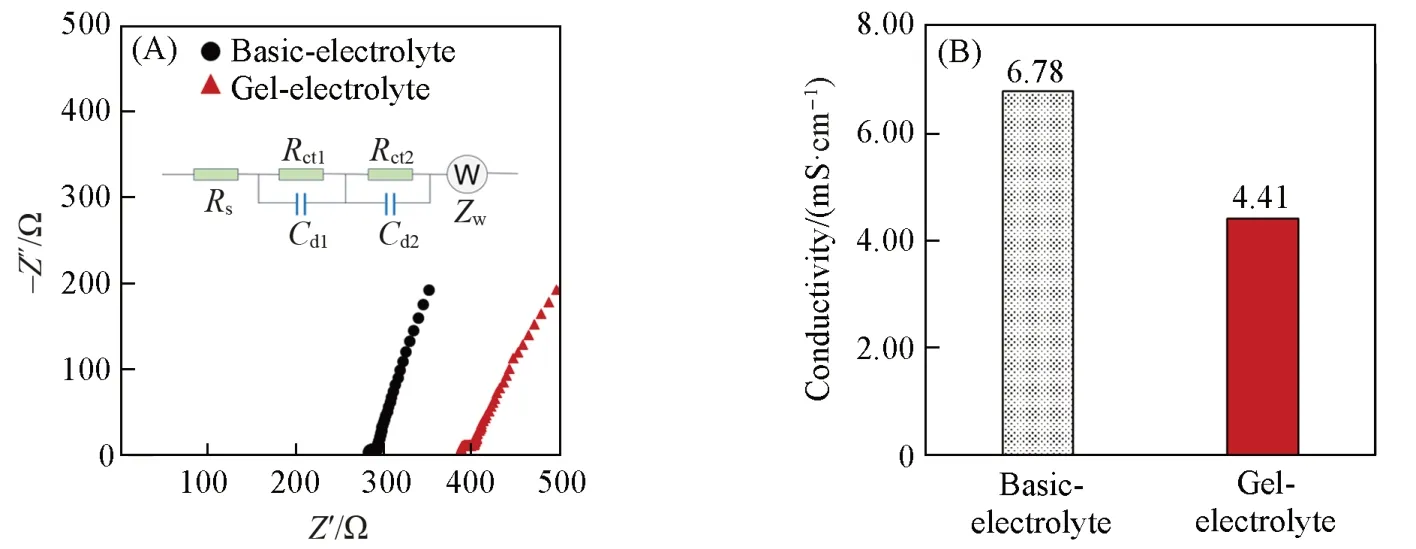
Fig.2 EIS test(A) and conductivity calculation results(B) of basic electrolyte and gel electrolyte
简单评估了凝胶电解质的力学性能(图3).使柱状的凝胶块径向受压[图3(A)],在受到一定压力的情况下,截面高度约降低1/3,呈椭圆状,表面保持光滑无裂纹[图3(B)].在撤去压力后,凝胶恢复完整的柱状[图3(C)].展示出了较好的力学性能,有利于提高电池的安全性.同时,通过热重曲线对凝胶电解质的热力学稳定性进行分析.如图4 所示,将基础电解液与凝胶电解质的热重曲线进行对比,其中两个插图分别为20~100 ℃区域和400~600 ℃区域的放大图.通过对比可知,凝胶聚合后,电解质开始挥发的温度比基础电解液延后,前20%的失重温度延后约20 ℃:从70 ℃延后到90 ℃.在温度达到100 ℃时,凝胶电解质的质量保持率约80%,基础电解液约为65%.在温度达到500 ℃后,凝胶电解质的固体残留约8.2%,高于基础电解质的5%.由此可知,凝胶聚合后,电解质的热力学稳定性有所增加,有利于提高电池的安全性.
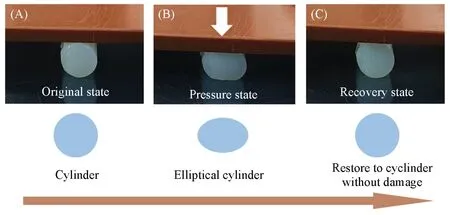
Fig.3 Performance demonstration of original state(A),pressure state(B) and recovery state(C) of gel electrolyte under pressure
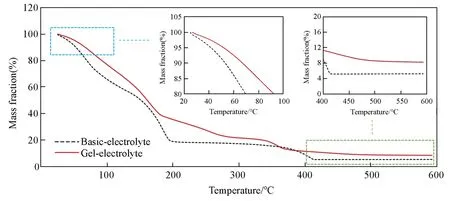
Fig.4 Thermogravimetric curves of basic electrolyte and gel electrolyte
2.2 凝胶电解质的红外光谱
利用红外光谱对聚合物单体1,5-戊二醇二丙烯酸酯、基础电解液和凝胶电解质进行了分析.图5(A)为聚合物单体1,5-戊二醇二丙烯酸酯的结构式;图5(B)为引发剂偶氮二异丁腈的结构式.图5(C)展示了聚合物单体1,5-戊二醇二丙烯酸酯、基础电解液和凝胶电解质的IR谱图.可见,聚合物单体在1630 cm-1处的特征峰归属为—COO—的反对称伸缩振动和C=C的伸缩振动;1409 cm-1处的特征峰归属为两端—CH2的变角振动;980 cm-1处的特征峰归属为C=C的扭曲振动;811 cm-1处的特征峰归属为—COO—的变角振动[31].但这几个特征峰在凝胶电解质中均未被检测到,说明了加入基础电解液中的聚合物单体已经被全部消耗,形成了聚合物.除了这几个特征峰,单体还有几个明显的信号峰,如1722 cm-1处的特征峰归属于—C=O双键的伸缩振动,1276 cm-1处的峰归属于C—O—C的反对称收缩振动,1186和1058 cm-1处的峰归属于C—O—C的伸缩振动;电解液在557 cm-1处存在一个特征峰,是来自于六氟磷酸钠中F—P—F 的对称伸缩振动[31,33].重要的是,通过对比可知凝胶电解质的红外光谱与基础电解质的几乎一致,说明通过加入聚合物原位聚合制备凝胶电解质,对电解质本身组分没有影响.

Fig.5 Structural formulas of polymer monomer 1,5-pentanediol diacrylate(A) and initiator azobisisobutyronitrile(B),infrared spectra of basic electrolyte,gel electrolyte and polymer monomer(C)
2.3 凝胶电解质钠离子电池的电化学性能
将制备的基础电解液和凝胶电解质钠离子软包电池在1.50~3.95 V的电压区间进行充放电测试.图6(A)展示了基础电解液和凝胶电解质软包钠离子电池在1C倍率下的充放电曲线(1C=1.0 A),两者几乎重合,容量发挥一致,说明了电解质凝胶化后,并没有影响电池常规电化学性能的发挥.图6(B)展示了基础电解液和凝胶电解质钠离子电池在1C倍率下的常温循环曲线.可见,两者均具有出色的循环稳定性,在循环300次后,凝胶电解质组的容量保持率为97.7%,略高于基础电解液组的97.3%,说明电解质凝胶化后,对电池的循环保持率有一定程度的改善作用.
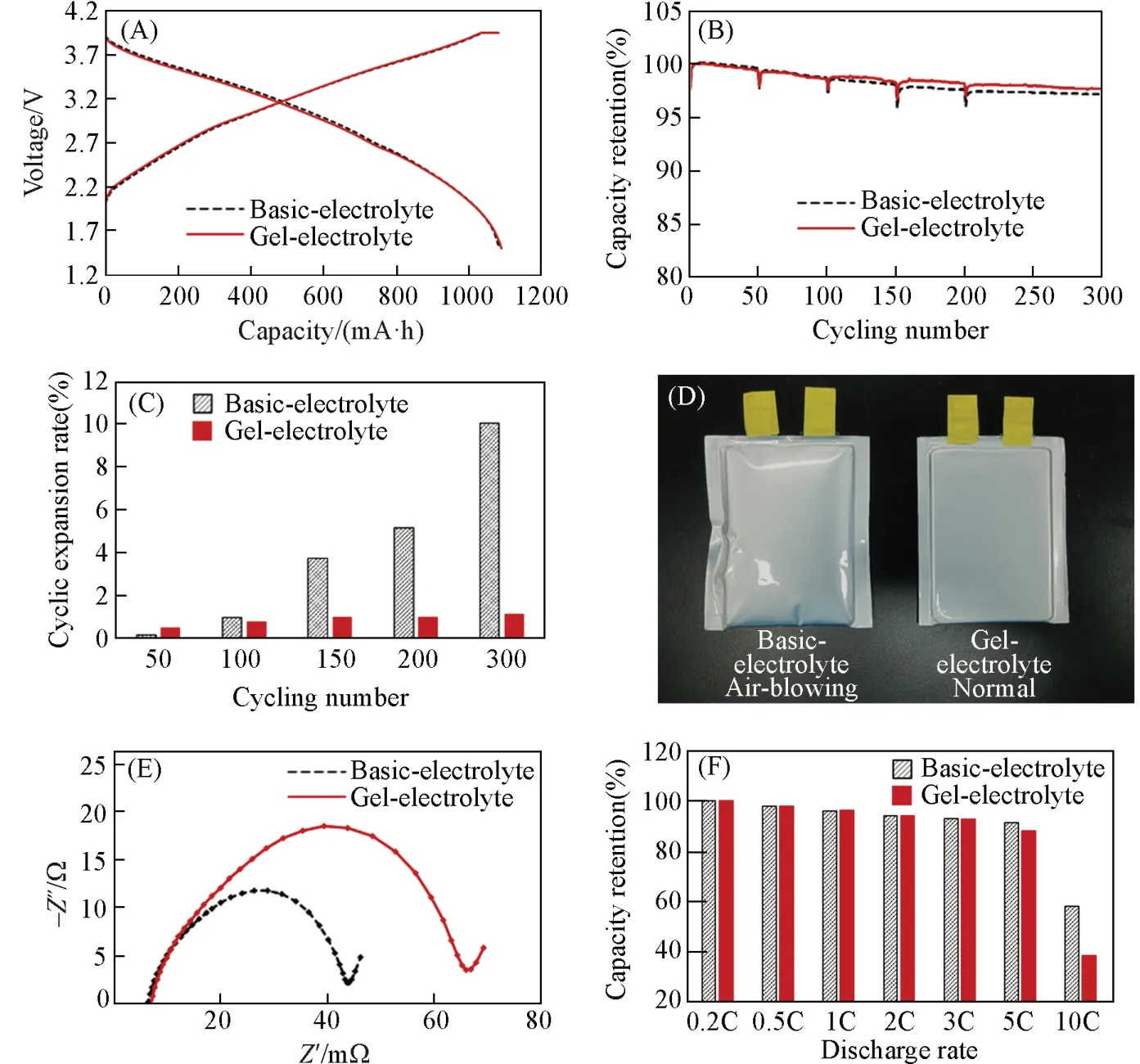
Fig.6 Charge/discharge curves(A) and normal temperature cycle curves(B) of soft packed sodium-ion battery with basic electrolyte and gel electrolyte at a rate of 1C,ambient temperature cycle expansion(C) and appearance photos after 100 cycles at 45 ℃(D) of basic electrolyte and gel electrolyte soft package sodium-ion battery,EIS curve(E) and rate performance(0.2C—10C)(F) of basic electrolyte and gel electrolyte soft package sodium-ion battery
重要的是,检测了软包电池循环过程中的膨胀情况.图6(C)给出了基础电解液和凝胶电解质软包钠离子电池常温循环膨胀数据.凝胶电解质软包钠离子电池在50,100,150,200和300次循环后,电芯的膨胀率为0.53%,0.82%,1.02%,1.04%和1.15%.而基础电解液软包钠离子电池在50,100,150,200 和300 次循环后,电芯的膨胀率为0.25%,0.99%,3.77%,5.17%和10.06%.通过对比可知,基础电解质软包钠离子电池随着循环次数增加,膨胀率增加的趋势明显,到300次时表面可观察到轻微鼓气现象.相对比而言,凝胶电解质软包钠离子电池在循环过程的电芯膨胀率相对稳定,在300次后仅为1.15%,说明了凝胶化后可以有效抑制电芯在循环过程中的产气现象,且此现象在高温循环会更加显著.图6(D)为基础电解液和凝胶电解质软包钠离子电池在45 ℃循环100次后外观照片的对比.可见,基础电解液组已经严重鼓气,但是凝胶电解质组外观正常.上述测试表明,电解质凝胶化后,可以保持与基础电解液相当的容量发挥,且在循环保持率方面略有优势.重要的是,可以有效缓解钠离子电池在循环过程中的产气现象,有利于提高钠离子电池的循环稳定性.
另外,对比了凝胶电解质钠离子电池和基础电解液钠离子电池的内阻,电化学阻抗谱(EIS)结果表明,凝胶电解质钠离子电池的内阻更高[图6(E)],这是由于凝胶电解质电导率低导致的.虽然凝胶电解质钠离子电池的内阻较大,但是对小倍率性能的发挥影响不大.图6(F)展示了两者在0.2C~10C的倍率性能.当倍率≤3C时,凝胶电解质钠离子电池的倍率容量发挥与基础电解质组一致,在3C的高倍率下具有92.5%的放电容量保持率,证明了凝胶电解质钠离子电池的倍率性能优异,可以满足大多数使用场景的需求.当倍率进一步增加时,凝胶电解质钠离子电池的倍率性能出现明显衰减,较基础电解液组的容量保持率低,这是由于凝胶电解质钠离子电池的内阻偏大导致的,因此该体系不适合高倍率的应用场景.
除此之外,对凝胶电解质软包钠离子电池的安全性能作了初步探索.图7(A)和(B)分别为基础电解液和凝胶电解质软包钠离子电池针刺后的光学照片.使用5 mm的钢针进行穿刺实验,均未发生冒烟或起火现象,说明钠离子电池具有良好的安全性能.进一步对比了两组电池在针刺过程中的温度变化情况[图7(C)].基础电解液软包钠离子电池在针刺后,电芯表面温度迅速升至116 ℃;相对而言,凝胶电解质软包钠离子电池被针刺后的温度上升趋势缓慢些,最高温度只有107 ℃,且其降温速率更快.上述结果表明,电解质凝胶后,可以减缓针刺测试的温升速率,降低其最高温度,并加快热量散发,有利于提高电芯的安全性.

Fig.7 Optical photos of sodium-ion battery with basic electrolyte(A) and gel electrolyte(B) soft package after acupuncture,temperature change curve of acupuncture test process of soft package sodium-ion battery with basic electrolyte and gel electrolyte in full charge state(C)
为了进一步了解凝胶电解质改善性能的原因,对电池进行首次库仑效率(ICE)测试分析和电芯拆解分析.图8(A)和(B)分别为基础电解液和凝胶电解质软包钠离子电池的ICE.基础电解液组的ICE为82.0%,这是通过计算放电容量(1181 mA·h)与充电容量(1441 mA·h)的比值得到的;而凝胶电解质组的ICE为85.3%(放电1191 mA·h,充电1396 mA·h).这是由于凝胶电解质包覆在正负极材料表面,有利于形成更均匀的固体电解质界面(SEI)膜和电化学界面(CEI)膜,因此凝胶电解质的首次充电容量偏低,放电容量偏高.另外,如图8(C)和(D)所示,在分选后的正极材料表面,凝胶电解质组的正极表面更加致密,而电解液组的正极表面相对疏松,该结果与文献[31,35,37]一致.由参考文献中更加具体的表征分析结果可以推测,凝胶电解质钠离子电池优异的电化学性能与电解质和电极之间形成的稳健界面密切相关,不仅有利于抑制电极和液体电解液之间的副反应,提高ICE和循环稳定性;还可以有效防止正极材料在循环过程中受到侵蚀,进而抑制了循环产气现象.进一步使用气相色谱对循环后的鼓气电芯进行了气体分析.气体的主要成分为二氧化碳(79.498%)和一氧化碳(17.791%),两者共占约97%.二氧化碳和一氧化碳为氧化性气氛,其产出的主要位置是正极表面.由此可推测,电芯产气的主要原因是正极材料在脱钠态下具有较高的氧化性,将电解液氧化分解,进而产生气体.在凝胶电解质体系中,凝胶电解质可以将正极材料表面较好地包覆,形成稳定的保护层;另外,降低电解液的流动性,减少电解液与正极材料表面的接触,因此可以较好地抑制电池产气.
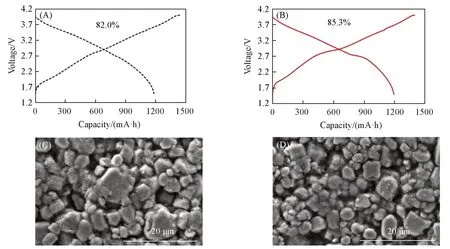
Fig.8 Coulomb efficiency test of the first cycle(A,B),SEM images of the cathode surface(C,D)of the basic electrolyte(A,C) and gel electrolyte(B,D) of soft packed sodium-ion batteries
3 结论
通过选择合适的聚合单体和引发剂结合,通过原位聚合制备了凝胶电解质软包钠离子电池.在保证容量发挥、循环稳定性和倍率性能等基础的电化学性能的同时,有效抑制了软包钠离子电池的循环产气.在循环300次后,循环膨胀率只有1.15%,约为基础电解质组的1/10,效果显著.同时,针刺实验结果表明,电解质凝胶后,电池温升速率减缓,其最高温度降低,热量散发加快,有利于提高电芯的安全性.因此,将凝胶电解质应用在钠离子电池中,可以有效解决现阶段遇到的产气问题,为钠离子电池开发提供了新的思路,具有很好的开发和应用前景.
