咔唑近红外荧光探针可视化线粒体及体内成像应用
2023-12-19顾亚琴丁劲峰陈金娥谢文娜肖林霞
顾亚琴,丁劲峰,陈金娥,谢文娜,肖林霞
(江苏医药职业学院,盐城 224002)
所有活细胞的细胞质都含有胞内细胞器和生物大分子,如蛋白质和核酸[1,2].这些细胞器执行其职责并影响重要的生物功能,包括代谢、能量运输和细胞增殖[3,4].所有这些功能都需要能量,而能量则由线粒体产生.它是活细胞内能量产生的枢纽,是细胞内钙稳态、信号传导和细胞自噬、凋亡的关键参与者[5,6].线粒体功能障碍通常会导致多种严重疾病,包括肿瘤、神经退行性疾病和心血管疾病以及肥胖症、糖尿病和非酒精性脂肪肝病(NAFLD)等在内的代谢疾病[5,7].因此,开展对线粒体的动态成像将有助于揭示相关疾病的发生、发展过程.自19 世纪50 年代以来,通过测量烟酰胺腺嘌呤二核苷酸(NADH/NAD+)的自发荧光来监测线粒体活性一直是最实用的方法[8],但因受到背景荧光干扰、低灵敏度及短发射波长的限制,制约了其在生物学领域的应用.在过去的十年中,荧光分子成像技术取得了巨大进步,并随着高分辨率显微镜技术的完善及细胞内分子事件的可视化[9],种类繁多的有机荧光分子被应用于线粒体的监测,如罗丹明类[10~12]、花菁或半花菁类[13,14]、BODIPY类[15]以及香豆素类[16],然而大部分线粒体荧光探针受到短发射波长以及小Stokes位移的限制,难以实现体内的荧光成像.近红外荧光探针的出现较好地克服了传统荧光探针的缺点,其具有发射波长长(650~900 nm)[17,18]、对细胞损伤小[19,20]、组织穿透性强[21]和自发荧光背景低[22]等优点,已广泛应用于细胞、组织等复杂生物系统中生物分子的检测、示踪和成像.
咔唑是一类芳香类含氮杂环化合物.在结构上,咔唑由2 个苯环和1 个吡咯环组成,具有双对称轴、优良的空孔传输能力[23]和刚性的平面结构,通常被用作电子给体分子,其衍生物由于原料容易获得[24]、热稳定性好且结构易于修饰[25],在有机发光二极管(OLEDs)和荧光传感器等领域得到了广泛应用.本文基于咔唑衍生物优良的物理化学和光学特性,设计合成了一系列具有大Stokes位移的近红外荧光探针(化合物6g~6j).大Stokes位移荧光探针由于减少了荧光传感中的自猝灭和自荧光,从而显著改善了生物成像应用中的信噪比.目前,大多数大Stokes位移的荧光染料通过引入给电子基使HOMO能级上升,能带隙变窄,斯托克斯位移变大,但却导致其荧光量子产率降低,而咔唑类荧光染料却在拥有大Stokes 位移的同时具有高荧光量子产率.实验结果表明,化合物6j 在水溶液中发射波长达668 nm,且具有大Stokes位移(146 nm)和高荧光量子产率(Φ=0.45),并表现出极好的线粒体靶向能力(P=0.90).该探针能对裸鼠卵巢癌移植瘤组织进行荧光成像,并能持续16 h以上,为临床上肿瘤的精准诊断和治疗提供了新策略.
1 实验部分
1.1 试剂与仪器
2,3,3-三甲基-3H-吲哚、1,1,2-三甲基-1H-苯并[e]吲哚、4-甲基喹啉、4-甲基吡啶、碘甲烷(CH3I)、氢化钠(NaH)、溴化苄和甲基溴化镁,分析纯,上海毕得医药科技股份有限公司;4-甲基吡啶、苯并[cd]吲哚-2(1H)-酮、碘化钾(KI)、溴乙烷和咔唑,分析纯,上海笛柏生物科技有限公司;乙酸乙酯、甲醇、乙醇、二氯甲烷、石油醚、N,N-二甲基甲酰胺(DMF)、乙腈、四氢呋喃(THF)和三氯氧磷,分析纯,安徽泽升科技有限公司;盐酸、哌啶、氢氧化钾和无水硫酸钠,分析纯,国药集团化学试剂有限公司.
Bruker AVANCE NEO 400M 和AVANCE 600M 型核磁共振波谱仪(NMR),瑞士Bruker 公司;RF-5301PC型荧光分光光度计(FL),日本岛津公司;UV-1800PC型紫外-可见分光光度计(UV-VIS),中国菁华仪器有限公司;IVIS Spectrum小动物成像系统,美国PerkinElmer公司;Leica TCS SP5 LSM共聚焦显微镜,德国徕卡公司;Agilent Technologies LC/MSD TOF液相色谱-质谱联用仪,美国Agilent公司.
1.2 中间体及目标产物的合成
化合物6g~6j的合成路线如Scheme 1所示.

Scheme 1 Synthesis route of compound 6g—6j
1.2.1 1,2,3,3-四甲基-3H-吲哚-1-碘盐(1A)的合成 在氮气保护下,将1.59 g(10 mmol)2,3,3-三甲基-3H-吲哚、1.44 g(10.1 mmol)碘甲烷和50 mL MeCN混合,于80 ℃搅拌反应8 h.将所得混合物减压浓缩并用乙酸乙酯洗涤残余固体,干燥后得到2.77 g粉红色固体粉末,粗收率92%.产品未经进一步纯化,直接用于下一步反应.1H NMR(400 MHz,DMSO-d6),δ:7.94~7.88(m,1H),7.86~7.80(m,1H),7.66~7.58(m,2H),3.98(s,3H),2.78(s,3H),1.53(d,J=1.1 Hz,6H).
1.2.2 1,1,2,3-四甲基-1H-苯并[e]吲哚-3-碘盐(1B)的合成 以2.09 g(10 mmol)1,1,2-三甲基-1H-苯并[e]吲哚代替2,3,3-三甲基-3H-吲哚,采用合成化合物1A的方法合成化合物1B,得到3.16 g灰白色固体,产率90%.1H NMR(400 MHz,DMSO-d6),δ:8.36(d,J=8.4 Hz,1H),8.29(d,J=8.9 Hz,1H),8.22(d,J=8.2 Hz,1H),8.09(d,J=8.5 Hz,1H),7.79(dd,J=8.4,6.9 Hz,1H),7.73(t,J=7.5 Hz,1H),4.08(s,3H),2.86(s,3H),1.75(d,J=1.1 Hz,6H).
1.2.3 1,4-二甲基吡啶-1-碘盐(2A)的合成 以0.93 g(10 mmol)4-甲基吡啶代替2,3,3-三甲基-3H-吲哚,采用合成化合物1A 的方法合成化合物2A,得到2.12 g 黄色固体,产率90%.1H NMR(400 MHz,DMSO-d6),δ:8.86~8.79(m,2H),7.96(d,J=6.3 Hz,2H),4.28(s,3H),2.60(s,3H).
1.2.4 1,4-二甲基喹啉-1-碘盐(2B)的合成 以1.43 g(10 mmol)4-甲基喹啉代替2,3,3-三甲基-3H-吲哚,采用合成化合物1A 的方法合成化合物2B,得到2.54 g 黄色固体,产率89%.1H NMR(400 MHz,DMSO-d6),δ:9.35(d,J=6.1 Hz,1H),8.62~8.39(m,2H),8.34~8.19(m,1H),8.07(dd,J=14.2,6.8 Hz,2H),4.58(s,3H),3.01(s,3H,CH3).
1.2.5 甲基苯并[cd]吲哚-2(1H)-酮的合成 在氮气保护下,将5 g(29.6 mmol)苯并[cd]吲哚-2(1H)-酮与50 mL DMF 混合,在0 ℃及搅拌下加入2.8 g(118.3 mmol)NaH,搅拌反应30 min 后,加入8.4 g(59.2 mmol)碘甲烷并在室温下搅拌反应5 h.将混合物倒入冰水中淬灭反应,用1 mol/L的盐酸调节pH值至中性,用饱和食盐水洗涤并用乙酸乙酯多次萃取,然后用无水硫酸钠干燥,减压浓缩.残留物经硅胶色层析分离纯化,用乙酸乙酯/石油醚(体积比1∶20)展开剂冲洗,得到4.95 g 黄绿色固体,产率91%.1H NMR(400 MHz,DMSO-d6),δ:8.18(d,J=8.1 Hz,1H),8.05(d,J=7.0 Hz,1H),7.80(dd,J=8.1,7.0 Hz,1H),7.64(d,J=8.3 Hz,1H),7.55(dd,J=8.5,7.0 Hz,1H),7.15(d,J=7.0 Hz,1H),3.35(s,3H).
1.2.6 1,2-二甲基苯并[cd]吲哚-1-碘盐(3)的合成 在氮气保护下,将986 mg(5 mmol)甲基苯并[cd]吲哚-2(1H)-酮与10 mL THF 混合,加入2 mL 3 mol/L 甲基溴化镁的THF 溶液,将混合物于60 ℃搅拌1 h.向混合物中加入10 mL 2 mol/L 盐酸.减压干燥除去THF,加入5 mL 1 mol/L KI 溶液,得到红色沉淀.粗产物经过滤后,用水和乙酸乙酯洗涤,得到1.36 g 橙色固体化合物3,产率84%.1H NMR(400 MHz,DMSO-d6),δ:8.99(d,J=7.2 Hz,1H),8.81(d,J=7.9 Hz,1H),8.57~8.40(m,2H),8.18(t,J=7.6 Hz,1H),8.02(t,J=7.8 Hz,1H),4.22(s,3H),3.20(s,3H).
1.2.7 化合物4a,4b,5a,5b 的合成 参照文献[26]方法合成化合物4a,4b,5a 和5b,其中化合物4a(N-乙基咔唑)为已知化合物.
化合物4b:1H NMR(400 MHz,DMSO-d6),δ:8.18(dt,J=7.7,1.0 Hz,2H),7.63(dt,J=8.2,1.0 Hz,2H),7.43(ddd,J=8.3,7.1,1.2 Hz,2H),7.29~7.15(m,7H),5.67(s,2H).
化合物5a:1H NMR(400 MHz,DMSO-d6),δ:10.06(d,J=1.4 Hz,1H),8.76(d,J=1.6 Hz,1H),8.29(d,J=7.8 Hz,1H),8.00(dd,J=8.5,1.9 Hz,1H),7.78(d,J=8.5 Hz,1H),7.70(d,J=8.2 Hz,1H),7.54(t,J=7.7 Hz,1H),7.31(t,J=7.5 Hz,1H),4.51(q,J=7.1 Hz,2H),1.34(t,J=7.1 Hz,3H).
化合物5b:1H NMR(400 MHz,DMSO-d6),δ:10.07(s,1H),8.80(d,J=1.6 Hz,1H),8.33(dt,J=7.8,1.0 Hz,1H),7.99(dd,J=8.5,1.6 Hz,1H),7.84(d,J=8.6 Hz,1H),7.72(dt,J=8.3,0.9 Hz,1H),7.52(ddd,J=8.3,7.1,1.2 Hz,1H),7.37~7.15(m,6H),5.76(s,2H).
1.2.8 (E)-2-[2-(9-乙基-9H-咔唑-3-)乙烯基]-1,3,3-三甲基-3H-吲哚-1-碘盐(6a)的合成 将3 g(10 mmol)化合物1A,2.28 g(10.2 mmol)化合物5a与50 mL 乙醇混合,滴加3~4滴哌啶作催化剂,将混合物于80 ℃搅拌反应6 h.将混合物减压浓缩,抽滤,滤饼用少量乙醇洗涤,干燥后得到4.25 g红色固体粉末状化合物6a,收率84%.1H NMR(400 MHz,DMSO-d6),δ:9.11(d,J=1.7 Hz,1H),8.65(d,J=16.1 Hz,1H),8.38(dd,J=8.6,1.6 Hz,1H),8.28~8.23(m,1H),7.89~7.82(m,3H),7.77~7.70(m,2H),7.65~7.57(m,3H),7.41~7.34(m,1H),4.55(q,J=6.5 Hz,2H),4.16(s,3H),1.85(s,6H),1.41~1.35(m,3H).13C NMR(150 MHz,DMSO-d6),δ:181.62,155.62,143.67,143.43,142.42,140.88,129.34,129.11,127.48,126.27,123.63,123.27,122.86,121.04,115.03,110.69,109.76,52.17,44.24,38.02,34.57,26.30,22.68,22.07,14.33.HRMS-ESI(M+)calcd.for C27H27N2+,m/z:379.2169;found:379.2174.
1.2.9 (E)-2-[2-(9-苯基-9H-咔唑-3-)乙烯基]-1,3,3-三甲基-3H-吲哚-1-碘盐(6b)的合成 以2.91 g(10.2 mmol)化合物5b 代替化合物5a,采用合成化合物6a 的方法合成化合物6b,得到4.66 g 红色固体,产率82%.1H NMR(400 MHz,DMSO-d6),δ:9.12(d,J=2.6 Hz,1H),8.69~8.60(m,1H),8.40~8.32(m,1H),8.26(dd,J=8.1,2.7 Hz,1H),7.92~7.84(m,3H),7.77~7.69(m,2H),7.64~7.53(m,3H),7.31~7.19(m,6H),5.79(d,J=3.4 Hz,2H),4.23~4.06(m,3H),1.84(d,J=3.0 Hz,6H).13C NMR(150 MHz,DMSO-d6),δ:181.68,155.47,144.06,143.70,142.43,141.44,137.61,129.36,129.18,128.00,127.58,127.30,126.63,123.70,123.28,122.92,121.30,115.09,111.23,111.17,110.05,52.21,46.44,44.25,34.53,26.24,22.69,22.08.HRMS-ESI(M+)calcd.for C32H29N2+,m/z:441.2325;found:441.2332.
1.2.10 (E)-2-[2-(9-乙基-9H-咔唑-3-)乙烯基]-1,1,3-三甲基-1H-苯并[e]吲哚-3-碘盐(6c)的合成 以3.51 g(10 mmol)化合物1B代替化合物1A,采用合成化合物6a的方法合成化合物6c,得到4.45 g红色固体,产率80%.1H NMR(400 MHz,DMSO-d6),δ:9.38(d,J=1.1 Hz,1H),9.24(d,J=2.3 Hz,1H),8.71(d,J=16.3 Hz,1H),8.50~8.43(m,3H),8.13(d,J=9.0 Hz,1H),8.03~7.90(m,3H),7.87~7.79(m,2H),4.80~4.52(m,2H),4.32(s,3H),2.08(s,6H),1.06(t,J=7.0 Hz,3H).13C NMR(150 MHz,DMSO-d6),δ:192.34,182.42,154.49,143.53,140.87,140.01,137.82,133.42,131.22,130.51,128.74,127.24,126.31,123.51,122.88,121.34,120.60,110.07,60.23,53.82,44.26,37.86,35.15,26.06,22.69,22.06,14.18.HRMS-ESI(M+)calcd.for C31H29N2+,m/z:429.2325;found:429.2328.
1.2.11 (E)-2-[2-(9-苯基-9H-咔唑-3-)乙烯基]-1,1,3-三甲基-1H-苯并[e]吲哚-3-碘盐(6d)的合成 以3.51 g(10 mmol)化合物1B代替化合物1A,2.91 g(10.2 mmol)化合物5b代替化合物5a,采用合成化合物6a的方法合成化合物6d,得到4.82 g红色固体,产率78%.1H NMR(400 MHz,DMSO-d6),δ:8.87~8.79(m,3H),8.58(d,J=16.1 Hz,1H),8.35~8.26(m,4H),8.22(dd,J=7.8,1.1 Hz,1H),8.16(dd,J=8.6,1.7 Hz,1H),7.92(ddd,J=8.4,6.1,1.8 Hz,2H),7.75(d,J=8.7 Hz,1H),7.72~7.64(m,2H),7.52(ddd,J=8.3,7.0,1.2 Hz,5H),7.30~7.23(m,1H),4.51(q,J=7.1 Hz,2H),2.42(s,6H),1.36(q,J=6.9 Hz,3H).13C NMR(150 MHz,DMSO-d6),δ:192.35,182.47,154.35,143.96,141.45,137.66,137.64,129.18,127.30,127.20,121.25,120.90,110.84,110.56,65.38,56.51,53.87,44.28,35.12,26.01,22.72,19.04,15.64.HRMS-ESI(M+)calcd.for C36H31N2+,m/z:491.2481;found:491.2490.
1.2.12 (E)-4-[2-(9-乙基-9H-咔唑-3-)乙烯基]-1-甲基吡啶-1-碘盐(6e)的合成 以2.35 g(10 mmol)化合物2A代替化合物1A,采用合成化合物6a的方法合成化合物6e,得到3.78 g橙黄色固体,产率86%.1H NMR(400 MHz,DMSO-d6),δ:8.83~8.75(m,2H),8.58(d,J=1.7 Hz,1H),8.20(ddd,J=13.4,6.6,1.4 Hz,4H),7.94~7.87(m,1H),7.75(dd,J=8.6,1.2 Hz,1H),7.68(dd,J=8.0,1.3 Hz,1H),7.57~7.49(m,2H),7.33~7.25(m,1H),4.50(q,J=7.2 Hz,2H),4.24(d,J=1.3 Hz,3H),1.39~1.31(m,3H).13C NMR(150 MHz,DMSO-d6),δ:153.57,145.22,142.82,141.42,140.63,126.95,126.70,123.25,123.21,122.61,121.66,120.99,120.42,120.16,110.35,110.20,47.15,37.74,14.26.HRMS-ESI(M+)calcd.for C22H21N2+,m/z:313.1699;found:313.1702.
1.2.13 (E)-4-[2-(9-苯基-9H-咔唑-3-)乙烯基]-1-甲基吡啶-1-碘盐(6f)的合成 以2.35 g(10 mmol)化合物2A代替化合物1A,2.91 g(10.2 mmol)化合物5b代替化合物5a,采用合成化合物6a的方法合成化合物6f,得到4.40 g 红色固体,产率90%.1H NMR(400 MHz,DMSO-d6),δ:8.81(d,J=6.7 Hz,2H),8.62(d,J=1.6 Hz,1H),8.27~8.13(m,4H),7.88(dd,J=8.8,1.6 Hz,1H),7.79(d,J=8.7 Hz,1H),7.69(d,J=8.3 Hz,1H),7.57~7.47(m,2H),7.33~7.18(m,6H),5.73(s,2H),4.24(s,3H).13C NMR(150 MHz,DMSO-d6),δ:153.49,145.15,142.61,142.02,141.21,137.84,129.14,127.91,127.22,126.94,123.31,122.68,121.65,121.05,120.62,110.76,47.17,46.26.HRMSES(IM+)calcd.for C27H23N2+,m/z:375.1856;found:375.1860.
1.2.13 (E)-4-[2-(9-乙基-9H-咔唑-3-)乙烯基]-1-甲基喹啉-1-碘盐(6g)的合成 以2.85 g(10 mmol)化合物2B 代替化合物1A,采用合成化合物6a 的方法合成化合物6g,得到3.97 g 红色固体,产率81%.1H NMR(400 MHz,DMSO-d6),δ:9.28(d,J=6.6 Hz,1H),9.14(d,J=8.6 Hz,1H),8.88(s,1H),8.51(d,J=6.6 Hz,1H),8.48~8.35(m,3H),8.27(t,J=9.5 Hz,2H),8.14(d,J=8.6 Hz,1H),8.08(t,J=7.8 Hz,1H),7.78(d,J=8.6 Hz,1H),7.70(d,J=8.2 Hz,1H),7.55(t,J=7.7 Hz,1H),7.32(t,J=7.4 Hz,1H),4.52(s,5H),1.37(t,J=7.2 Hz,3H).13C NMR(150 MHz,DMSO-d6),δ:153.51,148.02,145.37,141.74,140.69,139.29,135.34,129.43,128.00,127.17,127.01,126.59,123.34,122.75,122.37,121.06,120.26,119.73,116.65,115.58,110.27,44.88,37.78,14.29.HRMS-ES(IM+)calcd.for C26H23N2+,m/z:363.1856;found:363.1862.
1.2.14 (E)-4-[2-(9-苯基-9H-咔唑-3-)乙烯基]-1-甲基喹啉-1-碘盐(6h)的合成 以2.85 g(10 mmol)化合物2B代替化合物1A,2.91 g(10.2 mmol)化合物5b代替化合物5a,采用合成化合物6a的方法合成化合物6h,得到4.80 g 红色固体,产率87%.1H NMR(400 MHz,DMSO-d6),δ:9.30(d,J=6.7 Hz,1H),9.14(d,J=7.8 Hz,1H),8.91(s,1H),8.52(d,J=6.6 Hz,1H),8.44~8.38(m,2H),8.29(d,J=7.9 Hz,2H),8.15~8.06(m,2H),7.84(d,J=8.6 Hz,1H),7.72(d,J=8.2 Hz,1H),7.51(d,J=7.7 Hz,1H),7.37~7.28(m,2H),7.23(d,J=7.1 Hz,2H),5.77(s,2H),4.54(s,3H),1.24(s,3H).13C NMR(150 MHz,DMSO-d6),δ:153.47,148.08,145.17,142.37,141.29,139.28,137.91,135.35,129.46,129.14,128.93,128.12,127.90,127.55,127.29,127.13,126.93,126.61,123.44,122.84,122.30,121.09,120.56,119.75,116.97,115.69,110.75,46.31,44.92.HRMSES(IM+)calcd.for C31H25N2+,m/z:425.2012;found:425.2019.
1.2.15 (E)-2-[2-(9-乙基-9H-咔唑-3-)乙烯基]-1-甲基苯并[cd]吲哚-1-碘盐(6i)的合成 以3.09 g(10 mmol)化合物3代替化合物1A,采用合成化合物6a的方法合成化合物6i,得到3.19 g蓝色固体,产率62%.1H NMR(400 MHz,DMSO-d6),δ:9.35~9.31(m,1H),9.19(d,J=1.1 Hz,1H),9.12~9.09(m,1H),9.06(s,1H),8.51(d,J=6.5 Hz,1H),8.47~8.39(m,4H),8.35(s,1H),8.32~8.25(m,1H),8.18~8.05(m,2H),7.92~7.86(m,2H),4.60(q,J=6.2 Hz,2H),4.55(s,3H),1.39(t,J=7.1 Hz,3H).13C NMR(150 MHz,DMSO-d6),δ:155.97,150.39,143.80,142.21,140.71,138.51,135.29,130.74,129.05,128.33,128.16,127.16,123.32,123.24,122.68,121.19,120.43,119.22,114.80,110.40,46.75,37.84,14.60,14.29.HRMS-ESI(M+)calcd.for C28H23N2+,m/z:387.1856;found:387.1860.
1.2.16 (E)-2-[2-(9-苯基-9H-咔唑-3-)乙烯基]-1-甲基苯并[cd]吲哚-1-碘盐(6j)的合成 以3.09 g(10 mmol)化合物3代替化合物1A,2.91 g(10.2 mmol)化合物5b代替化合物5a,采用合成化合物6a的方法合成化合物6j,得到3.34 g蓝色固体,产率58%.1H NMR(400 MHz,DMSO-d6),δ:9.04~8.98(m,1H),8.88(s,1H),8.67(d,J=9.2 Hz,1H),8.59~8.51(m,2H),8.38~8.33(m,1H),8.29(dd,J=7.7,0.9 Hz,1H),8.20~8.12(m,2H),7.97~7.91(m,1H),7.90~7.83(m,2H),7.73(d,J=8.2 Hz,1H),7.58~7.49(m,1H),7.38~7.16(m,6H),5.20(d,J=7.3 Hz,2H),4.57(s,3H).13C NMR(150 MHz,DMSO-d6),δ:155.91,150.06,146.08,143.95,142.76,141.26,138.47,137.73,135.79,135.39,131.10,130.75,129.51,129.16,128.33,128.17,127.97,127.26,126.83,125.98,123.42,123.19,122.72,121.27,120.75,119.14,115.10,110.80,47.64,46.83,46.32,22.74,14.53,13.84.HRMS-ESI(M+)calcd.for C33H25N2+,m/z:449.2012;found:449.2019.
1.3 性能表征
1.3.1 紫外和荧光光谱测定 在脱氧DMSO 中制备荧光探针6a~6g 的储备溶液(1.0 mmol/L).荧光探针(5,10,20 μmol/L)检测溶液由含1%(体积分数)DMSO 的水、乙腈和甲醇溶液配制,紫外吸收光谱用UV1800PC型分光光度计记录.然后以最大吸收波长的激光作为激发源,记录550~900 nm范围内的发射光谱.
1.3.2 荧光量子产率的测定 参考文献[27]方法获得荧光探针6a~6g在不同溶剂中的荧光量子产率,结果列于表1.
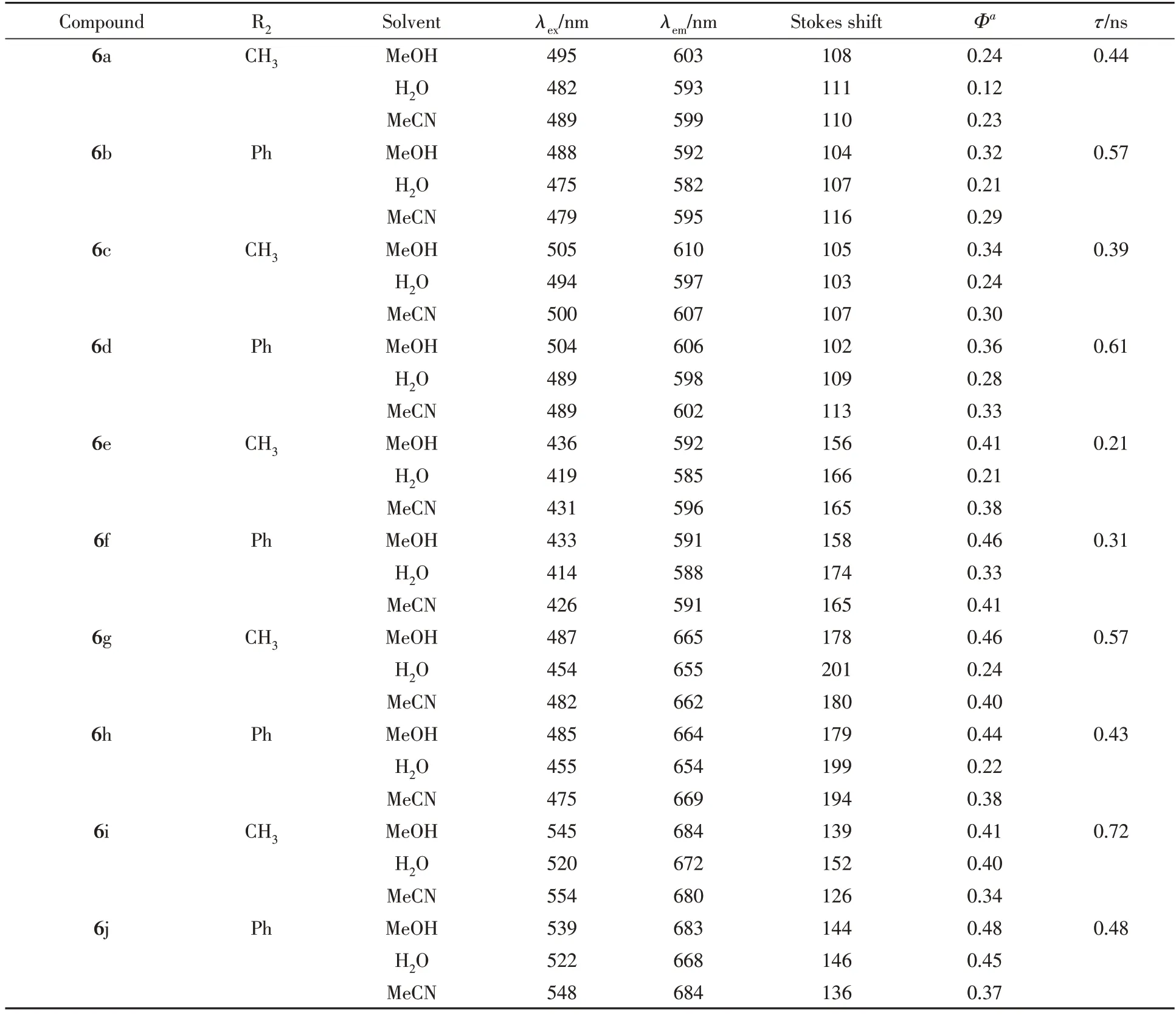
Table 1 Photophysical properties of carbazole derivatives in different solvents
1.3.3 荧光稳定性测试 光稳定性:将探针溶液以200 μL/孔的浓度加入96 孔不透明板中,采用NIR小动物成像系统成像.选择600~700 nm滤光片连续照射6 h,激光功率为3 W.生理条件稳定性:对照组将探针溶液加入等体积的PBS 缓冲液中;其余各组探针溶液分别添加20 μmol/L H2O2,GSH,Na+,K+,Cu2+,Fe2+,Zn2+,Vc,NQO1,NTR和H+;于37 ℃孵育60 min后,测定上述溶液的荧光光谱.
1.3.4 细胞毒性 采用HeLa 细胞系评估近红外荧光探针(6a~6j)的细胞毒性.首先,将细胞在37 ℃,5% CO2的96 孔板中培养24 h,然后去除培养基,将细胞暴露于不同浓度(1,10,100,1000,10000 和20000 nmol/L)的荧光探针中再培养24 h.随后,采用噻唑蓝比色法(MTT)评估HeLa细胞的细胞活力.
1.3.5 细胞共聚焦成像 通过共聚焦激光显微镜评估了化合物在HeLa细胞内的细胞器定位.将1×105HeLa细胞接种到35 mm玻璃底细胞培养皿中并孵育12 h,然后将所有细胞用PBS溶液洗涤2次,并在DMEM 培养基中与20 μmol/L 的荧光探针一起孵育4 h.然后,用PBS 溶液洗涤细胞并用Mito-tracker green 或Lyso-tracker green 染色1 h.荧光成像采用Leica TCS SP5 LSM 共聚焦显微镜成像,使用40×物镜;荧光探针激光激发:450~550 nm,滤光片组:600~700 nm.Mito Tracker Green,激光激发:490 nm激光,滤光片组:490~550 nm.Lyso-tracker green,激光激发:510 nm 激光,滤光片组:510~550 nm.
1.3.6 体内成像实验 BALB/c裸鼠(6~8周龄,18~20 g)购自南通大学实验动物中心.当肿瘤体积达到约500 mm3时进行实验.实验前将BALB/c 小鼠随机分组,将荧光探针6j(40 mg/kg)尾静脉注入荷瘤BALB/c裸鼠体内,在选定的时间点用含2.5%异氟烷的氧气麻醉小鼠,并使用IVIS Lumina成像系统捕获全身NIR荧光图像.最后,小鼠被安乐死,并立即收集它们的心、肝、脾、肺、肾、肠道和肿瘤组织器官,在IVIS Lumina系统上进行离体荧光成像.
2 结果与讨论
2.1 荧光探针的合成与结构表征
荧光探针分子6a~6g的结构和合成路线如Scheme 1所示.首先,发色团在乙腈和碘甲烷作用下季胺化,以较高产率获得季铵盐1A,1B,2A和2B.另外,以1,8-萘内酰亚胺为原料,通过在NaH和碘甲烷作用下发生N-甲基化反应,并与格氏试剂甲基溴化镁进一步反应获得发色团3,产率较高且无需纯化.接着咔唑9 位N 在氢氧化钾条件下与卤代烷烃发生烷基化反应,并在POCl3和DMF 作用下发生Vilsmeier-Haack反应,获得醛基咔唑衍生物5a和5b.最后,发色团3与咔唑醛基发生Knoevenagel缩合反应,以较高产率和纯度获得目标化合物.上述反应条件温和、后处理方便且不需要贵金属催化,有利于降低制备成本.所有产物在空气中都非常稳定,并通过核磁共振波谱和高分辨质谱进行了结构表征.
2.2 荧光探针的光谱特性
图1及表1示出了荧光探针的紫外-可见吸收光谱、荧光发射光谱、Stokes 位移以及荧光量子产率数据.该系列咔唑荧光探针的最大发射波长均>580 nm,其中发色团为1,4-二甲基喹啉-1-碘盐和1,2-二甲基苯并[cd]吲哚-1-碘盐的荧光探针6g~6j 最大发射波长均>650 nm(其中6i 的最大发射波长达到672 nm).值得注意的是,即使在水溶液中其最大发射波长也都达到近红外区.另外,荧光探针6g~6j的Stokes位移>100 nm,荧光量子产率也较高,优异的光学特性为体内外荧光成像提供了基础.不同溶剂对探针荧光量子产率及其最大吸收和发射波长的影响并不是特别显著,表明探针分子受溶剂影响较小.

Fig.1 Normalized absorbance and emission spectra of probes 6g—6j(A—D) in different solvents
2.3 荧光探针的稳定性
为了进一步探究荧光探针6g~6j的稳定性,进行了光稳定性实验.结果显示,荧光探针6g~6j在长达6 h的光照下仍能够保持较强的荧光强度(图2).另外,生命体拥有复杂的生理环境,实验中考察了各种生理环境中的物种对探针荧光的影响.结果表明,绝大多数的生理物种对探针的荧光没有显著影响,但是酸性环境能够提高探针的荧光强度,可能是季铵盐基团在不同酸碱环境中使探针光学特性发生变化所致.
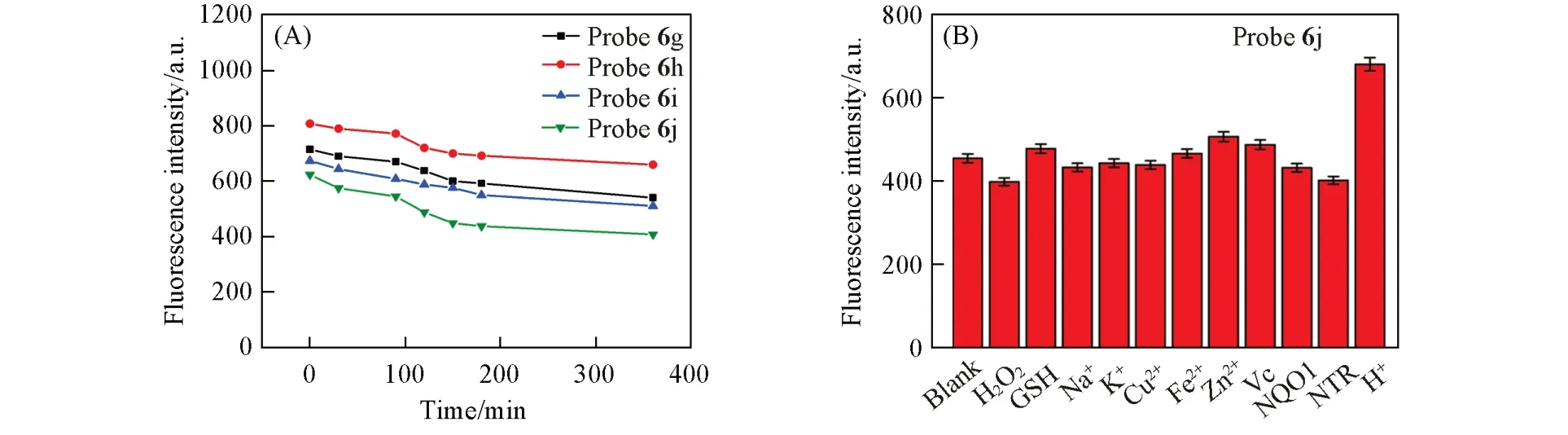
Fig.2 Optical and physiological stability of different probes
2.4 探针的细胞毒性及细胞摄取能力
采用噻唑蓝比色法(MTT)评估了探针6a~6j 的细胞毒性.结果表明,探针细胞毒作用较弱(IC50>20 μmol/L)(图3),可见荧光探针安全性高.用正常人卵巢上皮细胞(IOSE-80)和人宫颈癌细胞(HeLa)对探针的摄取能力进行了分析.实验结果表明,用探针6j 处理两种细胞后,随着孵育时间的变化,可以观察到探针的红色通道荧光增强,表现出时间依赖性变化.其中,HeLa 细胞对探针6j 的摄取速率明显高于正常细胞,且在6 h后比正常细胞的荧光值提高了约3倍(图4).

Fig.3 Cytotoxicity of probes

Fig.4 Normal and HeLa cell uptake capacity in vitro
2.5 荧光探针对线粒体的靶向能力
研究表明,线粒体代谢与肿瘤发生、发展密切相关,从而使线粒体成为癌症治疗的有前途的新靶点[28].目前,带正电荷的三苯基膦(TPP)在线粒体靶向癌症治疗中占据优势[29~31],这归因于超极化的肿瘤细胞膜和线粒体膜可能允许选择性地积累线粒体靶向药物[28].因此,基于肿瘤细胞的线粒体膜电位高于正常细胞,使用离域亲脂性阳离子作为载体的线粒体靶向策略是提高小分子抗肿瘤作用的优势策略.设计之初,我们选择芳香亲脂性阳离子片段作为发色团,并与亲脂性咔唑母核连接来达到线粒体靶向作用.荧光共聚焦实验结果表明,荧光探针和商用Mito-Tracker Green(线粒体探针)、Lyso-Tracker Green(溶酶体探针)一起孵育(图5).探针6g~6j 均与Mito-Tracker Green 的荧光信号显著重叠,Pearson相关系数(PCC)均>0.8,其中探针6j线粒体定位最佳,推测是咔唑N-9位引入的芳香环进一步增加了探针的脂溶性,使其更容易在线粒体蓄积.然而,探针与其他细胞器没有定位作用,如溶酶体,其Pearson相关系数(PCC)较低.以上结果表明,该类探针在线粒体中选择性积累,有可能成为准确诊断肿瘤的潜在策略.另外,线粒体膜电位是监测细胞健康状态的重要生理参数.由于该类探针在线粒体中选择性积累,因此将其用于精确监测线粒体膜电位变化(Δψm).使用降低线粒体膜电位的化学氧化磷酸化抑制剂-间氯苯基腙(CCCP)处理后进行线粒体损伤示踪,结果显示,CCCP处理后探针的荧光明显降低,与商用Mito-Tracker Green 结果保持一致且荧光变化更为显著(图6),表明该类探针还可用于监测线粒体膜电位变化(Δψm).

Fig.5 Colocalization assay of probe and commercial reagents
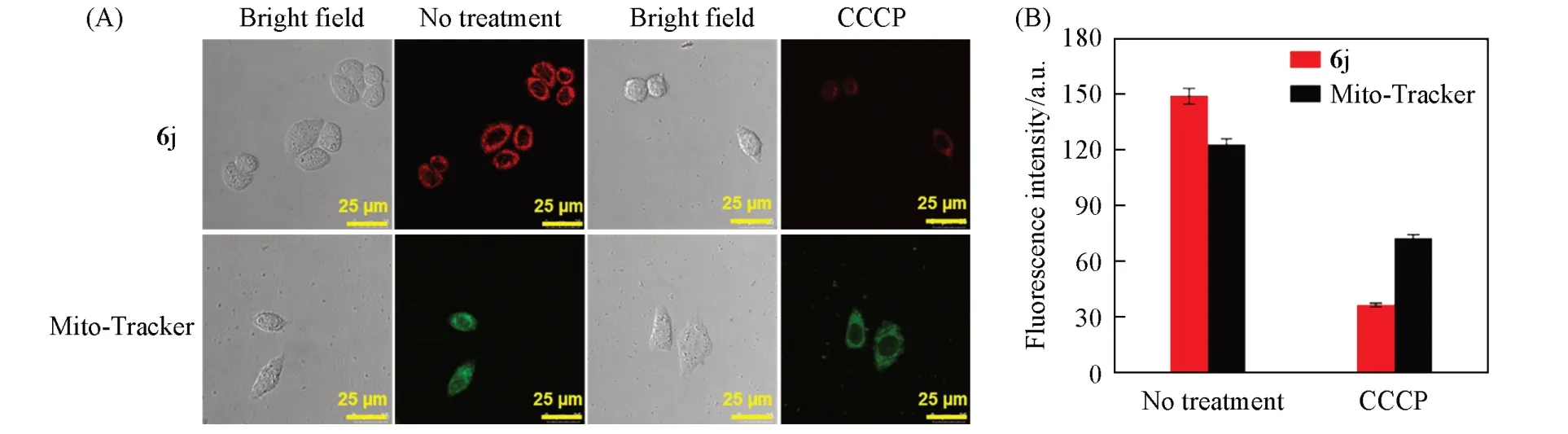
Fig.6 Performance of probe 6j in mitochondrial membrane potential
2.6 荧光探针体内成像
由于探针6j优异的光物理特性及对线粒体的高靶向能力,因此将其应用到小鼠体内荧光成像.所有小鼠均静脉注射探针6j,荷瘤小鼠肿瘤部位的荧光强度随时间逐渐增强.如图7所示,荷瘤小鼠在注射8 h后表现出强烈的荧光,并保持在高强度水平至少12 h.此外,还收集了小鼠其它主要器官(心脏、肝脏、肺、脾脏、肾脏和肿瘤).除肿瘤部位外,其它器官无明显的荧光信号.上述结果表明,荧光探针在体内主要分布在肿瘤部位,探针6j可作为肿瘤诊断探针,该探针通过实时监测线粒体的变化来诊断肿瘤疾病.

Fig.7 Real-time in vivo fluorescence imaging of mice and isolated major organs
3 结论
以咔唑为母核,与不同的亲脂性阳离子通过条件温和、处理方便的方法合成了一系列线粒体靶向的近红外荧光探针6g~6j.性能测试结果表明,该类探针具有近红外发射、大Stokes位移和高荧光量子产率.细胞实验结果表明,该类探针不仅可以进入活细胞,而且对细胞线粒体靶向性良好,荧光成像能力显著.小鼠体外成像结果显示,探针6j在体内能够分布在肿瘤组织并能进行荧光成像,为临床上肿瘤的精准诊断提供新的策略.
