子宫内膜增生症病史对不孕症患者IVF/ICSI-ET助孕结局的影响
2023-11-01王晓飞张美微邵小光王磊
王晓飞,张美微,邵小光,王磊
(大连市妇女儿童医疗中心(集团)生殖与遗传医学中心,辽宁 大连 116000)
子宫内膜增生症是指子宫内膜长期受到雌激素的刺激而缺少孕激素拮抗,呈持续增生的一种疾病。其病理分类分为子宫内膜增生不伴不典型增生 (endometrial hyperplasia without atypia,EH) 和子宫内膜不典型增生 (endometrial atypical hyperplasia,AH)。近年来其发生率明显升高,最新一项研究[1]显示,在接受体外受精/卵胞质内单精子注射-胚胎移植 (in vitrofertilization/intracytoplasmic sperm injection and embryo transfer,IVF/ICSI-ET) 助孕的不孕症患者中,子宫内膜增生症的发生率可达3%。近年来,越来越多的不孕症患者在辅助生殖助孕过程中被诊断为子宫内膜增生症。2017年《中国子宫内膜增生诊疗共识》 [2]规范了子宫内膜增生症的诊治,并建议对有生育要求的患者经孕激素治疗逆转内膜后应积极助孕。2022年8月新发布的《中国内膜增生管理指南》[4]提出,AH的内膜逆转后,助孕方式推荐辅助生殖技术[3-4]。既往研究[6]显示,AH及早期子宫内膜癌患者治疗达到完全缓解后,会因各种不利因素导致妊娠率较低。但关于子宫内膜增生症患者在孕激素治疗后IVF/ICSI-ET助孕的妊娠结局的相关研究较少。本研究拟分析有EH或AH病史的不孕症患者经孕激素治疗达完全逆转后行IVF/ICSI-ET助孕的临床结局,并探讨不同病理类型对子宫内膜厚度及妊娠结局的影响。
1 材料与方法
1.1 研究对象
采用回顾性队列研究,分析2017年1月至2020年12月于大连市妇女儿童医疗中心 (集团) 行IVF/ICSI助孕患者的临床资料。将患者分为2组,研究组为既往有子宫内膜增生症病史且经孕激素治愈的患者,对照组为同期单纯因输卵管因素接受IVF/ICSI助孕的患者,按照年龄与研究组进行匹配。随访终点为获得活产或使用完所有可利用胚胎。
子宫内膜增生症诊断标准:经宫腔镜或诊断性刮宫获取子宫内膜,病理学检查结果提示为EH/AH。EH指子宫内膜过度增生,超出正常子宫内膜增殖期晚期的范畴,可为弥漫性或局限性。AH指子宫内膜腺体的增生明显超过间质,具有相同或相似于高分化子宫内膜样癌的细胞学特征,但缺乏明确的间质浸润[3]。治愈标准:经口服孕激素或宫内放置曼月乐环规范治疗,复查宫腔镜活检或分段诊刮达到病理完全缓解。
纳入标准:年龄<42岁;IVF/ICSI助孕后进行过胚胎移植;临床资料及随访资料完整;包括新鲜及解冻移植周期。排除标准:夫妻双方任何一方染色体异常者;复发性流产者;子宫异常患者,包括子宫畸形、子宫腺肌病、宫腔黏连;男方因素不孕者。本研究已获得大连市妇女儿童医疗中心(集团)伦理委员会批准。所有患者知情同意。
1.2 周期方案
按照本中心诊疗常规进行控制性超促排卵,当≥2~3个主导卵泡直径≥18 mm时,给予注射用人绒毛膜促性腺激素 (human chorionic gonadotropin,hCG,宁波人健药业集团股份有限公司) 10 000 U扳机,扳机后36 h采卵。根据病史及男方精液情况,给予IVF/ICSI助孕。移植方案:取卵后第3天或第5天对胚胎行玻璃化冷冻或新鲜周期移植。解冻移植方案:采用自然周期、激素替代周期或降调节-激素替代周期准备内膜。排卵正常者采用自然周期解冻移植。黄体支持方案:地屈孕酮 (达芙通,雅培贸易上海有限公司) 10 mg,2次/d口服;黄体酮注射液 (广州白云山医药集团股份有限公司) 40 mg,1次/d肌注。于使用孕激素的第3天解冻卵裂期胚胎,第4天移植。如为囊胚,于第5天解冻并移植。
1.3 观察指标
优质胚胎评分标准:采卵后第3天胚胎细胞数≥6个,细胞碎片率≤10%;囊胚采用Gardner评分,4BB及以上级别为优质胚胎。优胚移植率 (%) =移植优质胚胎数/移植胚胎数×100;着床率=孕囊数/总移植胚胎数×100;临床妊娠率 (%) =临床妊娠周期数/移植周期数×100;晚期流产率 (%) =孕28~36周晚期流产周期数/临床妊娠周期数×100;活产率 (%) =活产周期数/移植周期数×100。
1.4 统计学分析
采用SPSS 25.0软件进行统计分析。计量资料2组间比较时,符合正态分布者采用两独立样本t检验,不符合正态分布者采用秩和检验;多组间比较时,符合正态分布者采用单因素方差分析,不符合正态分布者采用非参数检验。计数资料用率 (%) 表示,组间比较采用χ2检验。P< 0.05 (双侧) 为差异有统计学意义。
2 结果
2.1 基线数据分析
研究组共纳入85例,其中EH 50例,AH 35例。对照组纳入145例。一般资料比较,2组年龄、激素水平、多囊卵巢综合征 (polycystic ovarian syndrome,PCOS) 患者所占比例、每周期移植优质胚胎数,差异均无统计学意义 (P> 0.05)。研究组体质量指数(body mass index,BMI) 显著高于对照组 (P< 0.01),原发不孕比例显著高于对照组 (P= 0.002),不孕时间显著长于对照组 (P= 0.001)。见表1。将2组基础数据单因素分析中存在显著差异的因素进行二元logistic回归分析,结果显示,BMI是子宫内膜增生症的危险因素 (OR=1.295,95%CI:1.139~1.473)。见表2。
表1 2组患者一般临床资料比较 Tab.1 Comparison of general clinical characteristics between the two groups

表1 2组患者一般临床资料比较 Tab.1 Comparison of general clinical characteristics between the two groups
BMI,body mass index;E2,estradiol;FSH,follicle-stimulating hormone;AMH,anti-Müllerian hormone;PCOS,polycystic ovarian syndrome.
ItemControl group (n = 145) Endometrial hyperplasia group (n = 85)Z/t/χ2P Age (year) 32.29±3.4933.02±3.87-1.4210.155 BMI (kg/m2) 23.00±3.5026.59±3.86-5.341<0.001 Infertility duration (year) 3.85±3.03 4.89±2.76-3.3150.001 Rate of primary infertility (%) 57.977.69.1830.002 Basal E2 (pg/mL) 44.46±37.1444.90±36.29-0.7070.480 Basal FSH (IU/L) 6.91±2.12 6.13±1.991.8950.059 Basal AMH (ng/mL) 3.63±2.91 2.75±3.59-1.9220.055 Rate of PCOS (%) 29.734.10.4960.481

表2 内膜增生症危险因素logistics回归分析Tab.2 Logistics regression analysis of risk factors for endometrial hyperplasia
进一步将研究组分为EH和AH亚组再进行比较,发现2组年龄、BMI、不孕时间、原发不孕率、周期移植胚胎数及优质胚胎数比较,差异均无统计学意义 (均P> 0.05)。但AH组患者的子宫内膜厚度低于EH组,差异有统计学意义 (P= 0.031)。见表3。
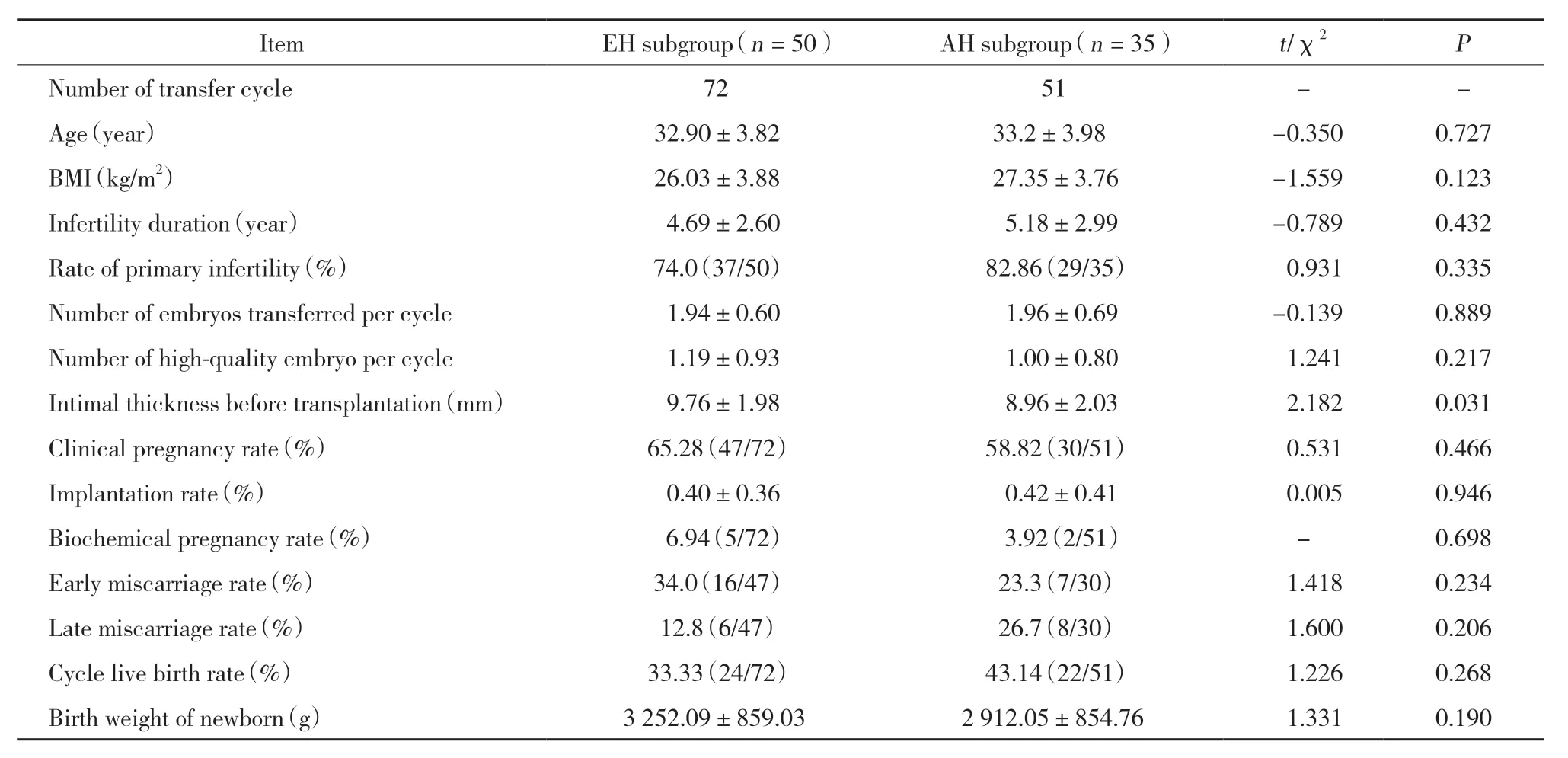
表3 AH组与EH组一般情况及妊娠结局比较Tab.3 Comparison of gerneral clinical characteristics and pregnancy outcomes between AH and EH groups
2.2 临床助孕结局比较
因研究组与对照组BMI存在显著差异,进一步将2组按BMI分层比较妊娠结局,即按BMI分为正常体质量 (BMI 18.5~<24.0 kg/m2)、超重 (BMI 24.0~28.0 kg/m2)、肥胖 (BMI>28.0 kg/m2)。每个分层中2组间移植的优质胚胎数比较,差异无统计学意义 (均P> 0.05)。在超重组及肥胖组的人群中有子宫内膜增生症病史患者的内膜厚度显著低于对照组 (P=0.034,P= 0.017)。但各层患者中2组间临床妊娠率、生化流产率、早期流产率、晚期流产率及移植周期活产率、新生儿出生体质量比较,差异均无统计学意义 (均P> 0.05)。见表4。
进一步将研究组分为EH亚组和AH亚组,比较2个亚组的临床妊娠率、生化流产率、早期流产率、晚期流产率、每周期活产率及新生儿出生体质量,均无统计学差异 (P> 0.05)。见表3。
3 讨论
子宫内膜增生症是妇科常见疾病,其中,EH未来进展为子宫内膜癌的风险为1%~3%,AH患者合并子宫内膜癌风险高达19%~45%[7]。不孕症患者通常在进行不孕诊疗的过程中发现子宫内膜增生症,因此在该人群中的检出率高于正常人群。1项对接受IVF/ICSI 治疗的不孕症患者的横断面研究[8]显示,该人群子宫内膜增生症的发生率约为3%。子宫内膜增生症的危险因素包括不孕、排卵障碍、异常子宫出血、肥胖、空腹血糖升高等[2]。本研究显示,在IVF/ICSI助孕的患者中,BMI是子宫内膜增生症的独立危险因素。研究[8]显示,PCOS也是EH的一个危险因素。本研究发现,子宫内膜增生症患者中PCOS所占比例高达34.1%,与既往研究结果一致。
本研究中,子宫内膜增生症患者原发不孕的比例更高,不孕时间更长。其原因与该类患者具备的不孕相关因素偏多有关,如长期无排卵或稀发排卵、内膜异常,不利于胚胎着床。INOUE等[9]研究认为,子宫内膜增生症药物治疗后妊娠结局的影响因素包括妊娠年龄、内膜病变是否复发、排卵期子宫内膜厚度。meta分析研究[10]显示,BMI对IVF助孕患者的妊娠结局有负面影响,活产率降低,如肥胖患者合并PCOS时,预后较差。本研究中,研究组与对照组PCOS患者所占比例无明显差异,可排除该项因素对研究结果的影响。因2组间BMI差异显著,故按照BMI进行分层,以排除该混杂因素的影响。在不同BMI分层的患者中,研究组与对照组妊娠结局无差异。范亚珍等[11]用倾向匹配评分法比较了78例子宫内膜增生症患者的IVF助孕结局,发现不孕症合并子宫内膜增生症患者经药物治疗后,不影响IVF-ET助孕的累积临床妊娠率、累积活产率及新生儿体质量,结论与本研究相似。
本研究发现,在超重及肥胖人群中,子宫内膜增生症患者子宫内膜厚度薄于对照组,且AH患者子宫内膜厚度薄于EH患者。子宫内膜增生症的治疗多采用口服醋酸甲羟孕酮 (medroxyprogesterone acetate,MPA)。虽然MPA可引起子宫内膜的组织学变化[12],包括腺体与基质的比率降低、腺体细胞数量减少、基质蜕膜化和有丝分裂减少,可能导致子宫内膜萎缩和变薄。MPA 治疗停止后组织功能恢复可能需要相当长的时间。超重是子宫内膜增生症及内膜癌经孕激素治疗后复发的危险因素。因此合并较高的BMI及AH的患者,口服孕激素治疗时间、剂量以及宫腔镜检查的次数都会增加,也是影响其子宫内膜厚度的不利因素。虽然子宫内膜厚度存在组间差异,但最终的妊娠结局未受显著影响。SHAKERIAN等[13]对560个移植周期的研究也显示,无论是新鲜周期还是解冻周期移植,根据子宫内膜厚度无法预计活产率。但由于本研究样本数量较少,无法明确子宫内膜增生症患者子宫内膜厚度与活产率的相关性。
本研究显示,不同病理类型对IVF/ICSI助孕妊娠结局无明显影响。有研究[14]回顾性分析了64例子宫内膜复杂性增生患者治疗后的IVF助孕结局,发现无论是否合并AH,其生育结局无差异。
对于有生育需求的子宫内膜增生症患者,在大剂量孕激素治疗前应尽量明确不孕的病因,制定好助孕方案,以便在完成治疗后,即至少1次子宫内膜病理结果提示为阴性,可立即开始助孕。保留生育能力的子宫内膜增生症及早期内膜癌的患者治疗后进行IVF 治疗不会增加复发的风险[15]。子宫内膜增生症治愈后的患者IVF助孕时的卵巢刺激方案包括常规的短方案、拮抗剂方案、微刺激方案和孕激素促排卵 (progestin-primed ovarian stimulation,PPOS)方案等。目前没有关于不同促排卵方案的有效性及复发风险的报告。CHEN 等[16]比较了PPOS、拮抗剂、微刺激3种方案,发现PPOS方案组的优质胚胎率更高;诱导排卵的年龄和子宫内膜病变的治疗时间是子宫内膜疾病复发的2个稳定预测因子。建议促排卵治疗期间可以联合使用芳香化酶抑制剂,以降低促排卵期间血清的雌激素水平[17]。目前认为胚胎移植的策略可借鉴子宫内膜癌治疗后胚胎移植的经验,建议在控制性促排卵周期争取进行新鲜胚胎移植,以争取尽早妊娠。对需要行冷冻胚胎移植患者最好采用自然周期进行内膜准备。合并子宫内膜异位症、子宫腺肌症的患者推荐使用GnRha后小剂量雌激素人工周期方案[18]。
综上所述,既往有子宫内膜增生症的不孕症患者,虽然其不孕时间长,原发不孕比例高,经孕激素治疗后行IVF助孕的整体妊娠结局并未受到明显影响。不同病理类型及BMI影响胚胎移植前的子宫内膜厚度,但并不影响其移植周期活产率。因此,IVF/ICSI助孕可帮助经孕激素治疗后的子宫内膜增生症患者获得较好的妊娠结局。
