CO2对Fe2O3催化剂NH3-SCR脱硝性能影响
2023-10-12乔玉洁,龚蕾,董世城,王辉
乔 玉 洁, 龚 蕾, 董 世 城, 王 辉
(大连理工大学 环境学院,辽宁 大连 116024 )
0 引 言
固定源(工厂、电厂等)和移动源(汽车、飞机、船舶等)排放尾气中的氮氧化物(NOx)不仅对人体、植物具有直接毒性,而且在一定程度上会对环境造成污染和破坏.目前,国内外应用最广泛的NOx脱除技术是选择性催化还原(selective catalytic reduction,SCR)技术,还原剂多采用NH3.在实际运行过程中,烟气/尾气中的气体组成较为复杂,不仅含有NOx,同时还会存在SO2、CO2、H2O、碱金属、碱土金属、重金属等可能会使催化剂失活的成分[1-3].在这些可能会使催化剂失活的成分中,对CO2的研究较少,但CO2已成为烟气/尾气中的重要组分,体积分数为5%~13%[1,4].所以,研究CO2对烟气/尾气脱硝性能的影响是非常必要的.
目前CO2对NH3-SCR反应的影响研究尚未达成共识.Zhang等发现CO2的加入增加了催化剂的表面酸度,催化剂对NH3的吸附能力增强,进而提高了催化剂的NH3-SCR性能[5].但也有研究指出CO2的存在抑制了NH3-SCR反应.Kim等发现在反应气氛中引入CO2后,Cu-SSZ-13催化剂的NH3-SCR性能发生了变化.由于CO2和NO在活性位点Cu2+存在竞争吸附,单齿碳酸盐物种覆盖了活性位点,NO在催化剂表面的吸附活化被抑制,参与NH3-SCR反应的关键物种——硝酸盐物种——变少,从而使得NOx转化率降低[1].Wang等在FeCe复合氧化物催化剂上也得到了CO2对SCR反应活性产生抑制的结果,说明CO2的加入影响了催化剂表面对NH3或NOx的吸附活化行为[6].基于此,CO2对NH3-SCR反应的影响研究是非常及时且重要的.
Fe2O3基催化剂因价格低廉、材料来源广泛、绿色环保、氧化还原能力优异而成为NH3-SCR领域的研究热点.本文以Fe2O3为对象,研究CO2对其脱硝性能的影响,并运用一系列原位手段从NH3及NOx的吸附行为变化来探究脱硝性能变化的原因,同时确定CO2加入后的反应机理.考虑到实际应用中CO2占比以及目前CO2相关研究中多采用较低浓度[5-6],本文选用5% CO2来进行相关研究.
1 材料与方法
1.1 实验试剂及气体
本实验催化剂制备所用的实验试剂均为分析纯,来自国药集团化学试剂有限公司.主要使用的实验试剂有九水硝酸铁(Fe(NO3)3·9H2O)和尿素(CO(NH2)2).所有溶液均由去离子水配制而成.
本实验所用气体均来自大连浚枫气体化学品有限公司,包括1% NH3/He,标准气;1% NO/He,标准气;纯CO2,≥99.999%;30% O2/He,标准气;纯He,≥99.999%;纯Ar,≥99.999%.
1.2 催化剂的制备
本研究采用尿素法制备Fe2O3催化剂.首先,将尿素在室温下搅拌溶解于250 mL去离子水,向其中加入九水硝酸铁并在室温下搅拌12 h,将得到的悬浊液置于油浴锅中在90 ℃搅拌24 h.然后,将溶液静置至室温,去掉上清液并进行离心、干燥操作.最后,将干燥好的样品用研钵磨成粉末,并将其以5 ℃/min的升温速率由室温升至500 ℃焙烧5 h.
1.3 催化剂的活性测试
催化剂的NH3-SCR活性测试在固定床石英反应器中于常压下进行,反应温度设定在150~475 ℃,气体流量控制在300 mL/min,体积空速为50 000 h-1,进料气组成(体积分数)为500×10-6NO、500×10-6NH3、3% O2、5%/10%/15% CO2(使用时)以及平衡气体He.整个过程中的反应气及反应后尾气中的NO和NO2气体体积分数由42i HL NO-NO2-NOx分析仪(Thermo Scientific)检测得到,进料气及反应后尾气中的NH3体积分数则由JFQ-1150E型NH3气体分析仪(北京均方)检测.NOx转化率按如下公式计算:
C(NOx)=((φ(NO)in+φ(NO2)in)-
(φ(NO)out+φ(NO2)out))/
(φ(NO)in+φ(NO2)in)×100%
其中φ(NO)in、φ(NO2)in分别代表NO和NO2的进气体积分数;φ(NO)out、φ(NO2)out分别代表NO和NO2的出气体积分数.
1.4 催化剂的表征
1.4.1 X射线衍射测试 X射线衍射技术是用来研究催化剂晶相结构的有力工具.所有样品的数据结果均是在德国布鲁克公司生产的D8 Advance型布鲁克X射线衍射仪上测试得到的,测试扫描角度范围为20°~80°.
1.4.2 程序升温脱附实验 氨气程序升温脱附实验(NH3-TPD)、氮氧化物程序升温脱附实验(NOx-TPD)和二氧化碳程序升温脱附实验(CO2-TPD)均在与OmniStar 320型质谱分析仪耦合的固定床石英反应器上进行.实验前,将0.1 g催化剂在He气氛(50 mL/min)条件下于300 ℃预处理1 h,然后冷却至室温.之后将预处理样品暴露于1% NH3/He或1% NO/He+3% O2/He或5% CO2/He+3% O2/He或1% NH3/He+5% CO2/He+3% O2/He或1% NO/He+5% CO2/He+3% O2/He这几种气体气氛(总流量为30 mL/min)条件下进行吸附实验直到达到吸附饱和.待质谱信号稳定,在He气氛中以10 ℃/min的升温速率从室温升到700 ℃.
1.5 原位漫反射傅里叶变换红外光谱研究
原位漫反射傅里叶变换红外光谱(in situ DRIFTS)是在FTIR光谱仪(布鲁克VERTEX 70)上测得的.实验前,将样品在He气氛中400 ℃预处理1 h以去除杂质,然后冷却至200 ℃.将预处理的催化剂暴露于不同气氛(100 mL/min)条件下得到对应谱图.气体组成如下:500×10-6NH3/He、500×10-6NO/He(使用时)、3% O2/He(使用时)、5% CO2/He(使用时).
2 结果与讨论
2.1 CO2对催化剂NH3-SCR脱硝性能和结构性质的影响
对Fe2O3催化剂进行了有无CO2条件下的NH3-SCR活性测试,所得活性曲线如图1所示.当引入5% CO2后,Fe2O3催化剂的NH3-SCR活性在整个温度区间内都存在不同程度的下降,这说明CO2抑制了Fe2O3催化剂的脱硝性能.同时可以看到CO2对NH3-SCR反应的抑制程度随温度发生变化.在温度低于300 ℃时,CO2的抑制作用较强,催化剂的NOx转化率降低了约20%;随着温度的升高,这种抑制作用开始减弱,催化剂在300~475 ℃这个温度区间内NOx转化率最多只降低了8%,对该现象在后续的研究中会进行进一步的解释说明.此外,以300 ℃为界,选取了250、350 ℃两个温度点来研究CO2体积分数对催化剂NH3-SCR活性的影响,结果如图2所示.随着CO2体积分数的提高,在两个温度点催化剂的活性都呈现降低趋势;但高温段(350 ℃)的降低趋势要明显低于低温段(250 ℃),即在不同CO2体积分数下,高温段CO2对活性的抑制作用仍显著弱于低温段.

图1 NH3-SCR活性曲线

图2 不同CO2体积分数的NH3-SCR活性柱状图
为了探究CO2是否会对Fe2O3催化剂结构造成影响,对未反应的Fe2O3催化剂以及引入5% CO2反应后的Fe2O3催化剂进行了XRD表征,结果如图3所示.由谱图可知,加入CO2后Fe2O3催化剂的XRD衍射峰峰强明显增强且没有新的衍射峰出现,衍射峰峰强增强说明CO2加入后,Fe2O3催化剂的粒子发生了聚集,催化剂结晶度提高;但同时没有新的衍射峰出现,说明CO2的加入并未对催化剂晶相结构造成影响.

图3 Fe2O3催化剂的XRD谱图
2.2 催化剂表面CO2相关吸附物种的确定
为了探究CO2存在时催化剂NH3-SCR活性下降的原因,运用原位DRIFTS技术和CO2-TPD实验来确定CO2在催化剂表面的存在状态.
图4(a)、(b)分别展示了200 ℃时CO2吸附的原位DRIFTS谱图和CO2-TPD谱图.由图4(a)可知,催化剂表面出现5个吸收峰,分别位于1 569、1 454、1 425、1 373、1 352 cm-1.这5个吸收峰可归属为3类碳酸盐物种:第一类是双齿碳酸盐物种,位于1 569 cm-1[7-9];第二类是位于1 454和1 425 cm-1处的多齿碳酸盐物种[7,10];第三类是由于吸收峰部分重叠在谱图中呈现双峰效果的1 373和1 352 cm-1的单齿碳酸盐物种[8-10].这3类碳酸盐物种在He吹扫后仍存在于催化剂表面,说明CO2加入后能够在催化剂表面形成稳定的碳酸盐物种.由图4(b)可知,催化剂表面出现了一个宽的脱附峰,温度范围在300~550 ℃.查阅文献发现,在该温度范围内可以出现的碳酸盐物种多为单齿碳酸盐、双齿碳酸盐和多齿碳酸盐[7,11],与原位DRIFTS谱图结果一致.此外,CO2相关吸附物种的脱附峰在高于300 ℃时出现,这说明CO2相关吸附物种的热稳定性在300 ℃开始变差,且随着温度的不断升高,CO2相关吸附物种在催化剂表面越难形成.因此,在活性实验中,当温度高于300 ℃时,CO2对催化剂NOx转化率的抑制作用开始减弱.

(a) 200 ℃时CO2吸附的原位DRIFTS谱图
2.3 催化剂上CO2和NH3/NOx之间的关系
在NH3-SCR反应中,通过催化剂表面NH3和NOx的吸附行为可以判定反应遵循的路径.CO2加入后在催化剂表面形成的稳定碳酸盐物种可能会影响NH3或NOx的吸附活化过程.基于此,运用原位DRIFTS和TPD实验进行了有无CO2条件下的NH3及NOx吸附实验.
2.3.1 CO2对NOx吸附行为的影响 图5(a)、(b)分别展示了有无CO2条件下200 ℃时NOx吸附的原位DRIFTS谱图和NOx-TPD谱图.在200 ℃下,将500×10-6NO+3% O2/He通入Fe2O3催化剂30 min后,催化剂表面出现了5个吸收峰.1 600 cm-1的吸收峰可归属于气态或弱吸附的NO2物种[12-14];1 560 cm-1的吸收峰峰强最强,归属于双齿硝酸盐物种[15-17];同时还观察到单齿硝酸盐物种(1 378、1 355 cm-1)和桥接/螯合亚硝酸盐物种(1 238 cm-1)[15,18-20].在He吹扫30 min后,NOx吸收峰仍然存在于催化剂表面,且峰强轻微减弱,说明Fe2O3催化剂对NOx物种的吸附能力较强.在CO2存在的条件下,催化剂表面出现了与没有CO2引入时相同位置的吸收峰,考虑到在1 569、1 373和1 352 cm-1出现的碳酸盐物种的吸收峰,1 560、1 378和1 355 cm-1的吸收峰可以归属于碳酸盐物种和硝酸盐物种的重叠峰;而其他位置的峰归属保持不变.同时发现NO2吸附物种的吸收峰峰强降低.基于以上结果可知,CO2加入后催化剂表面吸附的硝酸盐物种种类未发生变化,但对应的各物种的吸附量变少,尤其是NO2物种和主要的硝酸盐吸附物种.这说明CO2的存在对催化剂表面NOx的吸附有一定的抑制作用.由图5(b)可知,加入CO2后NOx的吸附量明显减少,通过峰面积积分计算得到NOx吸附量减少了约17%.由此可知CO2的存在会导致Fe2O3催化剂表面NOx吸附量降低,这与图5(a)的结果一致.

(a) 200 ℃时NOx吸附的原位DRIFTS谱图
CO2加入后抑制了硝酸盐物种在催化剂表面的吸附,尤其是使参与快速NH3-SCR反应的关键物种NO2以及硝酸盐物种的形成受到了抑制.综上可以得出结论,在Fe2O3催化剂表面,NOx和CO2之间存在竞争吸附.

综上所述,CO2的加入改变了催化剂对NH3的吸附行为,由于碳酸盐物种在催化剂表面的形成以及其后续作为新的酸性位点吸附NH3物种,催化剂对NH3的吸附能力变强;同时CO2抑制了催化剂表面的NH3氧化过程.
2.4 CO2对反应路径的影响
由前文可知CO2的加入抑制了催化剂表面对NOx相关物种的吸附,本文就CO2加入后对NOx吸附物种反应性的影响进行相关探究.在对Fe2O3催化剂进行有无CO2条件下的NOx预吸附后,又在200 ℃下向催化剂表面通入NH3,谱图如图7(a)所示.由图可知,无论CO2是否存在,催化剂表面硝酸盐物种(1 570、1 378、1 355 cm-1)均在NH3引入后逐渐被消耗;同时出现了Lewis酸性位点的配位NH3物种(1 188 cm-1).但在CO2存在条件下,NO2与NH3物种之间的反应速率明显变慢(图7(b)).
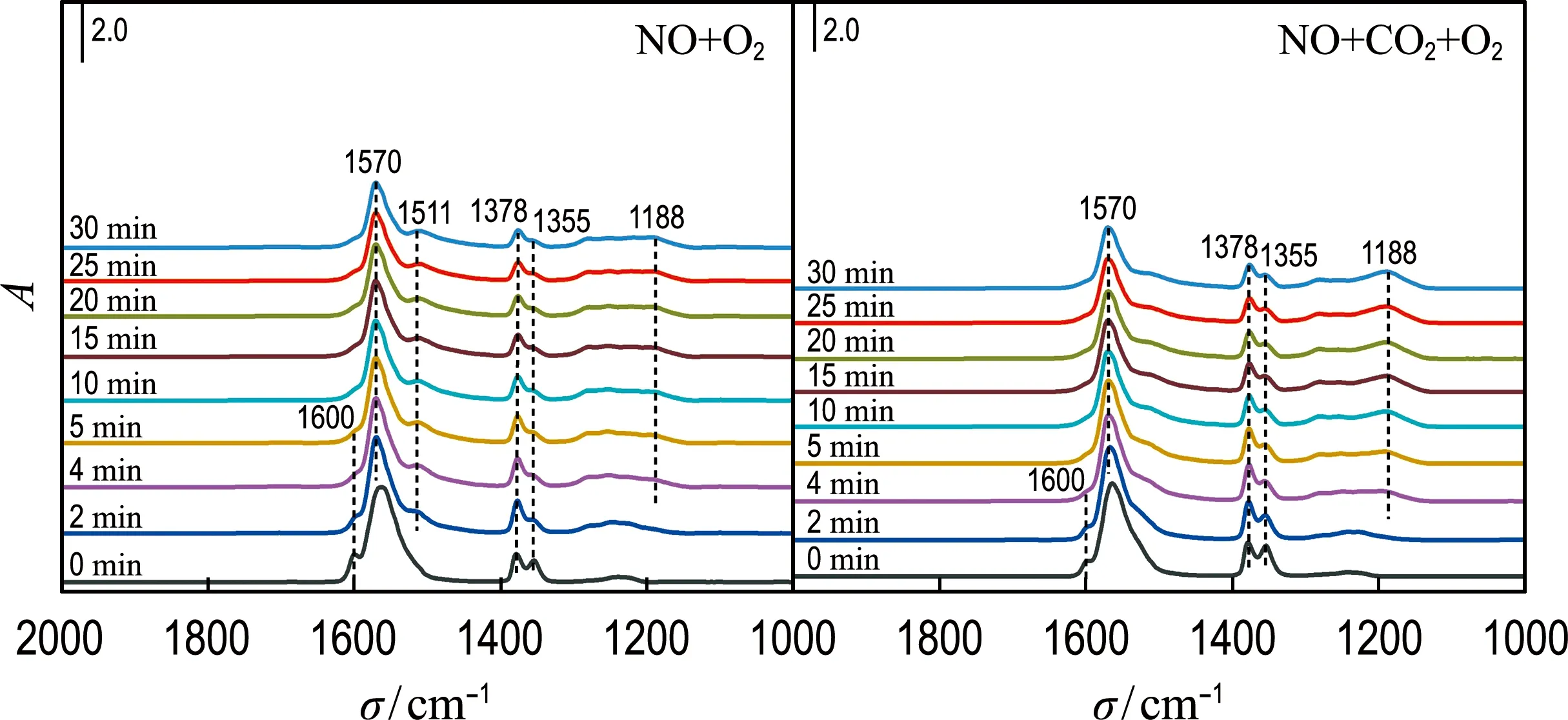
(a) 200 ℃下通入NH3的原位DRIFTS谱图
综上所述,推断得到CO2存在下Fe2O3催化剂的NH3-SCR反应路径,如图8所示.CO2的加入促进了催化剂表面对NH3物种的吸附;但同时由于CO2和NOx之间的竞争吸附,催化剂表面参与快速NH3-SCR反应的NO2物种和其他参与反应的硝酸盐物种的生成被抑制.催化剂的主要反应活性物种减少,NH3-SCR反应活性自然降低.
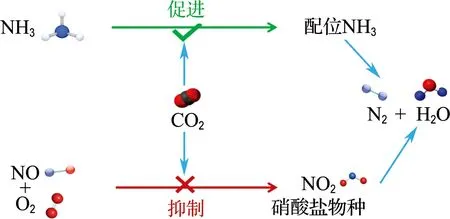
图8 Fe2O3催化剂反应路径抑制图
3 结 语
CO2抑制了Fe2O3催化剂的NH3-SCR反应活性,通过原位漫反射傅里叶变换红外光谱和程序升温脱附实验等手段发现CO2可以在催化剂表面形成稳定的碳酸盐物种,同时这些碳酸盐物种可以作为新的酸性位点促进催化剂对NH3的吸附.但由于CO2和NOx之间的竞争吸附,催化剂表面的NO2物种和硝酸盐物种的形成被抑制,从而导致NH3-SCR反应过程变慢,催化剂的脱硝效率下降.
