奥希替尼联合PC 方案化疗治疗晚期非小细胞肺癌的临床观察
2023-09-02张慧君
张慧君
(河南省西平县人民医院肿瘤内科 西平 463900)
肺癌的发病率与病死率均居恶性肿瘤首位,其中超过80%为非小细胞肺癌(Non-Small Cell Lung Cancer,NSCLC),包括鳞癌、大细胞癌、腺癌等,患者癌细胞扩散转移较晚、生长分裂速度慢,以致早期缺乏典型表现[1~2]。NSCLC 患者早期症状以胸痛、血痰、发热、气促为主,易与呼吸道疾病的症状混淆,无法及时检出、尽早治疗,导致5 年生存率较低。临床针对错失手术机会的NSCLC 患者多选用化疗,以促进肿瘤细胞凋亡,控制患者病情,尽可能延长生存时间,改善预后[3]。目前较为成熟的化疗方案为PC 方案,即顺铂+培美曲塞,为临床常用方法,能够杀灭肿瘤细胞,改善患者症状,但易产生免疫抑制,诱发诸多不良反应,患者耐受性较差,整体效果有待提升[4]。随着医学快速发展,临床治疗NSCLC 已开启精准医学时代,一定程度上延长了患者生存时间[5]。奥希替尼为新研发的靶向药物,用于治疗NSCLC 可增强疗效,提高患者免疫力,但其安全性与有效性仍存在一定争议[6]。鉴于此,本研究探讨奥希替尼联合PC方案化疗治疗晚期NSCLC 的临床效果。现报道如下:
1 资料与方法
1.1 一般资料 选择2019 年10 月至2022 年10月医院收治的NSCLC 晚期患者82 例,按治疗方案不同分为对照组和观察组各41 例。观察组男24 例,女17 例;年龄43~75 岁,平均年龄(58.74±6.57)岁;体质量41~86 kg,平均体质量(72.46±6.81)kg;临床分期:Ⅲb 期28 例,Ⅳ期13 例;类型:腺癌38 例,鳞癌3 例;基础疾病:高血压12 例,糖尿病15 例,骨质疏松13 例;文化程度:初中及以下15 例,中专及高中18 例,大专及以上8 例。对照组男25 例,女16例;年龄43~73 岁,平均年龄(58.38±6.54)岁;体质量41~85 kg,平均体质量(72.18±6.39)kg;临床分期:Ⅲb 期29 例,Ⅳ期12 例;类型:腺癌37 例,鳞癌4 例;基础疾病:高血压14 例,糖尿病14 例,骨质疏松15 例;文化程度:初中及以下14 例,中专及高中20 例,大专及以上7 例。两组一般资料比较,差异无统计学意义(P>0.05)。本研究经医院医学伦理委员会批准(审批号:20190602)。
1.2 入组标准 纳入标准:符合NSCLC 临床相关诊断标准[7],且经影像学、病理学明确诊断为晚期;患者已错失手术机会,需进行化疗;既往无相关药物治疗史,首次进行化疗;患者及其家属对本研究均知情并签署知情同意书。排除标准:不耐受本研究治疗方案,或存在严重过敏反应;已出现全身转移;伴有精神疾病或认知障碍,抗拒治疗;伴有脏器功能衰竭或免疫性疾病;存在视听障碍,无法进行正常交流。
1.3 治疗方法 对照组行PC 方案治疗。第1 天使用500 mg/m2注射用培美曲塞二钠(国药准字H20103287),第1~5 天使用20 mg/m2注射用顺铂(国药准字H20023236),静脉滴注给药。基于此,观察组加用甲磺酸奥希替尼片(国药准字HJ20181062),口服,80 mg/d。一个周期共21 d,两组均治疗4 个周期。
1.4 观察指标 比较两组疗效、肿瘤标志物水平、免疫指标、毒副反应。(1)疗效。患者治疗效果划分标准参考《实体瘤治疗疗效评价标准-RECIST》[8]制定:经治疗后,患者所有症状、病灶均消失,且持续4周为完全缓解;经治疗后,患者所有症状、病灶均得到明显改善,病灶缩小>50%,且持续4 周为部分缓解;经治疗后,患者所有症状、病灶均有所改善,病灶缩小<50%,且持续4 周为稳定;经治疗后,患者所有症状、病灶未见改善甚至加重,出现新病灶或病灶扩大25%为进展。疾病控制率=完全缓解率+部分缓解率+稳定率。(2)肿瘤标志物水平。两组患者分别于治疗前、治疗4 个周期后,在患者空腹状态下取4 ml 静脉血,先进行离心操作,离心速度3 000 r/min,离心时间10 min,取血清待测。检测指标包括血管内皮生长因子(Vascular Endothelial Growth Factor,VEGF)、血清癌胚抗原(Carcino Embryonic Antigen, CEA)、 糖 类 抗 原 125(Carbohydrate Antigen-125,CA125),检测方法为酶联免疫吸附法。购入北京万泰生物药业有限公司试剂盒,所有操作需严格按照说明书进行。(3)免疫指标。分别于治疗前、治疗4 个周期后,取两组患者3 ml 空腹静脉血,离心速度3 000 r/min,持续操作15 min,取血清用于检测CD3+、CD4+、CD8+水平,并计算CD4+/CD8+比值。(4)毒副反应。比较两组皮疹、瘙痒、肝肾损伤、白细胞下降等发生情况。
1.5 统计学方法 采用SPSS22.0 统计分析软件,计数资料以%表示,采用χ2检验,计量资料以(±s)表示,采用t检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组疗效对比 观察组总有效率为90.24%(37/41),高于对照组的70.73%(29/41),差异有统计学意义(P<0.05)。见表1。

表1 两组疗效对比[例(%)]
2.2 两组肿瘤标志物水平对比 两组治疗后CEA、VEGF、CA125 水平均降低,且观察组水平明显低于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组肿瘤标志物水平对比(±s)

表2 两组肿瘤标志物水平对比(±s)
CA125(U/ml)治疗前 治疗后对照组观察组组别 n CEA(U/ml)治疗前 治疗后VEGF(pg/ml)治疗前 治疗后41 41 t P 12.84±2.49 12.69±2.36 0.280 0.780 8.41±1.57 4.34±1.08 13.676 0.000 241.92±33.17 243.73±32.95 0.248 0.805 160.49±25.36 126.26±16.78 7.208 0.000 133.78±12.83 134.12±12.47 0.122 0.904 51.64±7.25 27.53±4.31 18.304 0.000
2.3 两组免疫指标对比 两组治疗前免疫指标比较,差异无统计学意义(P>0.05);治疗后,观察组CD3+、CD4+、CD4+/CD8+均高于对照组,CD8+低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组免疫指标对比(±s)

表3 两组免疫指标对比(±s)
CD4+/CD8+治疗前 治疗后对照组观察组组别 n CD3+(%)治疗前 治疗后CD4+(%)治疗前 治疗后CD8+(%)治疗前 治疗后41 41 t P 31.89±5.46 31.73±5.28 0.135 0.893 24.24±3.44 47.81±5.97 21.904 0.000 13.89±2.27 13.94±2.16 0.102 0.919 10.15±2.12 29.13±3.51 29.638 0.000 22.88±3.29 22.53±3.32 0.480 0.633 26.89±2.56 20.08±1.65 14.317 0.000 1.69±0.31 1.64±0.35 0.685 0.496 1.32±0.31 1.93±0.46 7.041 0.000
2.4 两组药物安全性对比 观察组毒副反应发生率为7.32%(3/41),低于对照组的24.39%(10/41),差异有统计学意义(P<0.05)。见表4。
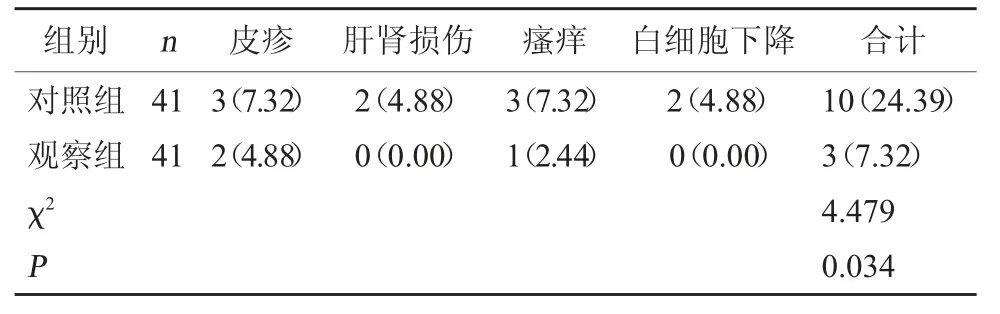
表4 两组药物安全性对比[例(%)]
3 讨论
肺癌为常见的恶性肿瘤,根据其病理形态不同可分为小细胞肺癌与NSCLC,以NSCLC 发生率更高,常见于老年人群,随着老龄化进程加快,其发生率也随之升高[9]。老年人常伴有多种基础疾病,生理机能减退,加之NSCLC 早期症状表现不明显,待出现症状就诊时已处于晚期,此时进行手术治疗已丧失意义,一般选择内科保守治疗。随着医学技术的快速发展,NSCLC 的化疗方案越来越多,其中PC 方案为首选方案,该方案在抑制肿瘤细胞增殖方面效果较好,可减少细胞转移,治疗效果已获得认可[10]。但在临床应用中发现,PC 化疗方案易产生免疫抑制作用,诱发严重的毒副反应,部分患者甚至因无法耐受而被迫中断治疗,降低治疗效果,影响患者预后,因此寻找更加安全高效的治疗方案有重要意义。
PC 方案即顺铂+培美曲塞,前者为常用的抗肿瘤药物,对癌细胞复制有抑制作用,通过抑制癌细胞的蛋白质核糖核酸(RNA)合成,阻断病灶增殖扩大,在多种实体肿瘤的治疗中均有应用。后者为多靶点抗代谢药物,对嘧啶、嘌呤合成酶的表达有较好的抑制作用,可阻断细胞分裂,控制病灶增长,从而改善患者病情[11]。肿瘤标志物参与了恶性肿瘤发生、发展的整个过程,CEA、VEGF、CA125 均为临床常用的肿瘤标志物指标,恶性肿瘤患者的上述指标均有明显升高,监测水平变化可反映肿瘤细胞活性,对评估治疗效果、预后均有重要参考价值[12]。恶性肿瘤、化疗药物均会对机体免疫功能造成一定损害,降低机体耐受力,影响整体治疗效果与患者生存质量,因此提高患者免疫功能对治疗有重要意义。PC 方案治疗NSCLC 有一定效果,但其带来的毒副反应也不容忽视,临床应用存在一定弊端。近些年,恶性肿瘤分子靶向治疗在临床得到应用,主要通过靶向药物作用于信号通路的关键分子,对癌细胞增殖、侵入进行抑制,发挥靶向治疗作用,且能够保证治疗安全性,避免对周围正常组织细胞造成损害[13]。奥希替尼即为新一代靶向药,可对表皮生长因子受体(EGFR)信号通路发挥作用,与EGFR 进行竞争性结合,阻断络氨酸激酶活化,对癌细胞增殖、转移进行抑制,从而导致其凋亡[14]。本研究结果显示,观察组总有效率(90.24%)高于对照组(70.73%),毒副反应少于对照组;两组治疗前CEA、VEGF、CA125 水平、免疫指标比较未见明显差异;两组治疗后CEA、VEGF、CA125 水平均降低,且观察组水平更低;治疗后,观察组CD3+、CD4+、CD4+/CD8+均高于对照组,CD8+低于对照组。表明NSCLC 患者采用奥希替尼联合PC 方案化疗效果较好,利于降低CEA、VEGF、CA125 水平,改善患者免疫指标,且毒副反应更少,临床应用安全可靠。和瑞莲等[15]研究显示,奥希替尼靶向治疗非小细胞肺癌近远期效果确切,对血清肿瘤标志物表达有较好的抑制作用,可增强患者免疫力,安全性较高,患者生存期有所延长,与本研究结果有相似之处,进一步佐证了奥希替尼的有效性与安全性。分析其原因为,奥希替尼能够抑制癌细胞扩散,特异性杀灭癌细胞,防止癌细胞生长或转移,利于控制患者病情,下调肿瘤标志物水平,改善患者免疫功能[16]。奥希替尼为靶向药物,临床中严格遵循医嘱用药可达到增效减毒的效果,与PC 方案联合治疗NSCLC 切实可行。
综上所述,NSCLC 患者采用奥希替尼联合PC方案化疗效果较好,利于降低CEA、VEGF、CA125水平,改善患者免疫指标,且毒副反应更少,临床应用安全可靠。
