超高压处理对大米蛋白水解物/小麦淀粉复合体系的影响
2023-08-18高雨晨闫冰冰夏姚姚李圆圆杜先锋
林 丽,高雨晨,闫冰冰,夏姚姚,李圆圆,杜先锋*
(1 安徽农业大学 合肥 230036 2 六安市食品药品检验中心 安徽六安 237161)
淀粉作为膳食的重要组分,其消化性与糖尿病人的糖代谢和血糖应答水平密切相关[1]。淀粉的消化速率受食物组分间相互作用的影响。在富含淀粉的食品体系中,蛋白质是影响淀粉消化的重要组分[2]。大米蛋白质的生物学价值高于其它主要谷物(小麦、玉米和大麦)。此外,大米蛋白通常被认为是低致敏性的。近年来,较多研究关注蛋白质水解产物对淀粉消化性的影响,研究发现蛋白质水解产物对淀粉消化性的影响程度大于完整蛋白[3]。
超高压加工是一种新兴的非热加工技术,可以用来开发高淀粉含量食物作为低能量食物中的脂肪替代品[4]。近年来,已有超高压处理对各种植物源淀粉和蛋白质结构、物理和化学性质影响的研究[5]。超高压处理淀粉-脂肪酸复合物与淀粉-多酚复合物是目前的研究重点[6-7]。目前已利用超高压处理技术获得了改性淀粉、蛋白质等单体[8-9],而研究仅局限于超高压对单一物质的理化特性的影响,对淀粉和蛋白质水解物复合体系的影响研究鲜见报道。
1 材料与方法
1.1 材料与试剂
小麦淀粉,上海源业生物科技有限公司;大米蛋白质,江西金农生物科技有限公司;碱性蛋白酶(B8360),北京索拉比奥生物技术有限公司;淀粉酶(A109182)、糖化酶(A107823),上海阿拉丁生化科技有限公司;葡萄糖氧化酶、过氧化物酶(GOPOD),长春汇力生物技术有限公司。所用化学药品均为分析纯级。
1.2 仪器与设备
HHP-600 超高压食品处理设备,中国包头科发高压食品加工公司;Nicoletteis is 50 傅里叶红外光谱仪,美国赛默尔飞世尔公司;TTR-Ⅲ型X射线衍射仪,日本理学公司;Meso MR23-060H-I核磁共振分析仪,上海纽迈科技有限公司;RVA Super3 快速黏度分析仪,NEWPORT 科技公司;DHR-1 流变仪,美国TA 公司;真空冷冻干燥机,德国Christ 公司。
1.3 方法
1.3.1 超高压处理WS/RPH 复合物的制备 大米蛋白质经碱性蛋白酶水解2 h 制备RPH2,RPH2再经中性蛋白质水解2 h 制备RPH4,水解度分别为10 和14。RPH2 和RPH4 与WS 以12%(质量分数)的比例充分物理混合30 min。将混合物制备成质量分数10%的悬浮液,沸水浴20 min 后立即转移到便携式杀菌锅(120 ℃,15 min),将制备好的复合凝胶迅速装入聚丙烯袋中真空密封。分别在150,250,350,450 MPa 的压力下,由高压装置处理悬液20 min。传压介质为水,温度为室温,超高压设备达到指定压力时开始计时。制备的样品标记为WS-12%RPH2-150,WS-12%RPH4-150,WS-12%RPH2-250,WS-12%RPH4-250,WS-12% RPH2 -350,WS -12% RPH4 -350,WS -12%RPH2-450,WS-12%RPH4-450。处理完成后置于4 ℃冰箱老化3 d,结束后置于-80 ℃冰箱冷冻,真空冷冻干燥48 h,磨粉过100 目筛,储存在干燥器中。
1.3.2 傅里叶变换红外光谱(FTIR)测定 将一定量的KBr 粉磨碎,与样品粉混合研磨,压制成样品薄片,收集红外光谱仪400~4 000 cm-1的波数。采用Omnic8.0 软件进行光谱处理。为进一步研究RPH 对WS 近程有序度的影响,对900~1 200 cm-1段的特征峰进行反卷积。计算强度比(IR)分别为1 047/1 022 cm-1和10 22/995 cm-1。
1.3.3 X 射线衍射(XRD)测定 在进行XRD 分析之前,将样品在室温下(相对湿度100%)平衡24 h。样品的XRD 图谱使用40 kV Cu Kα 辐射记录。所有样品均在2θ=5~50°的角度范围内进行扫描,扫描速度为8°/min。应用MDI-Jade 6.0 软件(Material Data Inc,Livermore,California,USA)计算淀粉的相对结晶度(RC)。
1.3.4 快速黏度分析 采用快速黏度分析仪(RVA)测定了WS/RPH 配合物的黏度特征值。将25.0 mL 去离子水和3.0 g 样品混合粉末加入快速黏度分析仪的铝筒中。测试程序设置如下:加热之前,样品在960 r/min 搅拌10 s 后,10 s 内速度降低到160 r/min,在50 ℃保持10 s,然后加热到95℃保持150 s,升温和降温的速度均为0.2 ℃/s。
1.3.5 复合凝胶的横向弛豫时间测定 将制备的样品(1.5 mL)置于玻璃瓶中密封。玻璃瓶在32 ℃水浴中平衡10 min 后放入核磁共振管中。选择Q-FID 程序校准LF-NMR 分析仪。选择CPMG 序列作为测试序列。回声时间(TE)为2 ms,回声次数(NECH)为1 000 次,重复采集次数(NS)为8次,对得到的反演图像进行分析。
1.3.6 动态流变性的测定 取超高压处理后的凝胶样品置于流变仪测定平台上。测定间隙设置为1 000 μm,测量温度设置为25 ℃,测定0.1~10 Hz扫描频率范围内G′、G″的变化。
本文旨在利用数据缓存Redis和SSM集成框架搭建一种适用于盾构机数据处理运用的系统,对此在盾构机数据采集的基础上对系统进行结构的分层设计。整个系统基于B/S模式进行开发,而盾构数据通过机载的数据采集器用PLC采集得来,需要解包、转换、缓存和持久化。因此整个系统的工作流程是先将机载系统采集的数据解析后进入Redis,然后按照前端请求进行实时的数据请求响应,同时将盾构固有数据和实时数据同步存储到MySQL中,为后续的故障预测、数据分析等大量数据运用处理过程事务提供数据源。所以根据数据流动和功能划分,本文将整个系统软件结构分为数据层、应用层和表示层[9],如图1。
1.3.7 淀粉体外消化率的测定 体外消化试验按照Englyst 等[10]建立的方法进行。200.0 mg 的样品与乙酸钠缓冲液(15.0 mL,pH 5.2)涡流混合,沸水浴糊化15 min。将混合酶溶液(10.0 mL)加入每个样管中,充分涡旋,置于37 ℃水浴中,磁力搅拌并准确计时。在消化反应0,20,120 min 时,取1.0 mL 样品于离心管中,加入4.0 mL 无水乙醇。用GOPOD 法测定离心(4 000 r/min,20 min)后上清液中葡萄糖含量。WS/RPH 配合物的快消化淀粉(RDS)、慢消化淀粉(SDS)、抗性淀粉(RS)的计算公式如下:
式中,G0——酶解前淀粉悬浮液中游离葡萄糖含量(mg);G20——淀粉水解20 min 酶解物中葡萄糖含量(mg);G120——淀粉水解120 min 酶解物中葡萄糖含量(mg);M——样品质量(mg)。
2 结果与分析
2.1 超高压处理WS/RPH 复合物的红外光谱图
可通过红外光谱鉴定淀粉衍生的官能团,每个官能团相关的特征吸收峰仅出现在特定范围内,并且每个官能团的吸收频率受大米水解蛋白的添加量及超高压处理的压力条件等某些因素的影响[11]。WS、WS-12%RPH、经超高压处理的WS-12%RPH 获得的红外吸收光谱如图1 所示。HHP处理后,WS/RPH 复合物没有显示出额外的吸收峰,说明超高压处理并没有使体系产生新的化学键。然而,现有峰的强度发生了变化。3 400 cm-1处的特征峰代表-OH 缔合氢键的对称伸缩振动峰[12]。在FTIR 光谱中,波数1 047 cm-1附近的吸收峰与淀粉的晶体结构有关,1 022 cm-1附近的吸收峰与无定形结构有关,在1 047 cm-1和1 022 cm-1处的吸收峰强度比值R1047/1022 可用于表征样品的短程有序结构。较大的值表示有序性越高。R1022/995 值可以反映双螺旋结构的变化[13]。150,250,350 MPa 处理WS/RPH 体系后,3 400 cm-1吸收峰发生了轻微的蓝移,说明体系由于超高压条件处理后,分子结构更加紧密,分子间产生相互作用增加,氢键作用力增强。表1 显示了超高压处理后WS 和WS/RPH 复合物的R1047/1022 和R1022/955 值。结果表明,150,250,350 MPa 处理增加了WS/RPH 复合物的R1047/1022 值,WS-12%RPH2-250 和WS-12%RPH4-250 的R1047/1022 值分别为0.89 和0.86,与WS 相比显著增加(P<0.05)。当压力增加到450 MPa 时,复合物的R1047/1022 值降低,而依旧比WS 高,这与XRD计算的结晶度结果一致。复合物在150~350 MPa处理后R1022/995 值最小。这些结果表明WS-12%RPH-350 复合体系中短程有序结构和双螺旋结构较多[14]。据推测,RPH 通过氢键与小麦淀粉相互连接,对小麦淀粉的结晶区具有保护作用。同时,超高压处理对WS 和RPH 结构产生影响进一步改变其相互作用,合适的压力条件下,复合物中淀粉与水解蛋白的氢键作用增强,老化过程中淀粉的共结晶范围增大,从而使复合物的有序性增加。在450 MPa 处理后,复合体系的R1047/1022值下降,表明短程有序结构和双螺旋结构下降,这是因为过高的压力会破坏淀粉分子内及蛋白质水解物与淀粉间的相互作用。
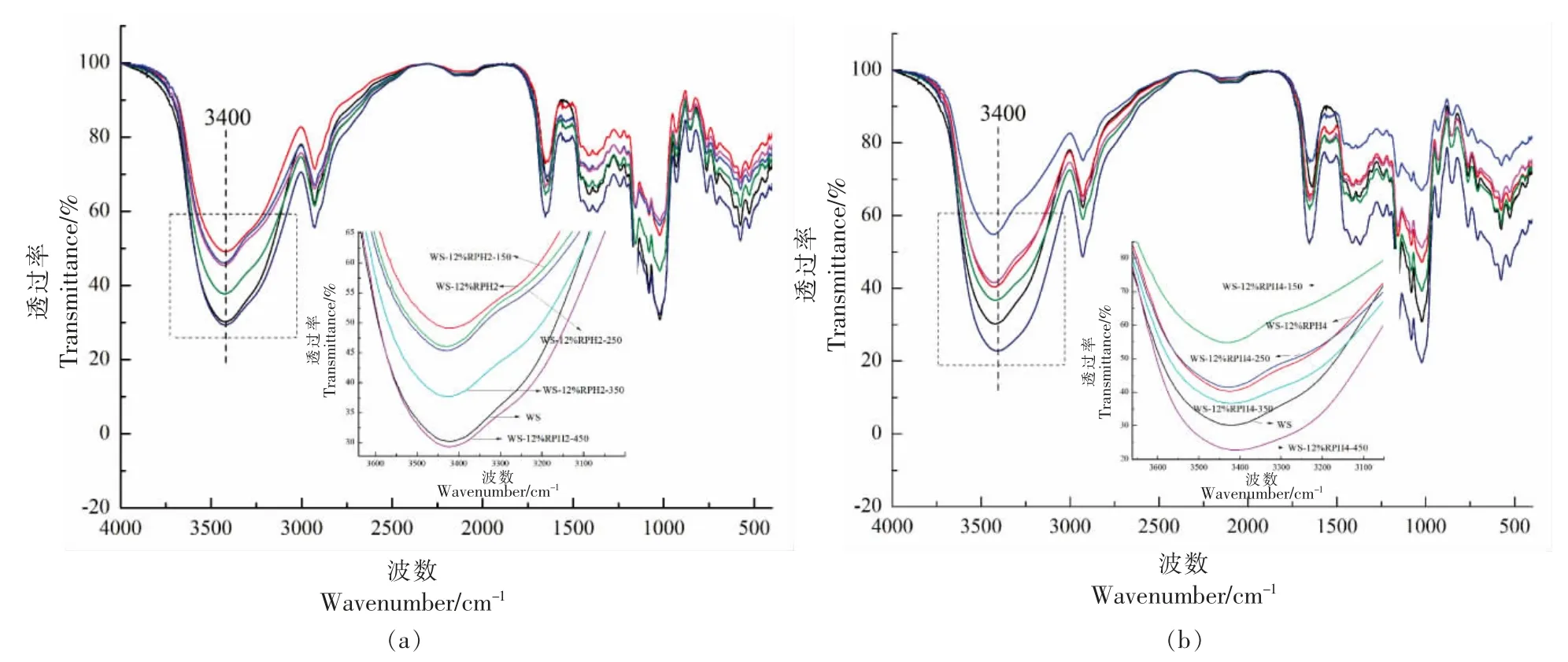
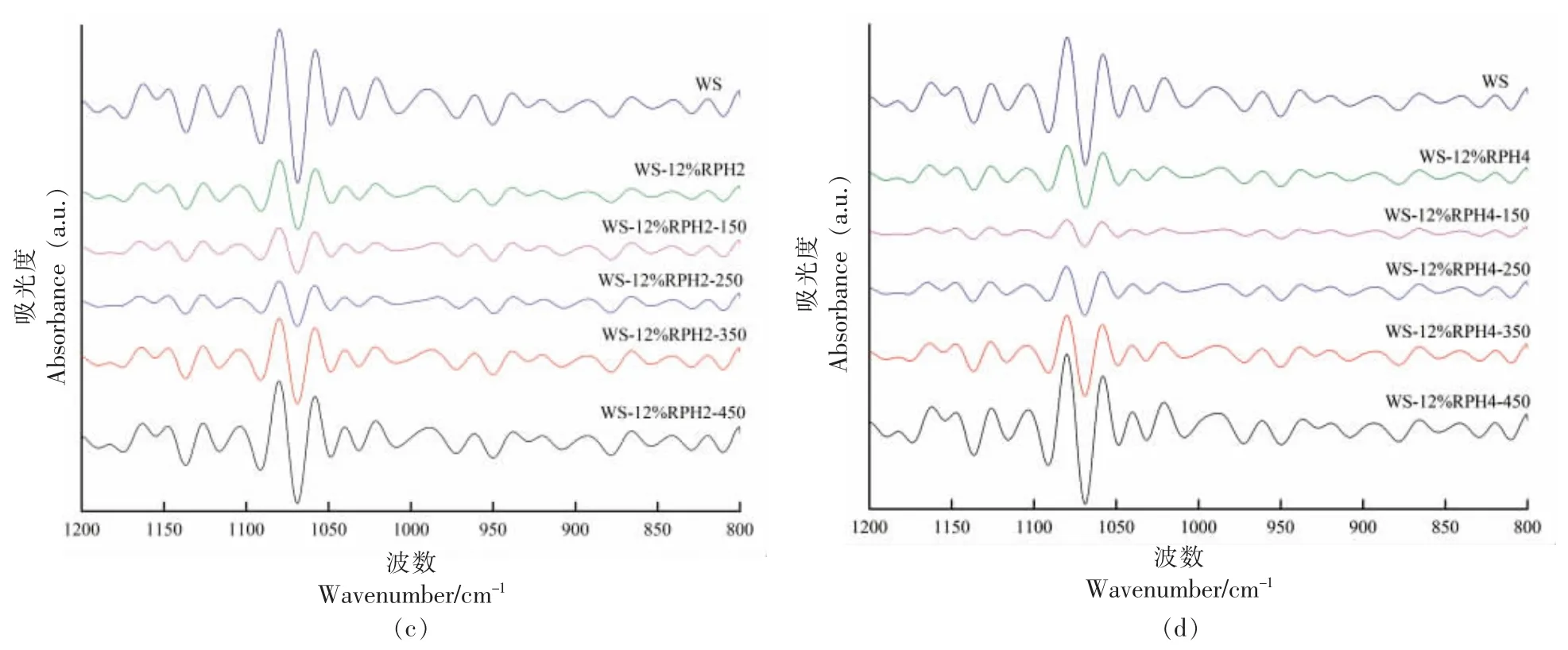
图1 超高压处理WS/RPH 复合物的傅里叶变换红外光谱和反卷积傅里叶变换红外光谱Fig.1 Fourier transform infrared spectroscopy and deconvolution Fourier transform infrared spectroscopy of WS/RPP complexes after HPP

表1 超高压处理后WS/RPP 复合物的1 047/1 022 cm-1 和1 022/995 cm-1 强度比Table 1 1 047/1 022 cm-1 and 1 022/995 cm-1 strength ratios of WS/RPP complexes after HPP
2.2 超高压处理WS/RPH 复合物的晶体结构
图2 为小麦淀粉和WS/RPH 复合物经超高压处理并老化后的X-衍射图谱,加入RPH 后未出现新的衍射峰,说明RPH 对复合物的晶体类型没有影响。同时可以看出,HPP 对WS/RPH 复合体系的晶型也没有影响。添加12%RPH 的复合物的相对结晶度高于WS。WS-12%RPH2 样品进行350 MPa 处理后,相对结晶度增加到17.185%(P<0.05)。这可能是由于压力的压缩增韧效应,350 MPa 压力处理加强了分子间的相互作用,支链淀粉分子链上的羟基通过氢键形成新的双螺旋结构,晶体结构得到改善[15]。也可能是因为超高压处理进一步破坏了淀粉颗粒,RPH 更容易与淀粉结合,使复合物中的共结晶现象更广泛[16-17]。
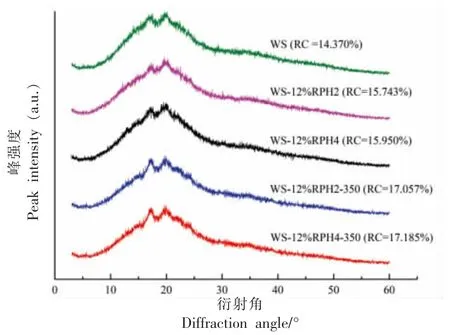
图2 超高压处理WS/RPH 复合物的X-衍射图Fig.2 X-ray diffraction pattern of WS/RPP complexes after HPP
2.3 超高压处理WS/RPH 复合物的糊化特性
研究发现复合物的糊化特性受超高压处理的影响显著(表2)。随着超高压处理压力的增加,样品的糊化时间推迟。与WS 相比,超高压处理样品的峰值黏度显著降低(P<0.05),说明超高压处理对水解蛋白及淀粉结构的处理促进了其相互作用,使复合物的结构更加致密。同时,超高压促进复合物产生的共结晶现象在老化过程中进一步增强,形成较紧密结构[18]。崩解值主要反映了当加热和施加剪切力时淀粉颗粒的稳定性。WS/RPHHHP 复合物的崩解值显著低于WS 与WS-RPH(P<0.05)。崩解值的降低表明超高压处理使WS与RPH 结合更加致密,这可能导致浸出的直链淀粉减少[19]。
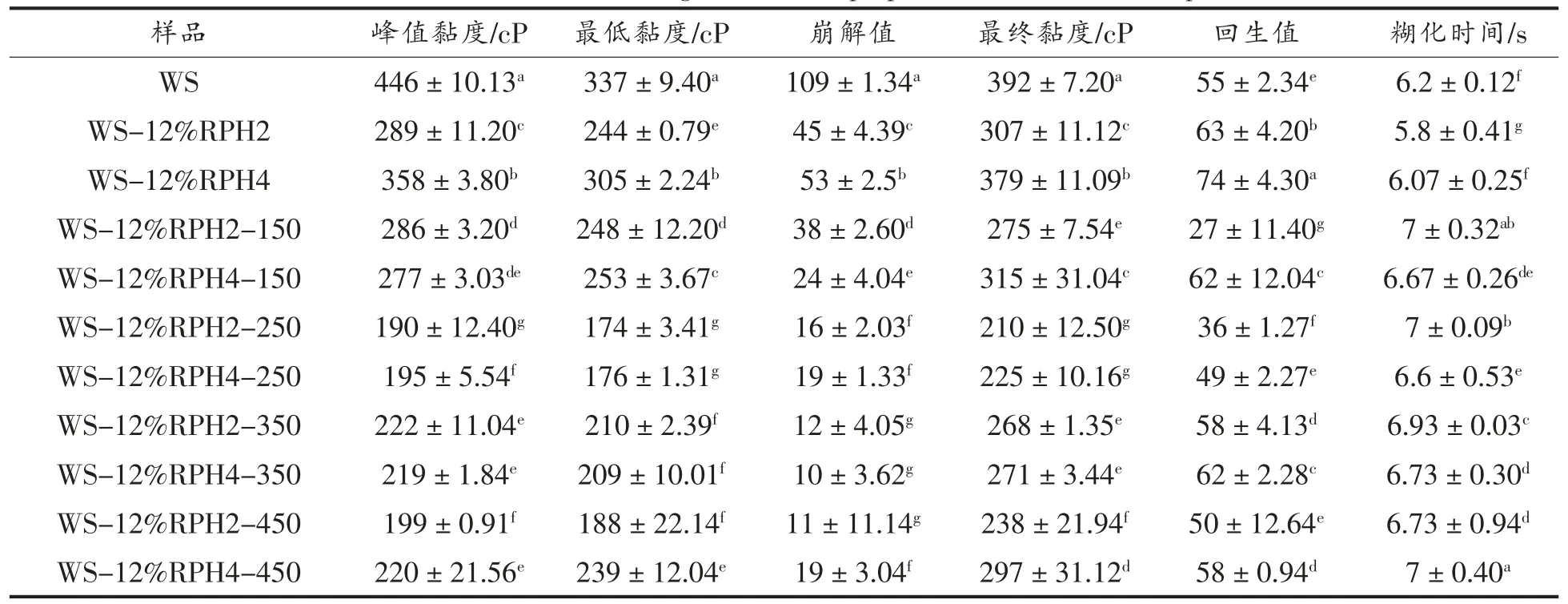
表2 HPP 对WS/RPP 复合物糊化特性的影响Table 2 Effect of HPP on gelatinization properties of WS/RPH complexes
2.4 超高压处理WS/RPH 复合物的水分分布分析
低场核磁共振技术(LF-NMR)用于测量氢分子的自旋-自旋弛豫和迁移率,它是分析淀粉凝胶中质子弛豫的实用工具。信号来自样品中的所有质子,因此可以很好地表达质子的分布和迁移率[20]。利用LF-NMR 技术分析复合物的水分分布、水分子存在形式及水分迁移情况。试验测定了4℃老化过程中样品的水分分布,图4 分别为第1,3,7,15 天的结果。
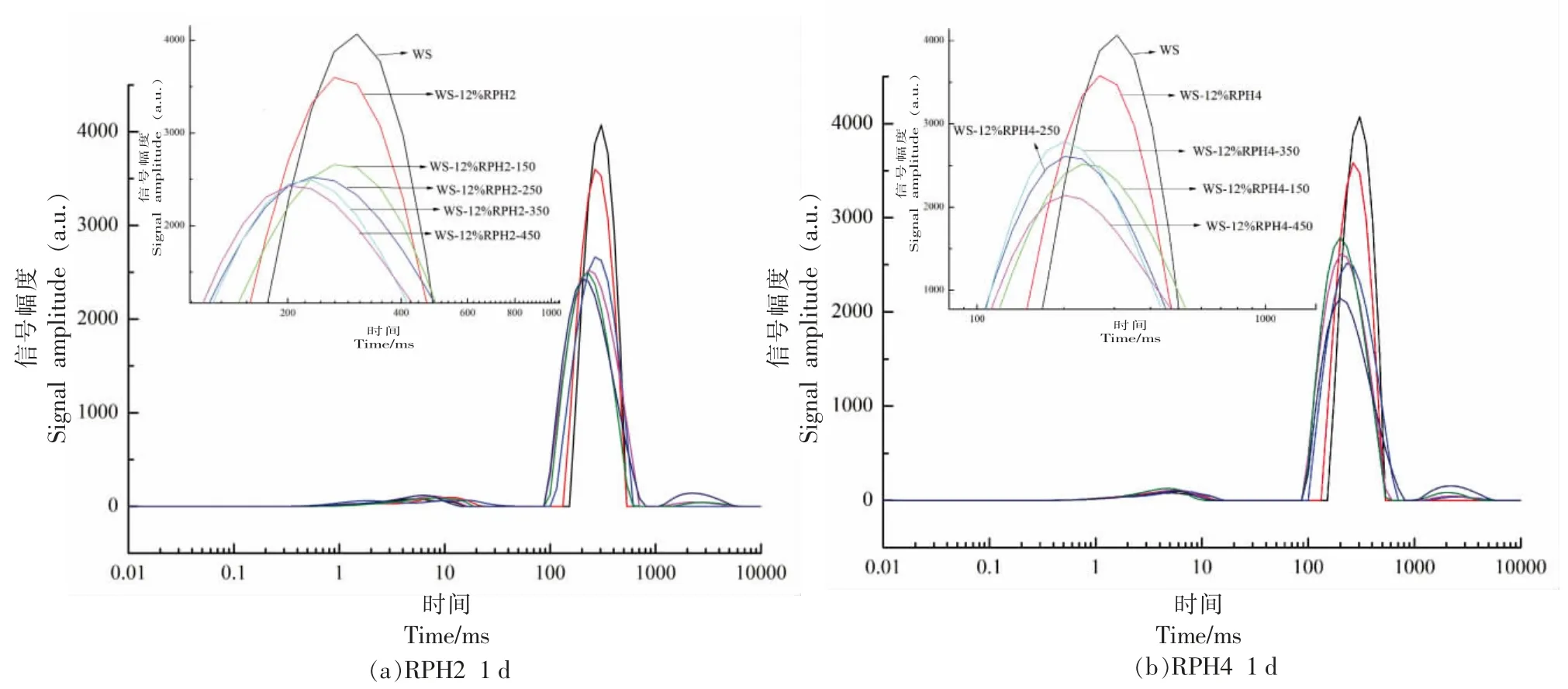
图4 超高压处理WS/RPH 复合物凝胶的弛豫时间谱图Fig.4 Relaxation time spectra of WS/RPP complexes gel after HPP
LF-NMR 技术测量中得到自旋-自旋弛豫时间,又称为横向弛豫时间,用T2表示。复合物超高压处理后的LF-NMR 弛豫测定结果显示,复合物中的水大致分为3 种相态:结合水、不易流动水以及自由水3 个区段[21]。氢质子受束缚越大或自由度越小,T2弛豫时间越短,在T2谱上峰位置较靠左;反之则T2弛豫时间越长,在T2谱上峰位置较靠右。所以弛豫时间可以间接表明水分的自由度[22]。
总体来看,超高压处理后复合物弛豫时间缩短,水分流动性减弱。此外,不同压力处理的复合物信号幅度变化程度不同。信号幅度代表质子密度,信号幅度下降也说明水分流动性减弱[23]。弛豫图上每个样品对应的峰面积占比反映了相应的水分含量的变化,可以发现超高压处理样品的水分活度减小。较高压力下自由水含量减少的现象尤为明显,450 MPa 时下降至最小值。压力处理后各组分峰的位置向左移动,自由水向结合水转化,均说明水分子与蛋白质分子、淀粉分子的相互结合作用增强,水的自由度降低,水分流动性减弱[24-25]。此外,在高压条件下,水被迫进入淀粉颗粒并增加了它们的水合程度。这主要是通过HPP 对淀粉层状和晶格结构的影响来实现的。虽然压力引起的压缩会降低淀粉层状距离和晶格空间,但在预糊化处理后,水已经渗透到层状块中。水迁移后,层状距离和晶格空间均增加[11]。扩散的水被高压截留在淀粉晶体结构中,这是超高压处理样品水分活度降低的另一个原因。
2.5 HPP 处理WS/RPH 复合物的动态流变行为
淀粉糊凝胶体系的黏弹性与淀粉基食品的实际应用性能有关,通过动态流变试验可测定黏弹性的大小。G′为弹性模量,反映的是体系的弹性性质,即固体行为能力,G″为损耗模量,反应的是体系的黏性特征,即体系的流体特性[26]。
超高压处理下的WS/RPH 复合体系的动态黏弹性如图5 所示。从图中可以看出,小麦淀粉的弹性模量G′和损耗模量G″最低,小麦淀粉及所有复合体系的G′和G″都具有频率依赖性,且每个样品的G′都大于其对应的G″,表现为一种典型的弱凝胶行为[27]。相对单独的淀粉体系而言,添加RPH后,复配体系凝胶的G′和G″略微增加,然而随着超高压处理压力的增大而明显增加,说明超高压处理提高了复合物的黏弹性。HPP 条件处理下的复合物相较于对照组,G′和G″明显增加,其中最高为WS-12%RPH2-350 和WS-12%RPH4-450。随着频率升高,G′和G″也逐渐升高。造成这种现象的原因可能是淀粉和RPH 之间发生氢键相互作用,分子链缠结点增多,从而增强复合凝胶体系的网络结构。并且后续的超高压处理可以增强淀粉与RPH 的相互作用,从而促进复合凝胶体系的网络结构形成[28]。
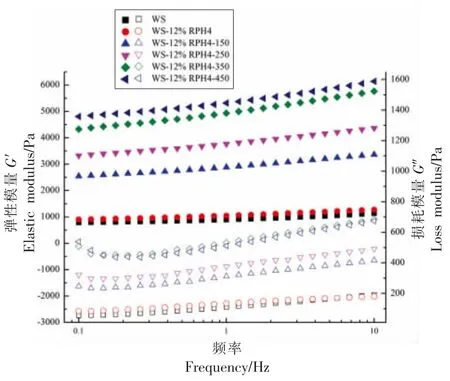
图5 超高压处理WS/RPH 复合体系的动态模量Fig.5 Dynamic modulus of high presser processed WS/RPH complexes
2.6 激光共聚焦测定结果分析
复合物的CLSM 染色图像如图6 所示。复合物中的小麦淀粉用尼罗蓝标记(第3 列图,标记为-3),蛋白质用尼罗红染料标记(第2 列图,标记为-2)。重叠图像(第1 列图,标记为-1)中的深色区域表示淀粉与蛋白质之间形成复合物。
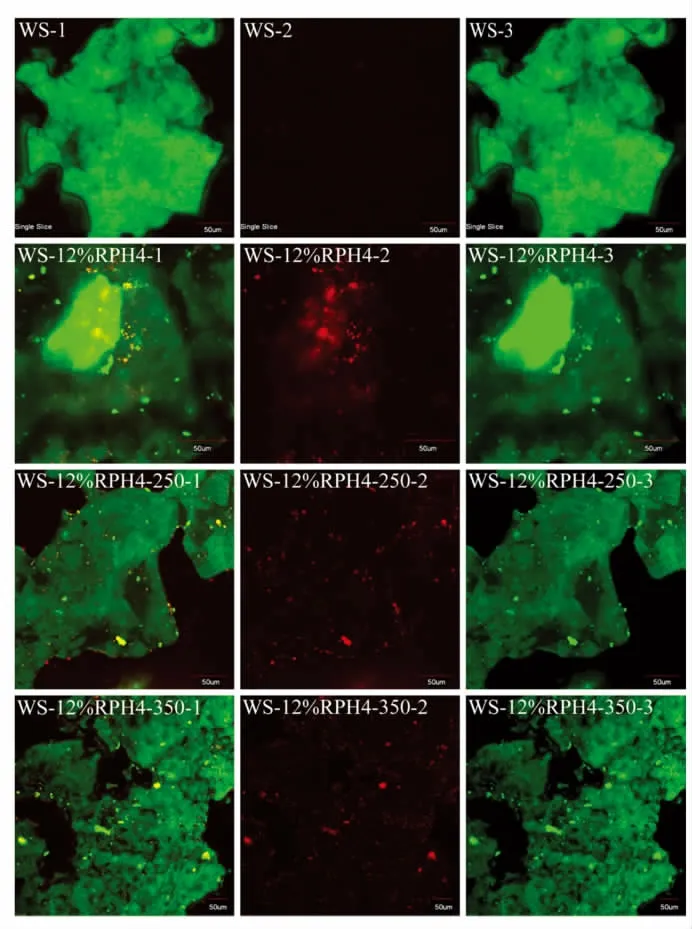
图6 超高压处理WS/RPH 复合物的激光共聚焦染色图像Fig.6 Laser confocal staining images of WS/RPH complexes after HPP
染色图像显示RPH 嵌入淀粉内部,原因是蒸煮过程中淀粉颗粒崩解,从而使RPH 渗入颗粒内部。叠加图像显示,酶促水解的大米蛋白质可以嵌入淀粉内部,并在淀粉表面形成一层涂层,即蛋白质通过这两种方式与淀粉相互作用。蛋白质与淀粉的相互作用导致形成淀粉的涂层阻淀粉葡糖苷酶的作用[29]。从图中可以发现,水热处理后蛋白质在淀粉中分布不均匀,有团聚现象。而超高压处理样品中蛋白质在淀粉中分布均匀。这是由于高压作用下,蛋白质和淀粉结构发生改变,促进蛋白质渗入淀粉团内部,相互作用增强,这与本试验对RDS 含量测定和RVA 研究结果的解释一致。
2.7 HPP 处理WS/RPH 复合物的体外消化模拟
超高压处理后的WS/RPH 复合物的水解曲线如图7 所示。RDS、SDS、RS 水平如表3 所示。水解率随消化时间的延长而增加。小麦淀粉RDS、SDS和RS 含量分别为54.85%,15.08%,30.07%。添加12%RPH 后,水解率和RDS 含量显著降低(P<0.05)。HHP 处理后,复合物的水解速率和RDS 含量进一步降低,RS 和SDS 水平进一步升高。然而在450 MPa 条件下,WS-12%RPH4 复合物的RDS 含量显著增加,说明该条件下的超高压处理使得一部分SDS 和RS 向RDS 转变,可能是超高压处理破坏了WS 与RPH 的结合力,并使得淀粉一部分由定形区转变到无定形区,加快了WS/RPH 复合物的消化能力。结合前人的研究,超高压处理后的结果表明,由于压缩和增韧效应,复合物的稳定性提高,导致体外消化率显著降低[30]。在压强较高的条件下,WS 与RPH 的结合通过外力作用得到提升,分子间结构重排,由无定形区转到定形区,定形区域的含量增加,从而延缓了其消化性[31]。

图7 HPP 处理后的WS/RPH 复合物的水解曲线Fig.7 Hydrolysis curve of WS/RPH complexes treated by HPP

表3 HPP 对WS/RPH 复合物淀粉体外消化率的影响Table 3 Effect of HPP on starch digestibility of WS/RPH complexes in vitro
3 讨论
到目前为止,超高压处理技术对淀粉和蛋白质水解物复合体系影响的研究未有报道,本试验验证了350 MPa 处理可以促进RPH 进入淀粉内部,增强复合物内部分子间相互作用,提高淀粉分子的有序性,降低水分流动性,增加黏弹性,这些影响使复合物的体外消化性降低。本研究发现超高压具有进一步降低淀粉蛋白质复合物消化性的潜力,也为超高压处理在低消化性食品生产中的应用提供了思路。
