化橘红配方颗粒与饮片汤剂的化学等量性和药效等效性研究
2023-07-11谭婉清王术玲刘潇潇黄俊忠广州中医药大学广东广州50006广东省药品检验所广东广州50663
谭婉清,王术玲,刘潇潇,黄俊忠(.广州中医药大学,广东 广州 50006;.广东省药品检验所,广东 广州 50663)
化橘红为芸香科植物化州柚Citrusgrandis‘Tomentosa’或柚Citrusgrandis(L.)Osbeck 的未成熟或近成熟的干燥外层果皮。前者习称“毛橘红”,后者习称“光七爪”“光五爪”[1],是“中国四大南药”和“十大广药”之一,更是岭南八大道地药材之首,有着“一片值千金”的说法[2]。化橘红主要用于治疗风寒咳嗽、痰多、久咳、气管炎、哮喘、食积伤酒和呕恶痞闷等。研究[3-7]表明,化橘红具有显著的化痰止咳、抗炎、抗氧化、免疫调节、预防糖尿病心肌功能损伤等药理作用。此外,日常将其泡水饮用,可用于缓解咳嗽、多痰、消化不良和炎症等[8],化橘红也被用于制成解酒和抗氧化等相关的保健食品[9-10],可见,化橘红应用广泛。中药配方颗粒包装密封性良好,不易变质,便于运输、贮存、保管,且可直接采用颗粒剂冲服饮用,服用剂量相对较小,也便于携带[11]。本研究建立化橘红配方颗粒与饮片汤剂的薄层色谱(TLC)鉴别和高效液相色谱(HPLC)指纹图谱,并测定其主要成分柚皮苷和野漆树苷的含量,综合分析比较配方颗粒与饮片汤剂间的共有特征组分群的相似性及其含量的等量性。同时,通过氨水喷雾引咳小鼠试验和小鼠酚红排泌祛痰试验,观察化橘红配方颗粒与饮片汤剂的药效等效性,以期为中药配方颗粒的临床应用提供参考。
1 材料
1.1 仪器TLC Visualizer 薄层数码成像仪(广州无线电集团有限公司);LC-20AT 液相色谱仪(日本岛津公司);1290 Infinity Ⅱ超高压液相色谱仪(美国Agilent 公司);T1000 十分之一电子天平和T200 百分之一电子天平(常热市双杰测试仪器厂);Sartorius BP211D 万分之一电子天平(北京赛多利斯仪器系统有限公司);XS205DU 十万分之一电子天平(德祥科技有限公司);C22-CS13 电陶炉(浙江绍兴苏泊尔生活电器有限公司);TW12 水浴箱[优莱博技术(北京)有限公司];WP-UPT-10 实验室专用超纯水机(四川沃特尔水处理设备有限公司);ZH-E11 超声雾化器(江苏航医疗设备有限公司);L5S 紫外可见分光光度计(上海仪电分析仪器有限公司);3-18R 台式高速冷冻离心机(湖南可成仪器设备有限公司);RE-5299旋转蒸发器(巩义市予华仪器有限责任公司)。
1.2 试药柚皮苷(批号:110722-201312)、野漆树苷(批号:111919-201804),中国食品药品检定研究院;咳特灵胶囊,广州白云山制药总厂,批号:4220025;苯酚红,天津市大茂化学试剂厂,批号:20160321;化橘红配方颗粒,广东一方制药有限公司,每1 g 配方颗粒相当于饮片2.0 g,编号:kl1~kl6;化橘红饮片,广东一方制药有限公司,编号:yp1~yp6;化橘红饮片,广州白云山中药饮片有限公司,编号:yp0。甲醇、乙腈为色谱纯;水为超纯水;其余试剂均为分析纯。
1.3 动物SPF 级KM 小鼠,雌雄各半,体质量(18±2)g,广州锐格生物科技有限公司,生产许可证号:SCXK(粤)2021-0059。实验动物饲养在广州中医药大学实验动物中心SPF 级动物房,实验获得广州中医药大学实验动物伦理审查委员会批准(批件号:ZYD-2022-128)。动物饲养在恒温环境下[(23±1)℃,12 h/12 h 明暗交替],自由饮食饮水,定时更换小鼠垫料,适应性喂养1 周。
2 方法与结果
2.1 化橘红配方颗粒与饮片汤剂的薄层色谱比较
2.1.1溶液的配制
(1)柚皮苷对照品溶液 取柚皮苷对照品适量,精密称定,加甲醇制成每1 mL 含60 μg 的溶液,即得。
(2)化橘红饮片汤剂供试品溶液 分别取6 批化橘红饮片各6 g,于250 mL 的烧杯中,加入100 mL水,盖上玻片,浸泡30 min;大火煮沸转小火煎煮30 min,倒出药汁至250 mL 容量瓶中;再加入80 mL水,重复煎煮30 min,合并药汁,放冷;用水定容至刻度,摇匀,精密移取25 mL 于分液漏斗中;用饱和正丁醇萃取3 次,每次25 mL;合并正丁醇萃取液,水浴蒸干,用甲醇定容至25 mL,摇匀;取4.2 mL至5 mL 试管中,置通风橱自然挥发至1 mL,即得yp1、yp2、yp3、yp4、yp5、yp6 批汤剂试供试品溶液。
(3)化橘红配方颗粒供试品溶液 分别取6 批化橘红配方颗粒3 g 于250 mL 的烧杯中,加入150 mL沸水,冲化搅拌均匀,放冷;转移至250 mL 的容量瓶中,并用水定容至刻度;摇匀,精密移取25 mL于分液漏斗中,用饱和正丁醇萃取3 次,每次25 mL;合并正丁醇萃取液,水浴蒸干;用甲醇定容至25 mL,摇匀,取4.2 mL 至5 mL 试管中,置通风橱自然挥发至1 mL,即得kl1、kl2、kl3、kl4、kl5、kl6 批颗粒供试品溶液。
2.1.2测定 吸取6 批化橘红饮片汤剂供试品溶液、柚皮苷对照品溶液和6 批化橘红配方颗粒供试品溶液各2 μL,分别点样于同一高效硅胶G 薄层板上,以乙酸乙酯-丙酮-冰醋酸-水(8∶4∶0.3∶1)为展开剂,展开,取出,晾干。喷以5%三氯化铝乙醇溶液,在105 ℃加热1 min,置紫外光灯(365 nm)下检视。结果显示化橘红配方颗粒和饮片汤剂各样品斑点高度相似,且在柚皮苷相应的位置上,均显相同颜色的荧光斑点。见图1。
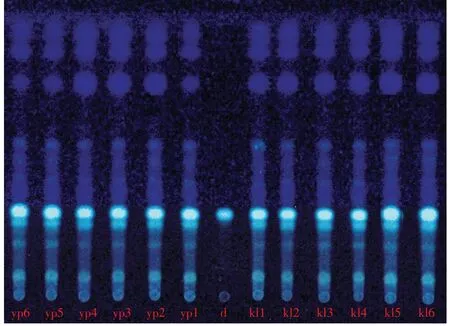
图1 化橘红配方颗粒与饮片汤剂的薄层色谱图Figure 1 TLC of Citri Grandis Exocarpium dispensing granules and their slice decoction
2.2 柚皮苷的含量测定
2.2.1溶液的配制
(1)柚皮苷对照品溶液 配制同“2.1.1”项下。
(2)化橘红饮片汤剂供试品溶液 分别取6 批化橘红饮片各6 g,于250 mL 的烧杯中,加入100 mL水,盖上玻片,浸泡30 min。大火煮沸转小火煎煮30 min,倒出药汁至250 mL 容量瓶中;再加入80 mL 水,重复煎煮30 min。合并药汁,放冷,用水定容至刻度,摇匀,精密移取25 mL 于分液漏斗中;用饱和正丁醇萃取3 次,每次25 mL,合并正丁醇萃取液,水浴蒸干,用甲醇定容至25 mL,摇匀;精密移取1 mL 至25 mL 容量瓶中,用甲醇稀释至刻度,摇匀,即得yp1、yp2、yp3、yp4、yp5、yp6 批汤剂供试品溶液。
(3)化橘红配方颗粒供试品溶液 分别取6 批化橘红配方颗粒3 g 于250 mL 的烧杯中,加入150 mL沸水,冲化搅拌均匀,放冷;转移至250 mL 的容量瓶中,并用水定容至刻度,摇匀,精密移取25 mL于分液漏斗中,用饱和正丁醇萃取3 次,每次25 mL;合并正丁醇萃取液,水浴蒸干,用甲醇定容至25 mL,摇匀;精密移取1 mL 至25 mL 容量瓶中,用甲醇稀释至刻度,摇匀,即得kl1、kl2、kl3、kl4、kl5、kl6 批颗粒供试品溶液。
2.2.2色谱条件 采用Ultimate®AQ-C18色谱柱(4.6 mm×250 mm,5 μm);以甲醇-醋酸-水(35∶4∶61)为流动相;检测波长为283 nm;柱温为30 ℃;流速为1 mL·min-1。理论塔板数按柚皮苷峰计算应不低于1 000[1]。色谱图见图2。
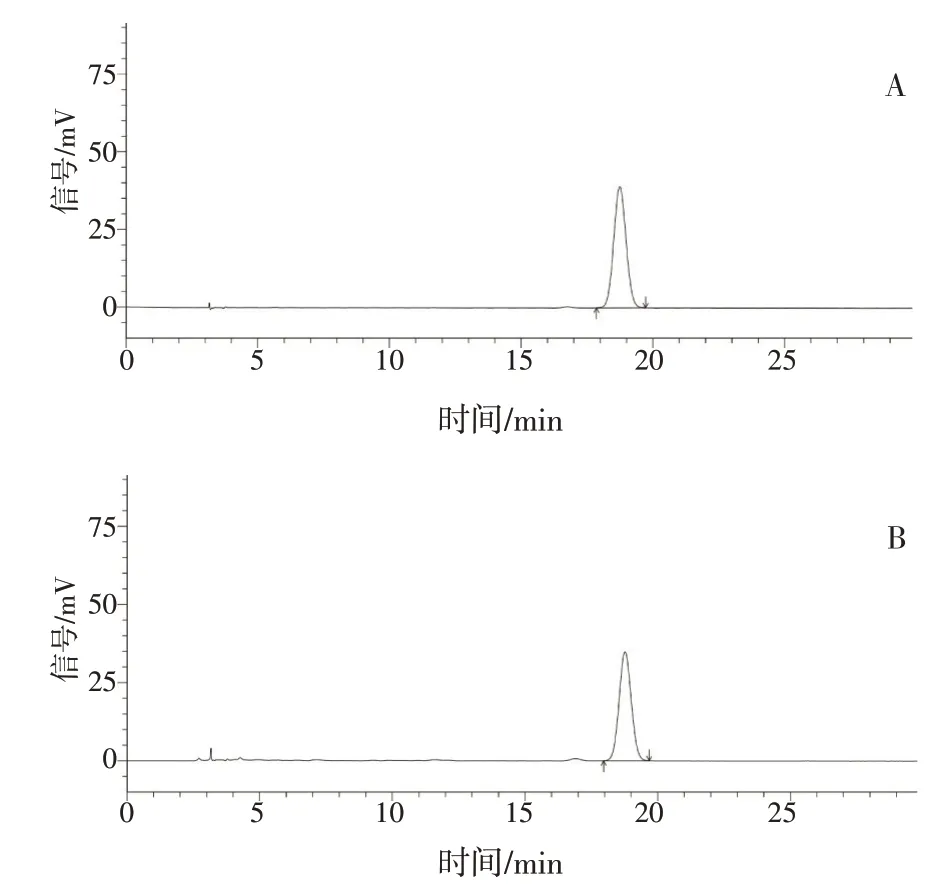
图2 柚皮苷的高效液相色谱图Figure 2 The HPLC chromatograms of naringin
2.2.3方法学研究
(1)线性关系考察 取柚皮苷对照品适量,配成柚皮苷浓度分别为6.0、15.0、30.0、60.0、150.0 μg·mL-1的系列对照品溶液,按上述色谱条件测定峰面积。以浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得柚皮苷回归方程为:Y=2.028×104X-1.434×104,相关系数(r)=0.999 9。结果表明柚皮苷在6.0~150.0 μg·mL-1范围内,线性关系良好。
(2)精密度试验 取同一份柚皮苷对照品溶液,连续进样6 次,结果柚皮苷峰面积的RSD 为0.4%,表明精密度良好。
(3)稳定性试验 取同一份yp0 供试品溶液,分别在0、1、2、4、8、16、24 h 进样,结果柚皮苷峰面积的RSD 为0.3%,表明柚皮苷在24 h 内稳定。
(4)重复性试验 分别按“2.2.1”项下化橘红饮片汤剂供试品溶液制备方法平行制备6 份yp0 供试品溶液,精密吸取各10 μL,注入液相色谱仪,测定。结果柚皮苷含量的RSD 为2.3%,表明重现性良好。
(5)回收率试验 分别精密移取重复性试验项下萃取前的溶液0.5 mL 至分液漏斗中,加入适量柚皮苷对照,加水至25 mL,混匀,用饱和正丁醇萃取3 次,每次25 mL,合并正丁醇萃取液,水浴蒸干,用甲醇定容至25 mL,摇匀。精密吸取各10 μL,注入液相色谱仪,测定。结果平均回收率为100.7%,RSD 为2.5%,表明方法准确度良好。见表1。
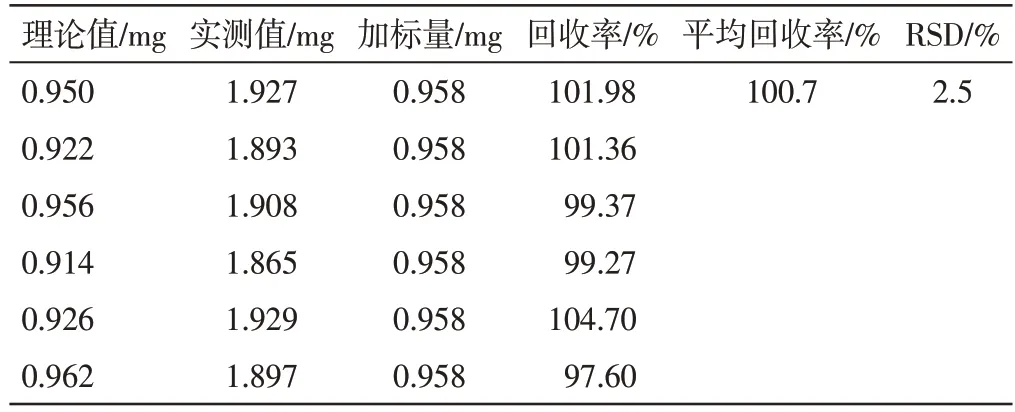
表1 柚皮苷的回收率试验结果(n=6)Table 1 Recovery test results of naringin(n=6)
2.2.4含量测定 分别精密吸取柚皮苷对照品溶液、6 批化橘红饮片汤剂供试品溶液和6 批化橘红配方颗粒供试品溶液各10 μL,注入液相色谱仪,测定。结果见表2。利用SPSS 25.0 统计软件,数据以[M(P25,P75)]表示,采用威尔科克森符号秩检验。结果化橘红配方颗粒和化橘红饮片汤剂含量差异无统计学意义(P>0.05),表明化橘红配方颗粒与化橘红饮片汤剂柚皮苷含量相当。见表2。

表2 化橘红配方颗粒与化橘红饮片汤剂中柚皮苷含量[M(P25,P75),n=6]Table 2 The content of naringin in Citri Grandis Exocarpium dispensing granules and their slice decoction[M(P25,P75),n=6]
2.3 野漆树苷的含量测定
2.3.1溶液的配制
(1)野漆树苷对照品溶液 取野漆树苷对照品适量,精密称定,用甲醇制成每1 mL 含30 μg 的溶液,即得。
(2)化橘红饮片汤剂供试品溶液 分别取6 批化橘红饮片各6 g,于250 mL 的烧杯中,加入100 mL水,盖上玻片,浸泡30 min,大火煮沸转小火煎煮30 min,倒出药汁至250 mL 容量瓶中,再加入80 mL水,重复煎煮30 min。合并药汁,放冷,用水定容至刻度,摇匀;精密移取25 mL 于分液漏斗中,用饱和正丁醇萃取3 次,每次25 mL。合并正丁醇萃取液,水浴蒸干,用甲醇定容至25 mL,摇匀,即得yp1、yp2、yp3、yp4、yp5、yp6 批化橘红饮片汤剂供试品。
(3)化橘红配方颗粒供试品溶液 分别取6 批化橘红配方颗粒3 g 于250 mL 的烧杯中,加入150 mL沸水,冲化搅拌均匀,放冷;转移至250 mL 的容量瓶中,并用水定容至刻度;摇匀,精密移取25 mL于分液漏斗中,用饱和正丁醇萃取3 次,每次25 mL;合并正丁醇萃取液,水浴蒸干,用甲醇定容至25 mL,摇匀,即得kl1、kl2、kl3、kl4、kl5、kl6 化橘红配方颗粒供试品。
2.3.2色谱条件 COSMOSIL C18(4.6 mm×250 mm,5 μm);以甲醇为流动相A,以1%冰醋酸溶液为流动相B,梯度洗脱(0~14 min,25%~55%A;14~20 min,55%~25%A;20~29 min,25%A);检测波长为266 nm;柱温为30 ℃;流速为1 mL·min-1。理论塔板数按野漆树苷峰计算应不低于3 000。色谱图见图3。
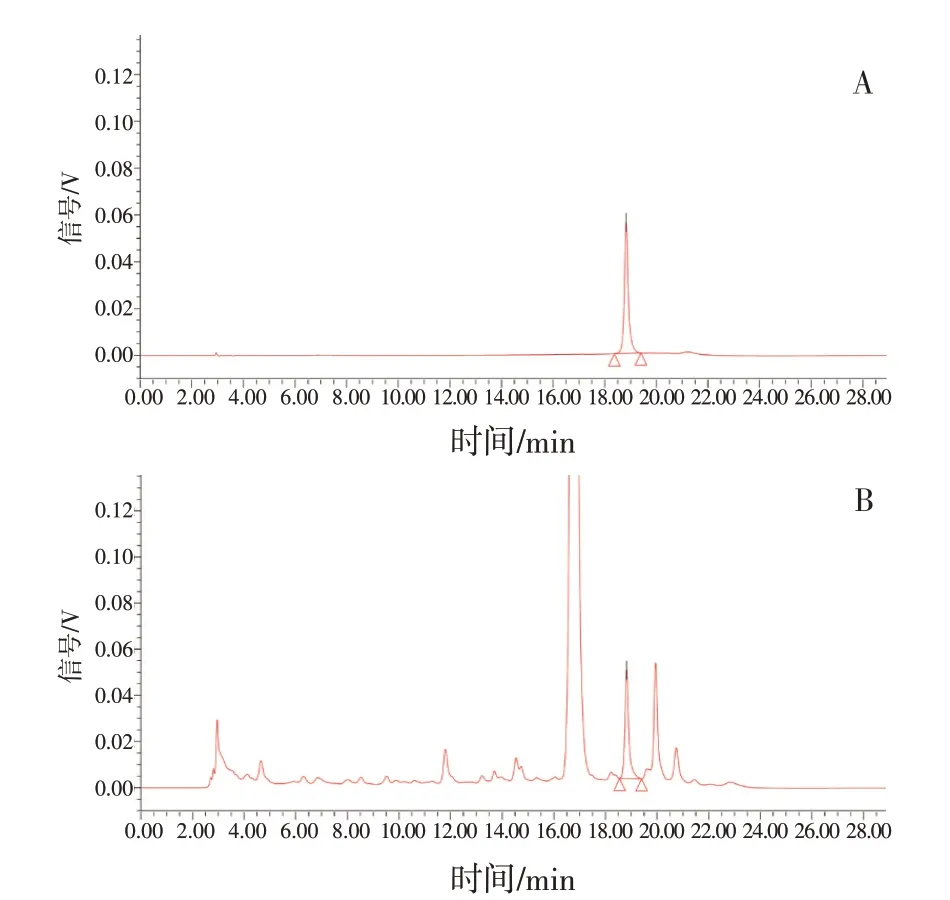
图3 野漆树苷的的高效液相色谱图Figure 3 The HPLC chromatograms of rhoifolin
2.3.3方法学研究
(1)线性关系考察 取野漆树苷对照品适量,配成野漆树苷浓度分别为2.5、12.5、31.2、62.5、125.0 μg·mL-1的系列对照品溶液,按上述色谱条件测定峰面积。以浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得野漆树苷回归方程为:Y=2.126×104X+2.027×104,相关系数(r)=0.999 7。结果表明野漆树苷在2.5~125.0 μg·mL-1范围内,线性关系良好。
(2)精密度试验 取同一份野漆树苷对照品溶液,连续进样6 次,结果野漆树苷峰面积的RSD 为0.1%,表明精密度良好。
(3)稳定性试验 取同一份yp0 供试品溶液,分别在0、1、2、4、8、16、24 h 进样,结果野漆树苷峰面积的RSD 为0.3%,表明野漆树苷在24 h 内稳定。
(4)重复性试验 分别按“2.3.1”项下化橘红饮片汤剂供试品溶液制备方法平行制备6 份yp0 供试品溶液,精密吸取各10 μL,注入液相色谱仪,测定。结果野漆树苷含量的RSD 为3.0%,表明重现性良好。
(5)回收率试验 分别精密移取重复性试验项下萃取前的溶液各12.5 mL 至分液漏斗中,加入适当野漆树苷对照品,加水至25 mL,混匀。用饱和正丁醇萃取3 次,每次25 mL,合并正丁醇萃取液,水浴蒸干,用甲醇定容至25 mL,摇匀。精密吸取各10 μL,注入液相色谱仪,测定。结果回收率为94.3%,RSD为2.7%,表明方法准确度良好。见表3。
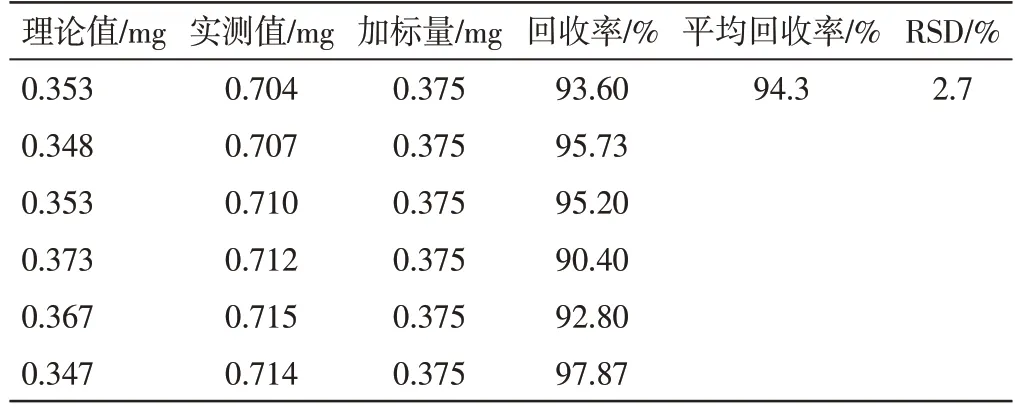
表3 野漆树苷的回收率结果试验(n=6)Table 3 Recovery test results of rhoifolin(n=6)
2.3.4含量测定 分别精密吸取野漆树苷对照品溶液、6 批化橘红饮片汤剂供试品溶液和6 批化橘红配方颗粒供试品各10 μL,注入液相色谱仪,测定。结果见表8。利用SPSS 25.0 统计软件,数据以均数±标准差(±s)表示,采用两组独立样本t检验。结果配方颗粒和饮片汤剂的含量差异无统计学意义(P>0.05),表明化橘红配方颗粒与饮片汤剂国野漆树苷含量相当。见表4。
表4 化橘红配方颗粒与化橘红饮片汤剂中野漆树苷含量(±s,n=6)Tabble 4 The content of rhoifolin in Citri Grandis Exocarpium dispensing granules and their slice decoction(±s,n=6)

表4 化橘红配方颗粒与化橘红饮片汤剂中野漆树苷含量(±s,n=6)Tabble 4 The content of rhoifolin in Citri Grandis Exocarpium dispensing granules and their slice decoction(±s,n=6)
注:*折算为饮片质量含量
序号yp1 yp2 yp3 yp4 yp5 yp6含量/%0.24 0.16 0.14 0.10 0.24 0.16含量/%0.17±0.06序号kl1 kl2 kl3 kl4 kl5 kl6含量*/%0.20 0.14 0.16 0.15 0.20 0.14含量*/%0.16±0.03
2.4 化橘红配方颗粒和饮片的特征图谱的建立与比较
2.4.1溶液的配制
(1)对照品溶液 柚皮苷对照品溶液制备同“2.1.1” 项;野漆树苷对照品溶液制备同“2.3.1”项。
(2)化橘红饮片汤剂供试品溶液 分别取6 批化橘红饮片6 g,于250 mL 的烧杯中,加入100 mL水,盖上玻片,浸泡30 min。大火煮沸转小火煎煮30 min,倒出药汁至250 mL 容量瓶中。再加入80 mL 水,重复煎煮30 min。合并药汁,放冷,用水定容至刻度,摇匀,即得yp1、yp2、yp3、yp4、yp5、yp6 批化橘红饮片供试品溶液。
(3)化橘红配方颗粒供试品 分别取6 批化橘红配方颗粒3 g 于250 mL 的烧杯中,加入150 mL 沸水,冲化搅拌均匀,放冷,转移至250 mL 的容量瓶中,并用水定容至刻度,摇匀,即得kl1、kl2、kl3、kl4、kl5、kl6 批化橘红配方颗粒供试品溶液。
2.4.2色谱条件 Waters ACQUITY HSS C18(2.1 mm×100 mm,1.8 μm);以乙腈为流动相A,0.1%甲酸溶液为流动相B,梯度洗脱(0~5 min,5%~15%A;5~10 min,15% A;10~15 min,15%~20%A;15~30 min,20%~50%A;30~35 min,50%~90%A;35~40 min,90%A);检测波长为320 nm;柱温为30 ℃;流速为0.3 mL·min-1;进样量为1 μL。
2.4.3方法学研究 精密度试验:取yp0 制备的化橘红饮片汤剂溶液,连续进样6 次,以柚皮苷色谱峰为参照峰S,化橘红各特征峰与S 峰的相对保留时间和相对峰面积的RSD 均小于3.0%,表明仪器精密度良好。重复性试验:平行制备6 份yp0 批化橘红饮片汤剂溶液,按“2.4.2”项下条件进样,以柚皮苷色谱峰为参照峰S,化橘红各特征峰与S 峰的相对保留时间的RSD 均小于3.0%,表明该方法重复性良好。稳定性试验:取同一份yp0 的化橘红饮片汤剂溶液,在0、1、2、4、8、16、24、36 h 进样,以柚皮苷色谱峰为参照峰S,化橘红各特征峰与S 峰的相对保留时间和相对峰面积RSD 均小于3.0%,表明供试品溶液在36 h 内稳定性良好。
2.4.4特征图谱测定结果 将柚皮苷对照品、野漆树苷对照品、6 批化橘红饮片汤剂溶液和6 批化橘红配方颗粒溶液,按“2.4.2”项下条件测定,记录色谱图,以6 号峰为参照峰(S),计算其他各共有峰的相对保留时间,结果其相对保留时间的RSD<0.2%。采用《中药色谱指纹图谱相似度评价系统》(2012 年版)分别建立化橘红饮片汤剂和化橘红配方颗粒对照特征图谱,并进行比较,共有峰数目相同。见图4。

图4 化橘红配方颗粒与饮片汤剂的特征图谱图Figure 4 The charactertistics chromatograms of Citri Grandis Exocarpium dispensing granules and their slice decoction
2.4.5化橘红配方颗粒与饮片汤剂的相似度比较 将6 批化橘红饮片汤剂和6 批化橘红配方颗粒的特征图谱导入《中药色谱指纹图谱相似度评价系统》(2012 年版),以yp1 样品特征图谱为参照,进行多点校正和峰匹配,并生成对照特征图谱,匹配数据后计算相似度。结果显示,6 批化橘红饮片汤剂和6 批化橘红配方颗粒与对照图谱的相似度均不低于0.9,6 批化橘红饮片汤剂与6 批化橘红配方颗粒的特征图谱之间的相似度也均不低于0.9,表明化橘红配方颗粒与饮片汤剂间成分种类基本相同,见表5。

表5 化橘红配方颗粒和化橘红饮片汤剂的相似度评价结果Table 5 Similarity evaluation results of Citri Grandis Exocarpium dispensing granules and slice decoction
2.5 氨水喷雾引咳小鼠试验(止咳试验)
2.5.1溶液的配制
(1)化橘红汤剂溶液 取化橘红饮片50 g,加入350 mL 水,室温下浸泡30 min 后开始煎煮,煎煮时间为30 min,趁热滤过;过滤后药渣加水300 mL,再继续煎煮30 min,趁热滤过;合并滤液,浓缩至少于100 mL,放冷至室温,加水至100 mL,混匀,即得0.5 g·mL-1(高剂量)的化橘红饮片汤剂。取适量高剂量药液分别稀释至0.25 g·mL-1(中剂量)和0.05 g·mL-1(低剂量)的化橘红饮片汤剂,4 ℃冰箱储存备用。
(2)化橘红配方颗粒溶液 取化橘红配方颗粒25 g,加入80 mL 沸水使溶解,放冷至室温,加水至100 mL,混匀,即得相当于化橘红饮片0.5 g·mL-1的高剂量供试液。同法制备中、低剂量化橘红配方颗粒供试液(相当于化橘红饮片0.25、0.05 g·mL-1),4 ℃冰箱储存备用。
(3)咳特灵药液 取咳特灵胶囊10 粒,倾出内容物,精密称定,称取1 粒的质量,用44 mL 温水溶解,放冷至室温,即得小叶榕干浸膏含量约为8.2 mg·mL-1、马来酸氯苯那敏含量约为0.032 mg·mL-1的咳特灵溶液,4 ℃冰箱储存备用。
(4)5%酚红溶液的制备 取5 g 苯酚红,用少量1 mol·L-1的氢氧化钠使溶解,用0.9%氯化钠溶液定容至100 mL,混匀,即得。
2.5.2分组与给药 取健康昆明种小鼠64 只,体质量(18±2)g,雌雄各半,随机分为8 组,分别为模型对照组,阳性药对照组,化橘红饮片低、中、高剂量组,化橘红配方颗粒低、中、高剂量组。模型对照组给予0.9%氯化钠溶液,阳性药对照组给予咳特灵药溶液,化橘红饮片组和化橘红配方颗粒组给予相应浓度药液,每天1 次,每次按20 mL·kg-1灌胃,连续5 d。
2.5.3方法和结果 给药前12 h 内禁食不禁水,末次给药1 h 后,将各组小鼠放入1 000 mL 钟形玻璃罩中,用12.5%氨水喷雾15 s,观察小鼠的咳嗽动作(张大嘴,腹肌收缩,有时会有咳嗽声),记录小鼠的咳嗽潜伏期(小鼠放入钟形玻璃罩中至出现咳嗽动作的时间)及2 min 内的咳嗽次数。采用SPSS 25.0统计软件分析数据,计量资料符合正态分布,采用均数±标准差(±s)表示。多组间比较采用单因素方差分析,方差齐,采用LSD 检验。
与模型对照组相比,化橘红饮片中、高剂量组和化橘红配方颗粒低、中、高剂量组咳嗽潜伏期均明显延长,差异均具有统计学意义(P<0.05)。化橘红配方颗粒与化橘红饮片相应浓度组相比,差异均无统计学意义(P>0.05)。见表6。与模型对照组相比,化橘红饮片低、中、高剂量组和化橘红配方颗粒中、高剂量组小鼠2 min 内咳嗽次数明显减少,差异均具有统计学意义(P<0.05)。化橘红配方颗粒与化橘红饮片相应浓度组相比,差异均无统计学意义(P<0.05)。见表7。可见,化橘红配方颗粒与化橘红饮片止咳效果相当。
表6 各组小鼠咳嗽潜伏期比较(±s,n=7)Table 6 Comparison of cough latency among each group of mice(±s,n=7)

表6 各组小鼠咳嗽潜伏期比较(±s,n=7)Table 6 Comparison of cough latency among each group of mice(±s,n=7)
组别模型对照组阳性对照组化橘红饮片低剂量组化橘红配方颗粒低剂量组化橘红饮片中剂量组化橘红配方颗粒中剂量组化橘红饮片高剂量组化橘红配方颗粒高剂量组潜伏期/s 23.7±6.4 38.9±8.8 26.4±5.1 31.7±9.5 43.1±6.2 44.0±3.3 51.3±6.2 53.4±4.6 P 值与模型组比较-0.000 0.442 0.027 0.000 0.000 0.000 0.000相同浓度两组比较--0.138 0.808 0.544
表7 各组小鼠2 min 内的咳嗽次数比较(±s,n=7)Table 7 Comparison of cough frequency within 2 minutes amony each group of mice(±s,n=7)

表7 各组小鼠2 min 内的咳嗽次数比较(±s,n=7)Table 7 Comparison of cough frequency within 2 minutes amony each group of mice(±s,n=7)
组别咳嗽次数/次P 值相同浓度两组比较模型对照组阳性对照组化橘红饮片低剂量组化橘红配方颗粒低剂量组化橘红饮片中剂量组化橘红配方颗粒中剂量组化橘红饮片高剂量组化橘红配方颗粒高剂量组76.1±12.3 55.7±6.8 64.9±6.8 70.9±6.0 58.7±8.7 56.4±4.8 52.6±8.9 46.6±4.7与模型组比较-0.000 0.009 0.207 0.000 0.000 0.000 0.000--0.153 0.583 0.153
2.6 小鼠酚红排泌祛痰试验(祛痰作用)
2.6.1溶液的配制 同“2.5.1”项下。
2.6.2分组与给药 分组同“2.5.2”项下。模型对照组给予0.9%氯化钠溶液,阳性药对照组给予咳特灵溶液,化橘红饮片组和化橘红配方颗粒组给予相应浓度药液,每天1 次,按20 mL·kg-1灌胃给药,连续7 d。取酚红适量,用1 mol·L-1的氢氧化钠溶液配制成每毫升含酚红2、4、6、8、10 μg 的溶液。在546 nm 波长处测定吸光度值,以酚红浓度(X)为横坐标,吸光度值(Y)为纵坐标,绘制标准曲线,得酚红回归方程为:Y=0.068 3X+0.048 6,相关系数(r)=0.999 6。
2.6.3方法和结果 试验开始前12 h 内禁食不禁水,末次给药0.5 h 后,各组小鼠分别按体质量(10 mL·kg-1)腹腔注射5%酚红溶液。0.5 h 后,处死小鼠,剪开颈部皮肤,小心分离气管(操作过程中避免出血),剥离气管周围组织,剪取自甲状软骨气管至气管分支处的一段气管放入试管。注入1 mol·L-1的氢氧化钠溶液0.1 mL 和0.9%氯化钠溶液2 mL,充分震荡,离心,取上清液,在546 nm 波长处测定吸光度。代入回归方程,计算酚红的浓度。
采用SPSS 25.0 统计软件分析,计量资料中化橘红高剂量组不符合正态分布,结果采用M(P25~P75)表示,采用曼-惠特尼检验。与模型对照组相比,化橘红饮片中剂量组和化橘红配方颗粒中、高剂量组小鼠酚红排泌明显增加,差异具有统计学意义(P<0.05),表明化橘红配方颗粒中、高剂量与化橘红饮片汤剂中剂量能促进酚红排泌。化橘红配方颗粒与化橘红饮片相应浓度组相比,差异均无统计学意义(P>0.05)。见表8。可见,化橘红配方颗粒与化橘红饮片祛痰效果相当。

表8 各组小鼠酚红排泌量的比较(n=6)Table 8 Comparison of the phenolsulfonphthalein excretion among each group of mice(n=6)
3 讨论
在化橘红配方颗粒与饮片汤剂的特征指纹图谱研究中,对比了甲醇-水、乙腈-水、乙腈-2%冰醋酸溶液、乙腈-0.1%甲酸溶液和乙腈-0.1%磷酸溶液5 种不同流动相,结果以乙腈-0.1%甲酸溶液作为流动相时,柚皮苷色谱峰峰型较好,且整体色谱峰比较丰富,故选用乙腈-0.1%甲酸溶液作为流动相进行优化梯度。在190~400 nm 范围内对供试品溶液进行扫描,在320 nm 下,色谱基线比较平稳,色谱峰信息比较丰富,所以选择320 nm 作为化橘红特征图谱的测定波长。比较了不同色谱柱[Waters ACQUITY HSS C18(2.1 mm×100 mm,1.8 μm)、Agilent SB-C18(2.1 mm×100 mm,1.8 μm)、ACE Excel Super C18(2.1 mm×100 mm,1.7 μm)]的特征图谱。结果显示,3 种色谱柱所获得的化橘红特征峰与参照峰相对保留时间的RSD 均小于3.0%,表明该方法耐用性良好。
化橘红的有效成分中黄酮类化合物含量最高,是主要的生物活性物质,柚皮苷和野漆树苷又占到总黄酮含量的84%以上[12]。李吉华[13]实验结果显示,化州柚中野漆树苷的含量远高于普通柚子,野漆树苷含量可以作为化州柚和柚来源的药材鉴别特征之一,故本研究选择柚皮苷和野漆树苷作为指标性成分来评价配方颗粒与饮片汤剂的主要成分的等量性。参考广东省地方标准DB 4409/T 06-2019[14]中野漆树苷含量测定方法的流动相,在190~600 nm 范围内对野漆树苷进行扫描,发现野漆树苷在266 nm 和337 nm 处有最大吸收。对化橘红供试品溶液进行分析,发现337 nm 下杂峰较多,266 nm 下基线较平稳,所以选择266 nm 作为野漆树苷的测定波长。对比了乙腈-水、甲醇-水、甲醇-1%冰醋酸溶液不同流动相,结果显示野漆树苷在乙腈-水中出峰比较快,与其他杂峰分离度欠佳,而在甲醇-水和甲醇-1%冰醋酸中,与其他杂峰的分离度能满足要求,且甲醇-1%冰醋酸中的理论塔板数比甲醇-水中的高,故选甲醇-1%冰醋酸作为流动相,并对梯度进行优化。比较了不同色谱柱[COSMOSIL C18(4.6 mm×250 mm,5 μm)、TechMate C18-ST(4.6 mm×250 mm,5 μm)、CAPCELL PAK C18MG(4.6 mm×250 mm,5 μm)]的色谱图,结果显示,3 种色谱柱的理论塔板数和分离度均能达到系统适用性要求,表明该方法耐用性良好。
氨水喷雾引咳小鼠试验中,化橘红饮片中、高剂量和化橘红配方颗粒各剂量均能延长咳嗽潜伏期,化橘红饮片各剂量和化橘红配方颗粒中、高剂量能减少小鼠2 min 内的咳嗽次数;相同剂量的化橘红配方颗粒与饮片汤剂对小鼠止咳潜伏期和咳嗽次数的作用均无统计学意义(P>0.05)。
小鼠酚红排泌实验中,化橘红配方颗粒中、高剂量与化橘红饮片汤剂中剂量能促进酚红排泌。但化橘红饮片高剂量组与模型对照组比较差异无统计学意义,可能与小鼠的个体差异有关。相同剂量的化橘红配方颗粒与饮片汤剂对小鼠酚红排泌量的作用差异无统计学意义(P>0.05)。
本研究结果表明,化橘红配方颗粒与化橘红饮片汤剂在化学组分上相一致,其主要成分柚皮苷和野漆树苷的含量均相当,化橘红配方颗粒与化橘红饮片止咳祛痰作用效果相当,显示化橘红配方颗粒与化橘红饮片汤剂具有化学等量性和药效等效性。
