宏基因组二代测序技术在恶性血液病并发感染中的诊断价值分析
2023-07-08姜春辉
姜春辉
(北京高博博仁医院分子诊断科,北京 100070)
感染属于临床恶性血液病患者十分常见的一种并发症,主要因患者自身免疫功能低下所致。恶性血液病患者需要接受放化疗治疗,或应用糖皮质激素、免疫抑制等药物,会对自身的免疫功能造成影响,极大程度地增加了感染的风险。目前,临床诊断恶性血液病患者是否合并感染的技术较多,包括炎症指标检测、影像学检查、病原体检测等,但传统病原体培养检测技术易出现漏诊、误诊的情况,且难以鉴别病原体类型,治疗方案也多是根据临床经验制定,可能影响治疗效果,甚至延误治疗[1]。因此,寻找一种准确、快速的诊断方法成为临床深入研究的课题。宏基因组二代测序(mNGS)技术是近几年新发展形成的病原体检测技术,能够一次检测完成百万以上碱基对的核酸序列,通过与基因组数据库进行对比,从而可鉴别病原体种类,制定针对性的治疗方案[2]。本次研究以2019 年4 月至2022 年4 月我院收治的260 例恶性血液病疑似并发感染患者为研究对象,对比分析传统病原体培养检测技术与mNGS 技术诊断恶性血液病合并感染的价值,现报道如下。
1 资料与方法
1.1 一般资料
选择2019 年4 月至2022 年4 月我院收治的260例恶性血液病疑似并发感染患者作为研究对象,其中男性140 例,女性120 例;年龄7 ~93 岁,平均年龄(45.94±5.25)岁;其中,130 例患者确诊为急性髓系白血病,74 例患者确诊为急性淋巴细胞白血病,24 例患者确诊为骨髓增生异常综合征,14 例患者确诊为淋巴瘤,18 例患者确诊为其他恶性血液病。纳入标准:(1)确诊为恶性血液疾病,且符合相关诊断标准;(2)体温超过37.5℃,考虑并发感染;(3)同意配合本次诊疗研究。排除标准:(1)临床资料缺失;(2)样本污染;(3)抵触配合研究。本研究取得医院伦理委员会批准。
1.2 方法
1.2.1 样本采集 对患者临床症状的发作情况进行统计和评估,于寒战或高烧发作的预估高峰前30 ~50 min采集检验样本,包括:外周血、脑脊液、支气管灌洗液、胸腹水等。
1.2.2 传统病原体培养方法 体液样本均使用血培养仪培养,并对样本中的病原体种类给予鉴别,严格按照生产厂家提供的说明书进行操作。
1.2.3 mNGS 检测方法 体液样本采集后放于室温下保存并立即检测。提取体液中的游离核酸,需要将样本以4000 r/min 的转速离心10 min,取上层清液进行DNA 提取,使用柱提法进行微生物DNA 提取。取适量纯化后的DNA 样本,在DNA 片段化的同时采用转座酶法进行末端修复和接头的连接,以确保低起始量的DNA 建库成功。DNA 文库纯化后进行PCR 富集,利用Realtime 方式对文库浓度进行绝对定量,以Q-Sep 100 进行插入片段大小的质控。待文库质控确认无误后,使用Nextseq550 测序仪上机测序,有效数据不少于20 M。测序完成后,利用生物信息软件对DNA 序列信息给予分析。先通过测序标签对样本进行拆分、剪切接头、过滤掉低质量片段及长度低于35 bp 的序列等操作,获取高质量的DNA 序列。再将其与病原数据库中的参考序列进行比较,比对成功的序列要再去除高重复序列(duplication)、低质量比对序列等。根据生物信息分析后得到的结果计算检出病原的参数,包括比对序列数、覆盖度以及测序深度等。对数据库中的细菌、真菌、病毒等分类标准进行结果判读。
1.3 观察指标
(1)检出率、敏感性、特异性。以临床综合诊断结果为金标准,分别计算传统病原体培养检测技术与mNGS 技术对恶性血液病并发感染的检出率,以及诊断恶性血液病并发感染的敏感性与特异性。细菌/ 病毒阳性标准:覆盖率超过其他微生物10 倍以上;真菌阳性诊断标准:覆盖率超过其他真菌5 倍以上。敏感性= 真阳性例数/(真阳性例数+ 假阳性例数)×100.00% ;特异性= 真阴性例数/(真阴性例数+假阴性例数)×100.00%。(2)多种病原菌检出率。分别计算两种诊断技术对不同病原菌的检出率。
1.4 统计学方法
以SPSS 25.0 软件作为结果统计学分析的专用处理软件,% 作为计数资料结果记录的格式,用χ² 检验,±s作为计量资料结果记录的格式,用t检验,P<0.05 表示具有统计学差异。
2 结果
2.1 传统病原体培养、mNGS 技术的检测结果
260 例恶性血液病患者经临床综合判断,确诊186 例患者并发感染,占比71.54%。传统病原体培养、mNGS 技术的检测结果如表1 所示。

表1 传统病原体培养、mNGS 技术的检测结果(例)
2.2 传统病原体培养、mNGS 技术诊断敏感性、特异性的比较
通过计算,mNGS 技术诊断恶性血液病合并感染的敏感性、特异性均明显高于传统病原体培养检测技术(P<0.05)。详见表2。
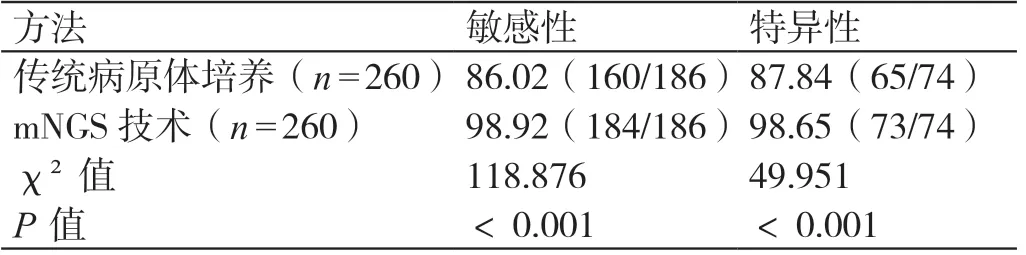
表2 传统病原体培养、mNGS 技术诊断敏感性、特异性的比较[%(例/例)]
2.3 传统病原体培养、mNGS 技术对多种病原菌的检出率
通过计算,mNGS 技术检出细菌、真菌及病毒的阳性率均明显高于传统病原体培养检测技术(P<0.05)。详见表3。

表3 传统病原体培养、mNGS 技术对多种病原菌的检出率[例(%)]
3 讨论
并发感染是临床患者病情快速加重或死亡的重要诱因。感染产生的多种炎性因子具有不同的细胞毒性,可直接对组织、系统的功能产生影响,给机体造成更大的负荷。尤其对于恶性血液病群体而言,其本身便有全身性症状,并伴有机体的免疫功能下降,同时需接受化疗、放疗、靶向治疗等多种方式干预,易引发骨髓抑制等问题,因此恶性血液病患者均表现出不同程度的免疫功能衰退特性,使其成为院内感染的高危群体[3-4]。此外,恶性血液病患者体内的粒细胞数量大幅度减少,甚至部分群体可能出现粒细胞缺乏的问题,这种情况会造成感染病原体后无法形成具有感染特性的病灶,最终严重影响临床对感染病原体种类的判断,延误治疗时机,甚至可引起多重病原体感染,使患者的病情在短时间内快速恶化。近年来,凭借现代医疗技术的不断革新和完善,虽然恶性血液病患者的死亡率得到一定控制,但并发感染后引起死亡的概率仍居高不下。国内大数据统计显示,恶性血液病患者并发感染后的死亡率可达23% 左右,而此类患者并发感染的概率则超过了50%,尤以血液系统、呼吸系统感染占比最高,前者的发生率甚至占所有恶性血液病并发感染的1/3 以上。因此,临床上在治疗恶性血液病并发感染时,需要快速、准确地判断导致感染的病原体种类,以便采取针对性的抗菌治疗措施,在最短的时间内控制感染,避免患者的病情加重,缩短整体治疗周期[5-6]。
既往临床针对感染的诊断方法以病原学检测为主,可通过分离、提纯样本中的微生物,并进一步培养,从而获得具体的微生物种类,使用的方法有免疫学检测、PCR 技术、微生物培养等。但这些方法均存在一定的局限性,即鉴别的准确性完全依赖于分离的活体菌株,若分离活体菌株的数量不足,则体外培养结果可能存在偏差,加之该培养过程需要至少48 h,而部分真菌、结核分枝杆菌等对外界生存环境要求苛刻的病原体种类所需的培养时间还会被进一步延长,甚至部分菌株完全不适合在体外分离培养,故可导致漏检、误检等问题[7]。在临床实践工作中,通过血样微生物培养方式得出的阳性率相对较低,且精准度也欠缺,加之消耗的周期较长,因而正在被逐渐淘汰。免疫学检测中的抗原/ 抗体检测可通过人体受到抗原刺激后产生的特异性抗体完成检测,从而快速、准确地判断病原体种类,但实际操作过程中会受到抗原包被、洗涤等客观因素的影响,导致假阳性问题的出现。同时,该检测技术在病毒种类的鉴别方面存在一定的不足,尤其是针对具有快速变异特性的病毒而言,检出率极低[8]。分子诊断技术属于新型检测技术的一种,但需借助PCR 技术对已知特定的核酸序列给予分辨,操作时需设计特定的引物,消耗的时间过长,且若患者存在多重感染的情况,会进一步增加检验的难度。近年来,随着医学界对恶性血液病研究的不断深入,发现此类患者并发感染时出现混合型、多重耐药菌感染的概率越来越高,使得病原体谱系越发复杂,给病原体的鉴别工作提出了更高的要求,传统检验方式越来越不适应现代临床需求。
mNGS 技术属于新型非靶向、广谱病原体筛查技术之一,能够获得采集样本中所有病原体的基因核酸片段,且无需对各片段给予分离、提纯等处理工序,大幅节省了整体检查时间,并且在检查过程中不会出现偏移现象。该技术的优势在于检测速度快、通量高、敏感度高、准确性高、覆盖面广等,可用于快速、精准检测病原体的工作当中[9]。mNGS 技术能够实现对病原体种类的全覆盖检测,且测序技术无偏倚性缺陷,因而敏感性、准确性均相对较高。该技术在检测DNA、RNA 核酸序列时使用的是平行排列测序法,从而能够实现对所有感染病原体的鉴别,为后续靶向治疗方案的拟定提供准确的参考,最大程度地减少了漏诊、误诊情况的发生,同时也能够缩短获取病原体种类的时间,为早期的抗感染治疗提供了保障,避免患者的病情进一步恶化,并减少了多重耐药菌株的出现。但需要注意的是,实际采样过程中无法完全避免核酸污染的情况,加之人体内本身也含有部分菌群,使得感染群体的原生菌群鉴别难度增加,因此操作过程中必须严格遵照无菌操作标准,最大程度地避免核酸污染的发生[10]。同时,mNGS 技术在应用时需标明检出基因的序列数,再参照人类现有的病菌基因数据库进行对比,从而判断、鉴别所感染的病原菌种类。但由于mNGS 结果的产生存在较高的复杂性,因此通常将检出序列数值最高者认定为病原体的主要数据,而少部分病原体的基因序列数值偏低,这类病菌在检测时往往会被认定为疑似病原体。另外,各地区医院搭建的病原菌数据库标准不同、解读人员依照的标准不同,使得不同医院间的诊断标准缺乏统一性,患者转院后的检查报告可能存在出入[11]。除此之外,虽然近几年国家对于医疗费用的控制仍在不断加强,使得多项临床检查的成本得以降低,其中就包括基因测序鉴别(目前国内大多数医院已经实现了“千元级”的基因测序),但对于普通群众来说仍属于高额医疗成本[12]。且mNGS 技术常被应用于重大疾病、突发性公共卫生事件、重症感染、免疫缺陷人群的检查等工作当中,这也使得其临床应用受到极大限制。
总之,临床可利用mNGS 技术诊断恶性血液病患者是否并发感染,具有较高的准确率和敏感性,同时可判断具体的病原体种类,为进一步制定治疗方案提供依据及支持,值得临床运用推广。
