不同规格鲎试剂对人血白蛋白热原进行检测的对比分析
2023-07-08佘姣姣张宝献龚志明何小锋刘泽彬
佘姣姣,张宝献,龚志明,何小锋,刘泽彬,高 语,谭 娜,刘 利,杨 柳
(华兰生物工程重庆有限公司,重庆 408100)
热原是人血白蛋白质量检测的重点项目之一。在人血白蛋白的整个生产过程中,包括采浆融浆、分离纯化、超滤浓缩、制备原液、稀配半成品和分装成品等生产环节。其中越接近最终成品的环节越容易引入细菌内毒素,可以直接进入成品的成分、分装成品的内包材和环境为检查重点。制备半成品所使用的原液、制备原液前相关环节(如纯化环节、超滤环节)的取样、原辅料(如稀配成品的溶液、稳定剂)、半成品和分装用的内包材均为重点检测样品。目前,各生产单位多以细菌内毒素检查法对人血白蛋白进行热原检查。由于鲎试剂的特异性,相关人血白蛋白生产过程pH 值的变化较大,这可能对内毒素的检测造成影响,从而引起假阴性;鲎试剂灵敏度改变、检查用水中内毒素含量超标、反应条件(空气流动性、pH)及内毒素工作标准品的稳定性差均可影响检测结果;人血白蛋白中组成成分极其复杂,任何离子干扰(Fe3+、Al3+等离子)或非内毒素的鲎反应等都可能造成假阳性[1-2]。目前,中国药典中并没有针对细菌内毒素检查法假阴性和假阳性问题的有效解决方案,只能在实验中采用适当的方法消除或减少假阴性和假阳性的出现。有研究指出,可通过对供试品进行更大倍数的稀释或通过过滤、中和、透析、加热处理等方法排除相关干扰。本文以《中国药典》(四部)2020 年版(以下简称《中国药典》)通则中的“1143 细菌内毒素检查法”“9251细菌内毒素检查法”为指导原则,采用凝胶法对人血白蛋白热原检测所需的鲎试剂生产厂家、灵敏度,供试品稀释倍数进行选择,旨在为建立该品种的细菌内毒素检查法提供科学依据。
1 材料
1.1 仪器
CU-600 型电热恒温水槽( 武汉恒丰中欣生物有限公司);T246 型漩涡混合仪振荡器( 上海瀚默机电科技有限公司);SFG-02B 型电热恒温鼓风干燥箱( 湖北恒丰医疗制药设备有限公司) ;其他器皿包括试管、移液器及移液器配套的枪头(无热原) 等。
1.2 药品与试剂
人血白蛋白〔Human Albumin;批号202008056,规格:10 g/ 瓶(10 g/L,50 mL);批号202008058,规格:10 g/ 瓶(10 g/L,50 mL);批号202008059,规格:10 g/ 瓶(10 g/L,50 mL);批号202008057,规格:5 g/ 瓶(5 g/L,50 mL);批号202008060,规格:5 g/ 瓶(5 g/L,50 mL);批号202008063,规格:5 g/ 瓶(5 g/L,50 mL)〕;鲎试剂(A 厂家,0.03 EU·mL-1、批号2006122,0.06 EU·mL-1、批号2002213/2009093/2012243,0.125 EU·mL-1、批号2005062,0.25 EU·mL-1、批号2003112,规格0.1 mL/支;B 厂家,0.03 EU·mL-1、批号20081029,0.06 EU·mL-1、批号20051022,0.125 EU·mL-1、批号20091032,0.25 EU·mL-1、批号20081030,规格0.1 mL/ 支) ;细菌内毒素工作标准品(A 厂家,批号1912102,规格10 EU/支);细菌内毒素检查用水(Water for Bacterial Endotoxins Test,以下简称BET 水,A 厂家,批号1906270,规格5 mL/ 支)。
2 方法与结果
2.1 鲎试剂灵敏度复核
A、B 两个厂家分别取4 批鲎试剂灵敏度的标示值(λ),将细菌内毒素工作标准品用BET 水溶解,置漩涡混合器上混匀5 min,然后制成浓度为2 λ、1 λ、0.5 λ 和0.25 λ 四个浓度的内毒素标准溶液,每稀释一步均应在漩涡混合器上混合30 s。取不同浓度的内毒素标准溶液,分别与等体积(0.1 mL)的鲎试剂溶液混合,每一个内毒素浓度平行做4 管;另外取2管加入等体积的BET 水作为阴性对照。按《中国药典》通则中“1143 细菌内毒素检查法”复核本试验所用鲎试剂的灵敏度,结果两个厂家各4 批鲎试剂灵敏度的测定值(λc)均在0.5 ~2.0 λ 范围内,符合《中国药典》中的规定,可用于细菌内毒素检查,详见表1。
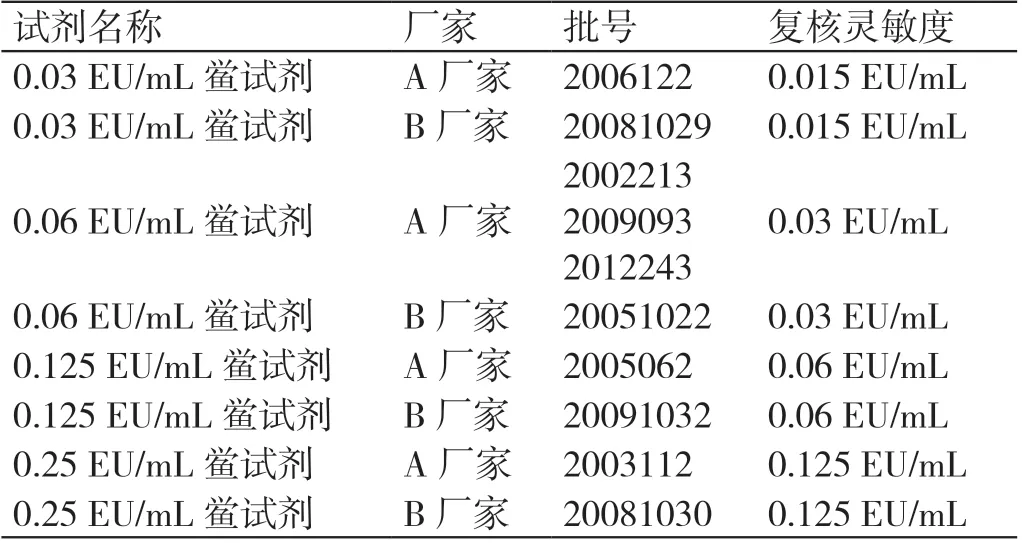
表1 鲎试剂灵敏度复核结果汇总
2.2 确定供试品最大有效稀释倍数
我司主要在产的人血白蛋白的规格分别为蛋白质浓度5 g/L、10 g/L,《中国药典》(三部)2020 年版人血白蛋白检定规程中规定其细菌内毒素限值(L)应分别小于0.83 EU/mL、1.67 EU/mL。按《中国药典》2020 年版通则中的“1143 细菌内毒素检查法”的规定,MVD=cL/λ,计算各灵敏度鲎试剂对应的样品最大有效稀释倍数(Maximum Valid Dilution,MVD) :MVD0.03=27(5 g/L)、MVD0.03=55(10 g/L)、MVD0.06=13(5 g/L)、MVD0.06=27(10 g/L)、MVD0.125=6(5 g/L)、MVD0.125=13(10 g/L)、MVD0.25=3(5 g/L)、MVD0.25=6(10 g/L);在不超过对应MVD 的稀释倍数下进行细菌内毒素检查。
2.3 干扰试验
采用A 厂家和B 厂家两个厂家的鲎试剂,4 种灵敏度(0.03 EU/mL、0.06 EU/mL、0.125 EU/mL、0.25 EU/mL)对5 g/L 和10 g/L 人血白蛋白待包装产品各3批进行干扰试验确认。5 g/L 的产品加BET 水分别稀释至初始浓度的1、6、13、27 倍备用;10 g/L 的产品加BET 水分别稀释至初始浓度的2、13、27、55 倍备用。以相应供试品溶液作稀释用液将细菌内毒素标准品逐步配制成干扰试验系列溶液:2 λ、1 λ、0.5 λ、0.25 λ;将细菌内毒素标准品用BET 水逐步配制成鲎试剂标示灵敏度对照系列溶液:2 λ、1 λ、0.5 λ、0.25 λ。按细菌内毒素检查法进行干扰试验,结果见表2。
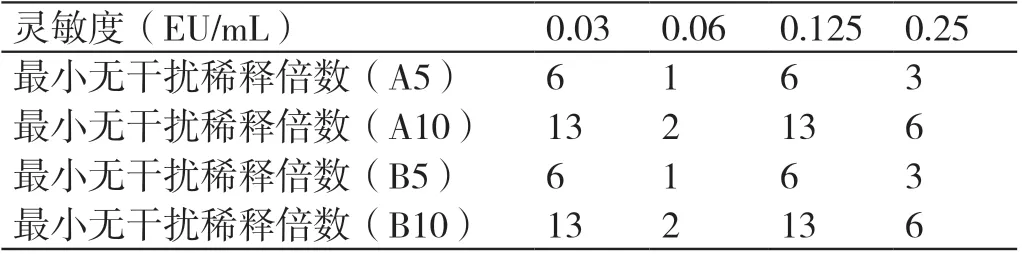
表2 人血白蛋白鲎试剂干扰试验结果
由表2 可知,灵敏度为0.06 EU/mL 的鲎试剂用于检测人血白蛋白热原的效果最佳,具有高灵敏度、少稀释的优势。试验结果表明,人血白蛋白对鲎试剂多表现为阴性干扰,即常出现假阴性,这可能与人血白蛋白中含有螯合剂、丝氨酸蛋白酶抑制剂等有关。另外,不同规格人血白蛋白的干扰物质有差异。
2.4 中间产品细菌内毒素检查
我司人血白蛋白的生产工艺流程是:由融浆经分离纯化、超滤浓缩等步骤制备原液,再由原液加稳定剂及稀释液等稀配成半成品,再将经巴氏灭活的半成品分装为待包装产品。生产过程中超滤等步骤可有效控制热原含量。有研究指出,巴氏灭活也可一定程度降低热原含量[3]。因此,理论上人血白蛋白待包装产品的热原含量最低。取5 g/L、10 g/L 人血白蛋白半成品、原液、待包装产品为供试品,使用灵敏度λ 为0.06 EU·mL-1的鲎试剂,按所建立方法进行细菌内毒素检查,结果见表3、表4。

表3 5 g/L 中间产品细菌内毒素检查结果

表4 10 g/L 中间产品细菌内毒素检查结果
结果表明,待包装产品的热原含量最低,原液与半成品的热原含量无必然关系。这是由于生产过程中原液经超滤浓缩滤去了热原物质,但在配制半成品的过程中有添加辅料,存在引入热原物质的风险。因此,试验结果与生产实际相符。
3 讨论
由于人血白蛋白生产过程需要加入多种稳定剂和稀释液,因此其组成成分极为复杂。大分子量血浆蛋白的疏水基团结合脂多糖影响内毒素活性、含有丝氨酸蛋白酶、Fe3+、Al3+等的干扰[4-5]以及非内毒素的鲎反应均可能造成检测结果的假阳性和假阴性,本文在尽可能少处理样品的前提下,选出了适宜规格的鲎试剂及供试品稀释方法。本次试验结果表明,在对供试品作最少处理的前提下,选用灵敏度λ 为0.06 EU·mL-1的鲎试剂,可适应人血白蛋白细菌内毒素检查的不同质量控制要求,具有简便、灵敏、快速、准确等优点。另外,巴氏灭活也可一定程度降低热原含量。
