蛇纹石中和渣制备氧化铁红和回收镍的工艺研究
2023-07-06吴玉楼杨喜云高凌宇陈莹丽
吴玉楼,杨喜云,高凌宇,陈莹丽
(中南大学 冶金与环境学院,湖南 长沙,410083)
有色冶金工业常会产生各种含铁渣,这些冶金渣常会带来不同程度的环境问题,传统的处理方案是堆存填埋或转化为建筑材料。冶金渣中常会伴随着大量的铁以及有价金属,如黄钾铁矾渣[1]、硫铁矿烧渣[2]、中和渣[3]。随着酸雨的加剧,重金属会进入土壤污染环境,必须将其回收[4]。目前,含铁冶金渣分离有价金属同时制备氧化铁红已经有大量的报道[5]。对于铁含量低于60%(质量分数)的铁渣,多采用传统的湿法处理工艺,即酸浸—还原—净化—沉铁[6]。
在蛇纹石制备镁产品工艺中,采用氧化镁中和蛇纹石酸浸液得到的中和渣含有大量Fe(质量分数36%)以及少量的Mg、Al、Cr、Ni、Co 和Mn 等有色金属[7]。关于蛇纹石中和渣的回收利用还没有相关的报道。实验发现,该中和渣与冶炼铁渣相似,极易溶于稀酸,适合采用传统的酸浸—还原—净化—沉铁工艺进行回收利用。但是蛇纹石中和渣与常规的冶炼铁渣相比,有色金属种类多、含量低,且含有一定量的镁,只能走低成本综合回收路线。传统工艺需要消耗大量的碱来中和酸浸中的余酸,大量的还原剂还原Fe3+,这些都会大大提升工艺成本,难以在工业中实现大规模生产。硫铁矿分为黄铁矿和磁黄铁矿,常作为选矿尾矿[8],成本低廉。黄铁矿FeS2[9]与磁黄铁矿Fe1-xS[10]都是还原剂,具有很好的还原性,可将溶液中Fe3+还原为Fe2+。磁黄铁矿还原时,多硫化物形成H2S,消耗溶液中H+,使pH 提高,导致Fe3+水解[11];温度越高,pH升高越多,Fe3+水解越严重[12]。而黄铁矿还原过程主要是Fe—S键的断裂,多硫化物形成硫酸,导致溶液pH 下降[13]。因此,采用由黄铁矿与磁黄铁矿组成的红透山天然硫铁矿作为还原剂,在还原的同时还能避免pH 快速提升,避免Fe3+水解,节省了还原剂和部分中和剂的成本。
在此,本文以蛇纹石酸浸液中和渣为原料、红透山硫铁矿为还原剂低成本回收中和渣中的Fe、Ni、Co 和Mn,制得高附加值氧化铁红和镍精矿,研究红透山硫铁矿还原中和渣酸浸液的反应过程以及温度的影响,同时探究除去Al、Cr,回收Ni、Co和Mn以及制备氧化铁红的最佳工艺条件。
1 实验
1.1 原料
中和渣来源于蛇纹石酸浸除杂中试试验,采用ICP-MS 分析各元素含量,结果如表1 所示,铁氧化物的物相分析结果如表2所示。硫铁矿来自辽宁省抚顺市红透山,干燥后经过球磨机械活化2 h后备用,采用XRF 分析各元素含量,结果如表3所示。NaOH和Na2S(国药集团生产)均为分析纯。

表1 中和渣的化学成分(质量分数)Table 1 Chemical composition of neutralization sludge%

表2 中和渣中铁氧化物的物相分析(质量分数)Table 2 Physical analysis of iron oxide in neutralization sludge %
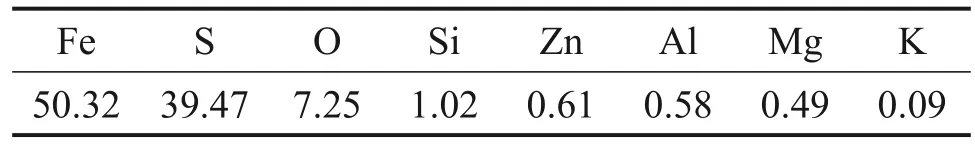
表3 硫铁矿的化学成分(质量分数)Table 3 Chemical composition of pyrite %
1.2 氧化铁红的制备过程
工艺流程图如图1所示。

图1 蛇纹石中和渣回收工艺流程图Fig.1 Flow chart of recovery of neutralization sludge
步骤1) 中和渣酸浸。采用1.4 mol/L 硫酸,控制液固比10:1,85 ℃浸出10 min,即得到中和渣酸浸液。
步骤2) 硫铁矿还原酸浸液。将100 mL 中和渣酸浸液与35 g 红透山硫铁矿加入容积为250 mL 的三颈烧瓶中,置于水浴锅中恒温,搅拌速度为500 r/min。还原反应一段时间后过滤得到还原液,反应后的硫铁矿洗涤、烘干、称质量。
步骤3) 中和沉淀去除Al 和Cr。将100 mL 还原液加入三颈烧瓶,达到一定温度后,采用蠕动泵将1 mol/L NaOH以一定流速加入以调节pH,达到指定的pH 后恒温陈化反应一段时间,然后过滤,滤液用于下一步处理。
步骤4) Na2S沉淀回收Ni、Co 和Mn。取100 mL除Al和Cr后的滤液恒温加热,采用蠕动泵以3 mL/min流速将0.1 mol/L Na2S加入滤液中,加完料后反应1 h,然后过滤得到纯净的FeSO4溶液,滤渣经洗涤、干燥后溶解于稀盐酸中,稀释至不同倍数用于ICP检测。
步骤5) 碳铵沉铁制备氧化铁红。取100 mL一定浓度纯化后的FeSO4溶液,采用0.5 mol/L NaOH调节pH,以用量系数1.5加入碳酸氢铵,采用空气压缩机以200 mL/min 的流速通入空气,在一定温度下反应5 h,过滤得到氧化铁黄,将氧化铁黄洗涤干燥,研磨后放入马弗炉,在一定温度下煅烧2 h得到氧化铁红。
1.3 分析检测
采用重铬酸钾法测定铁浓度[14],并采用ICPOES 分析Ni、Co、Al、Cr 和Mn 含量。采用XRD对还原反应前后硫铁矿进行物相分析,采用XRF对还原反应前后硫铁矿元素含量进行分析,采用SEM-EDS 观察还原反应过程硫铁矿的形貌和元素分布。以三环颜料公司产品H101为参照,采用比色计测定氧化铁红的着色力。
式中:CSO24-为质量浓度,g/L;m0为恒质量的坩埚质量,g;m为坩埚最终质量,g;V为待测液体积,L。
采用XRD和XRF定量分析反应后硫铁矿中单质S的质量分数[15],并计算反应产生的S质量。
式中:ms为反应产生的S质量,g;X0和Xt分别为反应前后硫铁矿中单质S 的质量分数,%;M0和Mt分别为反应前后硫铁矿质量,g。
根据式(3)计算反应产生的H2S质量。
式中:mH2S为反应产生的H2S 质量,g;V0为反应溶液体积,L;a为反应初始pH;b为反应后pH;MH2S为H2S相对分子质量。
2 结果与讨论
2.1 硫铁矿还原中和渣酸浸液
采用硫酸浸出中和渣,在85 ℃、液固比10∶1条件下浸出10 min,得到酸浸出液主要元素组成如表4所示。

表4 中和渣硫酸浸出液中主要金属离子质量浓度Table 4 Main metal ion mass concentration in sulfate leaching solution of neutralization sludge g/L
2.1.1 反应温度对还原过程的影响
在还原时间为80 min 的条件下,考察反应温度对还原效果的影响,结果如图2所示。当反应温度为70~85 ℃时,随着温度升高,总Fe 和Fe2+质量浓度不断提高,Fe3+质量浓度不断降低,说明提高温度可以促进硫铁矿对Fe3+还原。而在85~95 ℃时,随着反应温度的升高,总Fe 和Fe3+质量浓度不断提高,但Fe2+质量浓度开始降低。在常压下,温度为20~100 ℃时,黄铁矿还原过程主要按照反应方程式(4)~(6)进行,发生氧化性溶解,Fe2+进入溶液,多硫化物形成硫酸或者单质硫[12]。磁黄铁矿还原过程与黄铁矿类似,发生氧化性溶解。另外,还会发生非氧化性溶解,按照反应式(7)~(9)进行[10]。由于磁黄铁矿氧化溶解与非氧化溶解处于竞争关系,较高的温度使得多硫化物没有参与Fe3+还原而是发生非氧化溶解形成H2S[16],磁黄铁矿氧化溶解不断受到非氧化溶解的抑制,最终使得硫铁矿的总还原能力随着温度提高不断降低。因此,还原最佳温度为85 ℃。

图2 温度对Fe2+和Fe3+质量浓度的影响Fig. 2 Influence of temperature on Fe2+ and Fe3+ mass concentration in reduction solution
2.1.2 反应时间对还原过程的影响
通过XRD 分析不同反应时间的红透山硫铁矿的组成,结果如图3 所示。从图3 可见,反应前,红透山硫铁矿主要含有FeS2、Fe7S8和S8;反应后,硫铁矿的物相没有发生变化,但是各个衍射峰强度增大。在28.78°、33.38°、37.32°、41.00°处观察到了立方结构的黄铁矿衍射峰;在30.17°、34.05°、43.90°、53.37°处观察到了六方结构的磁黄铁矿衍射峰;在17.64°、23.34°处观察到了S8衍射峰。采用Jade 软件分析得到黄铁矿与磁黄铁矿质量比为41∶9,接近4∶1[17]。而ALMEIDA 等[18]研究了黄铁矿与磁黄铁矿质量比为4∶1时的混合电化学行为,发现在磁黄铁矿存在的情况下,2种矿物会形成原电池,使得黄铁矿氧化溶解更加容易形成硫,当电极电位>0.8 V 时,有利于形成H2SO4,电极电位<0.8 V时,有利于多硫化物的形成[18]。通过式(10)[19]计算了各反应时间的氧化还原电位E,标准电极电位Eϴ由兰氏化学手册[20]查得。

图3 不同反应时间的硫铁矿XRD图谱Fig. 3 XRD patterns of pyrite for different reaction time
式中:E为电极电位,V;Eϴ为标准电极电位,V;R为摩尔气体常数,J/(mol·K);T为反应温度,K;n为电子转移数;F为法拉第常数,C/mol;CFe3+和CFe2+分别为Fe3+和Fe2+的质量浓度,g/L。
当pH 为0.94、温度为85 ℃、Fe3+质量浓度为36 g/L、Fe2+质量浓度为0.05 mg/L时,计算得到电极电位为1.19 V。在此条件下,采用红透山硫铁矿对酸浸液进行还原,不同反应时间的还原效果如图4(a)和(b)所示。从图4(a)和(b)可见,随着反应时间的延长,总Fe和Fe2+质量浓度不断提高,Fe3+质量浓度不断降低,电极电位降低,pH 升高。初始电极电位为1.188 V,大于0.8 V,红透山硫铁矿还原的主要产物为Fe2+和硫酸,溶液pH 并没有随之降低反而不断提高,说明了磁黄铁矿的非氧化溶解同步进行,反应剧烈。随着时间的推移,电极电位不断降低,反应时间大于10 min 时,电极电位低于0.8 V,硫铁矿氧化溶解偏向于形成单质硫,非氧化性溶解产生H2S,使得pH 上升。当反应进行150 min 时,Fe3+基本反应完全,氧化性溶解已经不再进行,但是磁黄铁矿仍然可以按照如式(11)[12]发生反应,pH 不断提高。当反应进行260 min 后,pH 达到2.9,继续延长时间,pH 变化非常缓慢,主要由于机械活化带来的高活性位点基本反应完全,为了防止Al 和Cr 水解,选择260 min作为最佳反应时间。

图4 反应时间对硫铁矿还原过程的影响Fig. 4 Influence of time on reduction of pyrite
采用XRF对反应前后的硫铁矿进行物相分析,XRF结果如图4(c)所示。可见:反应过程中,S的质量分数不断增加,Fe 的质量分数不断降低,其他元素在较小的范围内波动。这是因为Fe 更加容易溶出,而S会在表面形成多硫化物,只有部分发生分解。
结合反应式(7)~(9)计算得到反应过程中硫产物生成量的变化如图4(d)所示。可见:在0~3 h 时,硫产物生成量快速提高,3 h 后生成量趋于平稳。在pH=0.94、反应温度85 ℃、初始电极电位为1.19 V的条件下,根据式(12)~(15)计算得到硫转化产物组成为51.33%S、16.05%H2SO4和32.62%H2S,由于本体系在85 ℃下,为酸性环境,电位不断降低,因此与ALMEIDA等[18]研究的混合矿物电极反应产物不同,不同的氧化还原电位变化使得产物S与H2SO4的物质的量比也不同。
反应前后硫铁矿的SEM 照片如图5(a)所示。可见:反应过程中,红透山硫铁矿由片形堆积状向球形堆积态转化,并且反应后的矿物并没有发现有明显的S 包裹,说明在85 ℃下,硫铁矿表面溶解较为完全。与电极上的反应相比,加入搅拌容易导致生成的S 漂浮起来。260 min 硫铁矿EDS面扫描结果如图5(b)所示。可见:Fe和S的质量分数分别为15%和69%,说明硫铁矿不同面反应活性不一样[8]。采用EDS分析同一颗粒不同位点元素结果如图5(c)~(e)所示。可见:点1、2、3 处Fe 的质量分数分别为56.95%,53.38%,72.04%,S 的质量分数分别为35.87%、28.28、23.30%。

图5 不同反应时间的硫铁矿的SEM照片和EDS图谱Fig. 5 SEM images and EDS of pyrite for different reaction time
2.2 还原液中和沉淀去除Al、Cr
在pH 为4 的条件下,陈化时间对还原液各金属离子沉淀率的影响如图6(a)所示。随着陈化时间的延长,Al、Cr 沉淀率几乎不变,这与FARIS等[21]的研究结果一致,而由于Ni、Co、Mn 受到Al、Cr 和Fe 氢氧化物的不断吸附,Fe2+不断发生氧化水解,因此,Ni、Co、Mn和Fe的沉淀率不断提高。可见:陈化过程不仅会加大有价金属的损失,Fe2+在陈化过程的氧化水解也会提高碱用量,形成铁含量较高的中和渣也不利于过滤,除杂方式选择去除陈化过程。

图6 反应条件对金属离子沉淀率的影响Fig. 6 Influence of reaction condition on precipitation percentage of various metal ions
不同终点pH 对各金属沉淀率的影响如图6(b)所示。可见:随着终点pH的提高,Al和Cr沉淀率不断提高,在终点pH 超过3.7 时,Al 和Cr 沉淀率急剧上升,当终点pH 达到4.5 时,Al 和Cr 几乎脱除完全,沉淀率分别为99.57%和99.40%。终点pH提高,Fe2+氧化水解,Fe的损失略有提升,Ni、Co和Mn 也有少量的损失。在pH=4.2 时,Al 和Cr 沉淀率已经达到了99.00%和98.65%,而Ni、Co、Mn 和Fe 的沉淀率相对较小,所以选择pH=4.2 进行杂质脱除。
在pH为4.2的条件下,不同NaOH加料速度对各金属沉淀率的影响如图6(c)所示。随着加料速度的不断提高,更多位点都保持在瞬间高pH 状态,Al 和Cr 沉淀率不断提高,Ni、Co 和Mn 沉淀率也不断提高,而加料速度变快使得反应时间变短,Fe 沉淀率不断降低,当加料速度达到20 mL/min,Al 和Cr 沉淀率分别为99.61%和99.49%,而Ni、Co 和Mn 沉淀率较高,分别为18.02%、18.02%和18.55%。在加料速度为10 mL/min下,Al、Cr沉淀率为99.50%和98.97%,而Ni、Co、Mn 和Fe 的沉淀损失较少,分别为7.89%、8.72%、9.76%和6.34%,因此,选择加料速度为10 mL/min。
在pH 为4.2、加料速度为10 mL/min 的条件下,温度对各金属沉淀的影响如图6(d)所示。可见:升高温度可以促进各反应快速进行,Al 和Cr沉淀率不断提高,Ni、Co、Fe和Mn沉淀率也不断提高,因此,选择65 ℃最为合适,此时,Al和Cr几乎完全去除,Ni、Co、Fe 和Mn 沉淀率相对较低。
综上所述,采用去除陈化过程的反应方式,在最佳pH 为4.2、最佳加料速度为10 mL/min、最佳温度为65 ℃时,Al 和Cr 沉淀率分别为99.09%和98.45%,Ni、Co、Fe 和Mn沉淀率分别为6.92%、8.12%、5.87%和8.03%。
2.3 Na2S沉淀回收Ni、Co、Mn
采用Na2S 沉淀Ni、Co 和Mn,反应温度和Na2S 过量系数对Ni、Co 和Mn 沉淀率的影响如图7(a)所示。可见:在温度85 ℃下,Na2S 过量系数从4 提高到6,Ni、Co 和Mn 沉淀率不断提高,Ni和Co几乎沉淀完全,继续加大Na2S用量,在Na2S过量情况下形成了可溶性金属多硫配合物,导致Ni、Co和Mn的沉淀物重新溶解,Ni、Co和Mn沉淀率开始降低,因此,在过量系数为6时出现最高点。由于体系中存在的大量Fe2+,与Na2S 反应消耗了一定量Na2S,导致Na2S 过量系数大[22]。温度对反应的影响如图7(b)所示,Ni、Co和Mn沉淀率都不断随着温度升高而增大,Fe 的损失也不断提高,Fe沉淀率为5.77%,说明升高温度有利于硫化物的沉淀。确定反应最佳条件是Na2S 过量系数为6,温度为95 ℃,Ni和Co沉淀率分别达到99.93%和99.72%,Mn 沉淀率为90.1%,由于溶液中Mn质量浓度为75 mg/L,经过除杂后锰质量浓度降低为6.2 mg/L,对于后续硫酸亚铁溶液制备氧化铁红不会造成太大影响。镍和钴总回收率分别为93.01%和91.62%。

图7 反应条件对镍钴沉淀率的影响Fig. 7 Infulence of reaction condition on precipitation percentage of nickel and cobalt
采用ICP分析镍钴锰渣中各金属含量,结果如表5 所示。可见:镍钴锰渣中Al 和Cr 含量极大降低,Ni质量分数达到13.47%。对照YS/T 340—2014可得,镍钴锰渣达到标准中镍精矿1级品标准。

表5 镍钴锰渣的主要化学成分(质量分数)Table 5 Main chemical composition of slag of nickel cobalt manganese %
2.4 碳铵沉铁制备氧化铁红
2.4.1 碳铵沉铁条件的影响
设计L1643正交表,考察温度、溶液初始pH以及Fe2+初始浓度对氧化铁红着色力的影响,结果如表6 所示。可见:随着pH 的提高,着色力先提高后降低,在pH 为7.5 时达到最高,只是因为pH 过低使得成核速度过低,晶体长大,pH 过高使得成核速度过快,晶体团聚;随着Fe2+浓度的降低,着色力不断提高,这是因为反应过程并未加入分散剂,较低的浓度减缓了晶体团聚;而随着温度提高,着色力出现波动,这表明温度对着色力的影响不太大。根据极差发现,Fe2+浓度对氧化铁红着色力影响最大,其次为pH和温度。确定最佳沉铁条件为温度45 ℃、Fe2+浓度0.3 mol/L、pH 为7.5。在此优化条件下重复实验3 次,着色力平均值为125.45%。

表6 正交实验结果Table 6 Orthogonal experimental results
2.4.2 煅烧温度的影响
图8 所示为煅烧温度对氧化铁红颜色的影响。可见:在400~600 ℃范围内,随着煅烧温度的提高氧化铁红变得更鲜艳,在600~800 ℃时,提高煅烧温度使氧化铁红颜色不断暗沉。因此,最佳煅烧温度为600 ℃。

图8 温度对氧化铁红颜色的影响Fig.8 Effect of temperature on color of iron oxide red
2.4.3 氧化铁红表征
氧化铁红XRD 图谱如图9 所示。可见:在24.09°、33.14°、40.89°、57.49°和69.53°处观察到了氧化铁的衍射峰,制备的产品为氧化铁。根据GB/T 1863—2008测试氧化铁红各项指标,结果如表7 所示。可见:氧化铁质量分数为96.5%,105 ℃挥发物的质量分数为0.8%,筛余物(粒径45 μm)的质量分数为0.02%,水溶物的质量分数为0.5%,颜色与湖南三环颜料有限公司产品H101相近。将实测值与标准进行比较发现,制备得到的Fe2O3在氧化铁含量和105 ℃挥发物满足1类产品标准,水溶物的质量分数和筛余物(粒径45 μm)的质量分数满足2类产品标准。

图9 氧化铁红XRD图谱Fig. 9 XRD pattern of iron oxide red

表7 氧化铁红各技术指标与标准指标Table 7 Various technical indexes and standard indexes of iron oxide red
3 结论
1) 采用1.4 mol/L 硫酸浸出蛇纹石中和渣得到酸浸出液,以红透山硫铁矿还原中和渣酸浸液,确定最佳还原条件为反应时间260 min、温度85 ℃,在此条件下,Fe3+还原率为99.99%,还原液pH 达到2.9。还原后,硫产物组成为31.08%S、34.45% H2SO4、34.45% H2S;硫铁矿由片状聚集态变为球形大颗粒状,硫铁矿表面没有发现明显的S包裹。
2) 采用NaOH调节还原液pH脱除Al和Cr,选择去除陈化的反应方式,在pH为4.2、加料速度为10 mL/min、反应温度为65 ℃时,Al 和Cr 沉淀率分别达到99.09%和98.45%,Ni、Co、Fe 和Mn 的沉淀率均很低。
3) 采用Na2S 沉淀回收Ni、Co 和Mn,在Na2S过量系数为6、反应温度为95 ℃的条件下,Ni、Co 和Mn 回收率分别为99.93%、 99.72% 和90.10%,Fe 沉淀率为5.77%。镍总回收率为93.01%;钴总回收率为91.62%。得到的镍钴锰渣中镍质量分数达到了13.47%,可作为镍精矿出售。
4) 以碳酸氢铵沉淀净化除杂后的硫酸亚铁溶液,以用量系数1.5加入碳酸氢铵,在35 ℃下反应5 h,再在600 ℃煅烧2 h得到氧化铁红,颜色与三环颜料公司产品H101相近,着色力达到125.45%,氧化铁含量和105 ℃挥发物的质量分数满足GB/T 1863—2008中1类标准,其余各项指标符合中2类标准。
