免疫调节药物联合R-GemOx方案治疗复发/难治性弥漫大B细胞淋巴瘤的疗效及毒性影响评价
2023-06-08杨琳
杨琳

[摘要] 目的 觀察免疫调节药物联合R-GemOx方案治疗复发/难治性弥漫大B细胞淋巴瘤(relapsed/refractory diffuse large B-cell lymphoma,R/R-DLBCL)的疗效及毒性影响。方法 选取2017年5月至2019年4月杭州市临平区第一人民医院收治的R/R-DLBCL患者144例,采用随机数字表法分为对照组(n=72)和观察组(n=72)。对照组采用R-GemOx方案治疗,观察组在对照组基础上加用沙利度胺治疗。比较两组肿瘤负荷指标、白细胞介素-10(interleukin-10,IL-10)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)的表达差异,观察两组疗效和不良反应,随访36个月,记录平均生存时间。结果 治疗后,两组乳酸脱氢酶、β2-微球蛋白、IL-10、TNF-α均较治疗前下降,且观察组低于对照组,差异均有统计学意义(P<0.05)。观察组的客观缓解率和疾病控制率均高于对照组,但差异无统计学意义(P>0.05)。两组的不良反应主要以Ⅰ~Ⅱ级为主,观察组白细胞减少、血小板减少总发生率显著低于对照组(P<0.05)。随访36个月后,观察组平均生存时间显著长于对照组(P<0.05)。结论 免疫调节药物联合R-GemOx方案治疗R/R-DLBCL可降低肿瘤负荷指标、IL-10、TNF-α的表达,减少白细胞减少、血小板减少等不良反应的发生。
[关键词] 免疫调节药物;R-GemOx方案;弥漫大B细胞淋巴瘤;肿瘤负荷;不良反应
[中图分类号] R733.4 [文献标识码] A [DOI] 10.3969/j.issn.1673-9701.2023.11.017
Efficacy and toxicity evaluation of immunomodulatory drugs combined with R-GemOx regimen in the treatment of relapsed/refractory diffuse large B-cell lymphoma
YANG Lin
Department of Hematology, First Peoples Hospital of Hangzhou Linping District, Hangzhou 311199, Zhejiang, China
[Abstract] Objective To observe the efficacy and toxicity of immunomodulatory drugs combined with R-GemOx regimen in the treatment of relapsed/refractory diffuse large B-cell lymphoma (R/R-DLBCL). Methods A total of 144 R/R-DLBCL patients admitted to First People's Hospital of Hangzhou Linping District from May 2017 to April 2019 were selected and divided into the control group (n=72) and the observation group (n=72) according to the random number table method. The control group was treated with R-GemOx, and the observation group was treated with thalidomide on the basis of the control group. The differences in the expression of tumor burden indexes, interleukin-10 (IL-10) and tumor necrosis factor-α (TNF-α) between the two groups were compared, and the curative effect, adverse effects were calculated between the two groups. The follow-up was 36 months, and the average survival time was recorded. Results After treatment, lactate dehydrogenase, β2-microglobulin, IL-10 and TNF-α decreased in both groups compared with those before treatment, and the differences were lower in the observation group than those in the control group, all of which were statistically significant (P<0.05). The objective remission rate and disease control rate in the observation group were both higher than those in the control group, but the differences were not statistically significant (P>0.05). Adverse effects in both groups were predominantly grade Ⅰ to Ⅱ, and the total incidence of leukopenia and thrombocytopenia in the observation group was significantly lower than those in the control group (P<0.05). After 36 months of follow-up, the average survival time of the observation group was significantly longer than that of the control group (P<0.05). Conclusion Immunomodulatory drugs combined with R-GemOx regimen in the treatment of R/R-DLBCL can reduce the expression of tumor burden indicators, IL-10, and TNF-α, and reduce the occurrence of toxic and side effects such as leukopenia and thrombocytopenia.
![]() [Key words] Immunomodulatory drugs; R-GemOx regimen; Diffuse large B-cell lymphoma; Tumor burden; Toxic and side effects
[Key words] Immunomodulatory drugs; R-GemOx regimen; Diffuse large B-cell lymphoma; Tumor burden; Toxic and side effects
非霍奇金淋巴瘤是临床常见的淋巴造血系统恶性肿瘤,弥漫性大B细胞淋巴瘤是其中的常见亚型,采用标准一线化疗方案治疗后,50%~70%的患者可实现长期无病生存,但仍有相当一部分患者无法治愈,在病情缓解后又复发,或经多种治疗方案仍不能缓解,称为复发/难治性弥漫大B细胞淋巴瘤(relapsed/refractory diffuse large B-cell lymphoma,R/R-DLBCL)[1]。R-GemOx方案是治疗R/R-DLBCL的常用二线治疗方法,由利妥昔单抗、吉西他滨、奥沙利铂组成,可在一定程度上控制病情,但整体疗效并不理想[2]。研究发现,R/R-DLBCL患者机体处于严重的免疫紊乱状态,这不仅与疾病本身有关,还与化疗药物的使用有关,调节患者免疫功能有助于增强自身抗病能力,减少化疗产生的不良反应[3]。沙利度胺是一種免疫调节药物,在多种自身免疫性疾病的治疗中有所应用[4]。本研究将其应用于R/R-DLBCL的治疗中,观察免疫调节药物联合R-GemOx方案治疗R/R-DLBCL的疗效及不良反应,以期为临床提供参考。
1 资料与方法
1.1 一般资料
选取2017年5月至2019年4月杭州市临平区第一人民医院收治的R/R-DLBCL患者144例,采用随机数字表法分为对照组(n=72)和观察组(n=72)。纳入标准:①符合《中国弥漫大B细胞淋巴瘤诊断与治疗指南(2013年版)》[5]的标准,并经临床结合病理活检等综合诊断为R/R-DLBCL,其中疾病经治疗获得完全缓解后再次进展,并再次经组织病理学活检后仍确诊为DLBCL的患者称为复发性DLBCL;经过4周期一线R-CHOP或CHOP方案治疗后未达到部分缓解,或6周期一线化疗后未达到完全缓解,或经过一线化疗方案治疗失败患者称为难治性DLBCL;②年龄18~75岁;③Karnofsky评分>60分;④患者自愿加入。排除标准:①4周内有其他免疫调节剂使用史;②存在躯体其他部位原发性肿瘤;③3个月内有外伤史或预计生存期<6个月;④孕妇或哺乳期女性;⑤对化疗方案和免疫调节剂相关药物过敏严重;⑥重要脏器功能不全。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经杭州市临平区第一人民医院伦理委员会批准(伦理审批号:2017【11】号)。
1.2 方法
两组均给予保肝、护心、护胃等支持治疗,定期检测血常规、肝肾功能、凝血功能等,对照组采用R-GemOx方案治疗,静脉滴注利妥昔单抗375mg/m2,d0;静脉滴注吉西他滨1000mg/m2,d1、8;静脉滴注奥沙利铂130mg/m2,d1,21d为一个化疗周期。观察组在对照组基础上加用免疫调节药物沙利度胺(生产单位:常州制药厂有限公司,批准文号:国药准字H32026129,规格:25mg)进行治疗,于化疗第1天起口服沙利度胺100mg/d,每周增量50mg/d直至目标剂量200~300mg/d,连续服药至化疗结束。两组均连续化疗6个周期。
治疗前后抽取患者空腹外周静脉血标本4ml,置于EDTA抗凝采血管,于取血后1h离心10min,3000转/min。分离血清,采用酶联免疫吸附法试剂盒(上海酶联生物科技有限公司)检测白细胞介素-10(interleukin-10,IL-10)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、乳酸脱氢酶(lactate dehydrogenase,LDH)、β2-微球蛋白(β2-microglobulin,β2-MG),检测仪器为酶标仪(深圳迈瑞医疗电子股份有限公司,RT-96A型)。
1.3 观察指标
①两组近期疗效:参考《中国弥漫大B细胞淋巴瘤诊断与治疗指南(2013年版)》[5]制定的标准,分为完全缓解(complete response,CR):肿瘤病灶消失持续>4周;部分缓解(partial response,PR):肿瘤病灶缩小>50%并持续>4周,无新病灶产生;疾病稳定(stable disease,SD):病灶缩小<50%,或增加<25%,无新病灶产生;疾病进展(progressive disease,PD):病灶增大≥25%,或新病灶产生。总缓解率(overall response rate,ORR)=CR+PR,疾病控制率(disease control rate,DCR)=CR+PR+SD。②两组肿瘤负荷指标(包括IL-10、TNF-α)、LDH和β2-MG水平。③两组的生存时间和不良反应:参考《WHO抗肿瘤药物急性及亚急性毒副反应评价标准》[6],同时随访36个月,随访日期截至2022年3月31日,记录两组平均生存时间。不良反应包括白细胞减少、血小板减少、贫血、肺部感染、消化道反应、肝功能异常,分为Ⅰ~Ⅳ级,等级越高,不良反应越厉害。
1.4 统计学方法
采用SPSS 19.0统计学软件对数据进行处理分析,计量资料以均数±标准差(![]() )表示,组间比较采用t检验,计数资料采用例数(百分比)[n(%)]表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
)表示,组间比较采用t检验,计数资料采用例数(百分比)[n(%)]表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 基线资料比较
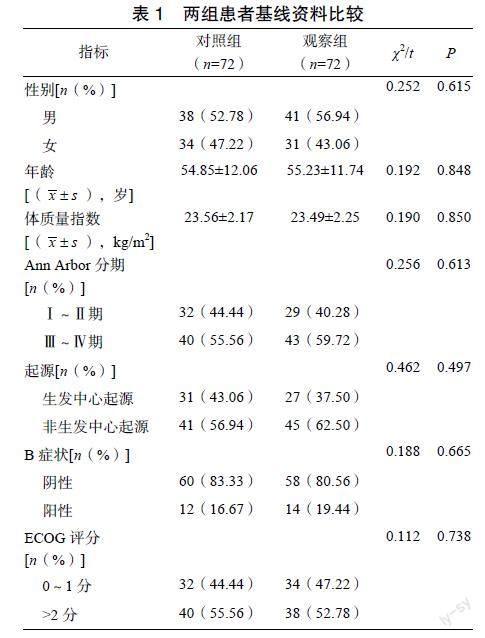
两组患者性别、年龄及其分期、起源、有无B症状、ECOG评分等基线资料比较,差异无统计学意义(P>0.05),见表1。
2.2 肿瘤负荷指标、IL-10、TNF-α比较
治疗后,两组的LDH、β2-MG、IL-10、TNF-α均较治疗前下降,且观察组低于对照组,差异有统计学意义(P<0.05),见表2。
2.3 近期疗效比较
观察组的ORR和DCR均高于对照组,但差异无统计学意义(P>0.05),见表3。
2.4 不良反应比较
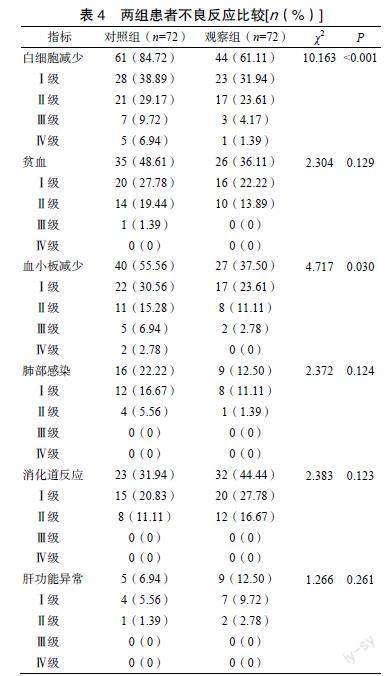
两组不良反应主要以Ⅰ~Ⅱ级为主,观察组白细胞减少、血小板减少发生率均低于对照组,差异均有统计学意义(P<0.05)。两组在贫血、肺部感染、消化道反应、肝功能异常发生率方面比较,差异均无统计学意义(P>0.05),见表4。
2.5 生存时间比较
随访36个月,对照组平均生存时间(17.82±3.98)个月,而观察组平均生存时间(19.27±4.11)个月,两组比较差异有统计学意义(t=2.151,P=0.033)。
3 讨论
R/R-DLBCL是一种难治性疾病,患者预后较差。其发病机制比较复杂,已有的研究认为与病毒感染、免疫抑制或亢进、环境恶化等因素有关[7]。R-GemOx方案(利妥昔单抗+吉西他滨+奥沙利铂)目前常用于R/R-DLBCL的治疗,其中,利妥昔单抗是一种单克隆人鼠嵌合抗体,可与跨膜抗原CD20特异性结合,产生细胞毒作用,诱导B细胞凋亡,是B细胞淋巴瘤的一线化疗药物。吉西他滨属于胞嘧啶核苷衍生物,可作用于肿瘤细胞DNA而发挥抗肿瘤作用,在R/R-DLBCL治疗中的疗效已被证实,有效率为20%~25%。奥沙利铂以肿瘤细胞DNA为靶部位,铂原子与DNA形成交叉联结,拮抗DNA复制和转录[8]。R-GemOx方案中的药物具有协同增效的作用。赵蓉爽等[9]研究认为,R-GemOx方案是治疗R/R-DLBCL安全、有效的二线化疗方案,其消化道不良反應更少,更适合于年龄较大、体质较差的R/R-DLBCL患者应用。
沙利度胺是一种谷氨酸衍生物,具有镇静、镇痛、抗血管生成、免疫调节及抗炎等多种药理作用,在Ⅱ型麻风病、盘状红斑狼疮、贝赫切特综合征等疾病的治疗中应用广泛[10]。张丽娟等[11]采用沙利度胺与DHAP方案(顺铂+阿糖胞苷+地塞米松)联用治疗复发/难治性弥漫性大B细胞淋巴瘤,发现其可有效延缓病情进展,且未增加不良作用,但样本量所限,还需延长随访时间对研究结果进行进一步临床验证。本研究发现,采用沙利度胺联合R-GemOx方案治疗者的ORR和DCR均高于单用R-GemOx方案治疗者,但差异无统计学意义,可能与本研究样本量较少所产生的偏倚有关。随访36个月,采用沙利度胺联合R-GemOx方案治疗者平均生存时间长于单用R-GemOx方案治疗者,提示免疫调节药物联合R-GemOx方案治疗R/R-DLBCL可延长患者的生存时间。究其原因,可能由于沙利度胺可通过调节TNF-α等多种细胞因子活性,促进T细胞、NK细胞活化,改善肿瘤组织的微环境,并提高机体自身抗肿瘤能力[12]。
LDH是一类NAD依赖性激酶,与乏氧环境和糖酵解有关。LDH是国际预后指数的危险因素之一,也是侵袭性淋巴瘤预后的评估指标之一[13-14]。β2-MG由淋巴细胞及其他有核细胞分泌,恶性肿瘤患者体内β2-MG水平升高与肿瘤细胞分泌β2-MG的功能亢进有关[15-16]。IL-10是免疫炎症反应的负调节因子,可抑制免疫应答、细胞毒反应,有利于肿瘤细胞生长、增殖[17-18]。TNF-α由活化的巨噬细胞、Th1细胞和中性粒细胞产生,可直接杀伤肿瘤细胞,诱导其凋亡,引起局部炎症反应和刺激机体免疫系统而发挥抗肿瘤活性,在恶性肿瘤患者体内明显升高[19-20]。本研究结果显示,治疗后,两组LDH、β2-MG、IL-10、TNF-α均较治疗前下降,且观察组患者的LDH、β2-MG、IL-10、TNF-α低于R-GemOx方案治疗者,提示沙利度胺联合R-GemOx方案治疗R/R-DLBCL可降低肿瘤负荷指标LDH、β2-MG以及IL-10、TNF-α的表达,这可能是其控制病情的重要机制。本研究结果显示,两组不良反应主要以Ⅰ~Ⅱ级为主,并未出现严重不良反应。两组在贫血、肺部感染、消化道反应、肝功能异常总发生率方面比较,差异无统计学意义。观察组的白细胞和血小板减少的总发生率明显低于对照组,究其原因,可能与沙利度胺对免疫功能的调节作用有关。
综上所述,免疫调节药物沙利度胺联合R-GemOx方案治疗R/R-DLBCL可降低肿瘤负荷指标、IL-10、TNF-α的表达,减少白细胞减少、血小板减少等不良反应的发生,为临床治疗提供一定的帮助。
[参考文献][1] TKACZ J, GARCIA J, GITLIN M, et al. The economic burden to payers of patients with diffuse large B-cell lymphoma during the treatment period by line of therapy[J]. Leukemia Lymphoma, 2020, 61(7): 1601–1609.
[2] ZLOTNICK M, AVIGDOR A, RIBAKOVSKY E, et al. Efficacy of gemcitabine as salvage therapy for relapsed and refractory aggressive non-Hodgkin lymphoma[J]. Acta Haematol, 2019, 141(2): 84–90.
[14] 周炼炼, 陈少谊. 弥漫大B细胞淋巴瘤化疗患者血清PDGF-BB、sCD40L及LDH变化与预后的相关性[J]. 国际检验医学杂志, 2021, 42(14): 1773–1776.
