响应面法优化全氢化棉籽油的制备工艺及产品表征
2023-05-10宋振佳杨瑞楠马传国司天雷
宋振佳,杨瑞楠,马传国,司天雷
河南工业大学 粮油食品学院,河南 郑州 450001
植物油加氢是油脂化学工业中一项重要的改性技术,氢化油的碘值≥5 g/100 g时被称为部分氢化油[1]。良好的稳定性和特殊的熔融性能使部分氢化油成为生产起酥油或人造黄油的普遍原料[2]。然而,部分氢化油是反式脂肪酸(trans fatty acids,TFAs)最主要的来源[3]。TFAs是包含有至少一个碳-碳反式双键的单不饱和脂肪酸或多不饱和脂肪酸,研究发现膳食摄入TFAs会导致血液中低密度脂蛋白胆固醇的增加和高密度脂蛋白胆固醇的降低,从而提高心血管疾病的患病风险[4-5]。因此在植物油氢化过程中降低TFAs含量对食品工业至关重要。
已知国标对“零”TFAs标签的数据要求为每份食品样品中TFAs含量≤ 0.3 g/100 g(相对TFAs含量≤ 0.3%)[6],满足上述条件的同时其碘值≤ 5 g/100 g[1]则可称“零”TFAs全氢化植物油。而目前关于植物油氢化的研究多集中在催化剂制备及其效果方面,涉及“零”TFAs全氢化植物油的研究较少。如杨希等[7]在传统加氢工艺条件下使用1.79% Pt/ZrO2催化氢化大豆油,在氢化油样碘值约为70 g/100 g时产生的反油酸含量为25.48 g/100 g。Iida等[8]利用自制的负载型催化剂TiO2(TiO-9)对大豆油进行加氢处理,在800 mg/kg Ni、反应温度为413 K、氢气压力为0.5 MPa、搅拌速度为1 700 r/min下氢化大豆油的碘值为70 g/100 g,反油酸含量最低为15.7%[9]。杜晶等[10]在催化转移加氢体系中利用自制的Pd/碳纳米管为催化剂,在最优工艺条件下得到的部分氢化大豆油中碘值为95.3 g/100 g,TFAs相对含量为10.2%。可见采用不同加氢条件及自制催化剂对植物油加氢所产生的TFAs含量虽然大幅降低,但对比国标要求其含量依然较高。
我国是棉花生产和种植大国,2020—2021年度我国棉籽油产量达123.2万t,约占世界总产量的23.8%[11-12]。棉籽油主要脂肪酸为棕榈酸(18.30%~25.68%)、油酸(12.28%~18.50%)和亚油酸(51.99%~60.88%)[13],其结晶习性为β′型[14]。因此,来源广泛且性质优良的棉籽油常被用作油脂氢化工业的原料。
鉴于目前关于植物油氢化研究中存在的TFAs含量较高的问题,为满足国标对“零”TFAs标签的数据要求,提升棉籽油的利用价值,作者以棉籽油为原料,探究棉籽油全氢化过程中镍(Ni)载量、反应温度、反应时间、搅拌速率对其碘值和TFAs相对含量的影响,并通过响应面试验优化工艺条件制备出零反式脂肪酸全氢化棉籽油,对其物理性质加以表征,为油脂氢化工艺提供参数依据,对推动以全氢化棉籽油为原料生产载体基质、塑性脂肪等高值化产品之相关产业的发展提供一定的数据支撑。
1 材料与方法
1.1 材料与试剂
精炼棉籽油:碘值117.3 g/100 g,益海(昌吉)粮油工业有限公司提供。
镍(Ni)催化剂: MONCATTM2021,镍含量21%~23%,德国EVONIK INDUSTRIES;37种脂肪酸甲酯混合标准品、亚油酸甲酯顺反异构体混合标准品、亚麻酸甲酯8种顺反异构体混合标准品:美国Sigma-Aldrich公司; 高纯H2(纯度≥99.999%): 河南源正特种气体有限公司;其他试剂均为国产分析纯。
1.2 仪器与设备
Parr 4760型非搅拌高压反应釜(300 mL):美国Parr Instrument Company; RCT basic IKAMAG® safety control磁力搅拌器: 德国IKA集团; MiNispec20/100RTS脉冲核磁共振仪、D8 Advance X射线衍射仪:德国Bruker公司;SD制冷加热循环水浴:美国PolyScience公司;ZEISS Axioscope 5偏光显微镜:德国Zeiss集团;气相色谱仪:GC-2030 日本岛津公司;TA-2000差示扫描量热仪:德国 NETZSCH集团。
1.3 方法
1.3.1 氢化试验
准确称取10 g精炼棉籽油于20 mL玻璃小瓶中,加入一定量的催化剂Ni和转子,旋紧瓶盖。置于300 mL反应釜内,重复3次排空气。在一定的温度、搅拌条件下,反应一定时间。用预热过的去头注射器和0.8 μm有机滤膜将氢化油中的Ni滤除。
考察Ni载量(0.02%、0.04%、0.06%、0.08%、0.10%),搅拌速率(500、600、700、800、900 r/min),温度(100、120、140、160、180 ℃),时间(30、60、90、120、150 min)各个自变量对氢化棉籽油碘值及TFAs相对含量的影响。
依据单因素试验结果,采用Design-Expert 13软件进行四因素三水平二响应值的响应面试验。
1.3.2 碘值
原料油以及氢化棉籽油碘值的测定按照GB/T 5532—2008执行。
1.3.3 熔点
氢化棉籽油的熔点按照GB/T 24892—2010进行测定。
1.3.4 脂肪酸组成的测定
参照GB 5009.168—2016 《食品安全国家标准 食品中脂肪酸的测定》。采用三氟化硼甲酯化方法对棉籽油脂肪酸进行甲酯化后,采用气相色谱法对其脂肪酸组成进行测定。通过对比标准品保留时间鉴定相应脂肪酸,对峰面积进行积分,采用面积归一化法定量测定脂肪酸百分含量。其中,TFAs相对含量=TFAs峰面积之和/所有脂肪酸峰面积之和。试验重复3次,结果取平均值。
气相色谱条件如下。Agilent HP-88石英毛细柱(100 m×0.25 mm,0.20 μm);进样口温度:260 ℃;柱温:140 ℃;火焰电离检测器 (FID)温度:260 ℃;分流比:50∶1;氮气流速:24 mL/min;氢气流速:32 mL/min;空气流速:200 mL/min;进样量:1 μL。
1.3.5 固体脂肪含量(solid fat content,SFC)
使用布鲁克MiNispec20/100RTS脉冲核磁共振仪测定样品在0~70 ℃的固体脂肪含量。80 ℃熔化30 min,在0 ℃冷却90 min,然后在每个测量温度下保持30 min,5 ℃为间隔(55~65 ℃时的间隔为1 ℃)。重复试验并计算平均值。
1.3.6 熔融和结晶行为
使用差示扫描量热仪(differential scanning calorimeter,DSC)监测样品的熔融和结晶行为。具体方法参照郭姝婧等[15]的研究,测定峰值熔化/结晶温度,熔化曲线的最后一个峰的顶点被认为是样品的熔点。重复试验,结果取平均值。
1.3.7 晶体结构
在D8 Advance X射线衍射仪上,使用铜X射线管(Cu-Kα,λ=1.541 8 Å,电压40 kV,电流40 mA)测定样品的多晶型。在0.5 °/min的扫描速度下,观察10°~ 35°(2θ)的短间距。重复试验并计算平均值。
1.3.8 微观形态
使用配备18 MP 数码相机(OMAX)的偏光显微镜观察结晶样品的形态,放大倍数为20×10和50×10。将熔化的样品放在预热的载玻片上,并加盖预热的盖玻片,在24 ℃下保持18 h。使用ImageJ.JS获取样本的数字图像。分形维数(D)通过粒子计数算法确定,其中粒子数量在不同长度的盒子内进行计数,在对数-对数图上线性回归的斜率对应于D[16]。
1.4 统计分析
使用 IBM SPSS Statistics 26、Origin 2019b处理数据。采用Design-Expert 13软件进行响应面试验设计及数据分析。根据Duncan′s多极差检验,认为在P<0.05时差异显著。
2 结果与分析
2.1 单因素试验
2.1.1 镍载量对氢化棉籽油碘值及TFAs相对含量的影响
工业常用加氢条件为温度150~220 ℃,搅拌速率500~2 000 r/min,催化剂浓度0.02%~0.14%,氢气压0.2~0.6 MPa[17-18]。Parr反应釜配置的SPAN压力表最小示数为0.6 MPa,探索更低氢气压受限,因而固定氢气压为0.6 MPa。在氢化温度140 ℃、搅拌速率700 r/min、时间90 min、氢气压0.6 MPa条件下考察镍载量(0.02%~0.10%)对氢化棉籽油碘值及TFAs相对含量的影响,结果如图1所示。

注:不同小写字母表示组间具有显著性差异(P<0.05)。图2—图4同。图1 镍载量对氢化棉籽油碘值及TFAs相对含量的影响Fig.1 Effect of nickel loading on iodine value and relative content of TFAs in hydrogenated cottonseed oil
随着镍载量的增加,氢化棉籽油碘值以及TFAs相对含量快速下降。当镍载量为0.08%时,碘值为(0.58±0.12) g/100 g(<5 g/100 g),TFAs相对含量为0.17%±0.02%(<0.3%),油样达到全氢化水平。继续增加镍载量,样品碘值及TFAs水平不再明显降低。上述现象可归因于镍含量的提高使更多的油被吸收到镍表面上,镍得到额外的活性位点,并随后降低了氢原子在镍表面的解吸速率,致使氢化水平升高,碘值及TFAs相对含量迅速降低[19]。但较高的镍载量使其颗粒聚集度增加,有效表面积减小,可能导致反应速率降低[10],因而碘值不再下降,TFAs水平略微提高。考虑到成本及全氢化要求,故控制镍载量为0.08%。
2.1.2 搅拌速率对氢化棉籽油碘值及TFAs相对含量的影响
在镍载量0.08%、氢化温度140 ℃、时间90 min、氢气压0.6 MPa条件下研究搅拌速率对氢化油样碘值及TFAs相对含量的影响。由图2可知,随着搅拌速率的加快,碘值以及TFAs相对含量大幅降低,这可能是由于加快搅拌速率提高了非均相反应中的传质速率,镍表面氢气浓度加大,反式异构化程度锐减所致。在搅拌速率为700 r/min时碘值为(0.70±0.15 ) g/100 g(<5 g/100 g),TFAs相对含量为0.18%±0.01%(<0.3%),继续提高搅拌速率,碘值和TFAs相对含量无显著性变化,原因在于搅拌速率在达到可以消除扩散阻力后,使镍表面氢气浓度稳定在一个较高的值,继续升高搅拌速率对氢化反应基本无明显影响[20]。综合上述分析,棉籽油全氢化的搅拌速率为700 r/min。

图2 搅拌速率对氢化棉籽油碘值及TFAs相对含量的影响Fig.2 Effect of stirring velocity on iodine value and relative content of TFAs in hydrogenated cottonseed oil
2.1.3 温度对氢化棉籽油碘值及TFAs相对含量的影响
在镍载量0.08%、搅拌速率700 r/min、时间90 min、氢气压0.6 MPa条件下研究温度对氢化油样碘值及TFAs相对含量的影响。如图3所示,随着温度升高,氢化棉籽油碘值逐步下降,在140 ℃达到(0.60±0.12) g/100 g(<5 g/100 g),继续升高温度碘值无显著性差异。这是由于提高温度有利于更多的氢气溶解于油中[17],加快了镍表面活性位点与不饱和脂肪酸上双键与氢原子的结合[21],油样中C18∶1和C18∶0含量升高,C18∶2和C18∶3含量降低,油样饱和度升高则碘值下降,油样中脂肪酸不饱和键数量下降,并趋于稳定,则碘值不再显著变化。100 ℃ 时油样TFAs相对含量极低,这是由于镍作为催化剂在120 ℃ 以下活性较低,可能并未达到催化加氢反应的活化能[22]。温度在120 ℃ 时氢化油样TFAs相对含量达到24% 左右,可能是在该温度下异构化选择性上升所致。140~180 ℃ 条件下,TFAs相对含量基本稳定在0.2% 以下,原因可能是温度的升高使催化剂活性升高到一定浮动区间,高温降低了油脂的黏度,体系流动性增强,从而促进镍更快地吸附氢原子,异构化程度降低,从而获得零TFAs氢化棉籽油。因此氢化温度为140 ℃。

图3 温度对氢化棉籽油碘值及TFAs相对含量的影响Fig.3 Effect of temperature on iodine value and relative content of TFAs in hydrogenated cottonseed oil
2.1.4 时间对氢化棉籽油碘值及TFAs相对含量的影响
镍载量0.08%、搅拌速率700 r/min、温度140 ℃、氢气压0.6 MPa条件下研究时间对氢化油样碘值及TFAs相对含量的影响。如图4所示,随着时间的延长,氢化棉籽油碘值与TFAs相对含量迅速降低,最后逐渐平稳。初始时棉籽油不饱和脂肪酸含量较高,反应所需底物充足,因而加氢速率快,随着氢化时间延长,不饱和脂肪酸浓度降低,可供异构化的底物量变少,导致氢化速率减小[23]。90 min时,氢化油样碘值为(0.60±0.17) g/100 g(<5 g/100 g),TFAs相对含量为0.17%±0.04%(<0.3%),继续延长时间无显著性差异。因此控制时间为90 min。

图4 时间对氢化棉籽油碘值及TFAs相对含量的影响Fig.4 Effect of time on iodine value and relative content of TFAs in hydrogenated cottonseed oil
2.2 响应面试验
2.2.1 响应面试验设计及结果
在单因素试验基础上,采用Box-Behnken方法,以镍载量(A)、搅拌速率(B)、温度(C)、时间(D)为自变量,以氢化棉籽油碘值与TFAs相对含量为响应值设计四因素三水平响应面试验。试验设计因素与水平如表1所示。表2为响应面试验设计及结果。

表1 响应面设计因素与水平Table 1 Factors and levels of response surface design
分别以碘值、TFA相对含量为响应值,将表2数据进行回归拟合,得到各因素对两个响应值的回归方程。回归方程分别为:
Y1=3.464-4.99A-7.25B-27.66C-11.93D+1.39AB+8.08AC+3.94AD+7.96BC+7.19BD+17.84CD-1.12A2+3.26B2+22.45C2+5.80D2;
Y2=2.95-2.15A-4.20B-13.88C-7.54D+1.30AB+2.31AC+1.83AD+3.93BC+6.30BD+9.81CD-0.673 2A2+1.71B2+9.80C2+2.94D2。式中Y1为碘值,Y2为TFAs相对含量。
2.2.2 响应面试验结果的方差及显著性分析

为更立体地反映自变量间的交互作用对响应值的影响,对3D响应面图进行分析。如图5(a)、(b)所示,随着温度的升高,镍载量与搅拌速率、搅拌速率与时间使碘值先降低再升高,但升高幅度较小。由图5(c)可知,随着温度升高、时间延长,碘值逐步下降至趋于零。结合表3中交互项F可知,各因素交互作用依次为CD>AC>BC。


表2 响应面试验设计及结果Table 2 Design and results of response surface analysis
由图6(a)、6(c)可知,随着温度的升高,TFAs相对含量先减小再增加,但增加的幅度偏小。由图6(a)、6(b)可知,搅拌速率加快,TFAs相对含量逐步降低;由图6(b)、6(c)可知,时间延长,TFAs相对含量先降低再升高,但升高幅度极小。结合表4中交互项F可知,各因素交互作用依次为CD>BD>BC。

表3 碘值回归方程方差分析Table 3 Variance analysis of iodine value regression equation

图5 交互作用对碘值影响的响应面Fig.5 Response surface plots describing effects of interactions on iodine value

表4 反式脂肪酸含量回归方程方差分析Table 4 Regression equation variance analysis of trans fatty acids content
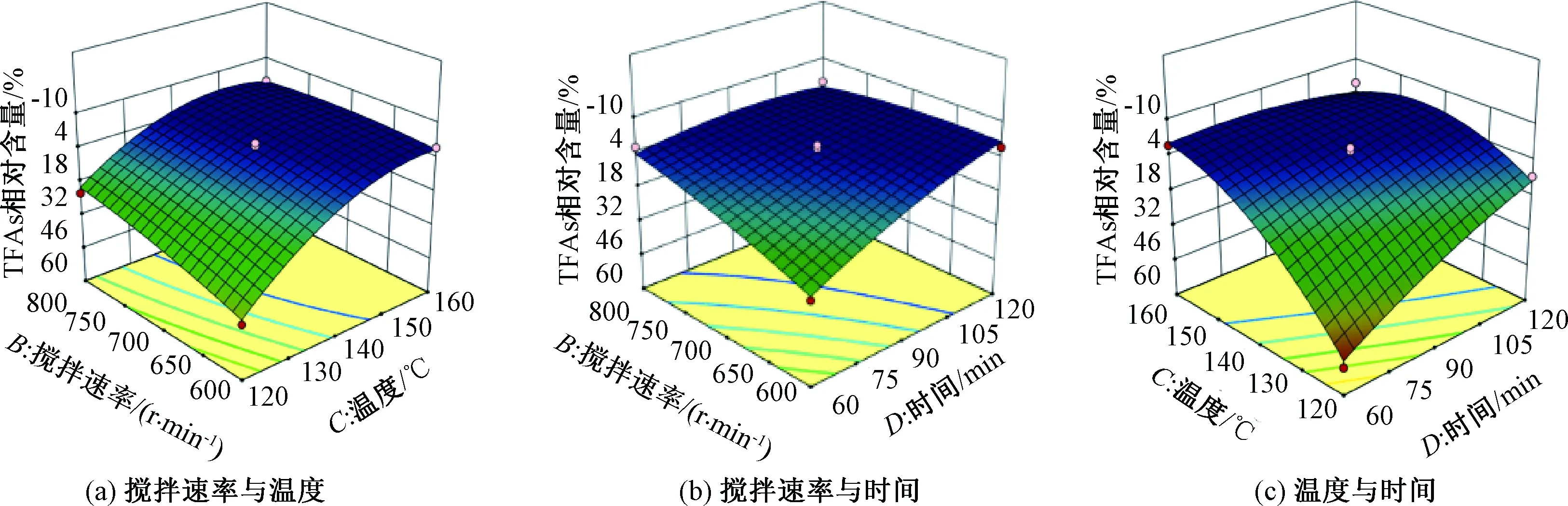
图6 交互作用对TFAs相对含量影响的响应面Fig.6 Response surface plots describing effects of interactions on relative content of TFAs
经Design-Expert 13软件分析得到最佳工艺参数:镍载量0.079%,搅拌速率617 r/min,温度138 ℃,时间115 min,相应模型预测碘值为3.60 g/100 g,TFAs相对含量为0.25%。在最佳工艺参数下进行3次平行验证试验,氢化棉籽油的碘值为(2.40±0.62) g/100 g、TFAs相对含量0.19%±0.02%,与预测值相近。该模型可较准确地预测氢化油样的碘值及TFAs相对含量,在该模型预测的最优工艺下可以制备“零”反式酸全氢化棉籽油。
2.3 全氢化棉籽油表征
2.3.1 全氢化棉籽油的SFC
固体脂肪含量是在一定温度下脂肪中固体的百分比,可对油脂的固相特性进行量化的描述[17]。合适的SFC曲线在很大程度上决定了油脂的塑性行为。由图7可知,在0~50 ℃范围内全氢化棉籽油的SFC在90%以上,且随温度升高基本不变;60~65 ℃范围内,SFC由66.8%±0.5%降为3.6%±0.8%,说明在此阶段大量脂肪由固脂熔化为液油。65~70 ℃,SFC逐渐趋于0%,因此可知全氢化棉籽油完全融化的温度为65 ℃左右,与所测得的全氢化棉籽油熔点(63.5±0.5) ℃相近,55~65 ℃之间塑性范围窄,可以作为原料参与酯交换以调整所需脂肪的塑性。

图7 全氢化棉籽油的SFCFig.7 Solid fat content of fully hydrogenated cottonseed oil
2.3.2 差示扫描量热图谱及脂肪酸组成
全氢化棉籽油的DSC图谱(图8)显示结晶曲线在46.3 ℃呈现单一放热峰,融熔曲线在50.9 ℃、60.5 ℃处出现吸热峰,中间出现放热峰归因于多晶型转变过程中的重结晶[25],吸热峰尾熔化终点为65.2 ℃,与65 ℃时的SFC相对应,说明样品中甘三酯熔融范围比较集中,组分较为单一[15]。如表5所示,全氢化棉籽油脂肪酸组成主要为棕榈酸和硬脂酸,两者含量可高达92%,大量的长链饱和脂肪酸使得全氢化棉籽油中存在高含量分子结构类似的高熔点甘三酯;结晶峰(46.6 ℃处)温度低于吸热峰是由于甘三酯进入晶格需要一定时间从而导致结晶出现“滞后”现象[26]。
2.3.3 X射线衍射图谱
X射线衍射图谱(图9)显示全氢化棉籽油在晶面短间距0.42 nm及0.38 nm处存在强衍射峰,在0.432 nm、0.406 nm处存在与强峰极近的较弱衍射峰。研究表明:短间距在0.46 nm的衍射峰为β型,在0.415 nm代表α型、β′型的两个强短间距分别为0.38 nm和0.42 nm,以及其他弱间距分别为0.427 nm、0.405 nm、0.397 nm和0.371 nm[27-28]。根据对比分析可知全氢化棉籽油的晶型为β′。在人造黄油和起酥油的基料油配方中,适量加入以β′ 型为主的高熔点全氢化棉籽油可以赋予产品优良的塑性、涂抹型及口感[29-30]。

表5 氢化试验前后棉籽油脂肪酸组成Table 5 Fatty acid composition of cottonseed oil before and after hydrogenation experiment %

图8 全氢化棉籽油的DSC图谱Fig.8 DSC melting and crystallization curves of fully hydrogenated cottonseed oil

图9 全氢化棉籽油的XRD图谱Fig.9 XRD spectrum of fully hydrogenated cottonseed oil
2.3.4 全氢化棉籽油的微观形态
如图10所示,全氢化棉籽油晶体轮廓明显,晶体形态呈发散针状形并聚集形成晶簇,且晶簇分布紧密。通常情况下,较有序成核的晶体网络具有较高的分形维数,而较无序成核的晶体网络分形维数较低[16]。通过应用ImageJ.JS粒子计数算法算出全氢化棉籽油偏光图分形维数D=1.60±0.02,此值与国外研究β′ 晶型图中较高的D(1.45~1.76)近似[31],因此全氢化棉籽油具备较有序成核的晶体网络结构,此有利于包裹液油,防止油脂在储藏过程中因油脂迁移而产生起霜现象[1]。

图10 全氢化棉籽油的偏光显微图Fig.10 Polarization micrograph of fully hydrogenated cottonseed oil
3 结论
通过单因素试验考察了棉籽油氢化过程中镍载量、搅拌速率、温度、时间对氢化棉籽油碘值及TFAs相对含量的影响,并利用响应面法优化了工艺条件,得到全氢化棉籽油最优制备工艺条件为镍载量0.079%、搅拌速率617 r/min、温度138 ℃、时间115 min。此条件下氢化棉籽油碘值为(2.40±0.62) g/100 g、TFAs相对含量0.19%±0.02%,满足了棉籽油零反式酸全氢化的要求。通过SFC、DSC、XRD以及偏光显微镜对全氢化棉籽油进行分析表征,结果表明其熔点高、组分单一并呈现出β′ 晶型的特征,可用于复配液态油通过酯交换等方法制备宽塑性专用油脂基料油。
