无定形态小分子糖对枣粉水分吸附及玻璃化转变的影响
2022-12-31杨忻瑞毕金峰陈芹芹金新文吴昕烨
杨忻瑞,毕金峰,陈芹芹*,金新文,吴昕烨,苟 敏
(1 中国农业科学院农产品加工研究所 农业农村部农产品加工重点实验室 北京100193 2 新疆农垦科学院农产品加工研究所 新疆石河子 832000)
枣(Zizyphus jujuba Mill.)是鼠李科(Rhamnaceae)枣属植物,它是落叶小乔木枣树的成熟果实,起源于中国,主要种植于黄河领域,现在世界上20 多个国家和地区都有种植[1-3]。如今,我国的枣品种多达1 000 多个,年产量占世界红枣总年产量的95%以上,且随着红枣近几年在生理和药理方面的应用越来越广泛,产量还在逐年上升[4]。现代研究显示,大枣中含有丰富的糖类、三萜类、氨基酸类等多种营养及功能性化学成分[5-8],其中,糖类成分为枣中含量较高的一类活性成分,且以可溶性多糖及小分子糖类成分为主。存在于枣中的小分子糖类成分以葡萄糖、果糖及蔗糖为主[4],该类成分是重要的营养物质,可供应机体能量,也是大枣中风味物质的前体物质,并与其补益功效发挥相关。
近年来,枣加工产品的种类和数量不断增多,随着人们对营养健康食品需求的提高,红枣及其制品作为药食同源食品越来越受到消费者的青睐,枣的深加工产品具有较大的市场潜力。目前市场上的枣产品已呈现多元化的趋势,除了传统的干枣和枣脯外,还出现了枣酒、枣醋、枣汁、枣粉等[9]。其中,枣粉能够更加充分地利用枣资源,解决枣不易贮藏的问题,且其营养丰富,食用方便,应用空间广阔,作为枣深加工产品备受消费者的喜爱。
枣粉中含糖量比较高,易受贮藏、运输和加工环境的影响而产生吸湿结块问题,影响加工利用率和食用安全性,导致流动性变差,外观品质下降。针对此问题,加工过程中常加入果胶酶进行酶解,或通过添加二氧化硅、硬脂酸钙、硬脂酸镁等抗结块剂,以减少枣粉黏结,增加流动性[10]。然而,前者成本较高,不适用于大规模的加工生产,后者与近年来越来越倾向于纯天然无添加的市场趋势不符,不符合天然产品的定位。贮存过程中,无定形小分子糖的玻璃化转变是导致枣粉吸湿结块及流动性下降的核心因素。玻璃化转变理论可以弥补水分活度作为食品稳定性衡量标准的缺陷[11]。根据非晶态无定形聚合物的力学性质随温度变化的特征,将食品分为玻璃态、橡胶态和黏流态,处于玻璃态的食品通常被认为是稳定的,玻璃化转变温度(Tg)已成为衡量食品品质的一个重要指标。宋慧慧等[12]基于玻璃化转变理论分析枸杞粉的玻璃化转变温度,通过构建水分含量与玻璃化转变温度的状态图确定枸杞粉具有良好稳定性的临界水分含量。周国辉[13]基于水分活度和玻璃化转变理论对大米淀粉体系的吸附等温线和Tg进行研究,发现提高大米淀粉体系的Tg有助于其稳定性。小分子糖含量对食品体系的水分吸附及Tg均会产生影响,向食品体系中加入一定量的糖后,其aw及水分含量会增加;含糖量较高的灰枣粉Tg较低[14]。麦芽糊精的添加显著增加了雪莲果粉的Tg[11]。此外,针对原料处理方式这一点,目前的研究多集中于直接研究原料中的糖组成[15],向原料中额外添加辅料[11],建立脱离原料基质的液体模拟体系[16]等方式,并不能除去原料中原有糖分的影响,或已脱离原物料固态基础。目前,无定形小分子糖含量及其组成对枣粉基质的水分吸附能力及玻璃化转变温度的系统性分析还鲜有报道。
本研究通过超声辅助法建立去糖枣片固态基质模拟体系(JSS),通过渗透改变固态基质模拟体系中的小分子糖组成,进而明确其对JSS 体系水分吸附、玻璃化转变及流动性的影响,旨在解决枣粉加工中易吸湿结块的问题。
1 材料与方法
1.1 材料与试剂
灰枣,中国新疆阿克苏当地果园。果糖、无水葡萄糖、食用蔗糖,北京萃锋科技有限公司。
1.2 仪器与设备
SB25-12DTN 超声波清洗器,宁波森茨生物科技有限公司;ZWH-KFY-BT4I/Hg 热泵干燥设备,正旭新能源设备科技有限公司;ICS-3000 离子色谱仪,赛默飞公司;X-射线衍射仪,美国Bruker Corp 公司;Q200 差示扫描量热仪,美国TA 公司;S-570 扫描电子显微镜,日本日立公司;动态水分吸附仪,英国SMS 公司;HR1848 飞利浦四合一榨汁机,珠海经济特区飞利浦家庭电器有限公司;Sigma 3K15 高速冷冻离心机,德国Sigma公司;水分活度仪,上海昌琨实业有限公司;FT4多功能粉质分析仪,英国Freeman Technology 公司;BSA224S 天平,赛多利斯科学仪器有限公司。
1.3 方法
1.3.1 去糖枣片固态基质构建 取500 g 灰枣用流动水清洗,去核器去核,切成约4.0 mm 的薄片。枣片去糖处理采用了Hou 等[17]等所述的方法并稍加修改。用去离子水在25 ℃下去除枣片中的糖,试验条件如下:将400 g 枣片放入4 L 去离子水中,置于超声波浴(40 kHz)中60 min。将溶有糖类物质的去离子水去除,然后在25 ℃下用4 L 的去离子水在超声波浴中将枣片重复去糖5 次,总共6 h,以获得去糖枣片基质JSS。
1.3.2 不同种类及比例小分子糖渗透实验 参照Ruiz-Cabrera 等[16]的方法并略作修改。在25 ℃条件下,将去糖枣片基质在不同种类及比例的糖溶液中搅拌渗透15 min(125 r/min),其中糖溶液浓度固定4%不变,枣片样品质量与溶液体积比固定为1/10。渗透后,用纱布迅速将枣片表面残余糖液吸干。糖溶液的种类及比例如表1 所示。在一元体系中,首先进行单种糖液的渗透;在二元体系中,选择两种小分子糖,且其比例符合原枣中的糖含量;在三元体系中,选择果糖(F)∶葡萄糖(G)∶蔗糖(S)=1∶1∶2 与F∶G∶S=2∶1∶1(均为质量比)两种比例,目的在于探究与原始枣粉含量贴近的情况下不同比例的小分子糖对JSS 特性的影响。

表1 糖溶液种类及配比Table 1 Type and proportion of sugar solution
1.3.3 枣粉制备工艺 采用热泵干燥设备对经不同糖溶液渗透后的枣片进行干燥,干燥温度为60℃,将枣片干燥至水分含量在4%左右。将干燥后样品分别置于粉碎机中粉碎10 s,重复3 次,共粉碎30 s。过60 目筛,得到的枣粉常温下放置在干燥器中保存。
1.3.4 指标测定方法
1.3.4.1 小分子糖含量测定 根据Simkovic 等[18]的方法进行了修改,通过配备脉冲安培检测(HPAEC-PAD)的高效阴离子交换色谱法对枣粉中的小分子糖含量进行分析。用50 mL 去离子水在超声波水浴中(40 kHz)提取2.0 g 枣粉30 min,然后在4 ℃下以12 000×g 离心20 min。收集上清液,采用水系0.22 μm 膜过滤后采用Dionex ICS-3000 系统进行小分子糖的测定。样品进样量为10 μL。采用Carbo PacTMPA20 色谱柱(3 mm×150 mm),A(水)和B(200 mmol/L NaOH)作为流动相,糖的梯度洗脱条件如表2 所示。

表2 小分子糖的梯度洗脱条件Table 2 Gradient elution conditions for small molecule sugars
1.3.4.2 X-射线衍射(XRD)测定 使用带有SolX检测器的Bruker D8 ADVANCE XRD 对所有经不同糖液渗透并干燥的枣粉进行结晶态或无定形状态测定。将所有样品放置在粉末载体上,以4 °/min的扫描速率在4°~60°的2θ 范围内进行测量[19]。
1.3.4.3 微观结构 采用扫描电镜(SEM)对枣粉的微观结构进行观察。将待测样品平铺与双面粘有导电胶的载物台上,经喷金处理后,置于扫描电子显微镜下观察枣粉1 000×倍的微观结构并采集图像。
1.3.4.4 水分含量及水分活度测定 依据GB/T 5009.3-2016 《食品安全国家标准 食品中水分的测定》[20]中的方法进行测定,称取1.5 g 粉体于干燥至恒重的铝盒中,于105 ℃干燥至恒重(两次测定差小于2 mg),测定结果以g 水/100 g 鲜样表示。称取1 g 枣粉样品,平铺在水分活度仪专用测试盒中,放入水分活度仪进行测定。
1.3.4.5 吸附等温线的测定 根据李聪等[21]的方法进行修改,称量约20 mg 样品置于样品盘中,将样品放置在温度25 ℃、氮气流速200 sccm、相对湿度(RH)0%的环境下干燥至质量恒重。然后环境RH 按10%增量自0%升至90%,设置每一阶段的dm/dt 值(m:样品质量;t:时间)为0.002 g/min,样品的质量每分钟记录一次。以水分活度为横坐标,以不同水分活度下平衡水分含量为纵坐标,绘制吸附等温线。
1.3.4.6 玻璃化转变温度(Tg)测定 参照侯皓男[22]和Hou 等[23]的方法并进行修改,使用差示扫描量热仪(DSC)来测定枣粉样品的Tg。将约7~9 mg 的样品称入坩埚中并用铝盖密封,使用空铝盘作为对照。样品温度以10 ℃/min 的速度从室温冷却至-70 ℃,平衡5 min,然后以10 ℃/min 的速度加热至100 ℃。通过热分析获得玻璃化转变的起始(Tgi),中间(Tgm)和结束(Tge)3 个温度,在该研究中,采用Tgm作为每个枣粉样品的Tg。
1.3.4.7 粉体流动性测定 粉体流动性选用FT4粉质仪Flowability 模式进行测定:设定螺旋搅拌角度5°,预处理搅拌速度40 mm/s,测定搅拌速度为100 mm/s。基本流动能(Basic flowability energy,BFE)是指在预处理后的指定体积粉末中建立一种特定流动模式时所需的能量,数值为叶片从粉末上端移动到底部所做的总功。
基本流动能计算公式:

式中,R——叶片的半径,mm;α——螺旋角,°;H——穿入粉体深度,单位;Fbase——螺旋桨垂直作用于颗粒床底部的作用力,N。
1.4 数据分析
采用SPSS 25.0 软件进行数据的方差分析,用Duncan's 法进行多重比较,采用Origin 2019软件绘图。数据以平均值±标准差表示,P<0.05 表示差异显著。每组试验均重复3 次。
2 结果与分析
2.1 小分子糖含量及XRD 分析
原始枣粉及JSS 体系经不同种类及比例糖溶液渗透后样品中小分子糖含量如表3 所示。在原始枣粉(9#)中,果糖含量为101.39 mg/g,葡萄糖含量为94.94 mg/g,蔗糖含量为232.90 mg/g,果糖、葡萄糖、蔗糖含量比例大致为1∶1∶2。根据前期渗透预试验结果,选择4%(w/w)糖液浓度进行渗透,使得到的枣片糖含量接近原始枣粉的糖含量。经去糖处理的JSS 体系(10#)中,果糖含量为1.43 mg/g,葡萄糖含量为1.55 mg/g,蔗糖含量为0.06 mg/g,去除率分别为98.59%,98.37%,99.97%,因此JSS 可作为无糖枣基质模拟体系开展进一步的渗透试验研究。经不同小分子糖渗透干燥处理后(1~8#),样品中果糖、葡萄糖、蔗糖含量范围分别为14.96~388.69,16.66~385.06,13.19~377.13 mg/g。样品中小分子糖总量在406.91~430.14 mg/g 之间,与原始枣粉中小分子糖总量(429.22 mg/g)较为接近。由图1a~d 可知,经不同比例小分子糖液渗透后,枣粉样品没有出现明显的结晶峰,表明样品及样品中的小分子糖此时处于无定形态。与结晶态相比,处于这种状态的原料具有更高的能级,因此不稳定[24]。由此可以得出,枣粉的不稳定性主要受小分子糖的严重影响。

表3 经不同种类及比例糖溶液渗透后JSS 体系中小分子糖含量Table 3 Small molecule sugar contents of jujube powder osmosed by different types and proportion of sugar solutions
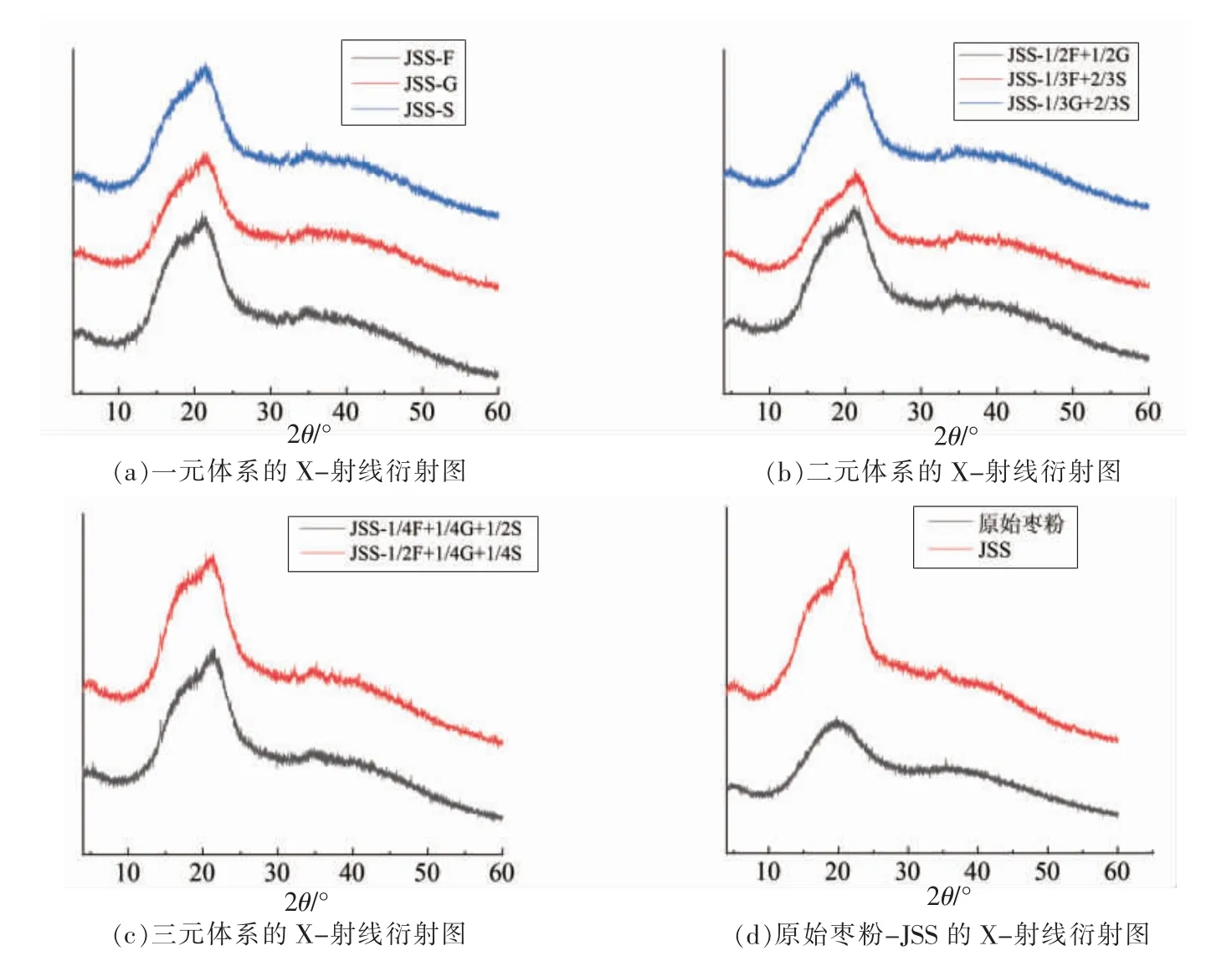
图1 经不同含量及比例糖溶液渗透枣粉的X-射线衍射图Fig.1 X-ray diffraction pattern of jujube powder osmosed with different content and ratio of sugar solution
2.2 无定形态小分子糖组成及含量对JSS 微观结构的影响
如图2j 所示,原始枣粉颗粒形状规则、表面光滑;去糖处理后,枣粉颗粒变为不规则的网状结构,且仅剩基质骨架(图2i)。这是由于超声处理后,枣粉颗粒中可溶性物质大量减少,形成较为空洞的基质骨架结构。Athmaselvi 等[25]发现含糖量较高的番石榴和山榄果冻干粉体颗粒为表面光滑的球形。吕健等[26]研究发现含糖量较少的西藏光核桃粉为不规则的片层状大颗粒,均与本试验结果具有一致性。
经不同糖液渗透后,可溶的糖类物质虽重新将不规则的网状结构填充,但表面仍旧呈不光滑状态,且表面附着有细小颗粒。在一元体系中,经果糖渗透后的枣粉颗粒表面最为光滑(图2a、2b、2c)。在二元体系中,枣粉颗粒表面均呈不规则的片状,仍存在部分空洞状结构(图2d、2e、2f)。三元体系中,糖类物质对网状结构的填充更为充分,表面为片层结构(图2g、2h)。

图2 不同含量及比例糖溶液渗透枣粉的微观结构Fig.2 The microstructure of jujube powder osmosed by sugar solutions with different content and proportion
2.3 无定形态小分子糖组成及含量对JSS 水分含量与水分活度的影响研究
对所有经不同种类及比例糖溶液渗透的枣粉样品进行热泵干燥,将湿基水分含量控制在约4%(图3a)。显著性差异结果显示(表3),样品中3 种小分子糖总量高的组别(2#、3#、4#、5#、8#、9#)水分含量显著高于小分子糖总量低的组别(1#、6#、7#、10#),这可能是由于含糖量高的样品水分吸附能力较强,干燥过程中水分不易与非水组分分离,导致水分含量较高。样品中3 种小分子糖总量无显著性差异的组别(2#、3#、4#、5#、8#、9#),水分含量虽均无显著性差异,但其水分活度受到不同比例小分子糖含量的影响(图3b)。例如8# 与9#中,3 种小分子糖总量虽无显著性差异(P<0.05),水分含量也无显著性差异,但8# 水分活度比9#高13.93%,且具有显著性差异,可能是由于8# 中果糖占比(50.32%)远高于9 组(23.62%),而果糖与水分子的结合比葡萄糖、蔗糖都更为紧密。侯春辉[27]研究发现,向胡萝卜脆片中加入一定量果糖或麦芽糖醇后,水分活度显著升高,与本研究结果规律相似。

图3 经不同种类及比例糖溶液渗透的枣粉的水分含量及水分活度Fig.3 Water content and water activity of jujube powder osmosed by different types and proportion of sugar solutions
2.4 无定形态小分子糖组成及含量对JSS 水分吸附的影响
枣粉的吸附等温线对于预测加工或存储过程中的稳定性非常重要[28],由于水分吸附行为导致枣粉吸湿结块,枣粉也就失去了最重要的外观品质。在目前研究的相对湿度范围内(RH 0~90%),根据Brunauer 等[29]的分类,所有样品的吸附等温线均为III 型典型S 形曲线。在恒定温度下,所有样品的平衡含水量都随着RH 的升高而显著增加(图4)。
由图4d 可知,原始枣粉在低湿度条件下(aw<0.4)水分吸附较慢,在高湿度条件下(aw>0.4)水分吸附速度迅速增长,并且在水分活度为0.9 时,水分吸附量达到58%以上。与其它经糖渗透的样品相比,在水分活度达到0.4 前,JSS 吸湿更快(图4a~d),这与其微观结构有关,此时期微观孔隙大,吸湿速率快。水分活度达到0.4 后,水分吸附增长变慢,此时期相对湿度较大,孔隙饱和较快,故吸湿速率降低。水分吸附是非常复杂的过程,吸附过程中可能伴随聚合物结构的变化[30]。添加糖类可能导致分子中亲水/吸水位点间的比例改变,进而导致其吸附特性发生变化。
一元体系中的水分吸附能力顺序为:JSS-F>JSS-G>JSS-S(图4a),由文献可知3 种小分子糖的水分吸附能力顺序为果糖>葡萄糖>蔗糖[31],与预期结果相符,表明JSS 对单种小分子糖的水分吸附能力无显著影响。在二元体系中,水分吸附能力顺序为JSS-1/2F+1/2G >JSS-1/3F+2/3S>JSS-1/3G+2/3S(图4b)。果糖与葡萄糖含量达95.90%的JSS-1/2F+1/2G 组(分别为201.04 mg/g,211.41 mg/g)水分吸附能力最强。JSS-1/2F+1/2G 组与JSS-1/3F+2/3S 组小分子糖总量无显著性差异,在aw为0.9 时,果糖与葡萄糖含量达95.90%的JSS-1/2F+1/2G 组(分别为201.04 mg/g,211.41 mg/g)水分吸附能力比果糖与蔗糖含量达95.50%的JSS-1/3F+2/3S 组(分别为153.53 mg/g 和257.23 mg/g)高出5.73%。在三元体系中(图4c),JSS-1/2F+1/4G+1/4S 组样品中果糖占比达50.32%,远高于JSS-1/4F+1/4G+1/2S 组样品(24.68%),当aw=0.9时,JSS-1/2F+1/4G+1/4S 组样品水分吸附能力比JSS-1/4F+1/4G+1/2S 组高21.68%。这是可能是由于果糖的Tg低并且在加工过程中没有结晶发生,因此无定形果糖具有更强的水分吸附能力。由于小分子糖总量显著降低,JSS 的水分吸附能力比原始枣粉降低104%(图4d)。

图4 经不同种类及比例糖溶液渗透的枣粉的吸附等温线Fig.4 Adsorption isotherms of jujube powder osmosed by different types and proportion of sugar solutions
2.5 无定形态小分子糖组成及含量对JSS 玻璃化转变温度的影响
有文献报道指出,食品的Tg是多组分相互作用的结果,不同比例的组分对Tg有显著影响[32-33]。如表4 所示,在一元体系中,玻璃化转变温度的趋势为1#<2#<3#,表明3 种小分子糖降低JSS的Tg 的顺序为果糖>葡萄糖>蔗糖,这与Lee 等[34]测定果糖、葡萄糖、蔗糖的Tg结果一致,也与Ruiz-Cabrera 等[16]报道的结果相似。在二元体系中,果糖含量占比46.74%的第4 组比果糖含量占比3.68%的第6 组Tg低20.00%。在三元体系中,果糖含量占比50.32%的第8 组比果糖含量占比24.68%的第7 组Tg低23.80%。石启龙等[35]报道,向南美白对虾肉中添加10%果糖后,其Tg降低,糖类的添加降低了单分子层含水率。Ruiz-Cabrera 等[36]报道了他们对果糖、葡萄糖、蔗糖和变量响应混合物的试验,发现随着果糖含量的增加,Tg降低,均与本研究结果相似,因此小分子糖含量能够显著影响食品的Tg。与原始枣粉相比,JSS 糖含量降低140.66%,Tg为30.75 ℃,这是由于其含糖量显著降低的缘故,表明降低小分子糖含量可以有效降低枣粉的Tg。

表4 不同种类及比例糖溶液渗透后枣粉的玻璃化转变温度Table 4 Glass transition temperature of jujube powder osmosed by different types and proportion of sugar solutions
2.6 无定形态小分子糖组成及含量对JSS 基本流动能的影响
粉体的基本流动能(BFE)越大,需要外界提供的能量越多,粉体流动性越差。由图5 可知,在一元体系中,体系BFE 的变化趋势为1# 组>2#组>3# 组,果糖占比由92.87%降至6.04%,BFE 降低19.87%,即体系流动性下降19.87%。在二元体系中,BFE 的变化趋势为4# 组>5# 组>6# 组,果糖占比由46.74%降至3.68%,BFE 降低17.12%,果糖降低BFE 的效率降低,可能是由于蔗糖与葡萄糖的占比有所增加。在三元体系中,体系BFE 的变化趋势为8#组>7#组,果糖占比由50.32%降至24.68%,BFE 降低21.18%,表明改变体系中3 种小分子糖的比例,降低果糖占比,可有效降低体系的基本流动能,增加粉体的流动性。这可能是由于小分子糖比例影响了粉体颗粒的表面粗糙程度、粒径等因素,使得颗粒间的黏结程度增大,粒径分布不均匀[21],宋慧慧等[12]在基于玻璃化转变及流动特性的枸杞粉贮藏稳定性的研究中发现,随着枸杞粉粒径的降低,使其发生流动所需要的能量越大,小分子糖比例与粉体粒径之间的关联有待进一步研究。

图5 不同种类及比例糖溶液渗透后的枣粉的流动性Fig.5 The flowability of jujube powder osmosed by different types and proportion of sugar solutions
2.7 相关性分析结果
进一步对JSS 体系经不同比例糖液渗透处理后的水分活度、水分吸附量(W,aw=0.9 时)、玻璃化转变温度、基本流动能以及果糖(F)、葡萄糖(G)、蔗糖(S)含量变化进行相关性分析。由表5 所示,aw与BFE 呈显著正相关;果糖含量与Tg呈极显著负相关;果糖含量与BFE 呈极显著正相关。这表明果糖对Tg和BFE 均产生显著影响。如图6 所示,将果糖含量与Tg进行线性拟合,得到相关性系数R2=0.9059,可知果糖与Tg之间存在一定的线性相关关系。通过PCA-X 获得载荷得分图,如图7 所示,PCA 获得两个主成分PC1 和PC2,分别解释了样品总体变异的49.8%和21.9%,其中果糖(F)和Tg在两个主成分方向上都呈负相关,果糖和BFE 在PC1 上呈正相关,在PC2 上呈负相关,进一步说明了果糖对Tg、BFE 均产生了显著影响。

图6 Tg-果糖含量线性拟合图Fig.6 Tg-fructose linear fitting graph

图7 不同种类及比例糖溶液渗透对JSS 水分吸附、玻璃化转变及流动性的PCA-X 载荷得分图Fig.7 PCA-X load score graphs of different types and ratios of sugar solution osmosis on JSS moisture adsorption,glass transition and fluidity

表5 不同种类及比例糖溶液渗透后枣粉的理化特性的相关性分析Table 5 Correlation analysis of physical and chemical properties of jujube powder after infiltration of different types and proportions of sugar solutions
3 结论
本试验通过超声辅助处理构建了去糖枣粉固态基质模拟体系(JSS),其中果糖、葡萄糖及蔗糖的去除率分别为98.6%,98.4%,99.9%,因此JSS可作为无糖枣基质模拟体系开展进一步的渗透实验研究。对经不同比例小分子糖溶液渗透的JSS的水分吸附特性、玻璃化转变温度及基本流动能(BFE)等进行测定和分析,结果表明,不同比例的无定形态小分子糖能够显著影响枣粉的水分吸附特性、Tg与BFE,且其中果糖含量与Tg呈极显著负相关,与BFE 呈极显著正相关。果糖占比降低25.64%时:粉体水分吸附量(aw=0.9)降低21.68%;粉体Tg升高23.80%,在较大程度上增加了体系的Tg,有利于粉体的稳定性;BFE 下降21.18%,显著增加了粉体的流动性。3 种无定形小分子糖降低JSS Tg的能力顺序为果糖>葡萄糖>蔗糖。此外,通过降低枣粉中小分子糖总量也可有效降低枣粉体系的水分吸附量、提高Tg与粉体流动性。综合来看,降低枣粉基质中果糖所占比例或降低枣粉中小分子糖总含量均对调控枣粉基质吸湿特性和改善枣粉易吸湿结块问题具有重要意义。然而,去糖枣粉固态基质是一个复杂的食品体系,枣粉基质中小分子糖与其它内源组分是否存在相互作用,以及该相互作用对枣粉吸湿特性的影响机制还有待进一步研究。
