新型酰基氨基酸类质子化离子液体的合成及其吸收CO2的研究
2022-12-05邱悦花儿
邱悦,花儿,2,3*
(1 北方民族大学化学与化学工程学院,宁夏 银川 750021;2 国家民委化工技术基础重点实验室,宁夏 银川 750021;3 宁夏太阳能化学转化技术重点实验室,宁夏 银川 750021)
离子液体(Ionic Liquids,ILs)通常是指由阴阳离子构成的熔点低于100 ℃的离子化合物[1-2]。它具有较高的热稳定性、较宽的液态范围、较高的离子电导率、对溶质的选择溶解性和不易挥发等物理化学性质[3],因此,其作为反应溶剂[4-5]、吸收剂、催化剂[6]和电解质在有机合成[7-8]、工业废气的吸收及电化学领域[9-10]受到研究者们的关注。通过改变所组成阴阳离子的种类,可以得到不同物理化学性质的ILs[11],因此经过设计的ILs具有更为广泛的应用性。而PILs (Protic ionic liquids, PILs)作为ILs的一大分支,除了具有ILs的上述特性以外,其结构中具有能够迁移的质子,表现出更加优良的性能。如果将PILs设计为具有多个氨基官能团的功能性PILs,可作为CO2、SO2、H2S等的优良的吸收剂[12-13]。
典型ILs的结构中一般都含有氟元素,比如PF6、BF4、TFA、TFSA及TFS类ILs,在回收处理过程中可能会对环境以及人体造成不良影响。氨基酸类ILs(Amino acid ionic liquids,AA-ILs),因其结构中不具有氟元素而易于生物降解[14-15],原料易得而成本低等优势,作为一种新型绿色环保型ILs,将成为今后的离子液体领域的热门课题[16-17]。
因此,本研究合成6种两类酰基氨基酸类质子化离子液体(Amino acid protic ionic liquids,AA-PILs),即己基乙二胺-酰基丙氨酸型和异辛基乙二胺-酰基丙氨酸型AA-PILs,并分析讨论其物理化学性质及吸收CO2的能力。该类AA-PILs结构中不含氟,可作为CO2等工业废气的绿色吸收剂。并且,其阳离子部位具有螯合胺结构(两个氨基),比单胺类PILs吸收CO2的能力更强,因此,选用其中异辛基乙二胺-酰基丙氨酸型AA-PILs开展了吸收CO2的研究。
1 材料与方法
1.1 材料
DL-丙氨酸(DL-Alanine, CAS No.302-72-7)、辛酰氯(Octanoyl chloride, CAS No.111-64-8)、癸酰氯(Decanoyl chloride, CAS No.112-13-0)、月桂酰氯(Dodecanoyl chloride, CAS No.112-16-3)均购置于多点化学,甲醇和石油醚购置于国药集团,氢氧化钠(天津科密欧)、硫酸和正己烷(天津大茂试剂)及乙醚(北京化工),以上均为分析级别。其中,乙醚在分子筛中浸泡过夜经蒸馏后使用。己基乙二胺(Hexylethylenendiamine, Hex-en)和异辛基乙二胺(Ethylhexylethylenendiamine, EtHex-en)均在实验室合成。
1.2 方法
1.2.1 酰基丙氨酸
以DL-丙氨酸与烷基(=辛、癸及月桂)酰氯为原料,分别合成了辛、癸及月桂酰基丙氨酸。以辛酰基丙氨酸(Octnoylalanine,简称HOctala)为例[18],其合成方法如下:将0.15 mol DL-丙氨酸,溶解于水、甲醇(体积比1∶3)混合溶剂后,用30%NaOH水溶液使其pH值调节至10.2~10.6之间。其中缓慢滴加0.15 mol辛酰氯的同时,继续用30%NaOH水溶液将pH调节保持在10.2~10.6之间,继续搅拌4 h。然后滴加30%硫酸水溶液调节其pH至3.8,自然过滤除去硫酸钠白色沉淀,得到无色透明澄清液体,并减压浓缩滤液后,再依次用甲醇、乙醚、石油醚及正己烷分散后减压浓缩,最后获得白色蓬松粉末状辛酰基丙氨酸(Octanoylalanine, HOctala)。同法合成得到的癸酰基丙氨酸(Decanoylalanine, HDecala)和月桂酰基丙氨酸(Dodecylalanine, HDodala)均为白色晶体。其结构式如图1所示。并通过13C-NMR测定及CHN元素分析,鉴定了其纯度。
1.2.2 AA-PILs的合成
(1)合成。将(辛、癸及月桂)酰基氨基酸和烷基(=己基、异辛基)乙二胺,以1∶1摩尔比,分别溶于甲醇后,通过酸碱中和反应,得到了两大类六种AA-PILs,即,以异辛基乙二胺为阳离子的近似室温ILs的异辛基乙二胺-辛酰基丙氨酸(HEtHex-Octala)型、异辛基乙二胺-癸酰基丙氨酸(HEtHex-Decala)型、异辛基乙二胺-月桂酰基丙氨酸(HEtHex-Dodala)型AA-PILs和以己基乙二胺为阳离子的室温下白色粉末状的己基乙二胺-辛酰基丙氨酸(HHex-Octala)型、己基乙二胺-癸酰基丙氨酸(HHex-Decala)型、己基乙二胺-月桂酰基丙氨酸(HHex-Dodala)型AA-PILs。其结构式如图2所示。通过13C-NMR测定(图3)及CHN元素分析(表1),鉴定了其纯度。

图1 酰基丙氨酸的化学结构式
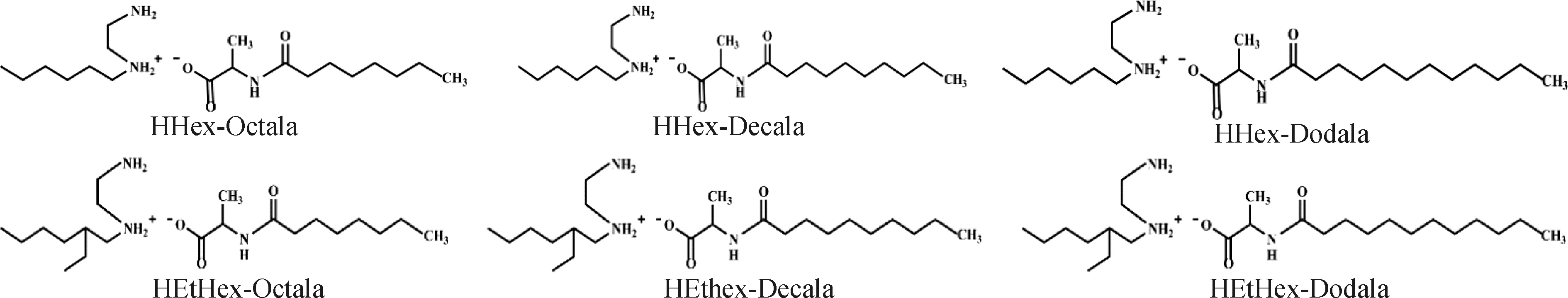
图2 AA-PILs的化学结构式
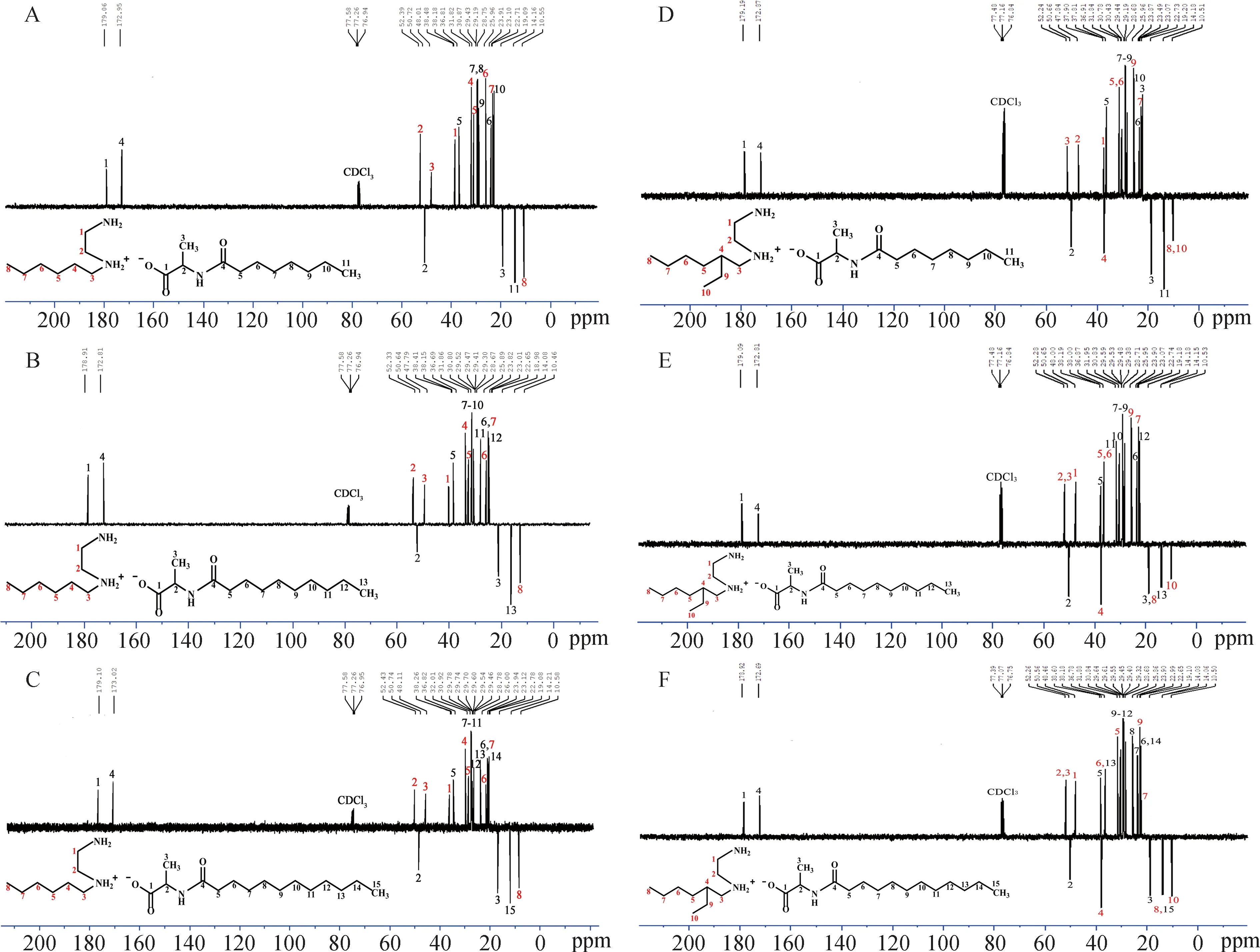
图3 AA-PILs的13C-NMR谱图
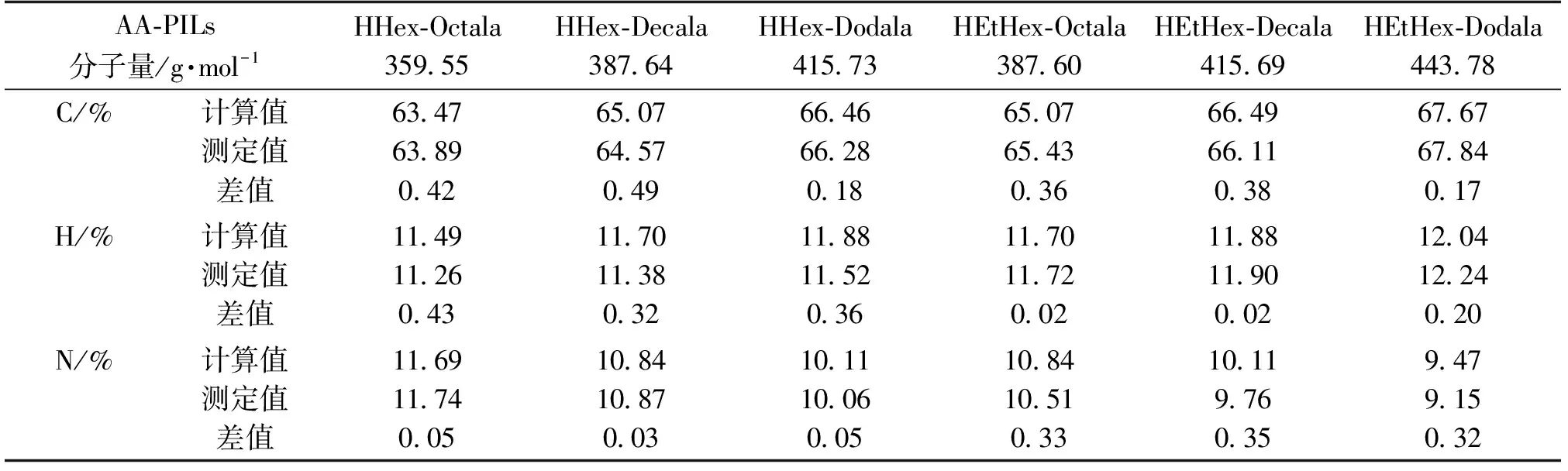
表1 AA-PILs的CHN元素分析结果
(2)13C-NMR 测定。利用Bruker 400 MHz核磁共振仪,以CDCl3为溶剂,测定了6种AA-PILs的13C-NMR谱图。
(3)水分含量的测定。本研究AA-PILs的极性较强而易于吸水[19]。因此,虽然进行了24 h的真空冷冻干燥,AA-PILs中含水量仍较高。利用Mettler Toledo的V20型卡尔费休水分仪测定6种AA-PILs的水分含量。
(4)CHN元素分析。利用Elementar Vario EL Cube元素分析仪和Elementar Analysensysteme GmbH 元素分析仪分别测定了己基乙二胺-酰基丙氨酸型AA-PILs(固态)以及异辛基乙二胺-酰基丙氨酸型AA-PILs(液态)的CHN元素的含量。
1.3 物性测定
1.3.1 溶解性
本研究6种AA-PILs的阴阳离子部位均具有亲水性基团和疏水性基团。开展了其在水和有机溶剂中的溶解性。
1.3.2 熔点
用差示扫描量热仪(TA Q20),将样品密封于铝盘中,在-50 ℃~150 ℃温度范围内,以3 ℃·min-1的升温速度,氮气为保护气氛条件下,测定了酰基丙氨酸以及AA-PILs的熔点。
1.3.3 热稳定性
热稳定性是评估离子液体物性及其应用的重要标准和基础。在加热中,将物质失重10%的温度定义为该物质的热分解温度[20]。使用Jupiter热重分析仪,研究了酰基丙氨酸以及AA-PILs的热稳定性。将样品密封于Al2O3坩埚中,以氮气为保护气、10 ℃·min-1的加热速率,在40 ℃~600 ℃温度范围内,测定其热分解温度。
1.3.4 吸收CO2后的物性
因为己基乙二胺-酰基丙氨酸型AA-PILs与异辛基乙二胺-酰基丙氨酸型AA-PILs的极性部位均含有两个氨基(乙二胺螯合结构),并且在吸收CO2过程中主要是氨基起到吸收作用,因此吸收能力应大致相同。又因为异辛基乙二胺型AA-PILs的熔点较低,均在30 ℃左右,在室温条件下的应用性更为优秀,因此选用3种异辛基乙二胺型AA-PILs进行吸收CO2的研究。
使用梅特勒-托利多FE28 pH计、1 mL Ostwald比重瓶(精度为±0.000 1 g·cm-3)、Lovis 2000M全自动微量粘度仪(精度为±1%)、梅特勒-托利多S230型电导率仪(精度为±1%),分别测定了3种AA-PILs/水混合体系(摩尔比1∶10)吸收CO2前后的pH值、密度、粘度及电导率值,全部实验中温度的控制由恒温油浴锅控制(精度为±0.1 ℃),在测定温度点保温15 min,每间隔5 min测定1次,取3次测定值的平均值。
2 结果与分析
2.1 13C-NMR 测定
6种AA-PILs的13C-NMR谱图如图3(a:HHex-Octala, b:HHex-Decala, c:HHex-Dodala, d:HEtHex-Octala, e:HEtHex-Decala, f:HEtHex-Dodala),谱图中可以看出,每个碳谱均符合其归属,无杂峰,可以判断其纯度高。
AA-PILs的-CH2NH2和-COO-中13C周围的电子云密度受电负性较强的N及O原子的影响,电子云密度降低,屏蔽效应减弱,共振信号在低场出现,化学位移(δ)值较大。例如,AA-PILs阴离子部位的C1, C4(δ=170~180 ppm)、C2, C5(δ=36~52 ppm)、以及阳离子部位的C1~C3 (δ=38~52 ppm)。相反,供电子基团使得临近13C周围的电子云密度增大,屏蔽效应增强,共振信号在高场出现,化学位移(δ)值较小。例如,与N、O原子较远的阴离子及阳离子烷基侧链部位13C谱的C6~C15以及C4~C10的δ值均在38 ppm以下。
2.2 水分含量的测定
HHex-Octala、HHex-Decala、HHex-Dodala、HEtHex-Octala、HEtHex-Decala及HEtHex-Dodala中水分含量分别为1.75%、2.60%、1.60%、1.53%、1.37%及1.48%(相当于w0=[H2O]/[AA-PIL]= 0.35、0.56、0.37、0.33、0.32及0.36)。将其作为初始含水量,进行了相关研究。
2.3 CHN元素分析
6种AA-PILs的CHN元素分析结果如表1所示,测定值与计算值差值均在±0.5%以内,纯度符合要求。
2.4 溶解性
本研究AA-PILs的阴阳离子部位均具有极性基团而极性较强。因此,易溶于水、甲醇及乙醇等极性溶剂。并且阴阳离子部位均具有较长的碳链,也显示疏水性,从而部分AA-PILs也能溶于氯仿等疏水性溶剂。表2中○、△和×分别代表w(g)/v(mL) 为 >10%(易溶),0.1%~10%(微溶)和 < 0.1%(难溶)。由表2可知,阳离子相同,阴离子不同时,在同种溶剂中,随着阴离子碳链的增长,其溶解度降低。而在阴离子相同条件下,阳离子为异辛基乙二胺时,与阳离子为己基乙二胺时比较,AA-PILs在水和甲醇中的溶解性更为优异,这主要是因为具有支链结构的异辛基乙二胺的极性比无支链的己基乙二胺较强。
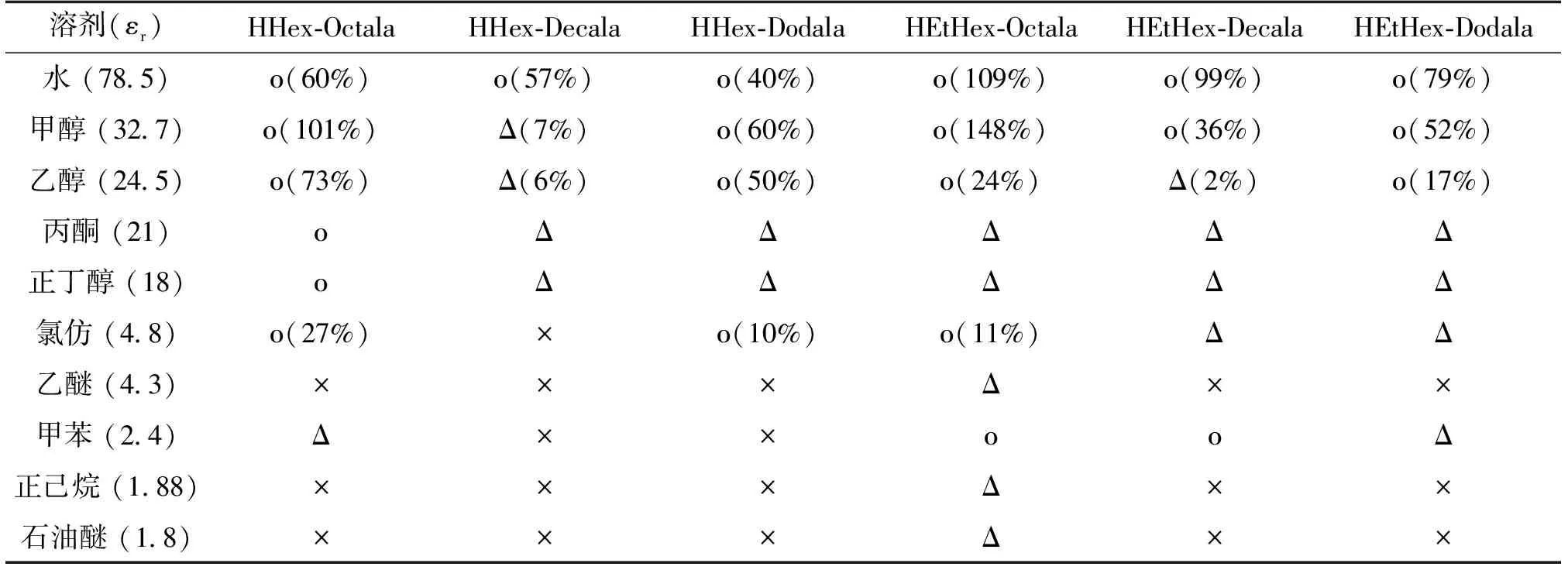
表2 AA-PILs在水和有机溶剂中的溶解性(25℃)
2.5 相转变温度
(1)酰基丙氨酸的熔点。3种酰基丙氨酸(HOctala、HDecala、HDodala)的熔点(Tm)分别为102.6 ℃、97.6 ℃、107.0 ℃,即其Tm在102 ℃±5 ℃(图4A)。可知,烷基侧链长度对其熔点影响不显著。
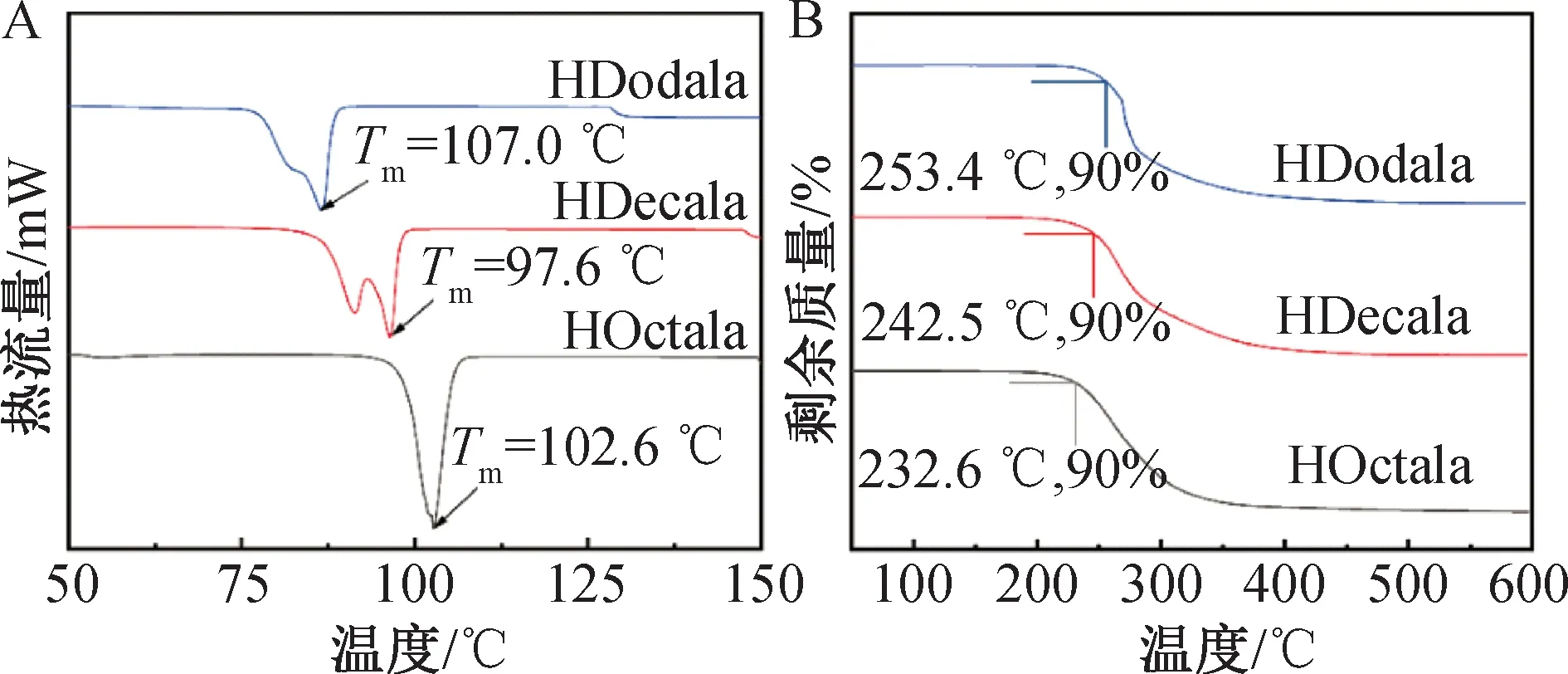
图4 3种酰基丙氨酸的熔点(A)及热分解温度(B)
(2)AA-PILs的相转变温度。6种AA-PILs的相转变温度如图4、表3所示,当阳离子部位为己基乙二胺时,即HHex-Octala、HHex-Decala及HHex-Dodala熔点在76.0±1.0 ℃范围内。然而,阳离子碳链结构中具有支链(2-乙基),即异辛基乙二胺(HEtHex+)时,其熔点降低至30 ℃左右。课题组前期研究的HEtHex-Hexala具有玻璃化转变温度(Tg=-35.6 ℃),液态范围宽[21]。因此,可以看出,AA-PILs分子结构的设计中,当阳离子结构具有支链时,可以降低AA-PILs的熔点,同时,如果将阴离子碳链长度(C8-C12)缩短至一定长度(例如C6)时也能够获得具有玻璃化转变的,室温或室温下呈液态的AA-PILs,其液态范围宽,从而可以扩大其应用范围(图5)。
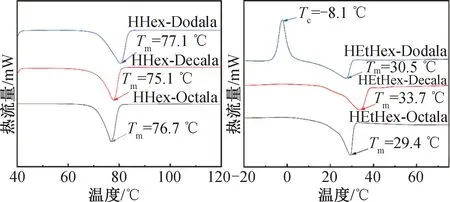
图5 AA-PILs的熔点
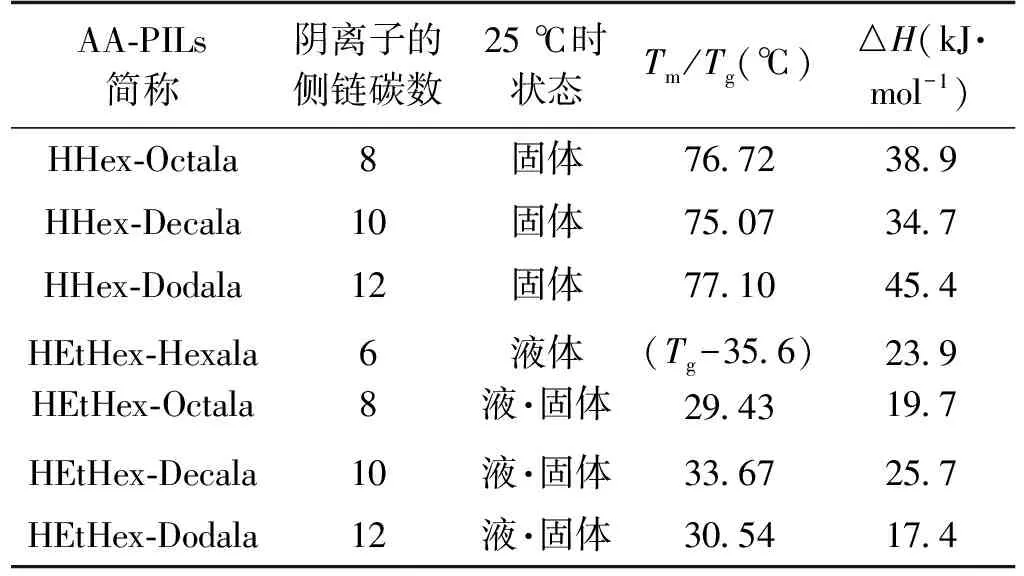
表3 AA-PILs阴离子部位碳链长度与相转变温度
2.6 热稳定性
热稳定性也是评估离子液体性能和应用的重要标准和基础,大多数离子液体具有良好的热稳定性,且蒸汽压极低,因此,AA-PILs可以代替传统挥发性有机溶剂,在有机合成、电化学及润滑剂领域中应用。本研究AA-PILs的阴离子原料为酰基丙氨酸,属于较弱酸,其酸性弱于碳酸。HOctala、HDecala、HDodala的热分解温度(Td)分别为232.6 ℃,242.5 ℃及253.4 ℃,即在243 ℃±10 ℃范围内。如图4B所示。由烷基乙二胺-酰基丙氨酸形成的AA-PILs阴阳离子间的相互作用较弱,因此,与含氟的本课题组TFS、TFSA型PILs比较[22],其热稳定性较低。AA-PILs的阳离子相同时,随着阴离子碳链增长(C8-C12)时,其热分解温度几乎不受影响。AA-PILs的结果详见图6。这可能是因为本研究AA-PILs阴阳离子间的氢键能在20~30 kcal·mol-1范围内、相互作用能在-135~-115 kcal·mol-1范围内,相差不大(本研究AA-PILs的阴阳离子间主要以分子与分子间氢键作用存在)[23]。
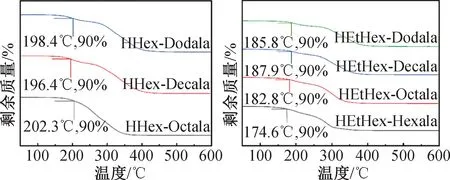
图6 AA-PILs的热分解温度
2.7 AA-PILs/水混合体系吸收CO2
用EtHex型AA-PILs/水混合体系(摩尔比1∶10)吸收CO2前后的pH、密度、粘度及电导率值如表4所示。结果显示,吸收CO2后混合体系的粘度增大,电导率升高,且其变化值较显著。同时也测定了吸收CO2前后的混合体系的13C-NMR谱图,以HEtHex-Decala为例(图7)。吸收CO2前后在175 ppm均出现酰基中的13C峰,而吸收CO2后均在165 ppm左右出现了新的13C峰,这可能是CO2与AA-PILs的氨基作用形成了氢键,进一步证明了AA-PILs吸收了CO2。另外,课题组通过密度泛函理论研究了HEtHex-Butala与CO2间的氢键作用,其氢键能小于4.00 kcal·mol-1,属于较弱强度的氢键作用。因此,综合考虑,本研究HEtHex-Acylala型AA-PILs均能够吸收CO2,并且初步判断AA-PILs吸收CO2为物理吸收。
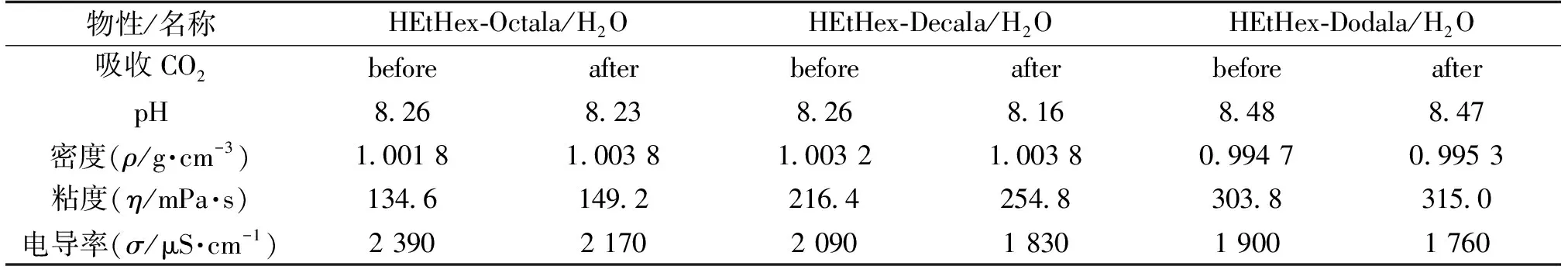
表4 AA-PILs/H2O(摩尔比1∶10)混合体系吸收CO2前后的pH、密度、粘度和电导率值
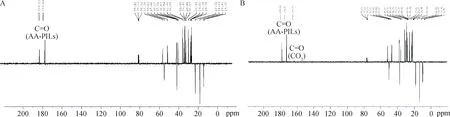
图7 HEtHex-Decala/H2O混合体系吸收CO2前(A),后(B)的13C-NMR谱图
2.7.1 粘度
由图8可知,当阳离子相同(HEtHex+)时,随着AA-PILs阴离子侧链碳数的增多,粘度呈增大趋势。并且,对于每个体系,吸收CO2后,与吸收CO2前比较,其粘度呈增大趋势,这可能是因为吸收CO2后AA-PILs与CO2分子间的作用力增强,形成氢键网络,使得粘度增大。
2.7.2 电导率
由图9可知,当AA-PILs阳离子(HEtHex+)相同时,随着AA-PILs阴离子侧链碳数的增多,电导率呈降低趋势。并且,对于每个体系,吸收CO2后,与吸收CO2前比较,体系的电导率值也呈降低趋势。
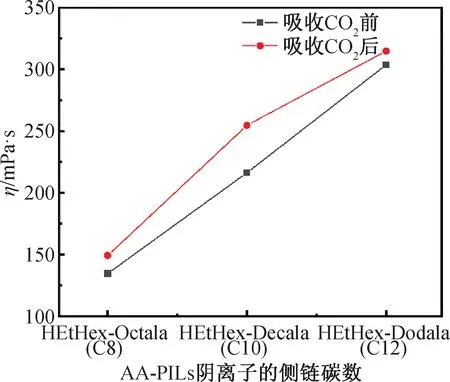
图8 AA-PILs/H2O体系吸收CO2前后的粘度值
这可能是随着阴离子部位碳链的增长和吸收CO2后,粘度增大而离子的迁移率降低导致。
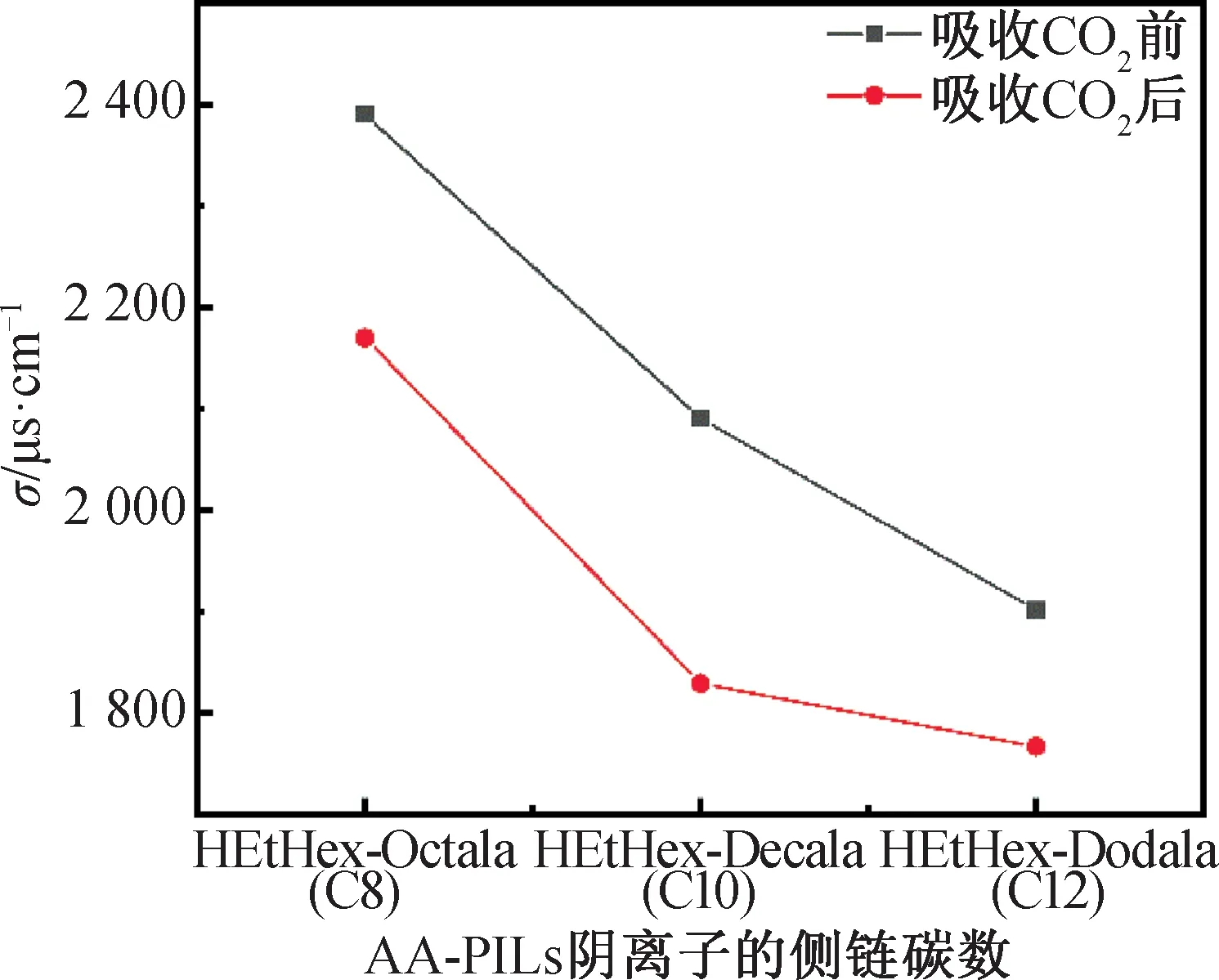
图9 AA-PILs/H2O体系吸收CO2前后的电导率值
3 结论
(1)合成了6种AA-PILs,其中HHex-Octala、HHex-Decala、HHex-Dodala、HEtHex-Decala、HEtHex-Dodala为新型AA-PILs。其阴离子设计为酰基氨基酸型,结构中不含氟,与传统含氟ILs比较,易于生物降解,绿色环保。
(2)本研究AA-PILs阴阳离子部位头部的极性较强,易溶于亲水性溶剂,同时,阴阳离子结构的侧链均为疏水性烷基基团也能溶于氯仿等疏水性溶剂。
(3)改变AA-PILs的阳离子结构,可以得到不同性能的AA-PILs,当其阳离子为己基乙二胺时,其熔点约为76 ℃,当阳离子为异辛基乙二胺时,其熔点下降至30 ℃左右。这说明了通过AA-PILs阳离子结构设计为具有支链时,可以获得熔点较低的AA-PILs。或同时进一步缩短阴离子部位的碳链长度时(比如C6),能够获得室温液态下的AA-PILs(比如HEtHex-Hexala)。
(4)AA-PILs/水混合体系(摩尔比1∶10)吸收CO2后,体系的粘度呈上升趋势,电导率值呈下降趋势。这说明了因为AA-PILs阳离子的极性部位为乙二胺,有利于吸收CO2。同时,它与传统胺类吸收剂和单胺类PILs比较,氨基数目多,对CO2的吸收能力强,与传统胺类吸收剂比较,易于生物降解,因此,其将成为CO2等工业废气的良好的可以作为CO2的绿色环保的吸收剂。另外,AA-PILs与水混溶后,既能够降低其粘度,又能够降低其成本。
