石灰铝法除氯工艺中铝源筛选及条件优化试验
2022-11-17黄鹏曾丽赵晓丹卢心澄赵琦琦周振
黄鹏, 曾丽, 赵晓丹, 卢心澄, 赵琦琦, 周振
(1.华能国际电力股份有限公司太仓电厂, 江苏 太仓 215424;2.上海电力大学 环境与化学工程学院, 上海 201306)
燃煤机组石灰石-石膏湿法烟气脱硫系统产生的废水具有水质复杂、 高盐分等特点, 处理难度大, 废水中Cl-浓度过高不仅会影响脱硫石膏品质和脱硫效率, 还可能造成设备腐蚀[1-2]。 脱硫废水中Cl-若能被有效去除, 可实现脱硫废水回用, 减少废水排放量甚至达到零排放[3-4]。
常见Cl-去除技术包括离子交换法、 膜分离法与石灰铝法等。 离子交换法设备投资低, 运行成本较低, 但树脂吸附容量有限, 需频繁清洗再生[5]。膜分离法清洁高效, 但运行成本昂贵、 易造成膜污染[6]。 石灰铝法是指向含氯废水中投加铝源与石灰生成难溶盐而去除Cl-[7]。 该方法适用于高盐废水中Cl-的去除, 常用铝源为NaAlO2, 其药剂利用率低、 投加量大、 成本高昂[8], 限制了石灰铝法在高盐废水中的应用, 因此亟需寻找替代性铝源实现废水中Cl-的高效去除。
本研究考察了不同铝源对石灰铝法去除Cl-效果的影响, 筛选出最佳铝源, 进一步探究了药剂投加量、 反应时间、 搅拌速率、 初始Cl-浓度、 温度等参数对其除氯效率的影响, 优化了石灰铝法除氯工艺条件, 为高盐废水中Cl-的高效去除提供理论支撑。
1 材料与方法
1.1 试验药剂
氯化钠、 氧化钙、 硝酸银、 铬酸钾, 以上试剂均为分析纯。 试验用铝源的主要成分及纯度见表1。

表1 铝源主要成分及质量分数Tab. 1 Main ingredient and mass fraction of Al source
1.2 试验用水
依据实际脱硫废水中Cl-浓度为150 ~400 mmol/L[9-10], 采用氯化钠配制Cl-浓度分别为150、200、 250、 300、 350 和400 mmol/L 的含氯废水作为试验用水。
1.3 试验方法
废水中先后投加石灰和铝源, 药剂投加量根据初始Cl-浓度以及钙、 铝、 氯元素物质的量之比确定, 采用六联搅拌仪匀速搅拌, 反应结束后静置、过滤, 测定滤液中Cl-浓度, 考察搅拌速率、 反应时间、 反应温度等对Cl-去除效果的影响。
1.4 分析方法
铝源和反应沉淀物经干燥、 研磨等处理后, 使用D8 Advance X 射线衍射仪(XRD)与JSM-7800F扫描电子显微镜(SEM)进行固体表征, 并采用Jade 6 软件进行XRD 分析。
按照GB/T 15453—2018《工业循环冷却水和锅炉用水中氯离子的测定》, 采用硝酸银滴定法测定Cl-浓度[11], 依据下式计算Cl-去除率(α)。
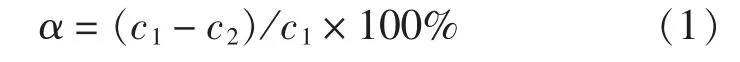
式中: c1、 c2分别为初始、 反应后Cl-浓度,mmol/L。
铝利用率(β)指实际参与反应的铝化合物的量与总投加量的比值, 计算公式如下:
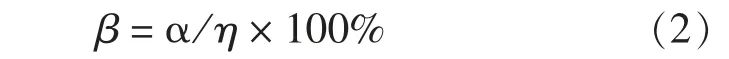
式中: α 为Cl-去除率; η 为铝、 氯的物质的量之比。
2 结果与讨论
2.1 铝源筛选试验
不同铝源的XRD 图谱见图1, 其中A、 B 2 种Al(OH)3的强衍射峰在18° 和20° 附近, 分别对应Al(OH)3(002)和(110)晶面的特征峰。 C、 D 2 种AlOOH 对 应的2θ 为28.199°, 38.387°, 48.817°,在这些位置均有宽化的衍射峰, 根据Scherrer 公式可知, 这2 种铝源晶粒细小, 结晶不完整[12]。
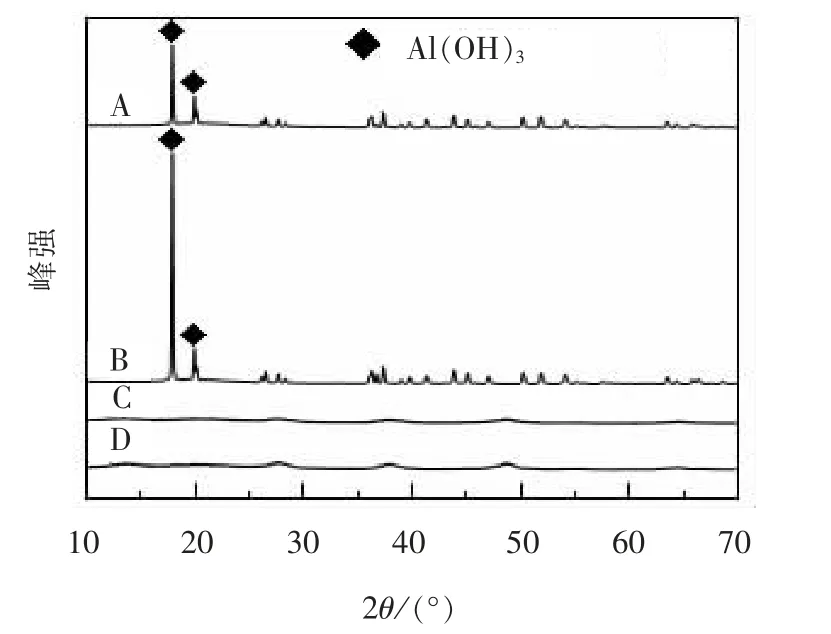
图1 不同铝源的XRD 图谱Fig. 1 XRD spectrum of different aluminum source
在初始Cl-浓度为200 mmol/L, 搅拌速率为400 r/min, 温度为35 ℃, 反应时间为2 h, n(钙) :n(铝):n(氯)=4.5 ∶1.5 ∶1 的条件下, 考察不同铝源对Cl-去除效果的影响, 结果如图2 所示。 在相同试验条件下, 大孔拟薄水铝石除氯效果明显优于其他3 种, Cl-去除率为53.5%, 铝利用率达到35.6%。 大孔拟薄水铝石除氯效果优越的原因是该药剂本身活性更强, 能在碱性条件下与Cl-结合生成(Ca2Al(OH)6)Cl·2H2O[13]; 相较于大孔拟薄水铝石, 其他铝源仅有少部分参与反应, Cl-去除率均低于15.0%, 这是因为其他铝源性质较稳定, 难以与石灰反应并捕获Cl-形成弗氏盐[14]。 后续试验将针对大孔拟薄水铝石进一步研究反应条件的影响。
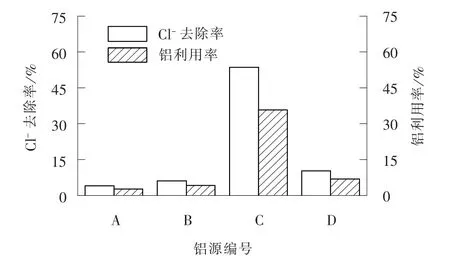
图2 不同铝源对Cl- 去除效果的影响Fig. 2 Effect of different aluminum source on Cl-removal
2.2 大孔拟薄水铝石除氯工艺条件优化
2.2.1 n(钙)/n(铝)对除氯效果的影响
在初始Cl-浓度为200 mmol/L, 搅拌速率为400 r/min, 反应温度为35 ℃, 反应时间为2 h 的条件下, 控制n(铝)/n(氯)为1.0、 1.5、 2.0, 考察n(钙)/n(铝)对Cl-去除效果以及铝利用率的影响,结果见图3。
由图3(a)知, 相同n(铝)/n(氯)条件下, 随着n(钙)/n(铝)的增加, Cl-去除率均有不同程度的提升, 当n(铝)/n(氯)为1.5 时, n(钙)/n(铝)从2.0增大到4.5, Cl-去除效果提升了13.6%。 然而, 当大孔拟薄水铝石投加量较低时(n(铝)/n(氯)为1.0), 增加石灰投加量对提高Cl-去除率作用较小。石灰铝法沉淀除氯的反应产物为弗氏盐[9], 其化学式中n(钙)∶n(铝) ∶n(氯) =2 ∶1 ∶1, 试验结果表明大幅增加钙、 铝的投加量才能使Cl-去除率提高至62.4%, 这是因为大孔拟薄水铝石难溶于水或碱性溶液中, 难以完全参与反应[15], 药剂利用率较低。 增加石灰投加量, 使溶液中存在大量Ca2+和OH-, 促进了[Ca2Al(OH)6]+层状结构的形成[16], Cl-会进入层板以平衡电荷, 最终形成弗氏盐沉淀。 因此增加n(钙)/n(铝)物质的量比可提高铝利用率。
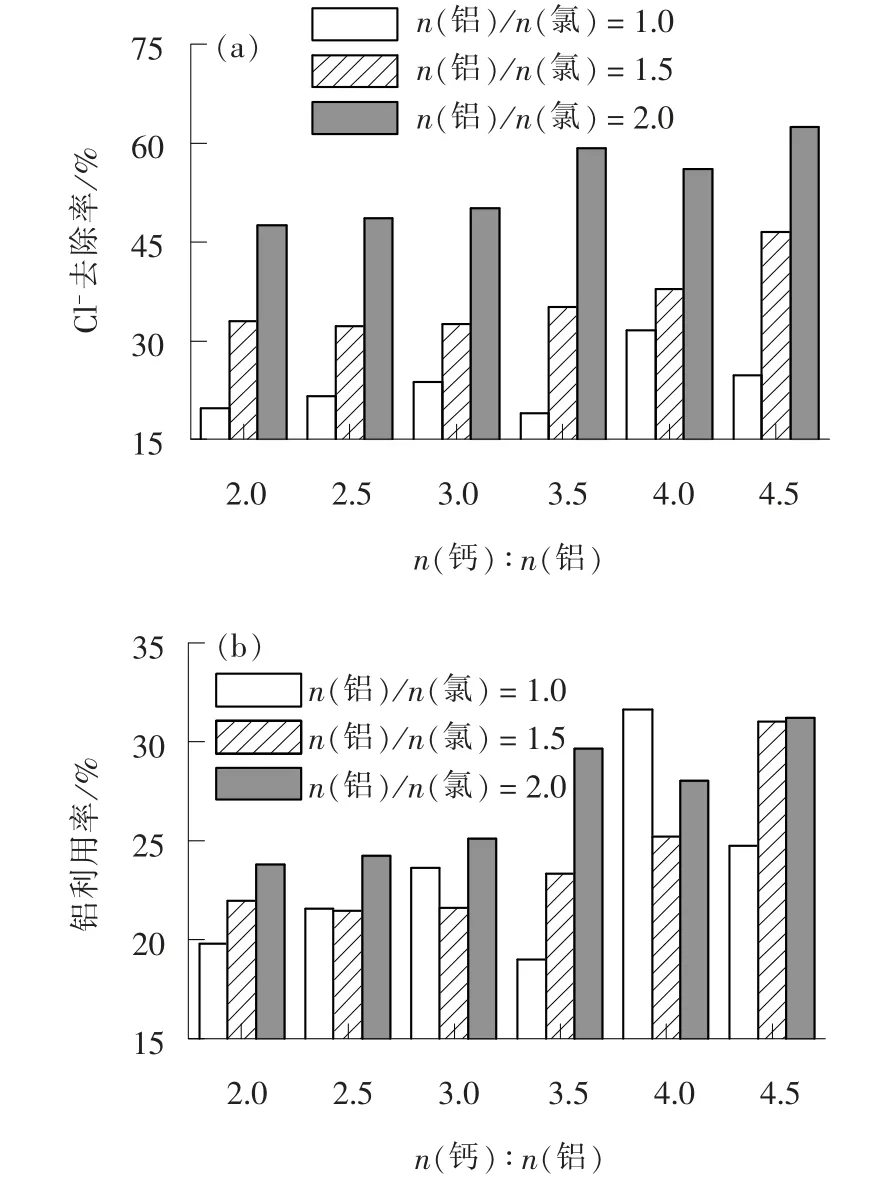
图3 n(钙) ∶n(铝) 对Cl- 去除效果及铝利用率的影响Fig. 3 Effect of n(Ca)∶n(Al) value on Cl-removal and alumium utilization rate
2.2.2 n(铝)/n(氯)对除氯效果的影响
在其他试验条件与上述试验条件相同的情况下,当n(钙)/n(铝)分别为3.5 和4.5 时, 考察n(铝)/n(氯)对Cl-去除效果及铝利用率的影响, 结果见图4。
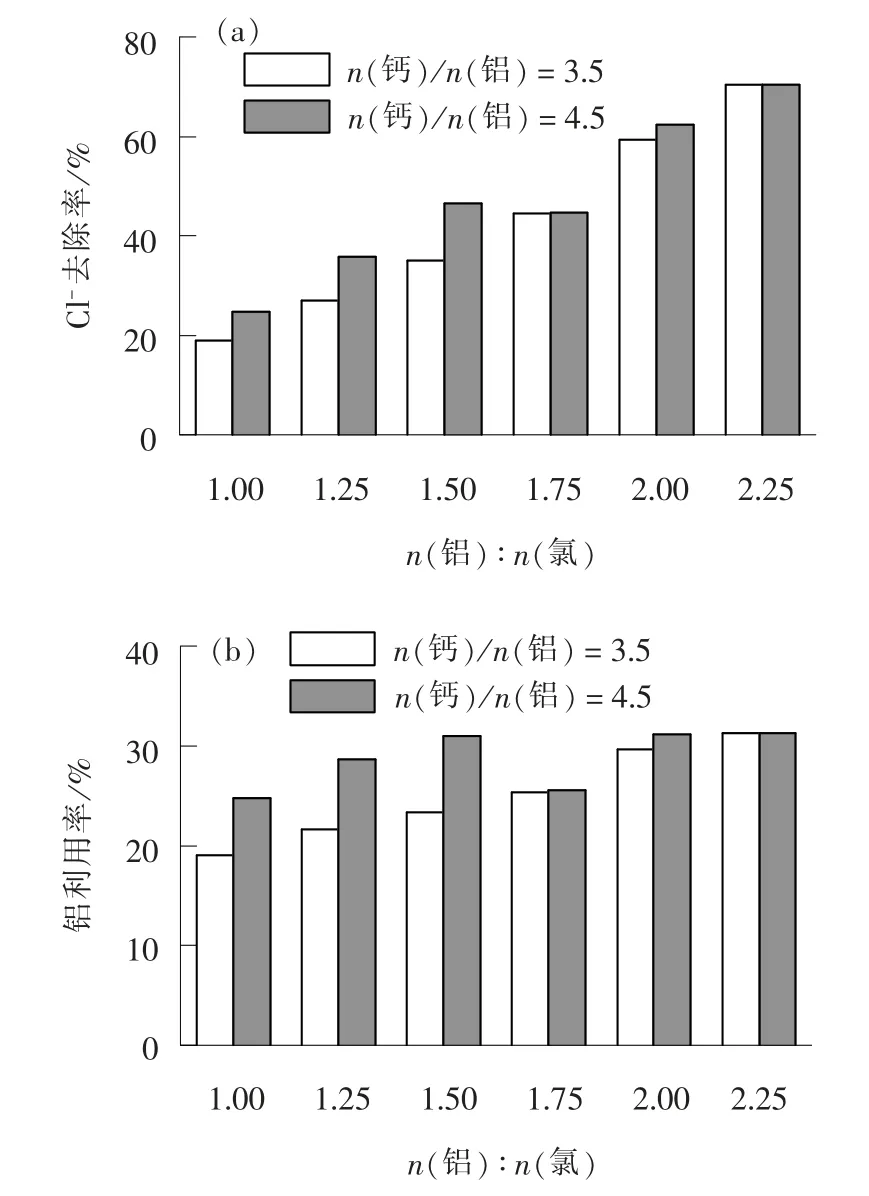
图4 n(铝) ∶n(氯) 对Cl- 去除效果及铝利用率的影响Fig. 4 Effect of n(Ca)∶n(Al) value on Cl-removal and alumium utilization rate
当n(钙)/n(铝)一定时, n(铝)/n(氯)增加能显著提升Cl-去除率, 当n(钙)/n(铝)为3.5 时, 随着大孔拟薄水铝石投加量的增加, 其铝利用率也随之升高; 而n(钙)/n(铝)为4.5 时, 铝利用率维持相近的水平。 说明当石灰和大孔拟薄水铝石投加量过大时, 离子浓度过高导致活度系数下降, 限制了弗氏盐沉淀反应的进行[17]。 因此, 当n(铝)/n(氯) >1.5 时, n(钙)/n(铝) 由3.5 增加至4.5, 对Cl-去除效果无显著作用。 此外, 药剂投加量过大会形成大量弗氏盐沉淀, 难以实现固液分离[9]。 因此, 以n(钙)∶n(铝) ∶n(氯) =7 ∶2 ∶1 为控制条件, 投加石灰和大孔拟薄水铝石进行后续试验研究。
2.2.3 反应时间对除氯效果的影响
向模拟废水中投加石灰和大孔拟薄水铝石, 在初始Cl-浓度为200 mmol/L, 搅拌速率为400 r/min, 反应温度为35 ℃的条件下, 考察反应时间对Cl-去除效果的影响, 结果见图5。
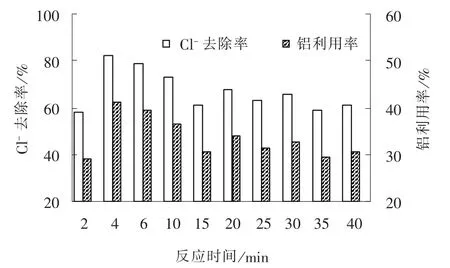
图5 反应时间对Cl- 去除效果的影响Fig. 5 Effect of reaction time on Cl-removal
Cl-去除率短时间内急剧升高, 反应4 min 时去除率达到最高, 随后逐渐下降, 15 min 以后稳定在61.0%~67.9%。 这是因为短时间内不仅有弗氏盐的出现, 还有未与Ca(OH)2结合的大孔拟薄水铝石[18], 大孔拟薄水铝石巨大的比表面积具有极强的吸附能力, 部分Cl-附着于其表面, 过滤时残留在固体中, 使得滤液中Cl-浓度显著下降。 由于弗氏盐存在沉淀-溶解平衡, 在搅拌作用下, 这种平衡不断被打破重建, 因此反应达到平衡后, Cl-去除率稳定在62.9%左右。
2.2.4 搅拌速率对除氯效果的影响
根据2.2.3 节的试验结果, 反应时间设定为30 min, 设置搅拌速率为30 ~600 r/min, 其他试验条件与2.2.3 节相同, 考察搅拌速率对Cl-去除效果的影响, 结果见图6。
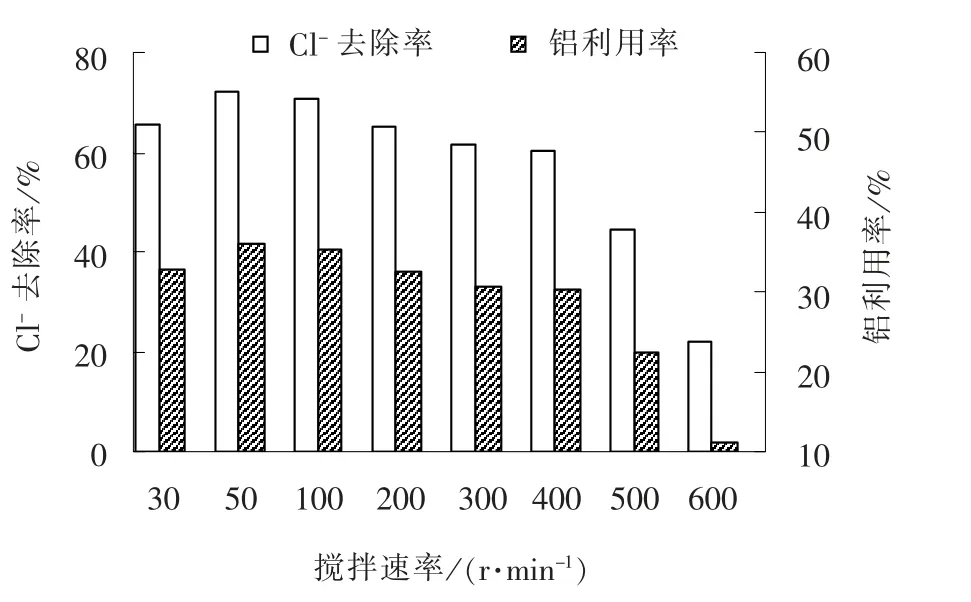
图6 搅拌速率对Cl- 去除效果的影响Fig. 6 Effect of stirring speed on Cl-removal
Cl-去除率随着搅拌速率的增大呈先升高后降低的趋势, 当搅拌速率大于500 r/min 时, Cl-去除率急剧下降。 说明大孔拟薄水铝石与CaO、 Cl-生成弗氏盐的过程需要在中低速搅拌条件下进行, 高速搅拌不利于[Ca2Al(OH)6]+与Cl-结合[7], 导致除氯效果变差。
2.2.5 初始Cl-浓度对除氯效果的影响
在n(钙) ∶n(铝) ∶n(氯) =7 ∶2 ∶1, 搅拌速率为400 r/min, 反应温度为35 ℃, 反应时间为30 min 的条件下, 考察初始Cl-浓度对其去除效果的影响, 结果如图7 所示。
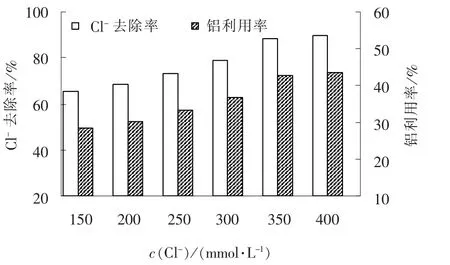
图7 初始Cl- 浓度对其去除效果的影响Fig. 7 Effect of initial Cl-concentration on Cl-removal
初始Cl-浓度为150 ~400 mmol/L 时, Cl-去除率与其呈正相关, 当初始Cl-浓度超过350 mmol/L 后, Cl-去除率上升趋势变缓, 这是因为初始Cl-浓度偏高, 相应的加药量也较大, 导致溶液中离子活度系数降低, 反应受限。 此外, 铝利用率也随初始Cl-浓度升高而增加, 表明大孔拟薄水铝石法适用于处理高浓度废水。
2.2.6 反应温度对除氯效果的影响
在初始Cl-浓度为200 mmol/L, n(钙)∶n(铝)∶n(氯)=7 ∶2 ∶1, 搅拌速率为400 r/min, 反应时间为30 min 的条件下, 考察反应温度对Cl-去除效果的影响, 结果见图8。
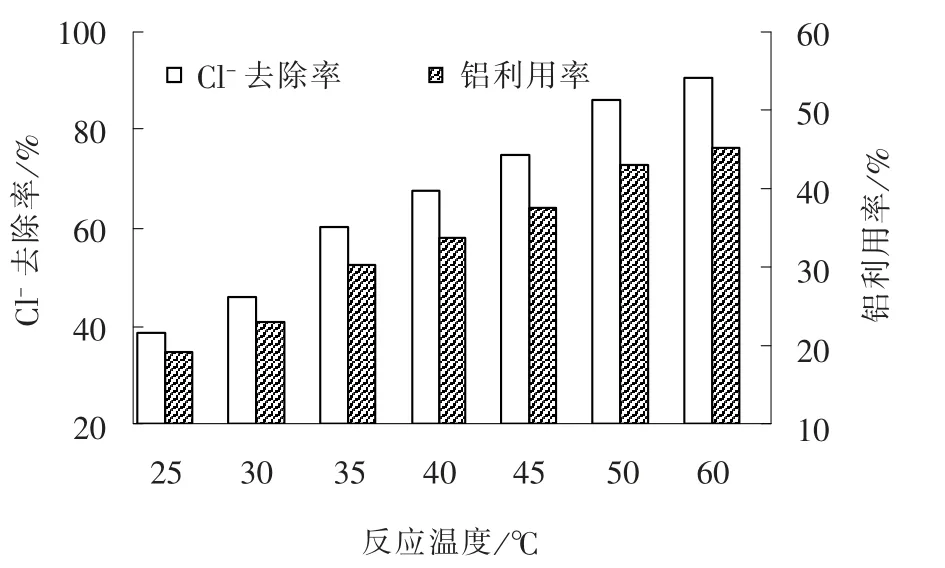
图8 反应温度对Cl- 去除效果的影响Fig. 8 Effect of reaction temperature on Cl-removal
随着反应温度的升高, Cl-去除率和铝利用率均呈线性增大, 说明高温条件促进了Cl-、 大孔拟薄水铝石和CaO 之间界面反应[19]。 此外, 升高温度会使沉淀物发生相变, 向能容纳更多Cl-的结构过渡。 温度从25 ℃升高至60 ℃, Cl-去除率升高了52.1%。 因此, 该反应为吸热反应, 可通过适当升温来提高除氯效果。
2.3 反应沉淀物固相表征
在初始Cl-浓度为200 mmol/L, n(钙)∶n(铝)∶n(氯)=7 ∶2 ∶1, 反应温度为60 ℃, 反应时间为30 min, 搅拌速率为50 r/min 的条件下, Cl-去除率达到95.3%。 对反应形成的沉淀物进行XRD 与SEM分析, 结果如图9 所示。
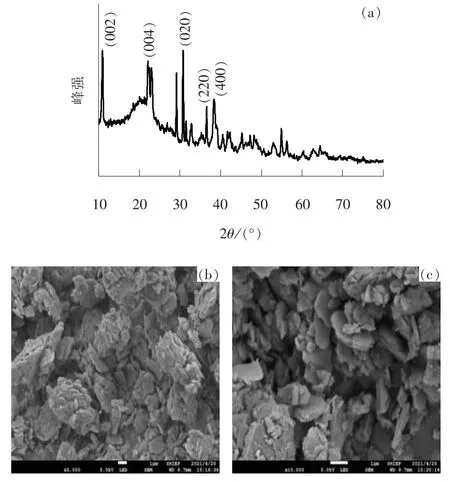
图9 除氯沉淀物XRD 与SEM 图片Fig. 9 XRD patterns and SEM images of precipitate
XRD 图谱显示所得沉淀产物峰强较低, 表明其晶粒尺寸较小。 经Jade 6 软件物相分析可知所得产物为(Ca2Al(OH)6)Cl·2H2O, 与弗氏盐成分一致[20],其典型特征峰d 值包括8.036 7、 3.961 6、 2.902 9、2.457 2、 2.338 3 nm, 对 应 的2θ 包 括11.000°、22.424°、 30.775°、 36.537°、 38.467°, 分别归属于(002)、 (004)、 (020)、 (220)、 (400)晶面。
由图9(b)可知, 反应沉淀物经扫描电镜放大5 000 倍后, 观察到颗粒以片状构成基本单元, 并团聚在一起成为大聚体分散在表面。 由图9(c)可知, 放大10 000 倍后, 片层状结构的基本结构单元更加清晰, 接近弗氏盐的六边形块状结构[21]。
3 结论
(1) CaO 与大孔拟薄水铝石能在短时间内捕获Cl-, 反应15 min 后达到稳定, 能有效去除Cl-。 增加药剂投加量能提高除氯效果, n(铝)/n(氯)对Cl-去除效果的影响程度大于n(钙)/n(铝); 当药剂的物质的量比一定时, Cl-去除率随初始Cl-浓度的升高而增大。
(2) 升高温度能显著提升Cl-去除率和铝利用率, 搅拌速率过高不利于除氯反应的进行。 当初始Cl-浓度为200 mmol/L, n(钙)∶n(铝)∶n(氯)=7 ∶2 ∶1, 搅拌速率为50 r/min, 反应温度为60 ℃, 反应时间为30 min 时, Cl-的去除率可达95.3%。
(3) 反应沉淀物固相表征结果表明, 大孔拟薄水铝石与CaO、 Cl-反应所得沉淀物的主要成分为(Ca2Al(OH)6)Cl·2H2O, 其形貌特性为以片层状的六边形基本结构单元组成团聚状颗粒分布。
