Fe3+-TiO2/AC三维电极处理氨氮模拟废水研究
2022-11-17健朱菊芬闫龙王玉飞范晓勇武建军
李 健朱菊芬闫 龙王玉飞范晓勇武建军
(1.榆林学院化学与化工学院,陕西 榆林 719000; 2.中国矿业大学化工学院,江苏 徐州 221116)
氨氮是水体主要污染物之一,主要来源于化工、冶金、石油加工等工业废水排放和生活污水中含氮有机物分解以及农田排水等[1]。 氨氮废水过量排放水体中易引起水体富营养化导致河流水华和海洋赤潮,造成水体发黑发臭,对生态环境影响很大[2,3]。 目前处理氨氮废水的方法主要有物化法和生物法,如化学沉淀法、吹脱法、离子交换法、生物硝化反硝化法和电化学法等[4]。 化学沉淀法、吹脱法、离子交换法等脱氮效率高,但是运行成本高、易造成二次污染。 生物硝化反硝化法虽脱氮率高、二次污染小,但对温度、氧含量和碳含量要求严格且基建成本高。 电化学法设备简单,易操作,污染小,反应条件温和[5,6]。
电化学法是一种新兴的高效绿色处理技术,与传统的二维电极系统相比,三维电极反应器在二维电解槽中填充了一种新的粒子,构成第三极,增大了反应的比表面积,提高电解效率,因而受到了广泛关注[7-11]。 袁梦等[12]采用微波法制备粉末活性炭负载四氧化三铁复合材料作为粒子电极,Ti/RuO2-IrO2电极为阳极,不锈钢板为阴极构成三维电极系统处理氨氮模拟废水,当电压为20 V,复合材料投加量为0.3 g,电解60 min 后,最佳氨氮去除率为78.25%。 丁红等[13]利用废铁屑构建废铁屑-Ti(RuO2)三维电极系统,处理实际高氮磷、低C/N 比污水。 发现30%体积的铁屑可将COD、NH3-N 去除率分别提高19.9%、31.8%,反应时间为80 min,电解电压为10 V 时NH3-N 去除率达96.8%。 TiO2是一种半导体材料,具有特殊的能带结构和晶格结构,常被用作光电催化剂[14-16]。 由于TiO2在实际应用中易团聚、难分离及重复性差常将其负载于活性炭,同时增加导电性[17,18]。
本研究用Fe 离子掺杂改性TiO2提高其电催化性能,制备Fe3+-TiO2/AC 粒子,以石墨板为阴阳极,Fe3+-TiO2/AC 为粒子电极,构建三维电极系统处理氨氮废水,考察电解电压、电解质NaCl 浓度、初始pH 值及粒子电极投入量对氨氮去除的影响,最后用响应曲面法对处理废水条件进行优化。
1 材料与方法
1.1 试验材料
实验用NaCl、H2SO4、NaOH、(NH4)2SO4、活性炭(粉)、钛酸丁酯、Fe(NO3)3均为分析纯,LH-N2试剂、LH-N3 试剂购买于兰州连华环保科技有限公司。
采用的氨氮模拟废水由硫酸铵和去离子水配制而成,浓度为50 mg·L-1硫酸铵溶液;用NaOH 或H2SO4调节溶液的pH 值。
JJ-1 精密增力电动搅拌器,QF17302 直流电源PHS-3C 雷磁精密酸度计、5B-3(B)COD 多元速测仪、FA2204B 电子天平。
1.2 粒子的制备
Fe3+-TiO2/AC 粒子采用泥浆法制备[18]。 称取2.6 g Fe(NO3)3,用7.2 mL 的蒸馏水溶解,得到试剂A;称取10 g 活性炭与36 mL 的钛酸丁酯混合于烧杯,在磁力搅拌器上搅拌约30 min,使其充分溶解,得到试剂B。 将置于分液漏斗中试剂A 缓慢滴入试剂B 中,用玻璃棒匀速搅拌,得到固体颗粒用机械搅拌器定速搅拌至均匀状物质,然后放入烘箱中烘干,待冷却至室温对其研磨,在马弗炉中500 ℃高温煅烧2 h,冷却后得到Fe3+-TiO2/AC 粒子。
1.3 实验装置
图1 是本实验三维电极系统反应装置,装置由直流电源、石墨电极板、粒子电极、电解槽及电动搅拌器组成。 采用NaCl 做电解质,反应主体(电解槽)为500 mL 圆柱体,在反应器内壁设置阳极和阴极,阳极和阴极为60 mm×110 mm×2 mm 规格相同的石墨板,自制Fe3+-TiO2/AC 粒子作为粒子电极填充于阳极和阴极之间,处理300 mL 的氨氮模拟废水。 试验电源为直流稳压电源:电压0~30 V,电流0~2 A。

图1 实验装置图Fig.1 Schematic diagram of the experimental device
1.4 分析方法
通过扫描电子显微镜(德国蔡司σ300)和X 射线粉末衍射仪(Bruker D8 Advance)对粒子电极的形貌和晶体结构进行分析,溶液pH 值使用pHS-3C酸度计测定,采用Design-Expert 软件进行响应面设计和优化。
根据国标《水质氨氮的测定纳氏试剂分光光度法》(HJ 535-2009),使用COD 多元速测仪对氨氮浓度进行测定:取一定样品震荡均匀,然后在每支试管中依次加入N3 和N2 试剂各1 mL,再次振荡均匀,静置10 min,将静置后的样品倒入比色皿中,放入多元速测仪中,读出每个样品的氨氮值。
氨氮去除率R的计算公式为:

式(1)中:C0为氨氮初始浓度,mg·L-1;Ct为电解tmin 时的氨氮浓度,mg·L-1。
2 结果与讨论
2.1 Fe3+-TiO2/AC 粒子的表征
2.1.1 Fe3+-TiO2/AC 的XRD 分析
图2 为制备的Fe3+-TiO2/AC 粒子的XRD 谱图。从图2 中可看出,粒子在2θ为25.40°、37.84°、48.16°、54.38°、62.70°、69.36°和75.84°分别对应锐钛矿晶面(101)、(004)、(200)、(105)、(204)、(220)和(215),与TiO2标准卡片(JCPDS 021-1272)对应一致的特征峰[19],2θ为27.98°、35.52°分别对应金红石晶面(110)、(101),与TiO2标准卡片(JCPDS 021-1276)对应一致的特征峰[20],2θ为33.22°、40.90° 分别对应晶面(104)、(113),与Fe2O3标准卡片(JCPDS 001-1053)对应一致的特征峰[21],说明了活性炭成功负载了纳米TiO2且主要以锐钛矿晶型为主,还有部分Fe2O3晶体,Fe3+未完全渗入TiO2中,未出现明显的无定形碳的特征峰,这可能是由于无定形碳峰强度较弱,被TiO2特征峰掩盖。
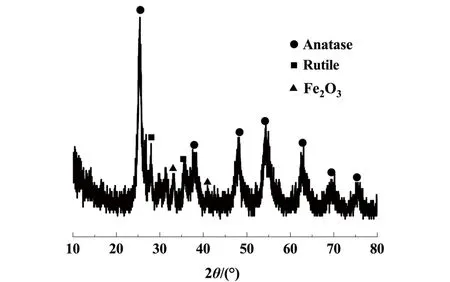
图2 Fe3+-TiO2/AC 的XRD 谱图Fig.2 XRD pattern of Fe3+-TiO2/AC
2.1.2 Fe3+-TiO2/AC 的SEM 分析
图3 是不同倍数下Fe3+-TiO2/AC 粒子的扫描电子显微镜图片。

图3 Fe3+-TiO2/AC 的SEM 图Fig.3 SEM image of Fe3+-TiO2/AC
从图3(a)可以看出,粒子表面不规则,分布着裂缝和孔隙,从图3(b)中看出粒子具有丰富的孔道,表面生长出近似白色粗糙颗粒,结合XRD 结果可说明TiO2较均匀负载在活性炭表面上。 此外,TiO2颗粒并没有完全堵塞活性炭的孔道,可能是生成的TiO2晶粒尺寸大于活性炭表面的微孔孔隙,Fe3+-TiO2/AC 粒子还具有一定的吸附性能。
2.2 三维电极系统对氨氮去除的影响因素
2.2.1 电解电压对废水氨氮去除的影响
设定实验条件:粒子电极投入量为3.4 g·L-1,电解质NaCl 浓度为5.0 g·L-1,初始pH 值为9.00,研究电解电压对氨氮去除的影响,结果如图4 所示。

图4 电解电压对氨氮废水去除的影响Fig.4 Effect of different electrolytic voltage on ammonia nitrogen removal
如图4 所示,随着电解电压的增加,氨氮的去除率不断增加,电压为18 和24 V 时,电解60 min 氨氮去除率相差较小。 其原因可能是增大电压,粒子电极可以极化形成无数个微电极,增强氧化作用,电催化氧化过程产生的Cl2或ClO-浓度增大,阳极·OH 的产生速率及阴极的还原速率提高,从而增大了氨氮的去除率[22,23]。 当外加电压过小时,施加在粒子电极上的电压就会不足,粒子电极无法到达阴阳极,相互之间可能存在接触,从而产生短路电流,电催化氧化效率较低;反之,当外加电压过大,旁路电流会增大而引发副反应,影响电催化氧化效率。综合考虑三维电极处理废水的效果和运行能耗等因素,后续实验电解电压选择18 V。
2.2.2 电解质NaCl 浓度对废水氨氮去除的影响
设定实验条件:粒子电极投入量3.4 g·L-1,电解电压为18 V,初始pH 值为9.00,探究电解质NaCl 浓度对氨氮去除的影响,结果如图5 所示。
如图5 所示,随着电解质NaCl 浓度增加,氨氮去除率也不断增大。 当电解质NaCl 浓度为6.7 g·L-1时,电解40 min 氨氮去除率为89.43%。 由于NaCl溶解水中引入Cl-,Cl-在三维电极的阳极被氧化生成Cl2,在水中转化为HClO 将NH4+氧化为N2,从而实现氨氮的去除。 主要反应方程如下[24,25]:

图5 电解质NaCl 浓度对氨氮去除的影响Fig.5 Effect of electrolyte concentration(NaCl)on ammonia nitrogen removal
阳极:

溶液:

另外NaCl 的投入改变了溶液电导率的大小,从而影响槽电压的分配,使得粒子电极上的电压也发生了改变。
2.2.3 初始pH 值对废水氨氮去除的影响
设定实验条件:粒子电极投入量为3.4 g·L-1,电解电压为18 V,NaCl 的投入量为6.7 g·L-1,探究初始pH 值对氨氮去除的影响,结果如图6 所示。

图6 不同初始pH 值对氨氮去除的影响Fig.6 Effect of different initial pH on ammonia nitrogen removal
如图6 所示,随着电解时间的增加,氨氮的去除率增加,在电解40 min 时,初始pH 值对氨氮去除影响大小为:pH=9>pH=11>pH=3>pH=5>pH=7。在偏碱性的溶液中,芬顿反应受抑制,Cl2在溶液中溶解度增大,活性氯增多,氨氮降解增大,初始pH值过大HClO 与ClO-发生反应(如式7),活性氯减少,降解氨氮效果减弱[17],但有可能部分NH+4与OH-反应生成NH3逸出,氨氮去除率较大;在初始pH 值小于7 的溶液中,电解产生的氯气较容易逸出[26],氨氮主要由电芬顿产生的·OH 氧化去除,而初始pH = 3 更有利于芬顿反应发生[27],比初始pH=5 氨氮降解效果较好。 在中性条件下,电极直接氧化作用与氯系氧化剂的间接氧化作用共同完成[28],但对氨氮的降解效果较差。

2.2.4 粒子电极投入量对废水氨氮去除的影响
设定实验条件:电解电压为18 V,电解质NaCl浓度6.7 g·L-1,溶液初始pH 值为9.00,探究粒子电极投入量对氨氮的去除的影响,结果如图7 所示。

图7 粒子电极投入量对氨氮去除的影响Fig.7 Effect of particle electrode dosage on ammonia nitrogen removal
从图7 可以看出,随着粒子电极投入量的增加,氨氮去除率先增大后减小,当粒子电极投入量为10.0 g·L-1时氨氮的去除效果最好,在40 min 左右氨氮去除率为96.86%。 其原因可能是在一定电压下,随着粒子电极投入量的增加,形成更多带电荷的微电极,电解氧化比表面积增加,电解氧化效率提高,从而提高降解率[29]。 如果粒子电极投入量过高,则会影响污染物在粒子电极表面的扩散,减慢传质速率,从而降低电解效率,粒子电极相互堆积,也可能发生短路,氨氮去除率下降[30]。
2.3 响应曲面法优化氨氮废水条件
2.3.1 响应曲面法设计
由于不同三维电极系统选取的电解质种类不同,电解质NaCl 浓度这一因素不具有普遍性,故选取废水初始pH 值、电解电压、粒子电极投入量为影响因子,以电解40 min 后氨氮去除率为响应值,采用Design-Expert 软件中Box-Behnken 程序设计废水氨氮处理响应曲面优化试验,其中废水初始浓度为50 mg·L-1,体积为300 mL,电解质NaCl 浓度6.7 g·L-1。 实验因素及自变量水平如表1 所示。

表1 实验因素及水平编码Table 1 Coding of test factors and levels
2.3.2 响应曲面模型
利用表1 所设计的三因素三水平进行响应曲面法实验,实验设计方案及分析结果见表2。 从表2中可以看出,实验的真实值与预测值的相对误差小于5%,此外,如图8 所示将实验真实数据与预测数据进行对比,试验各点紧密分布于斜线两侧,说明该模型可靠,适用于三维电极处理氨氮废水过程中优化条件的预测。

图8 氨氮去除率真实值与预测值的对应关系Fig.8 Comparison of model actual and predicted values of ammonia nitrogen removal
对表2 实验结果进行拟合和响应曲面模型的方差分析得出P值<0.0001(<0.05),失拟项的P值=0.2437(>0.1),表明模型影响显著,模型失拟不显著,模型与实际情况拟合程度良好,实验误差小,模型可用于实验的模拟。

表2 响应曲面法设计与实验结果Table 2 Design and test results of response surface
2.3.3 响应曲面分析
为了进一步研究初始pH 值、电解电压、粒子电极投入量间的交互作用和确定最适宜的氨氮去除条件,应用Design-Expert 软件得到相应的三维响应曲面图及其等高线图,如图9 所示。
由图9 可知,电解电压与初始pH 值和电解电压与粒子电极投入量之间的交互作用较为显著。电解电压与初始pH 值和电解电压与粒子电极投入量之间的交互作用主要为协同作用,如图9(a)所示,电压对氨氮去除影响的较明显,电压增大,氨氮去除率也增大,当电解电压为18 V,氨氮去除效果最好。 而初始pH 值对氨氮去除率的影响是先增加后降低,初始pH 值为9.8 时氨氮去除效果最好。如图9(c)所示,电压对氨氮去除影响明显,变化趋势与图9(a)相似。 增加粒子电极投入量,氨氮去除率先增加后降低,粒子电极投入量为3 g 左右氨氮去除率最大。

图9 各因素间交互作用对氨氮去除的影响Fig.9 Influence of interaction between factors on ammonia nitrogen removal
2.3.4 验证实验
利用Design Expert 软件对模型优化拟合,预测得到处理氨氮废水的最适宜实验条件是:电解电压为18 V,初始pH 值为9.10,粒子电极投入量为9.9 g·L-1。 在此实验条件下拟合的氨氮去除率为97.61%。 为验证软件拟合最适宜实验条件及实验结果是否可靠,进行实验验证,如表3 所示。 3 组平行实验的真实值与预测值的相对误差均小于5%,该模型对三维电极处理氨氮废水有较好的预测效果。

表3 最适宜实验条件下氨氮去除率的真实值与预测值比较Table 3 Comparison of actual and predicted values of ammonia nitrogen removal under optimal experimental conditions
与袁梦等[12]相比,处理氨氮模拟废水氨氮去除率增加了19.83%,电解时间缩短了20 min,推断其原因可能是:(1)粒子电极的作用:在电压作用下,粒子电极可以极化形成无数个微电极,负载TiO2的活性炭先将废水中的NH3-N 吸附聚集在表面,由TiO2作用产生了大量的·OH[式(8)~式(10)]将NH3-N 氧化降解,提高了NH3-N 氧化降解率和降解速率;另外Fe3+引入发生了类芬顿反应[式(11)~式(13)];(2)氯化钠作电解质作用:氯离子的存在提高了电解体系的氧化能力,提高了氨氮氧化分解[式(2)~式(6)]。
TiO2作用产生·OH 的反应方程式[31]:

Fe3+引入发生电类芬顿反应方程式[32]:

3 结论
1)制备了Fe3+-TiO2/AC 粒子电极,通过XRD和SEM 分析得出,活性炭表面生长出近似球形的白色粗糙颗粒,成功负载了纳米TiO2,主要以锐钛矿晶型为主。
2)电压的增加有利于废水氨氮的降解;溶液的初始pH 值对芬顿反应和氯系氧化反应影响较大;粒子电极投入量增加氨氮去除率也增加,投入过多氨氮去除率下降。
3)设计的响应曲面模型可用于模拟预测实验结果,得到处理氨氮废水的最适宜实验条件为:电解电压为18.00 V、初始pH 值为9.10,粒子电极投入量为9.9 g·L-1。 在此实验条件下,氨氮去除率可达到97.61%。
