二元溶剂萃取分离重油中芳烃的机理
2022-11-16崔华松彭东岳管翠诗
崔华松, 倪 清, 彭东岳, 管翠诗
(中国石化 石油化工科学研究院,北京 100083)
液-液萃取是分离石油体系中不同烃组分的常用方法,在石油炼制领域主要用于芳烃抽提和溶剂精制。液-液萃取遵循“相似相溶”原则,利用溶质在溶剂中溶解度的差异实现组分的分离。在重质油品中,芳烃组分具有多种结构,根据环数可分为一环、二环、三环、四环、五环芳烃以及更多环数的芳烃,通常将三环及以上芳烃称为稠环芳烃。从极性上看,饱和烃极性较小,芳烃由于离域π电子的存在,极性强于饱和烃,且随着环数增加极性增强,所以利用极性溶剂可以将饱和烃与芳烃萃取分离。常用的芳烃萃取溶剂包括糠醛、N-甲基吡咯烷酮(NMP)、环丁砜、二甲基亚砜(DMSO)、N,N-二甲基甲酰胺(DMF)等。对于减压馏分油,国内应用最广的萃取溶剂为糠醛,但是由于不同原料中烃类组成的不同,特别是当原料油中芳烃含量很高时,单一溶剂无法满足萃取分离要求[1]。为提高糠醛溶剂对芳烃的萃取选择性,可以在溶剂中引入一定量的第二元溶剂[2-3]。Luo等[4]对含有少量含氧副溶剂的糠醛作为重芳烃抽提溶剂的萃取机理进行了探究,通过量子化学计算发现,糠醛与副溶剂可形成氢键,使得极性较小的饱和烃更难进入到溶剂体系中,从而提高了对芳烃尤其是稠环芳烃的萃取选择性。另外,Hoseini等[5-6]发现,对于润滑油溶剂精制过程,向糠醛溶剂中加入少量饱和烃可以减少沉降时间,提高精制油的纯度,增大芳烃的选择性。
作为“相似相溶”原则的一种量化,溶解度参数理论不仅可以量化不同物质的相似性并对萃取过程进行解释[7-8],还可依据溶解度参数值对溶剂进行复配,获取萃取效果更加理想的复合溶剂[9]。溶解度参数δ[10]定义为物质的内聚能密度的平方根,相似溶解度参数的物质之间可以互相溶解。对于有机液体体系,其内聚能不仅依赖于结构单元之间的色散力,而且还取决于极性基团之间的极化作用和氢键作用,Hansen[11]将溶解度参数δ分为了3个分量,即色散溶解度参数δd、极性溶解度参数δp和氢键溶解度参数δhb。目前,Hansen提出的三维溶解度参数理论已广泛应用于农药配方的开发[12]、多环芳烃浸取溶剂的筛选[13]、固相萃取中各物质间相互作用的研究[14]及生物活性化合物的提取优化[15]等领域。常用有机溶剂的三维溶解度参数可由文献查取获得,大分子及高分子化合物的溶解度参数可由实验测定[16]、反气相色谱法[17]、Hansen三维溶解度软件法[18]、基团贡献法[19]或分子模拟获取[20]。
针对糠醛溶剂对于不同环数芳烃分离效率较低、难以有效脱除稠环芳烃组分、精制油收率较低等问题,笔者以芳烃含量较高的减压馏分油为原料,用溶解度参数理论优选引入适宜的第二元溶剂,对溶剂溶解度参数进行调控,使溶剂、溶质相平衡体系发生改变,从而改变萃取分离效果。同时,为解释不同环数芳烃萃取选择性产生变化原因,利用基团贡献法计算获取了6种模型分子的Hansen三维溶解度参数值,对比分子溶解度参数变化与萃取平衡分配系数、选择性的关系,从溶解度参数理论角度解释液-液萃取体系产生相平衡差异的原因,并由核磁共振氢谱(1H-NMR)中H质子化学位移证实了二元溶剂萃取效果产生变化的实质,为重油体系烃组分的萃取分离提供参考。
1 实验部分
1.1 原料和试剂
实验原料油为溶剂精制后的减压馏分油,取自中国石化某炼油厂,其主要性质列于表1。糠醛和极性调节剂(Polarity regulator, PR1),均为分析纯,国药集团化学试剂有限公司产品。

表1 减压馏分油主要性质Table 1 Main properties of vacuum distillates
1.2 实验仪器及步骤
萃取平衡装置如图1所示。萃取平衡装置主要包括超级恒温水及萃取平衡釜,溶剂回收装置主要包括三口烧瓶、加热套、氮气保护装置等。实验过程中,将原料油和溶剂分别加入到萃取平衡釜中,开启搅拌和恒温,待温度达到设定温度后,保持恒温并充分搅拌30 min;关闭搅拌,恒温静置沉降1 h;将分层后的精制液与抽出液分离置于三口烧瓶中,在氮气保护下回收溶剂。

图1 萃取平衡装置示意图Fig.1 Schematic diagram of extraction setup
1.3 分析仪器及方法
油品中烃类组成分析依据行业标准方法SH/T 0659—1998,仪器为GC6890/5976MS,实验条件为:进样量1.0 μL,分流比30∶1,石英毛细管色谱柱40 m×0.25 mm×0.25 μm,GC进样口温度350 ℃,GC/MS接口温度340 ℃,柱箱温度60 ℃,保持2 min,再以40 ℃/min升温速率升至350 ℃,停留5 min,MS离子源温度250 ℃,扫描范围50~700 amu。
溶剂的1H-NMR表征采用美国Agilent 700 MHz核磁共振波谱仪(5 mm双共振探头)。由于强极性溶剂,如DMSO-d6中的氧原子与待测分子的活泼氢原子之间能形成氢键相互作用,会影响对待测溶剂本身分子间氢键相互作用的探测,所以笔者选用极性较弱的CDCl3为溶剂,配制成质量分数为0.1%的溶液,混合均匀后待测。溶剂1H-NMR表征的实验参数为:测试温度20~25 ℃,扫描次数200,脉冲宽度4.30 μs,谱宽11160 Hz,观测核的共振频率699.889 MHz,采样时间0.7 s,延迟时间5 s,氘代氯仿锁场,TMS定标。
1.4 萃取平衡分析
液-液萃取中,物质的分离效率和能达到的分离极限取决于2种物质在萃取平衡后的分配系数和选择性[21],分配系数(D)表示萃取达到平衡后,被萃取物质在两相中的分配比例,即被萃取物在萃取相(抽出相)中质量分数与萃余相(精制相)中质量分数之比,它的大小代表溶剂溶解能力的强弱;选择性(β)则为2种物质分配系数的比值,β的大小表示萃取体系中溶剂对2种溶质的溶解差异性,β越大,2种组分的分离程度越大。D与β的计算如式(1)、式(2)所示;精制油质量收率(R,%)计算如式(3)所示。
(1)
(2)
(3)
式(1)~式(3)中:xi和yi分别为组分i在萃余相与萃取相中的质量分数,%;Di为组分i的分配系数;笔者以A代表油品中的各类芳烃,B代表油品中的饱和烃,β即为各芳烃相对于饱和烃的萃取选择性;mR为精制油质量,g;mF为原料油质量,g。
2 结果与讨论
2.1 不同溶剂萃取效果对比
以纯糠醛溶剂为一元溶剂,在一元溶剂中引入的第二元溶剂为溶解度参数较大的含羟基极性调节剂PR1,PR1在二元溶剂中的质量分数为2.5%,一元、二元溶剂萃取剂/原料油质量比(简称剂/油比)均为2∶1。在40 ℃下,随着PR1的引入,溶剂萃取的精制油收率由32.9%变为51.5%,二元溶剂萃取精制油的收率比一元溶剂精制油收率提高了近20百分点。根据烃组成分析数据,可得到饱和烃(Saturates,简称S)、单环芳烃(Mono-aromatics,简称MA)、双环芳烃(Di-aromatics,简称DA)、三环芳烃(3-Ring aromatics,简称3RA)、四环芳烃(4-Ring aromatics,简称4RA)、五环芳烃(5-Ring aromatics,简称5RA)在油品中的质量分数,结合萃取平衡相中的溶剂的质量收率,可计算得到各烃类组成的质量分数,从而获取各烃类的分配系数和萃取选择性。图2为2种溶剂萃取各烃类组分的分配系数的对比,图3为2种溶剂萃取芳烃选择性的对比。
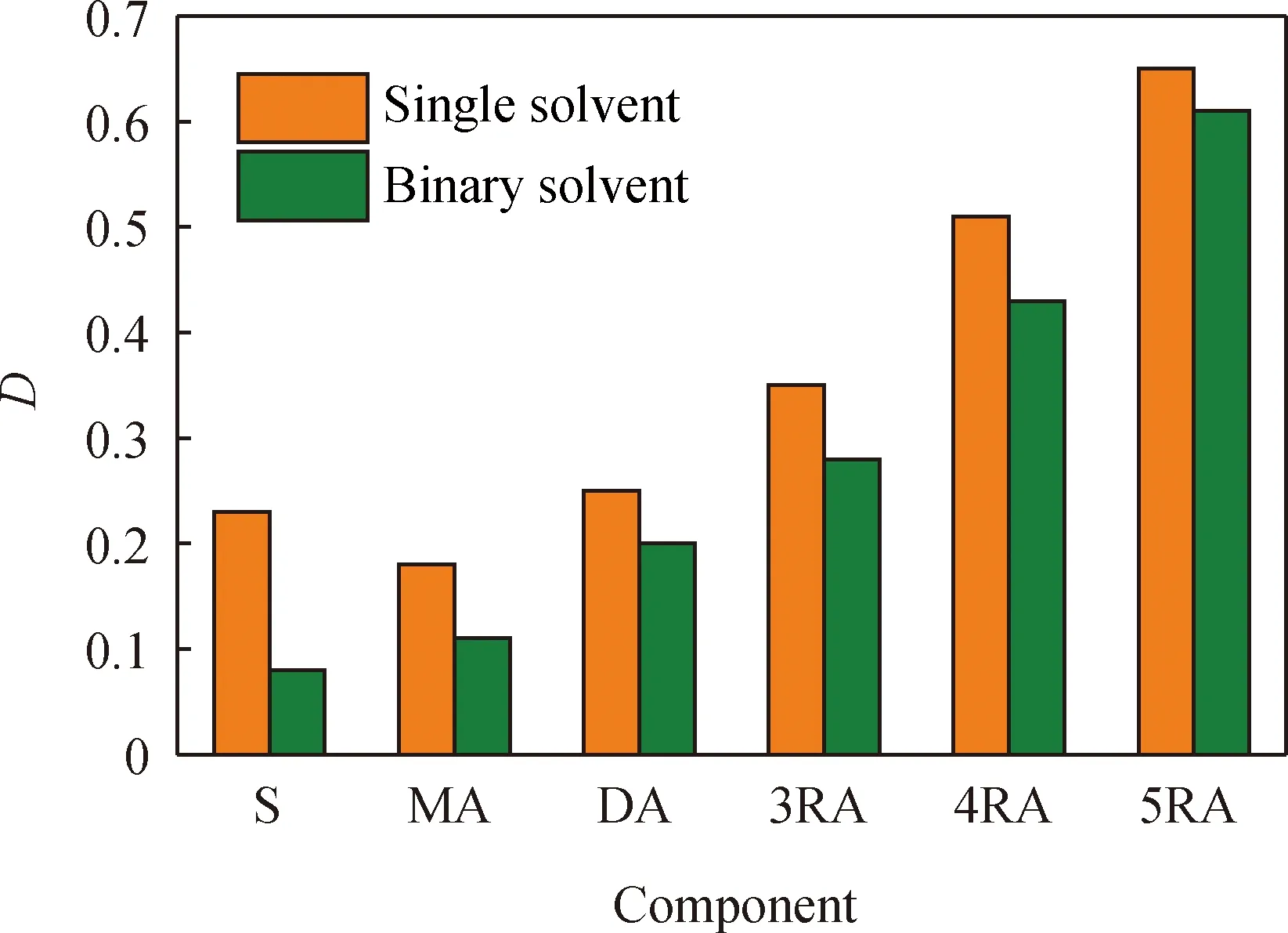
S—Saturates; MA—Mono-aromatics; DA—Di-aromatics;3RA—3-Ring aromatics; 4RA—4-Ring aromatics;5RA—5-Ring aromatics图2 2种溶剂萃取各烃类组分的分配系数(D)对比Fig.2 Comparison of distribution coefficient (D) ofhydrocarbons by bi-solvent extraction

MA—Mono-aromatics; DA—Di-aromatics;3RA—3-Ring aromatics; 4RA—4-Ring aromatics;5RA—5-Ring aromatics图3 2种溶剂萃取芳烃组分的选择性(β )对比Fig.3 Comparison of aromatics selectivity (β )with using bi-solvent extractionConditions: T=40 ℃; m(Solvent)/m(Oil)=2
由图2可以看出,无论是对于一元还是二元溶剂萃取平衡体系,芳烃的分配系数均随环数的增加而显著增加,说明芳烃在极性溶剂中的溶解度随芳烃环数的增加而单调增大。二元溶剂对各环芳烃的分配系数略低于一元溶剂,2种溶剂分配系数的差异随芳烃环数的增多而减小,二元溶剂萃取饱和烃的分配系数明显小于一元溶剂;相对于一元溶剂,二元溶剂对原料油中各组分的溶解能力减小,对饱和烃的溶解能力的降低最为显著。由图3可以看出,二元溶剂对各芳烃的萃取选择性明显高于一元溶剂,其中,三环、四环、五环芳烃的萃取选择性对比一元溶剂萃取分别增大了115%、133%和156%。
2.2 芳烃萃取选择性与各组分溶解度参数的关联
物质的溶解度参数大小代表了其分子间相互作用的强弱,分子间的相互作用决定了物质的互溶性[22-24]。减压馏分油组成复杂,为研究其烃类组成的溶解度参数与溶剂萃取规律的关系,根据原料组成,选取了饱和烃(S)、单环芳烃(MA)、双环芳烃(DA)、三环芳烃(3RA)、四环芳烃(4RA)、五环芳烃(5RA)6类结构的模型分子[25],如图4所示。

图4 各组分模型分子结构Fig.4 Molecular structures of different model compounds(a) Saturates; (b) Mono-aromatics; (c) Di-aromatics;(d) 3-Ring aromatics; (e) 4-Ring aromatics; (f) 5-Ring aromatics
为计算各模型分子的溶解度参数,采用Stefanis提出的一种新的用于计算Hansen溶解度参数的基团贡献法[26]。不同于利用基团对作用能(E)和分子体积(V)的贡献计算溶解度参数[27],该方法涉及了多种一级基团和基于共轭理论的二级基团,能够直接计算出复杂多环、杂环和具有芳族结构有机化合物的Hansen溶解度参数。式(4)为溶解度参数分量δi的计算式。
δi=(∑iNiCi+W∑jMjDj+A)
(4)
式(4)中,Ci是i型一阶基团对溶解度参数的贡献;Ni为化合物中i型一阶基团数量;当化合物中存在二级基团时,W为1;化合物中不存在二级基团时,W为0;Dj为j型二阶基团对溶解度参数的贡献,Mj为化合物中j型二阶基团的数量,A是分量计算中代入的数值,计算δd、δp、δhb的A分别为17.3231、7.3548、7.9793。
计算得到6种模型分子的Hansen溶解度参数值,如表2所示。

表2 模型分子的Hansen溶解度参数值Table 2 Hansen solubility parameters of different model molecules
由表2看出:模型分子的总溶解度参数与色散力溶解度参数均随芳烃环数的增多而增大,饱和烃模型分子S的δd最小,且它的δp和δhb均为0;由于烷烃长侧链的影响,单环芳烃分子MA的δp和δhb也为0,则溶解过程中S、MA与极性溶剂的极性力和氢键力作用较弱,故S、MA在极性溶剂中的溶解度很小。由于芳烃结构分子会通过π-π堆叠作用形成规整的结构,且堆叠的空间位阻随侧链的缩短而减小[20],所以芳烃模型分子的δp和δhb基本上随芳烃环数的增多而增大,说明在溶解过程中,芳烃与溶剂的极性力与氢键力作用会随着芳烃环数的增多而逐渐增强。而实验结果证明芳烃萃取平衡分配系数与选择性随芳烃环数的增多而增大,说明极性溶剂萃取体系中,芳烃溶解度参数的增大促进了芳烃在溶剂中的溶解。
2.3 PR1含量对萃取相平衡的影响
2.3.1 不同PR1含量对二元溶剂萃取的影响
如前所述,PR1的加入能使溶剂具有更高精制油收率及芳烃选择性。为了探究PR1对萃取平衡的影响,考察在40 ℃下,不同PR1含量对二元溶剂萃取平衡分配系数D、芳烃萃取选择性β、精制油收率R的影响,结果分别见图5、图6和图7。由图5可知,各组分的分配系数均随着溶剂中PR1含量的增加而降低,说明各烃类组分在溶剂中的溶解度随溶剂中PR1含量的增多而减小,其中,饱和烃组分的分配系数下降得最快,对比PR1质量分数为0和4%的溶剂萃取结果,饱和烃的分配系数由0.23降为0.04,五环芳烃的分配系数由0.65降为0.60,二者分配系数变化的差异极大。由图6可知,各烃类分配系数的变化导致芳烃的萃取选择性随第二元溶剂含量的增加而指数增大。由图7可知,各烃类分配系数的减小导致萃取精制油收率随PR1含量的增大而增大。

S—Saturates; MA—Mono-aromatics; DA—Di-aromatics;3RA—3-Ring aromatics; 4RA—4-Ring aromatics;5RA—5-Ring aromatics; PR1—Polarity regulator图5 不同PR1含量二元溶剂萃取的分配系数(D)变化Fig.5 Distribution coefficient (D) changes in binarysolvent with different PR1 contentsConditions: T=40 ℃; m(Solvent)/m(Oil)=2

MA—Mono-aromatics; DA—Di-aromatics;3RA—3-Ring aromatics; 4RA—4-Ring aromatics;5RA—5-Ring aromatics; PR1—Polarity regulator图6 不同PR1含量二元溶剂萃取的选择性(β)变化Fig.6 Selectivity(β)of binary solvent withdifferent PR1 contentsConditions: T=40 ℃; m(Solvent)/m(Oil)=2

PR1—Polarity regulator图7 不同PR1含量二元溶剂萃取精制油收率(R)变化Fig.7 Recovery yield (R) of binary solvent withdifferent PR1 contentsConditions: T=40 ℃; m(Solvent)/m(Oil)=2
2.3.2 不同PR1含量对二元溶剂溶解度参数的影响
为了探究溶剂PR1的加入促使溶剂萃取效果产生变化的原因,采用式(5)体积加和法对加入第二元溶剂后溶剂的溶解度参数进行计算,计算结果见表3。
δmix=∑φiδi
(5)
式(5)中:δmix为混合物的溶解度参数,(J/cm3)0.5;δi为物质i的Hansen溶解度参数分量,(J/cm3)0.5;φi为物质i的体积分数,%。
由表3可知,由于PR1的δ大于糠醛,其加入会增大溶剂的总溶解度参数,由PRI含量的变化可以看出,溶剂δhb的增大是总溶解度参数δ变大的主要原因。为获取溶质的溶解与溶解度参数的关系,Hansen和Skaarup[28]定义了汉森球体,即将三维溶解度参数绘制于三维坐标上,以溶质为中心绘制一个特殊的球体,位于球体内部的溶剂对溶质有较好的溶解性,球体半径称为溶质特征溶解度参数半径R0,2种物质的Hansen溶解度参数距离为Ra,当Ra (Ra)2=4(δd2-δd1)2+(δp2-δp1)2+(δhb2-δhb1)2 (6) 表3 不同PRI含量(质量分数)溶剂的Hansen溶解度参数Table 3 Hansen solubility parameters of solvents with different PR1 contents (mass fraction) 表4 溶剂与溶质的Hansen溶解度参数距离(Ra)Table 4 Ra between solvent and solute Ra/(J·cm-3)0.5 由表4可以看出,各个模型分子与溶剂的Ra随溶剂中PR1含量的增加而增大,这使得溶剂对溶质的溶解能力下降,表现为各个溶质分子的分配系数均减小。引起这种变化的实质是:PR1的加入使得溶剂分子间氢键力增大,溶质分子更加难以进入溶剂分子形成的氢键力网格中,所以溶剂对烃类溶解度减小。同时,PR1的加入使溶剂极性力溶解度参数略微增大,氢键力溶解度参数明显增大,说明溶剂具有了更强的极性。对同一芳烃而言,极性越强的溶剂与芳烃的静电作用越强[30],溶剂极性的增大,使具有极性力和氢键力等溶解度参数的芳烃与溶剂的极性力、氢键力作用变得更为显著,促进了芳烃由精制相转移至抽出相,而没有极性的饱和烃分子与溶剂没有氢键力和极性力的作用,所以饱和烃分子溶解度降低的幅度大于芳烃分子,因此各芳烃的萃取选择性增大。 2.3.31H-NMR表征对溶剂分子氢键作用的验证 为验证PR1的加入增强了溶剂分子的氢键力作用,采用核磁共振氢谱1H-NMR获取了不同PR1含量二元溶剂中各个H的化学位移变化,如图8所示。 由图8可知,糠醛的各个氢质子的化学位移随着溶剂中PR1含量的增加而略微减小,PR1中的羟基质子的化学位移随PR1含量的增加而明显增大,造成这一变化的原因应该是溶剂中氢键作用的增强。由不同PR1含量二元溶剂的1H-NMR变化趋势可知,PR1的化学位移有很强的浓度依赖性,说明PR1由分散态到聚集态过程中,溶剂分子间的氢键作用增强,导致PR1中H的电子云密度降低,屏蔽作用减弱,共振峰向低场移动。而研究表明,分子内的氢键作用不会导致溶剂质子化学位移的变化[31],所以,PR1含量的增加增强了溶剂分子间氢键的作用。而糠醛质子的化学位移变化很小,说明第二元溶剂在整个体系中更倾向于与同类分子形成氢键,从而导致整个体系氢键作用的增强。不同PR1含量二元溶剂核磁共振氢谱(1H-NMR)化学位移变化与溶剂氢键力溶解度参数明显增强的计算结果一致。综上,二元溶剂萃取示意图如图9所示。 PR1—Polarity regulator图8 不同PR1含量(质量分数)溶剂的1H-NMR谱图Fig.8 1H-NMR spectra of solvents with differentPR1 contents (mass fraction) PR1—Polarity regulator图9 二元溶剂萃取示意图Fig.9 Schematic diagram of binary solvent extraction (1)采用一元和二元溶剂对减压馏分油进行萃取分离实验,结果表明:芳烃在极性溶剂中的溶解度随芳烃环数的增多而增大。从基团贡献法计算结果可以看出:芳烃的溶解度参数也随芳烃环数的增多而增大,特别是极性溶解度参数和氢键溶解度参数的增大,有助于芳烃组分在极性溶剂中的溶解。 (2)糠醛溶剂中引入含羟基的极性调节剂PR1,增大了溶剂的极性溶解度参数和氢键溶解度参数,提高了溶剂对芳烃的萃取选择性。由溶解度参数体积加和法结合溶剂1H-NMR结果可以判断:第二元溶剂的加入实质是增强了极性有机溶剂中氢键的形成,这导致了溶剂质子化学位移的变化,表现为氢键溶解度参数的明显增大,使得溶剂对芳烃的萃取选择性显著提高。 (3)溶解度参数理论可以解释极性溶剂萃取分离重油中烃组分的机理,还可以指导二元甚至更多元溶剂的复配,随着溶解度参数计算方法愈加多样和计算结果愈加精确,萃取溶剂的筛选和萃取性能的预测会更加高效且合理。



3 结 论
