含铁氰化物和亚铁氰化物及草酸盐混合废水的处理
2022-11-09仇雅丽刘勇奇巩勤学刘更好
袁 琦,仇雅丽,赖 浪,胡 琴,刘勇奇,巩勤学,刘更好
(湖南邦普循环科技有限公司,湖南 长沙 410600)
氰化物经常以不同形式存在于如电镀、冶金、焦化、金属加工等多种工业废水中。因其对人体及自然水体生态系统的毒害性,国家在污水综合排放标准(GB8978-1996)中规定一般企业排放污水中总氰化物浓度不得超过0.5 mg/L[1]。目前处理氰化物的方法主要有化学氧化法、物理化学法、生物处理法、自然降解法、高压水解法、膜分离法、辐射法及离子交换法等[2]。在不同形态的氰化物中,与金属离子络合的氰化物如铁氰化物、亚铁氰化物等毒性相对较小,有着极强的稳定性,一般的化学氧化方法很难将其去除,生物处理法中的微生物也很难将其分解[3]。若这些含氰络合物进入复杂环境水体中,遇到稀酸或者更强的络合剂,则会发生反应释放剧毒的CN-。因此寻求经济且高效的铁氰化物、亚铁氰化物的处理方法,是目前众多学者研究的重点。
草酸在化工、医药行业中常被用作络合剂、还原剂等,其在废水中以有机物形式影响废水的COD。有机物也是废水处理中经常被关注的对象。常规处理有机物的方法有化学氧化法[4]、物理吸附法[5]、生物处理法[6]等。但一般化学氧化法和物理吸附法处理成本较高,生物法处理周期较长,尤其当废水中含有氰化物或重金属等抑制微生物的生长的成分时,生物法处理有机物的效率较低。
本文针对铁氰化物和草酸盐混合的化工废水,设计一套技术方案,为后期铁氰化物和草酸盐混合的化工废水处理产业化提供重要的参考意义。
1 实验部分
1.1 实验用水及特性
1.2 试剂与仪器
试剂:FeSO4·7H2O(AR);Ca(OH)2(AR);NaOH(AR);浓H2SO4(AR);Na2SO3(AR)。
仪器:A3AFG火焰原子吸收光谱仪,普析;5B-3C(V8))COD快速测定仪,连华科技;5B-1(V8)智能多参数消解仪,连华科技;PHS-3CpH计;JHS-1电子恒速搅拌机、SHZ-88水浴恒温振荡器;分析天平,梅特勒。
1.3 分析方法
总氰化物含量测定采用硝酸银容量法[7],COD测定用分光光度法[8],Mn2+含量测定用火焰原子吸收分光光度法[9]。
1.4 处理工艺及方法

图1 处理工艺流程图Fig.1 Process flow chart of treatment
具体实验方法:取一定体积的含铁氰化物和亚铁氰化物及草酸盐的混合废水,在室温下往其中加入适量的Ca(OH)2固体,搅拌反应1 h,絮凝沉淀过滤。取一定体积的滤液,往其中加入稀硫酸调节滤液pH,然后再往其中加入适量的FeSO4·7H2O固体,搅拌反应0.5 h,絮凝沉淀过滤。取滤液进行分析。
2 结果与讨论
2.1 重金属和COD联合处理实验
根据草酸根离子的性质,使用Ca(OH)2固体对含铁氰化物和亚铁氰化物及草酸盐的混合废水中草酸根离子和重金属离子进行处理,重点研究了Ca(OH)2投加量对反应后滤液中COD和Mn2+浓度的影响。其结果分别如图2和如图3所示。

图2 Ca(OH)2投加量对反应后滤液中COD的影响Fig.2 The influence of Ca(OH)2 dosage on COD in filtrate after reaction

图3 Ca(OH)2投加量对反应后滤液中Mn2+含量的影响Fig.3 The influence of Ca(OH)2 dosage on the content of Mn2+ in the filtrate after reaction

从图3可以看出,废水中的Mn2+与添加的Ca(OH)2固体作用非常明显。当Ca(OH)2投加量仅为10 g/L时,反应后滤液中的Mn2+浓度可降至0.5 mg/L以下,Mn2+的去除率接近100%。在碱性条件下,废水中的Mn2+可与游离的OH-结合,生成难溶于水的Mn(OH)2沉淀,从而达到去除重金属离子的目的。
从去除效率与处理成本考虑,针对COD在2000~2500 mg/L的含铁氰化物、亚铁氰化物及草酸盐混合废水,优选Ca(OH)2投加量为40 g/L。经过此投加量的Ca(OH)2处理后,滤液中COD在500 mg/L以下,Mn2+浓度在0.5 mg/L以下。
2.2 铁氰化物和亚铁氰化物处理实验
根据Fe(CN)63-、Fe(CN)64-的特性,选择使用FeSO4·7H2O固体对废水中的铁氰化物和亚铁氰化物进行处理。谷芳芳等[10]对含铁氰化物和亚铁氰化物废水处理的研究,是先调节pH至10,然后加入适量亚硫酸钠搅拌反应30 min,再加入适量硫酸亚铁,调节pH至6~7,加热至50~60 ℃搅拌反应30 min,最后静置。本实验在此基础上,研究亚硫酸钠投加量和温度以及FeSO4·7H2O固体投加量对废水中铁氰化物和亚铁氰化物处理的影响。
2.2.1 亚硫酸钠投加量的影响
调节经40 g/L氢氧化钙处理后的滤液的pH,改变亚硫酸钠固体投加量,投加过量FeSO4·7H2O固体,在55 ℃进行反应,平行量取4个水样进行实验,反应完成后过滤,检测滤液中的总氰化物含量。实验结果如表1所示。
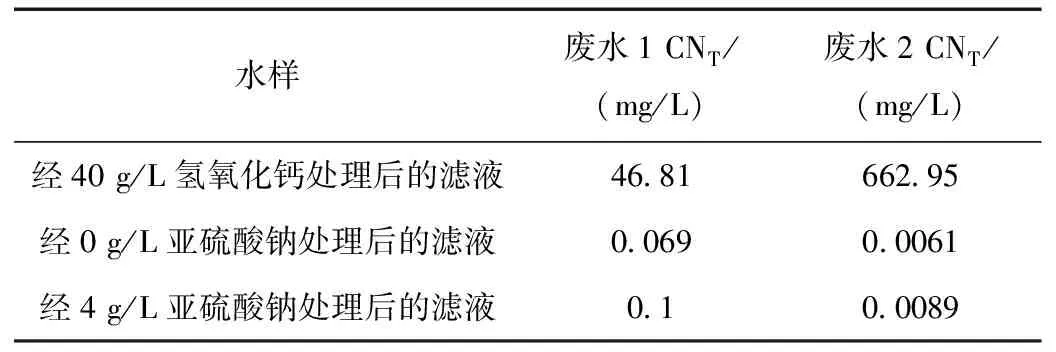
表1 亚硫酸钠投加量对铁氰化物和亚铁氰化物处理的影响Table 1 The influence of sodium sulfite dosage on the treatment of ferricyanide and ferrocyanide

2.2.2 温度的影响
调节经40 g/L氢氧化钙处理后的滤液的pH至6~7,投加过量FeSO4·7H2O固体,改变温度进行反应,平行量取2个水样进行实验,反应完成后过滤,检测滤液中的总氰化物含量。实验结果如表2所示。

表2 温度对铁氰化物和亚铁氰化物处理的影响Table 2 The influence of temperature on the treatment of ferricyanide and ferrocyanide
从表2中可以看出,在FeSO4·7H2O固体投加过量,Fe2+与 Fe(CN)63-、Fe(CN)64-充分结合的情况下,常温条件下搅拌也能使高氰化物浓度的废水中氰化物被处理至0.5 mg/L以下。考虑废水实际处理成本的问题,后续实验在常温条件下进行。
2.2.3 硫酸亚铁投加量的影响
调节经40 g/L氢氧化钙处理后的滤液的pH至6~7,改变FeSO4·7H2O固体的投加量,常温条件下进行反应,平行量取3个水样进行实验,反应完成后过滤,检测滤液中的总氰化物含量。实验结果如图4所示。
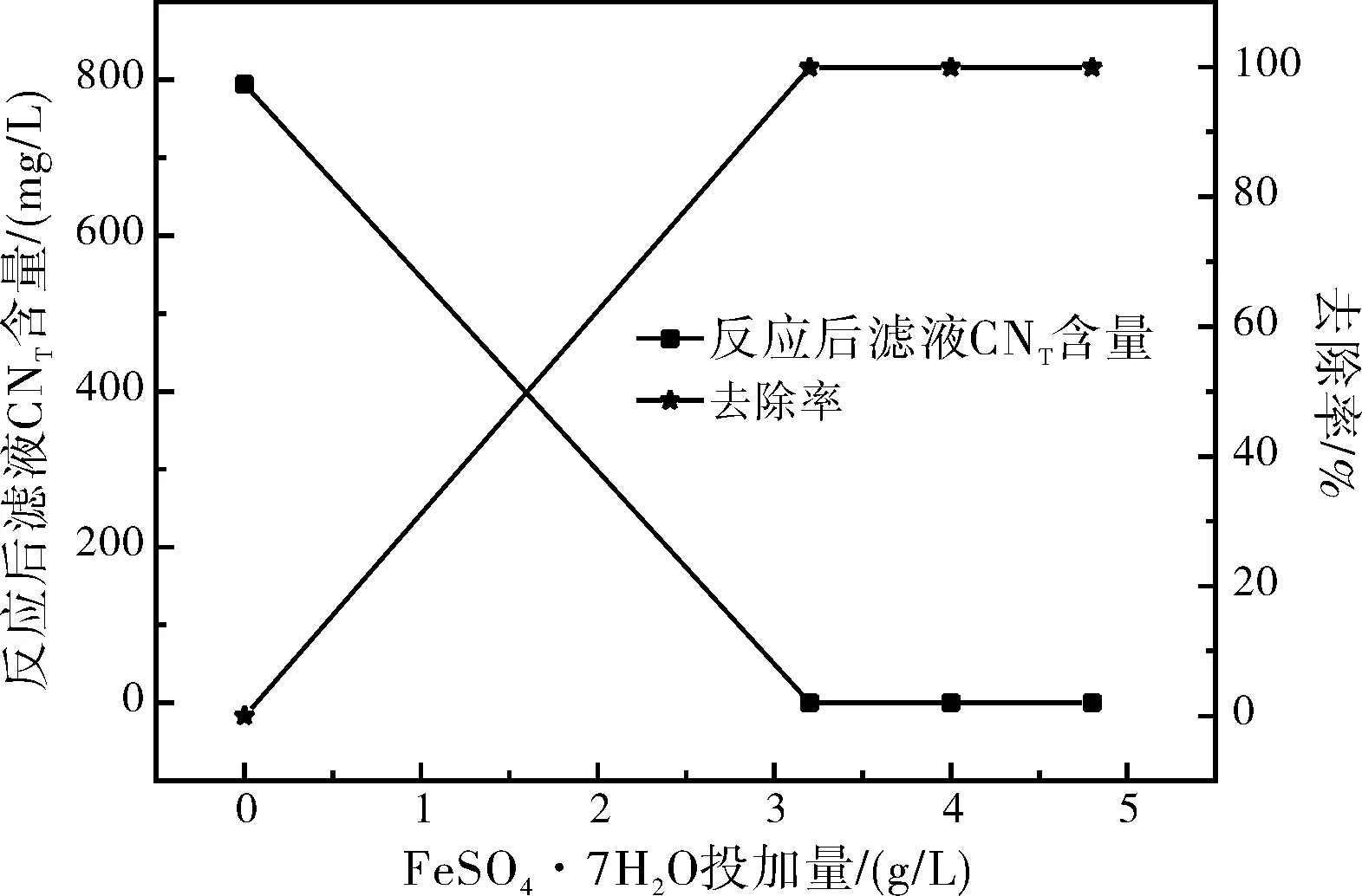
图4 FeSO4·7H2O投加量对反应后滤液中CNT含量的影响Fig.4 The effect of FeSO4·7H2O dosage on the content of CNT in the filtrate after the reaction

3 结 论
本处理工艺可在常温常压的条件下,通过40 g/L的Ca(OH)2固体同时处理含铁氰化物和亚铁氰化物及草酸盐的混合废水中COD和重金属离子,3.2 g/L的FeSO4·7H2O固体处理废水中的铁氰化物和亚铁氰化物,使废水满足污水综合排放标准(GB8978-1996)中COD<500 mg/L、Mn2+<1 mg/L、 CNT<0.5 mg/L的排放要求。
