高碳铬铁中硅、磷、锰元素含量测定新方法
2022-10-15李明明王东王亚朋武斌韩丹杜秀川
李明明,王东,王亚朋,武斌,韩丹,杜秀川
(鞍钢集团本钢板材股份有限公司,辽宁 本溪 117000)
高碳铬铁是轴承钢、不锈钢等钢种生产中不可缺少的合金。作为全球不锈钢生产大国之一,我国铬铁需求量巨大,国内铬铁产量无法满足市场的需求,因此需要进口铬铁来满足市场的缺口。根据近几年铬铁进口价格分析进口量,含碳量≤4%的铬铁价格是含碳量>4%的两倍多,高碳铬铁的进口占据绝对优势。
高碳铬铁中的硅、磷、锰含量对生产起到直接指导作用[1]。由于含碳量高,高碳铬铁试样溶解困难,国家标准中多采用过氧化钠作为碱熔试剂,使用镍坩埚碱熔试样。但是一次碱熔试样只能测一个元素,分析周期长,劳动强度大,而且在碱熔过程中,不仅过氧化钠对镍坩埚侵蚀大,镍坩埚使用次数有限,分析成本高,同时也引入了大量镍离子,增加了基体效应。因此,有必要研究一种方法,用同一母液连续检测高碳铬铁中硅、磷、锰三元素含量,既能降低检测成本,同时也大大提高检测效率。
1 实验部分
1.1 实验仪器
实验仪器采用UV-1601可见分光光度计,马弗炉。
1.2 主要试剂
(1)混合碱熔剂。无水碳酸钠:硼砂:过氧化钠=20:10:7。
(2)高氯酸(ρ约为 1.67 g/mL);盐酸(ρ约为1.19 g/mL),盐酸(1+1)、盐酸(1+10);硫氰酸铵(50 g/L);硝酸银(10 g/L);硫酸(ρ为 1.84 g/mL,1+1);磷酸(ρ约为 1.87 g/mL);亚硫酸氢钠溶液(100 g/L);抗坏血酸溶液(20 g/L)。
(3)磷-显色剂溶液。称取20 g钼酸铵溶解在100 mL温水中,然后加入 700 mL硫酸(1+1),冷却后用水稀释至1 L,混匀;称取1.5 g硫酸肼溶解于水中稀释至1 L,混匀;使用时取25 mL钼酸铵溶液,10 mL硫酸肼溶液及65 mL水混匀。
(4)锰-显色剂溶液。高碘酸钠溶液(100 g/L)。
(5)磷、锰标准溶液 1 000 μg/mL。 磷标准工作溶液:10 μg/mL; 锰标准工作溶液 100 μg/mL 和10 μg/mL;均是由磷、锰标准溶液逐级稀释而成。
(6)实验室用水符合GB/T 6682规定。
1.3 实验原理
碱熔融试样后,用盐酸溶解熔物,高氯酸冒烟处理,使硅成为不溶性硅酸,使磷氧化成正磷酸,盐酸挥铬,过滤、灼烧后称重,测硅的含量,滤液保留[2]。 反应式如下:
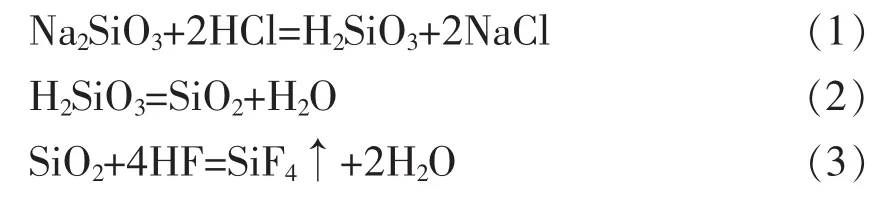
分取滤液,用亚硫酸氢钠将铁等还原,加入钼酸铵和硫酸肼,使之反应生成磷钼蓝,于分光光度计波长680 nm处测量其吸光度,依据工作曲线测磷的含量。反应式如下:
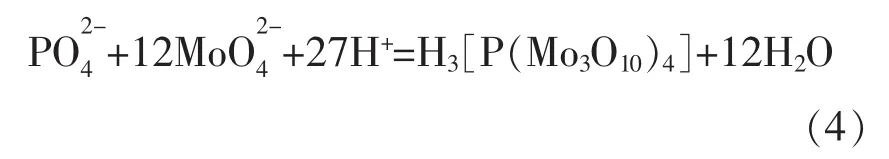
分取滤液,在5%硫酸-7.5%磷酸(体积分数)介质中,用高碘酸钠定量氧化锰(Ⅱ)为紫红色的锰(Ⅶ),于分光光度计波长525 nm处测量其吸光度。有色溶液24 h内很稳定,依据工作曲线测量锰的含量[3]。 反应式如下:
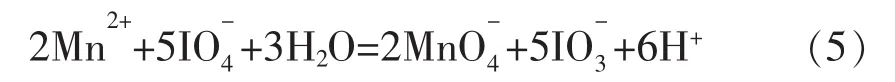
1.4 实验方法
1.4.1 试样的处理
称取两种标准物质FeCr55-C1000和GSB03-2536-2009各0.300 0 g,做如下相同操作。将其置于盛有3 g混合熔剂的无灰定量滤纸中,混匀,拧紧后放入凹型碳粉中,装入瓷坩埚,放入1 050℃的马弗炉中,熔融20 min,取出试样,冷却,放入300 mL烧杯中。
1.4.2 硅、磷、锰含量的分步测定
(1)盐酸挥铬及重量法测硅
向烧杯中加入30 mL盐酸(1+1),加热溶解。待试样熔块完全溶解后加入40 mL高氯酸,高温加热至冒白烟,继续加热,使高氯酸蒸汽沿烧杯壁呈回流状态。持续加热15~20 min,快速加入2 mL盐酸挥铬,重复加入盐酸挥铬5次,直至没有棕色烟。溶液剩2~3 mL即可,取下、冷却。加入5 mL盐酸,加入80 mL热水,加热煮沸约1 min,立即用中速定量滤纸过滤于400 mL的烧杯中,将粘附于烧杯壁上的残留物冲洗至滤纸上,先用温盐酸 (1+10)洗涤至无铁离子的反应(用硫氰酸铵溶液检查最后洗液,直至不呈现橙红色),再用温水洗涤至无氯离子的反应(用硝酸银溶液检查最后洗液,直至不呈现白色沉淀)。
加入10 mL高氯酸于烧杯中,高温回流15 min,尽干。重复上述酸溶盐类、过滤、冲洗操作,合并滤液保存于250 mL容量瓶中,待用。
合并沉淀于铂金坩埚内,烘干,低温灰化,1 050℃灼烧恒重,冷却,称重。为防止其他金属氧化物夹杂影响二氧化硅的纯度,加入5 mL氢氟酸和1 mL硫酸(1+1),低温挥硅,再高温赶尽硫酸烟,1 050℃灼烧恒重,前后两次的重量差为纯净二氧化硅的重量。
(2)磷钼蓝分光光度法测磷
分取25 mL滤液于100 mL两用瓶中,加入10 mL亚硫酸氢钠溶液,在沸水浴中加热至溶液无色,立即加入25 mL磷-显色剂溶液,再在沸水浴中加热15 min,取下,冷却至室温,用水稀释至刻度,混匀。
将溶液移入比色皿中,于分光光度计680 nm波长处,用空白为参比调零,测量其吸光度。移取空白溶液到一组100 mL两用瓶中,分别加入0、0.30、0.90、1.50、1.80、3.00 及 4.50 mL 磷标准工作溶液,依据实验方法测定吸光度值,以吸光度值为横坐标,磷的质量百分数为纵坐标,绘制校准曲线。
(3)高锰酸钠分光光度法测锰
分取20 mL滤液于50 mL两用瓶中,加入3 mL硫酸、4 mL磷酸、3 mL高碘酸钠溶液,放入沸水浴中加热待紫色出现后再保持30 min,取下、冷却、定容。
将溶液移入比色皿中,于分光光度计525 nm波长处,用空白为参比调零,测量其吸光度。移取空白溶液到一组50 mL两用瓶中,加入0、1、2及5 mL锰标准工作溶液(10 μg/mL),加入 1、2 及 3 mL 锰标准工作溶液(100 μg/mL),依据实验方法测定吸光度值,以吸光度值为横坐标,锰的质量百分数为纵坐标,绘制校准曲线。
2 测定条件的选择
2.1 碱熔方式的选择
高碳铬铁因碳含量高,不易被常规的混酸完全溶解,国家标准中通常采用过氧化钠与无水碳酸钠为碱熔剂在镍坩埚内高温熔融的方式[4-6]。本实验采用无灰滤纸包裹自制碱熔剂的方式代替传统镍坩埚碱熔方式。优点如下:不使用镍坩埚,降低碱熔成本;节省清洁维护镍坩埚的时间;简化后期酸溶过程,并且无镍离子引入。
2.2 碱熔剂的选择
为降低碱熔反应的剧烈程度、增强氧化性及分解能力,达到完全熔解试样的要求,本实验改变碱熔剂成分及配比[7],设计4种碱熔体系方案,确定最佳碱熔剂。按1.4.1所述,将标准物质GSB03-2536-2009熔解后,对比不同碱熔体系的碱熔效果见表1。

表1 不同碱熔体系的碱熔效果Table 1 Melting Sample Effects of Different Alkaline Fusion Systems
从表1可以看出,当碱熔剂中没有过氧化钠或是过氧化钠含量不足时,高碳铬铁试样不能完全溶解,当提高过氧化钠在碱熔剂中占比时,试样能被完全溶解,可见过氧化钠能有效提高碱熔剂的强度与活性。为确保高碳铬铁完全溶解,本实验选择方案4的配比,即水碳酸钠:硼砂:过氧化钠=20:10:7。
2.3 检测方法的选择
2.3.1 盐酸挥铬条件的选择
在高氯酸高温回流-盐酸挥铬过程中,重复挥铬5次,对比挥铬效果见表2。

表2 盐酸挥铬效果Table 2 Effect of Removing Chromium by Hydrochloric Acid
由表2可见,当重复挥铬4~5次后,试样中绝大部分铬离子去除,因此本实验选择挥铬5次。
2.3.2 磷测定条件的选择
显色方法的选择。氯化亚锡还原光度法具有检测速度快的优点,但其显色后不稳定、褪色速度快;乙酸丁酯萃取法具有显色稳定、计量精确等显著优点,但需要使用有机试剂萃取,气味大,对人体危害大;磷钼蓝光度法具有显色稳定、计量精确等优点,操作难度适中。因此,本实验采用磷钼蓝光度法。
硅干扰的消除。硅是影响磷元素检测的主要干扰元素之一[8]。在本实验中,硅在高氯酸冒烟、过滤中,以不溶性硅酸形式被分离,用于硅含量的测定,因此,硅不影响磷的显色反应。
其他元素干扰的消除。高价态铬、钒、铈、铁离子本身有颜色,对分光光度法的影响很大,针对这些有色离子都是高价态的共同特点,本实验有针对性的选择亚硫酸氢钠溶液为还原剂,加热后,溶液由黄色转变为无色,达到靶向还原上述有色高价离子的目的。
显色反应时间的确定[9]。分取5份25 mL试样溶液,从加入显色剂开始计时,每间隔5 min取出一个试样,检测其吸光度,绘制吸光度曲线。当试样溶液在沸水中稳定15 min后,试样的吸光度值已稳定,因此本实验选择显色时间为15 min。
2.3.3 锰测定条件的选择
酸度试验。在一定酸度条件下,锰离子能稳定存在于水溶液中。但是随着酸度的降低,锰离子稳定性降低。酸度更低时,可能进一步水解产生碱式盐或氢氧化物沉淀影响显色反应[10]。为确定最佳的显色酸度,取标准物质GSB03-2536-2009滤液,设计4个硫酸-磷酸加入方案,酸度实验结果见表3。

表3 酸度实验结果Table 3 Results of Testing Acidity
由表3可见,在低价锰离子被完全氧化的前提下,当硫酸-磷酸加入量分别为3 mL与4 mL时吸光度值最佳,因此,本实验选择方案3。
铬干扰的消除。高碳铬铁中铬含量基本都在60%以上,经碱熔-酸解后,试样溶液中含有大量的铬离子,影响锰的测定。本实验通过盐酸挥铬,消除了铬离子对锰的影响。
3 结果分析
按本实验方法进行10次检测,再与采用国标方法, 即 GB/T 5687.2-2007、GB/T 4699.3-2007、GB/T 5687.10-2006测定标准物质FeCr55-C1000和GSB03-2536-2009中硅、磷、锰三种元素含量对比,结果见表4。

表4 本实验测定值与标准物质认定值对比Table 4 Comparison of Determined Values and Certified Values Asked by Standard Substances %
由表4看出,本实验测定平均值与标准物质认定值基本一致,达到了国标法的检测效果。标准物质FeCr55-C1000中硅、磷、锰含量的相对标准偏差(RSD,n=10)分别为 0.16%、1.38%、1.43%;标准物质GSB03-2536-2009中硅、磷、锰含量的相对标准偏差(RSD,n=10)分别为 1.71%、1.19%、1.67%,均低于2%,满足实验结果准确度与精密度的要求,既降低检测成本,同时也大大提高检测效率。
4 结语
自制碱熔剂,无水碳酸钠:硼砂:过氧化钠为20:10:7,采用无灰滤纸包裹碱熔剂高温熔融试样,盐酸挥铬5次,磷钼蓝分光光度法测磷,高锰酸钠分光光度法测锰,实现了一次熔样连续测定高碳铬铁中的硅、磷、锰元素含量,解决了传统检测方法中镍坩埚熔样过程繁琐,铬、镍元素基体效应高,一次试样只能检测一个元素等问题。采用本实验测得标准物质硅、磷、锰元素含量平均值与其认定值基本一致,均低于2%,满足实验结果准确度与精密度的要求,既降低检测成本,同时也大大提高检测效率。
