丹参多酚酸盐注射液联合西医常规治疗对慢性心力衰竭疗效及安全性的系统评价及试验序贯分析
2022-10-14穆丽婷赵英强王保和
张 垚,杨 继,穆丽婷,赵英强,王保和
丹参多酚酸盐注射液联合西医常规治疗对慢性心力衰竭疗效及安全性的系统评价及试验序贯分析
张 垚1,杨 继1,穆丽婷2*,赵英强2*,王保和3
1. 天津中医药大学,天津 301617 2. 天津中医药大学第二附属医院,天津 300250 3. 天津中医药大学第一附属医院,天津 300381
系统评价丹参多酚酸盐注射液联合西医常规治疗对慢性心力衰竭的有效性和安全性。计算机检索中国知网、万方、维普、PubMed等数据库中相关随机对照试验(randomized controlled trials,RCTs),检索时间限定为建库至2022年3月20日。采用偏倚风险评估工具进行文献质量评价,使用RevMan 5.3、Stata 15.0软件进行Meta分析,通过TSA 0.9.5.10 Beta软件进行试验序贯分析,并按照GRADE标准进行证据质量评价。最终共纳入23个RCTs,共计2421例患者,纳入研究的整体方法学质量较低。Meta分析结果显示,与西医常规治疗相比,联合丹参多酚酸盐注射液可显著提高临床总有效率[OR=3.95,95% CI(2.92,5.35),<0.000 01],降低Lee心衰评分[MD=−0.95,95% CI(−1.37,−0.52),<0.000 1],提高6 min步行距离[MD=44.50,95% CI(32.02,56.97),<0.000 01],降低血浆B型脑钠肽(B-type natriuretic peptide,BNP)浓度[MD=−74.78,95% CI(−89.24,−60.33),<0.000 01];改善心功能指标,包括提高射血分数(left ventricular ejection fraction,LVEF)[MD=5.33,95% CI(4.33,6.32),<0.000 01],降低左室收缩末期内径(left ventricular end systolic diameter,LVESD)[MD=−5.73,95% CI(−8.04,−3.43),<0.000 01]、左室舒张末期内径(left ventricular end-diastolic diameter,LVEDD)[MD=−5.12,95% CI(−7.16,−3.08),<0.000 01] 及室间隔厚度(interventricular septal thickness,IVST)[MD=−1.12,95% CI(−1.60,−0.64),<0.000 01],提高心输出量(cardiac output,CO)[MD=1.12,95% CI(1.00,1.23),<0.000 01]、心脏指数(cardiac index,CI)[MD=1.12,95% CI(1.00,1.25),<0.000 01] 及每搏量(stroke volume,SV)[MD=9.34,95% CI(5.39,13.29),<0.000 01];降低炎症指标,包括白细胞介素-6(interleukin-6,IL-6)[MD=−1.84,95% CI(−2.36,−1.31),<0.000 01]、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)[MD=−0.74,95% CI(−0.83,−0.66),<0.000 01] 及超敏C反应蛋白(high-sensitivity C-reactive protein,hs-CRP)[MD=−0.97,95% CI(−1.27,−0.67),<0.000 01];降低心型脂肪酸结合蛋白(heart fatty acid binding protein,H-FABP)表达[MD=−9.74,95% CI(−12.21,−7.27),<0.000 01]。在不良反应发生率方面,两组比较差异无统计学意义[RR=0.63,95% CI(0.18,2.17),=0.47]。试验序贯分析进一步肯定了联合丹参多酚酸盐注射液对慢性心力衰竭患者的疗效。GRADE证据质量分级显示临床总有效率为中等质量证据,Lee心衰评分、LVESD等8项结局指标均为低质量证据,其余均为极低质量证据。与西医常规治疗相比,联合丹参多酚酸盐注射液能显著提高临床疗效,无明显不良反应,然而证据等级不高,期待开展更多高质量、大样本、多中心的RCTs,为丹参多酚酸盐注射液治疗慢性心力衰竭提供更充分的循证证据。
丹参多酚酸盐注射液;慢性心力衰竭;系统评价;试验序贯分析;GRADE证据质量评价
心血管疾病(cardiovascular disease)具有发病率高、死亡率高、致残率高、社会经济负担重等特点,严重危害人类身心健康。其中,慢性心力衰竭(chronic heart failure)是各种心血管疾病的严重表现和终末阶段,是一种以呼吸困难、乏力、体液潴留为主要临床表现的临床综合征,最终导致心脏泵功能下降。据2019年美国心脏协会心脏病和脑卒中数据显示,美国20岁以上人群中心力衰竭的病例数已增加到620万,到2030年,心力衰竭的发病率预计将增长46%,患病人数将超过800万。《中国心血管健康与疾病报告2019》显示我国心力衰竭患病人数为890万,心力衰竭的生存率较前已有所提高,然而,随着人口老龄化的加剧和心血管疾病诊疗策略的进步,将导致心力衰竭的患病率和发病率呈持续上升趋势[1]。针对慢性心力衰竭的治疗,现代医学的治疗方案主要为减轻水钠潴留、延缓心室重构为主[2]。近年来大量研究表明,中西医结合治疗慢性心力衰竭的疗效优于单纯西医治疗[3-6]。丹参多酚酸盐注射液主要有效成分丹酚酸B能够显著改善血管内皮功能、清除氧自由基、降低心肌酶活性、增加心肌供血,在改善心力衰竭的临床症状和心功能分级、降低炎症因子水平和提高生活质量等方面具有一定优势[7-8]。然而,尚缺乏相关文献系统评价丹参多酚酸盐注射液在慢性心力衰竭治疗中的有效性、安全性。本研究旨在从循证医学的角度分析丹参多酚酸盐注射液联合西医常规治疗在改善慢性心力衰竭患者的临床症状及心功能指标的有效性和安全性,并进行序贯试验研究与证据级别评价,以期为中西医结合治疗慢性心力衰竭提供参考。
1 资料与方法
1.1 纳入标准
1.1.1 研究类型 随机对照试验(randomized controlled trial,RCT)。
1.1.2 研究对象 符合慢性心力衰竭的诊断标准[2]。
1.1.3 干预措施 对照组采用西医常规治疗药物中的1种或多种,常规治疗包括给予纠正电解质失衡、低剂量吸氧及利尿、强心、扩血管、抑制肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone system,RAAS)过度激活等药物;试验组在对照组基础上联合丹参多酚酸盐注射液,加入5%葡萄糖注射液或0.9%氯化钠注射液,静脉滴注。
1.1.4 结局指标
(1)主要结局指标:临床总有效率,评价标准包括①心功能疗效:按照纽约心功能分级(New York Heart Association,NYHA)标准,经治疗后患者症状/体征明显改善,心功能改善2级且心功能到达I级为显效;治疗后症状/体征缓解,心功能改善1级或心功能达到Ⅰ~Ⅱ级为有效;未见心功能的改善或心功能恶化为无效。②心衰疗效:经治疗后Lee心衰评分减少>75%为显效,治疗后Lee心衰评分减少50%~75%为有效,治疗后Lee心衰评分减少<50%,治疗后Lee心衰评分>治疗前积分为恶化。③其他评价标准:包括以症状/体征改善与治疗期间是否发生不良反应作为疗效评价标准、以症状/体征结合LVEF改善情况作为疗效评价标准以及未具体说明的疗效评价标准。
临床总有效率= (显效例数+有效例数)/总例数
(2)次要结局指标:①Lee心衰评分;②6 min步行试验;③B型脑钠肽(B-type natriuretic peptide,BNP);④心功能指标:包括射血分数(left ventricular ejection fraction,LVEF)、左室收缩末期内径(left ventricular end systolic diameter,LVESD)、左室舒张末期内径(LVEDD,left ventricular end diastolic diameter)、室间隔厚度(interventricular septal thickness,IVST)、心输出量(cardiac output,CO)、心脏指数(cardiac index,CI)、每搏量(stroke volume,SV);⑤炎症指标,包括白细胞介素-6(interleukin-6,IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、超敏C反应蛋白(high-sensitivity C-reactive protein,hs-CRP);⑥血清心型脂肪酸结合蛋白(heart fatty acid binding protei,H-FABP);⑦心率变异性指标。
(3)安全性指标:不良反应发生率。
1.2 排除标准
(1)非RCT研究;(2)干预措施包含除丹参多酚酸盐注射液以外的其他中药、中成药或中药制剂;(3)数据不完整、统计方法错误;(4)缺乏主要结局指标的文献;(5)重复发表文献。
1.3 文献检索策略
计算机检索中国知网、万方数据知识服务平台、维普中文期刊全文数据库、中国生物医学文献数据库、Cochrane library、PubMed、Embase、Web of Science,以主题词检索与自由词检索相结合的方式进行检索,中文检索词:“丹参多酚酸盐注射液”“丹酚酸”“随机对照试验”“随机”“心力衰竭”“心功能不全”“心衰”等;英文检索词:“Salvia Miltiorrhiza Polyphenols Injection”“danphenolic acid”“randomized controlled trial”“random”“heart failure”“cardiac failure”“heart decompensation”“myocardial failure”“myocardiac dysfunction”“cardiomyopathy”等,检索时间限定为建库始至2022年3月20日,语种为中、英文。以PubMed为例,检索式见图1。
1.4 文献筛选与资料提取
文献筛选由2名研究者独立筛选文献、提取资料并交叉核对。如有分歧,则通过讨论或咨询高年资研究者解决。文献筛选时首先阅读题目,排除明显不相关的文献后,进一步阅读文献摘要和全文以确定是否纳入该篇文献。资料提取内容包括:文献作者、发表时间、纳入病例、干预方案、结局指标、方法学质量等信息。

图1 PubMed检索策略
1.5 文献质量评价
由2名研究者根据Cochrane Handbook 5.1中的“RCT偏倚风险评估工具”[9]对纳入文献进行评估。
1.6 统计学分析
1.6.1 Meta分析 使用Review Manager 5.3、Stata15.0进行统计分析。其中,二分类变量以比值比(odds ratio,OR)及其95%置信区间(confidence interval,CI)或相对危险度(relative risk,RR)及其95% CI表示效应量;连续性变量以均数差(mean difference,MD)及其95% CI表示效应量。通过检验对纳入研究的异质性进行检验,当>0.1且2<50%时,提示各研究间统计学异质性较小,采用固定效应模型分析;当≤0.1,2≥50%时,提示各研究间存在明显统计学异质性,并进行敏感性分析以明确异质性来源,若来源不明确,则采用随机效应模型分析。当同一结局指标含有≥10个研究时,则采用Egger检验评估发表偏倚,当>0.05表示无明显发表偏倚,≤0.05表示可能存在发表偏倚。
1.6.2 试验序贯分析 通过TSA 0.9.5.10 Beta软件进行试验序贯分析。
1.6.3 证据质量的GRADE评价 使用GRADE pro3.6.1系统进行证据质量评价,根据GRADE标准[10]评价各结局指标的证据质量。
2 结果
2.1 纳入研究的文献特征
初检共获得相关文献5127篇,按纳入、排除标准逐一筛选,最终纳入23项RCT[11-33]。23项研究共纳入2421例慢性心力衰竭患者,其中试验组1214例,对照组1207例。结局指标:以临床总有效率为结局指标的文献有19篇[11-12,14,16,18-22,24-33],其中以心功能疗效为评价指标的文献有12篇[11-12,14,20,22,25-27,30-33],以心衰疗效为评价指标的文献有5篇[16,21,24,28,30],以症状/体征改善与治疗期间是否发生不良反应作为疗效评价标准的文献有1篇[18],以症状/体征结合LVEF改善情况作为疗效评价标准的文献有1篇[29],未说明疗效评价标准的文献有1篇[19];以Lee心衰评分为结局指标的文献有3篇[13,21,24];以6 min步行试验为结局指标的文献有3篇[21,31,33];以BNP为临床结局指标的文献有4篇[19,22,29,32];以心功能指标为结局指标的文献有19篇[11,13-17,19-22,24-29,31-33],其中以LVEF为结局指标的文献有19篇[11,13-17,19-22,24-29,31-33],以LVESD为结局指标的文献有9篇[13-15,17,19,21-22,25,33],以LVEDD为结局指标的文献有12篇[13-15,17,19-22,25-26,32-33],以LVST为结局指标的文献有3篇[14,17,32],以CO为结局指标的文献有4篇[11,21,27,32],以CI为结局指标的文献有3篇[11,21,27],以SV为结局指标的文献有5篇[11,21,24,27,32];以炎症指标(IL-6、TNF-α、hs-CRP)为结局指标的文献有5篇[14,16-17,20,28];以H-FABP为结局指标的文献有3篇[11,21,27];以不良反应为结局指标的文献有8篇[12,14,18,24-25,29-30,33];以心率变异性、窦性心律震荡指标为结局指标的文献有1篇[23]。见表1。
表1 纳入研究的一般特征
Table 1 Basic characteristics of included RCTs
纳入研究第1作者及年份n/例(T/C)性别(男/女)/例年龄/岁病程干预方案疗程结局指标TCTCTCTC 张先维2020[11]50/5038/1236/1466.53±5.5665.18±5.43//C+SMPI 200 mg,1次·d−1,静脉滴注CWM1个月①⑤⑦ 李健2020[12]44/4424/2025/1964.4±5.564.5±5.8(7.6±2.0)年(7.5±2.2)年C+SMPI 200 mg,1次·d−1,静脉滴注CWM+磷酸肌酸钠1 g,1次·d−1,静脉滴注2个月①⑧ 刘爱根2019[13]35/3524/1123/1264.28±5.6364.31±5.62//C+SMPI 200 mg,1次·d−1,静脉滴注CWM+瑞舒伐他汀钙片5~10 mg,1次·d−1,口服10~14 d②⑤ 周联平2019[14]68/6838/3039/2962.8±3.662.9±3.7(6.7±0.6)年(6.8±0.5)年C+SMPI 200 mg,1次·d−1,静脉滴注CWM+厄贝沙坦150-300 mg,1次·d−1,口服2周①⑤⑥⑧ 骆玉玲2018[15]45/4524/2123/2264.58±3.0264.36±3.05//C+SMPI 200 mg,1次·d−1,静脉滴注CWM+缬沙坦80 mg,1次·d−1,口服14 d⑤ 陈刚2018[16]50/5028/2229/2155.8±9.654.7±9.5(41±18)个月(42±17)个月C+SMPI 200 mg,1次·d−1,静脉滴注CWM14 d①⑤⑥
续表1

纳入研究第1作者及年份n/例(T/C)性别(男/女)/例年龄/岁病程干预方案疗程结局指标 TCTCTCTC 李新国2018[17]47/4622/2519/2753.8±10.552.9±11.2(31.5±18.3)个月(32.7±19.4)个月C+SMPI 200 mg,1次·d−1,静脉滴注CWM14 d⑤⑥ 林能波2017[18]200/200129/71122/7845.18±3.3848.12±3.41(5.34±2.71)年(5.33±1.72)年C+SMPI 200 mg,1次·d−1,静脉滴注CWM+磷酸肌酸钠1 g,1次·d−1,静脉滴注14 d①⑧ 戚凤君2017[19]35/3520/1518/1766.82±7.9865.75±8.76(38.92±5.98)个月(38.65±6.02)个月C+SMPI 200 mg,1次·d−1,静脉滴注缬沙坦80 mg,1次·d−1,口服14 d①④⑤ 蒋亚宝2017[20]47/4629/1827/1956.6±8.357.4±8.9//C+SMPI 200 mg,1次·d−1,静脉滴注CWM14 d①⑤⑥ 薛恩忠2017[21]45/4026/1923/1767.2±4.168.7±3.8(4.3±1.5)年(4.1±1.2)年C+SMPI 200 mg,1次·d−1,静脉滴注CWM+磷酸肌酸钠1 g,1次·d−1,静脉滴注10 d①②③⑤⑦ 周少军2016[22]35/3518/1720/1574.1±6.973.8±6.7(38.4±5.9)个月(37.9±6.1)个月C+SMPI 200 mg,1次·d−1,静脉滴注CWM14 d①④⑤ 梅芳2016[23]63/6345/1844/1965.5±11.367.2±10.7//C+SMPI 80 mg,1次·d−1,静脉滴注CWM14 d⑨ 王邦俊2014[24]36/3618/1819/1767~7965~8522~49个月19~44个月C+SMPI 200 mg,1次·d−1,静脉滴注CWM14 d①②⑤⑧ 尚佳2014[25]87/9937/5041/5869.8±8.467.6±8.2//C+磷酸肌酸钠1 g+SMPI 100 mg,1次·d−1,静脉滴注CWM10 d①⑤⑧ 郑雁2014[26]36/3240/2874.93±6.33//C+SMPI 200 mg,1次·d−1,静脉滴注CWM10 d①⑤ 杨溶海2014[27]60/6043/1741/1965.9±16.466.3±16.9//C+SMPI 200 mg,1次·d−1,静脉滴注CWM6周①⑤⑦ 邱雅慧2013[28]40/4022/1824/1656.7±8.557.2±9.1(40±17)个月(38±16)个月C+SMPI 200 mg,1次·d−1,静脉滴注CWM14 d①⑤⑥ 严翼飞2013[29]22/2215/714/869.4±3.868.8±3.2(3.3±0.8)年(3.1±1.1)年C+SMPI 200 mg,1次·d−1,静脉滴注CWM12 d①④⑤⑧ 杨晓琨2009[30]24/2113/1110/1168.8969.95//C+SMPI 200 mg,1次·d−1,静脉滴注CWM14 d①⑧ 张涵亮2021[31]52/5132/2030/2174.12±2.2673.96±2.21(4.12±0.52)年(4.06±0.51)年C+SMPI 200 mg,1次·d−1,静脉滴注CWM+磷酸肌酸钠1 g,1次·d−1,静脉滴注2个月①③⑤ 沈继龙2014[32]34/3421/1319/1573.5±14.873.8±15.3//C+SMPI 200 mg,1次·d−1,静脉滴注CWM12周①④⑤ 闫文珍2015[33]59/5525/3426/2969.52±7.6067.23±6.20//C+磷酸肌酸钠1 g+SMPI 100 mg,1次·d−1,静脉滴注CWM14 d①③⑤⑧
T-治疗组 C-对照组 SMPI-丹参多酚酸盐注射液 CWM-西医常规治疗 /-未提及 ①临床总有效率 ②Lee心衰评分 ③6 min步行距离④BNP ⑤心功能指标(LVEF、LVESD、LVEDD、LVST、CO、CI、SV) ⑥炎症指标(IL-6、TNF-α、hs-CRP) ⑦H-FABP ⑧不良反应发生率 ⑨心率变异性指标
T-treatment group C-control group SMPI-Salvia Miltiorrhiza Polyphenols Injection CWM-conventional western medicine treatment /-not described ①clinical total effective rate ②Lee heart failure score ③6 min walking distance ④BNP ⑤cardiac function indicators (LVEF, LVESD, LVEDD, LVST, CO, CI, SV) ⑥inflammation indicators (IL-6, TNF-α, hs-CRP) ⑦H-FABP ⑧incidence of adverse reactions ⑨heart rate variability index
2.2 偏倚风险评估
偏倚风险评估结果显示,(1)随机序列的生成:有13项研究[11-14,17,19-22,24,28,31,33]使用随机数字表法分组,1项研究[30]使用Doll’s临床病例随机表,故评为低风险,其余研究均未说明具体分组方法,故评为不清楚;(2)分配隐藏:所有研究均未明确分配隐藏方法,故评为不清楚;(3)盲法:所有研究均未提及盲法,但有2项研究[15,23]结局指标均为客观指标,故评为低风险,其余研究评为不清楚;(4)结局数据的完整性:纳入的所有研究均未发现存在研究对象脱落或数据缺失的情况,故评为低风险;(5)选择性报告:纳入的所有研究均完整地报告了预先设定的结局指标,故评为低风险;(6)其他偏倚:纳入的所有研究均未报告样本量如何估算,但受试对象纳入、排除标准合理,组间基线具有可比性,故评为不清楚,见表2、图2。
表2 纳入研究的偏倚风险评估情况
Table 2 Risk of bias assessment of included RCTs
纳入研究随机序列生成分配隐藏对研究对象及研究者施盲对结局评估者施盲结局数据的完整性选择性报告其他偏倚 张先维2020[11]低风险不清楚不清楚不清楚低风险低风险不清楚 李健2020[12]低风险不清楚不清楚不清楚低风险低风险不清楚 刘爱根2019[13]低风险不清楚不清楚不清楚低风险低风险不清楚 周联平2019[14]低风险不清楚不清楚不清楚低风险低风险不清楚 骆玉玲2018[15]不清楚不清楚低风险低风险低风险低风险不清楚 陈刚2018[16]不清楚不清楚不清楚不清楚低风险低风险不清楚 李新国2018[17]低风险不清楚不清楚不清楚低风险低风险不清楚 林能波2017[18]不清楚不清楚不清楚不清楚低风险低风险不清楚 戚凤君2017[19]低风险不清楚不清楚不清楚低风险低风险不清楚 蒋亚宝2017[20]低风险不清楚不清楚不清楚低风险低风险不清楚 薛恩忠2017[21]低风险不清楚不清楚不清楚低风险低风险不清楚 周少军2016[22]低风险不清楚不清楚不清楚低风险低风险不清楚 梅芳2016[23]不清楚不清楚低风险低风险低风险低风险不清楚 王邦俊2014[24]低风险不清楚不清楚不清楚低风险低风险不清楚 尚佳2014[25]不清楚不清楚不清楚不清楚低风险低风险不清楚 郑雁2014[26]不清楚不清楚不清楚不清楚低风险低风险不清楚 杨溶海2014[27]不清楚不清楚不清楚不清楚低风险低风险不清楚 邱雅慧2013[28]低风险不清楚不清楚不清楚低风险低风险不清楚 严翼飞2013[29]不清楚不清楚不清楚不清楚低风险低风险不清楚 杨晓琨2009[30]低风险不清楚不清楚不清楚低风险低风险不清楚 张涵亮2021[31]低风险不清楚不清楚不清楚低风险低风险不清楚 沈继龙2014[32]不清楚不清楚不清楚不清楚低风险低风险不清楚 闫文珍2015[33]低风险不清楚不清楚不清楚低风险低风险不清楚

图2 纳入研究的总体偏倚风险评估
2.3 Meta分析结果
2.3.1 临床总有效率 共有19篇[11-12,14,16,18-22,24-33]文献以临床总有效率为结局指标。共纳入1726例患者,其中试验组866例,对照组860例,阳性结果分别为799例、656例。异质性检验2=0,=1.00,纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,合并总效应量[OR=3.95,95%CI(2.92,5.35)],合并总效应量的检验=8.92,<0.000 01。按临床总有效率的评价方式不同分组,其中,以心功能疗效为评价指标的文献有12篇[11-12,14,20,22,25-27,30-33],共纳入1191例患者,其中试验组596例,对照组595例,阳性结果分别为820例、674例。异质性检验2=0,=0.98,纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,合并总效应量[OR=3.76,95%CI(2.56,5.54)],合并总效应量的检验=6.72,<0.000 01;结果表明试验组与对照组比较,差异有统计学意义(<0.000 01);以心衰疗效为评价指标的文献有5篇[16,21,24,28,30],共纳入382例患者,其中试验组195例,对照组187例,阳性结果分别为173例、130例。异质性检验2=0,=0.99,纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,合并总效应量[OR=3.66,95%CI(2.09,6.42)],合并总效应量的检验=4.54,<0.00001;结果表明试验组与对照组比较,差异有统计学意义(<0.000 01);以症状/体征改善与治疗期间是否发生不良反应作为疗效评价标准的文献有1篇[18],合并总效应量[OR=4.26,95%CI(1.26,14.43)],合并总效应量的检验=2.33,=0.02;结果表明试验组与对照组比较,差异有统计学意义(=0.02);以症状/体征结合LVEF改善情况作为疗效评价标准的文献有1篇[29],合并总效应量[OR=3.62,95%CI(0.81,16.15)],合并总效应量的检验=1.69,=0.09;结果表明试验组与对照组比较,差异无统计学意义(=0.09);未说明疗效评价标准的文献有1篇[19],合并总效应量[OR=5.71,95%CI(1.13,28.75)],合并总效应量的检验=2.11,=0.03;结果表明试验组与对照组比较,差异有统计学意义(=0.03),提示在西医常规治疗的基础上,联合使用丹参多酚酸盐注射液可更显著地提高心力衰竭的临床总有效率。见图3。
2.3.2 Lee心衰评分 共有3篇[13,21,24]文献以Lee心衰评分为结局指标,共纳入227例患者,其中试验组116例,对照组111例,异质性检验2=0,=0.94,纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,在西医常规治疗的基础上,联合使用丹参多酚酸盐注射液可进一步降低Lee心衰评分0.95分,差异有统计学意义[MD=−0.95,95%CI(−1.37,−0.52),=4.40,<0.000 1]。见图4。
2.3.3 6 min步行试验 共有3篇[21,31,33]文献以6 min步行试验为结局指标。共纳入302例患者,其中试验组156例,对照组146例,总体异质性检验提示异质性较高(2=89%,<0.000 1),敏感性分析发现闫文珍等[33]的研究是造成异质性高的原因,可能与未阐明纳入病例的心衰病程有关。去除该项研究后,数据异质性较前明显降低(2=0,=0.99),采用固定效应模型分析。结果显示,与单用西医常规治疗对比,联合丹参多酚酸盐注射液可以提高6 min步行距离44.50 m,差异有统计学意义[MD=44.50,95%CI(32.02,56.97),=6.99,<0.000 01]。见图5、6。
2.3.4 B型脑钠肽(BNP) 共有4篇[19,22,29,32]文献以BNP为结局指标。共纳入252例患者,其中试验组126例,对照组126例,总体异质性检验提示异质性较高(2=85%,=0.000 2),敏感性分析发现沈继龙等[32]的研究是造成异质性高的原因,可能与检测BNP采用的试剂及检测方法不同有关,尚不明确。去除该项研究后,数据异质性较之前明显降低(2=0,=0.65),采用固定效应模型分析。结果显示,与单用西医常规治疗对比,联合丹参多酚酸盐注射液可以降低血浆BNP质量浓度74.78 pg/mL,差异有统计学意义[MD=−74.78,95%CI(−89.24,−60.33),=10.14,<0.000 01]。见图7、8。
2.3.5 心功能指标
(1)LVEF:共有19篇[11,13-17,19-22,24-29,31-33]文献以LVEF为结局指标。共纳入1762例患者,其中试验组883例,对照组879例,总体异质性检验提示异质性较高(2=82%,<0.000 01),故进一步进行敏感性分析,提示各研究之间稳定性较好,MD在4.81~5.52,不能明确异质性来源,使用随机效应模型进行合并效应量。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以提高LVEF 5.33%,差异有统计学意义[MD=5.33,95%CI(4.33,6.32),=10.52,<0.000 01]。见图9、10。

图3 临床总有效率的Meta分析森林图
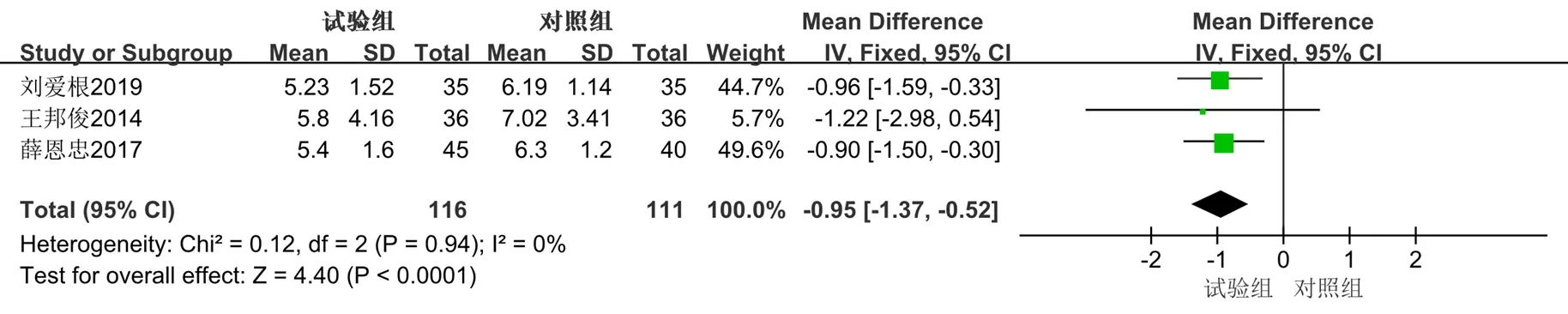
图4 Lee心衰评分的Meta分析森林图
(2)LVESD:共有9篇[13-15,17,19,21-22,25,33]文献以LVESD为结局指标。共纳入914例患者,其中试验组456例,对照组458例,总体异质性检验提示异质性较高(2=95%,<0.000 01),故进一步进行敏感性分析,提示各研究之间稳定性较好,MD在−6.22~−4.55,不能明确异质性来源,使用随机效应模型进行合并效应量。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以降低LVESD 5.73 mm,差异有统计学意义[MD=−5.73,95%CI(−8.04,−3.43),=4.88,<0.000 01]。见图11、12。
(3)LVEDD:共有12篇[13-15,17,19-22,25-26,32-33]文献以LVEDD为结局指标。共纳入1143例患者,其中试验组573例,对照组570例,总体异质性检验提示异质性较高(2=94%,<0.000 01),故进一步进行敏感性分析,提示各研究之间稳定性较好,MD在−5.49~−4.11,不能明确异质性来源,使用随机效应模型进行合并效应量。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以降低LVEDD 5.12 mm,差异有统计学意义[MD=−5.12,95%CI(−7.16,−3.08),=4.92,<0.000 01]。见图13、14。

图5 6 min步行试验的敏感性分析
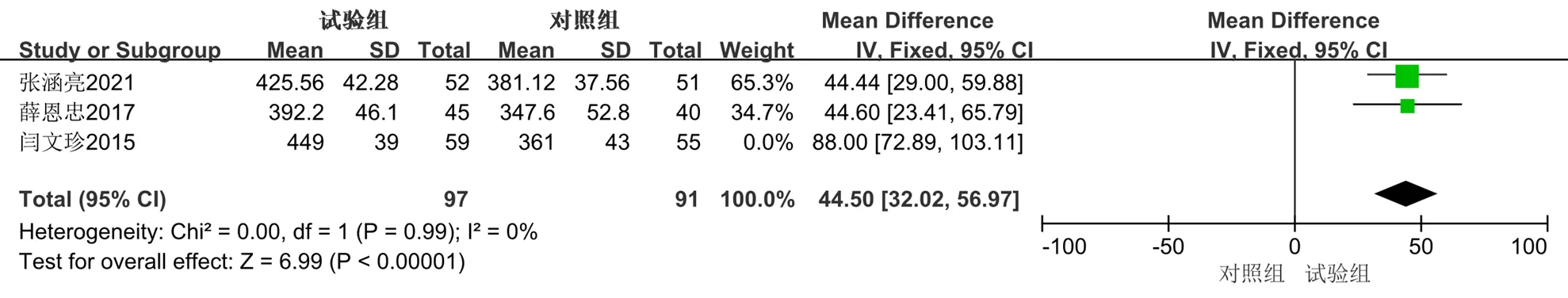
图6 6 min步行试验的Meta分析森林图
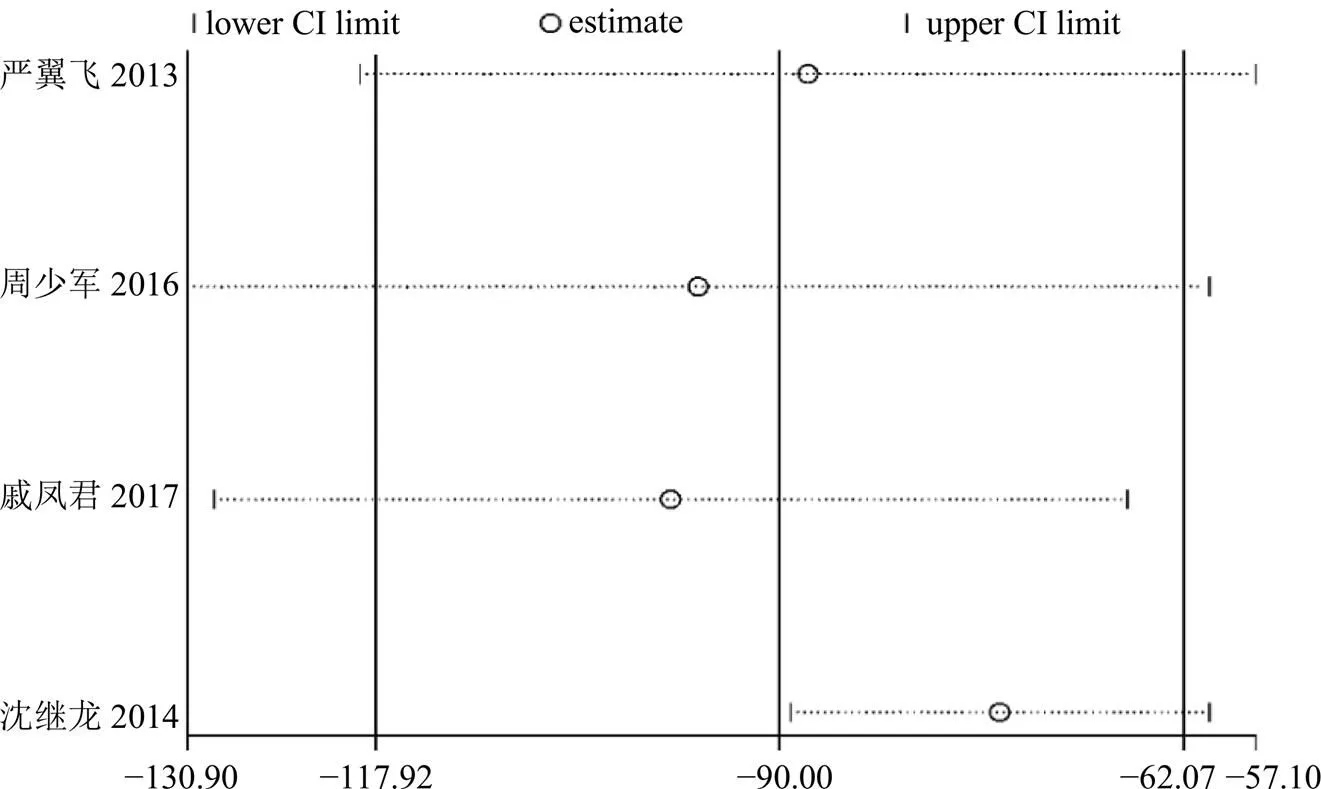
图7 BNP的敏感性分析

图8 BNP的Meta分析森林图

图9 LVEF的敏感性分析
(4)IVST:共有3篇[14,17,32]文献以IVST为结局指标。共纳入297例患者,其中试验组149例,对照组148例,异质性检验(2=0%,=0.69)提示纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以降低IVST 1.12 mm,差异有统计学意义[MD=−1.12,95%CI(−1.60,−0.64),=4.57,<0.000 01]。见图15。
(5)CO:共有4篇[11,21,27,32]文献以CO为结局指标。共纳入373例患者,其中试验组189例,对照组184例,异质性检验(2=4%,=0.37)提示纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以提高CO 1.12 L/min,差异有统计学意义[MD=1.12,95%CI(1.00,1.23),=18.75,<0.000 01]。见图16。
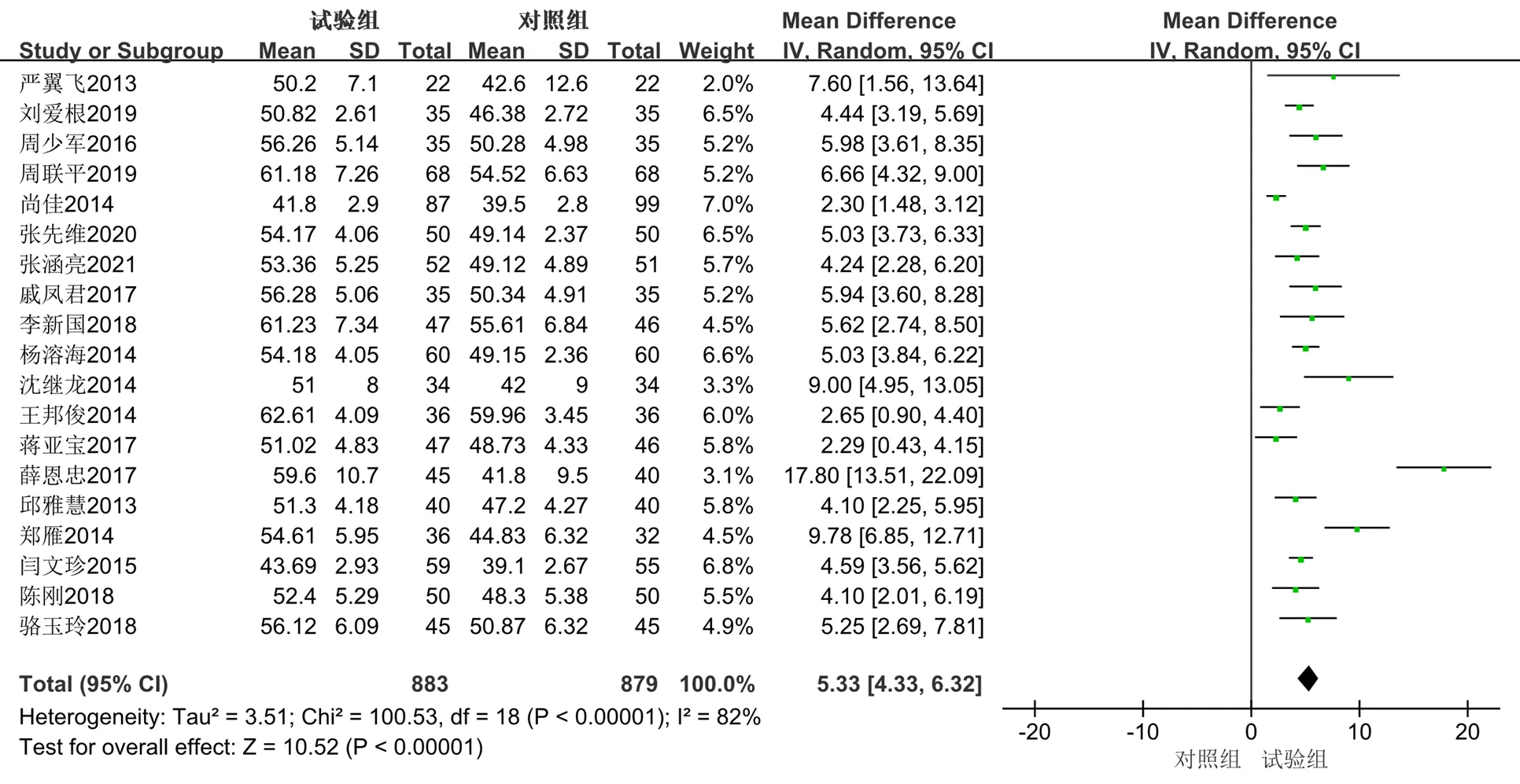
图10 LVEF的Meta分析森林图
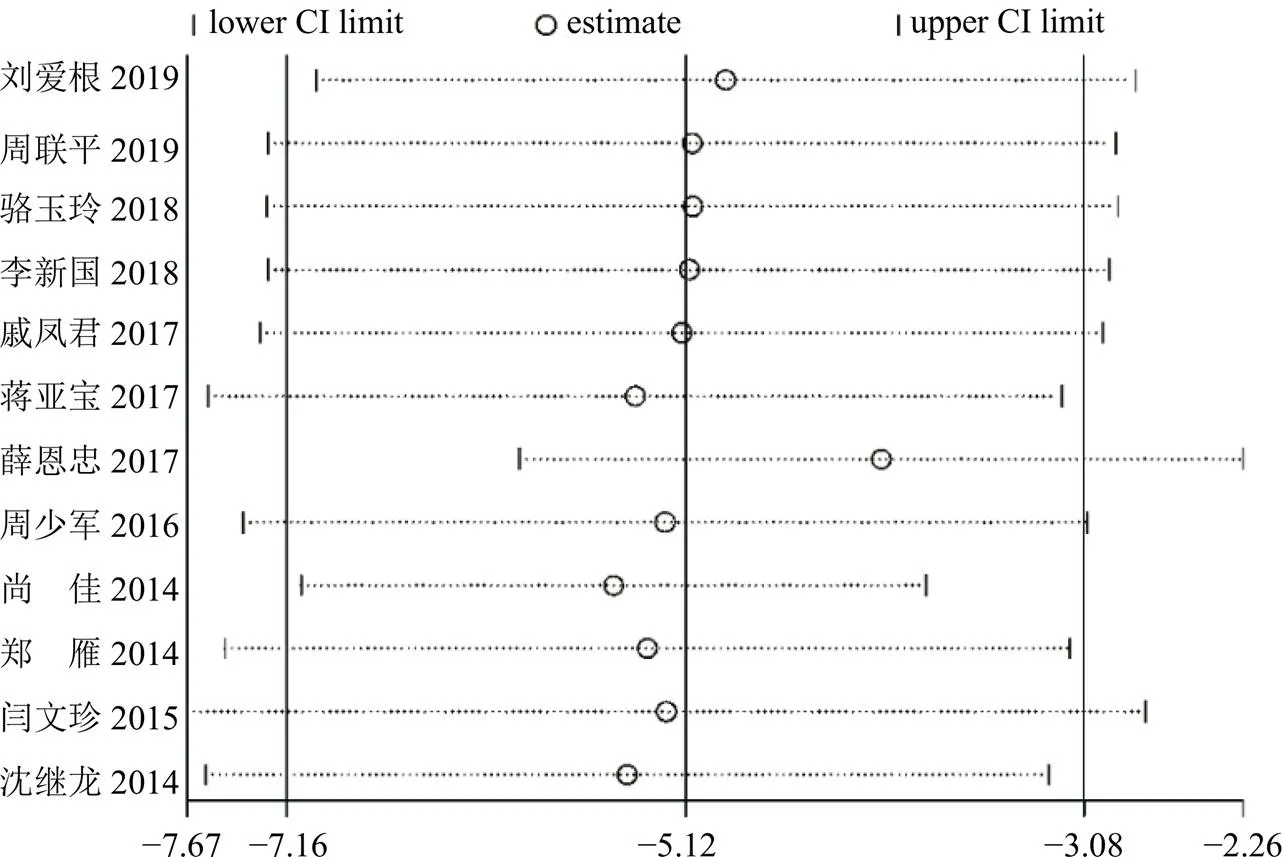
图13 LVEDD的敏感性分析
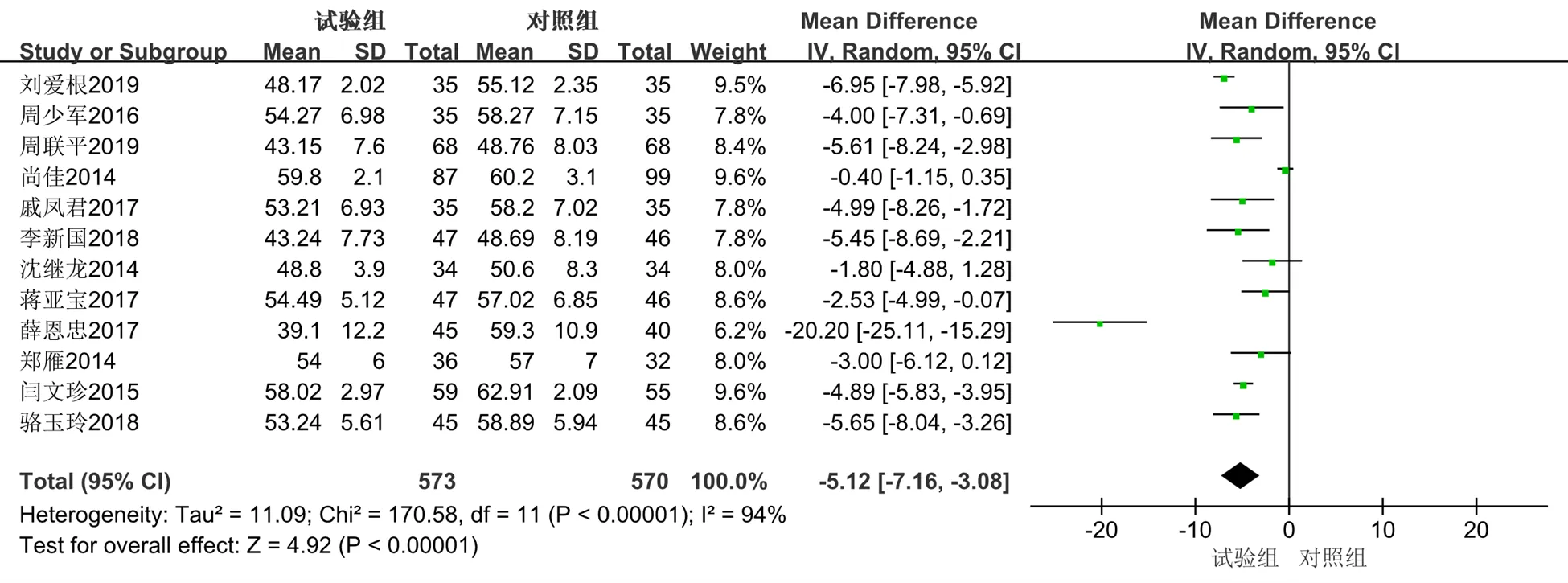
图14 LVEDD的Meta分析森林图
(6)CI:共有3篇[11,21,27]文献以CI为结局指标。共纳入305例患者,其中试验组155例,对照组150例,异质性检验(2=0,=0.61)提示纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以提高CI 1.12 L/(min·m2),差异有统计学意义[MD=1.12,95%CI(1.00,1.25),=17.43,<0.000 01]。见图17。
(7)SV:共有5篇[11,21,24,27,32]文献以SV为结局指标。共纳入445例患者,其中试验组225例,对照组220例,总体异质性检验提示异质性较高(2=88%,<0.000 01),故进一步进行敏感性分析,提示各研究之间稳定性较好,MD在7.33~10.88,不能明确异质性来源,使用随机效应模型进行合并效应量。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以提高SV 9.34 mL/min,差异有统计学意义[MD=9.34,95%CI(5.39,13.29),=4.64,<0.000 01]。见图18、19。

图15 2组LVST的Meta分析森林图
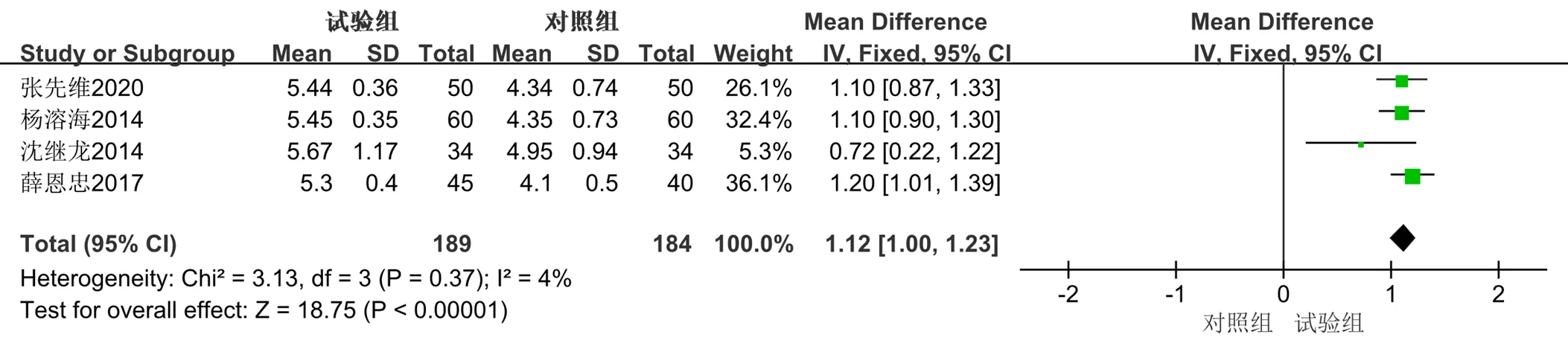
图16 2组CO的Meta分析森林图

图17 CI的Meta分析森林图

图18 SV的敏感性分析

图19 SV的Meta分析森林图
2.3.6 炎症指标
(1)IL-6:共有5篇[14,16-17,20,28]文献以IL-6为结局指标。共纳入502例患者,其中试验组252例,对照组250例,总体异质性检验提示异质性较高(2=50%,=0.09),敏感性分析发现蒋亚宝[20]的研究是造成异质性高的原因,可能与未阐明纳入病例的心衰病程有关。去除该项后,数据异质性较之前明显降低(2=36%,=0.20),采用固定效应模型分析。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以降低IL-6的水平1.84 ng/L,差异有统计学意义[MD=−1.84,95%CI(−2.36,−1.31),=6.86,<0.000 01]。见图20、21。
(2)TNF-α:共有5篇[14,16-17,20,28]文献以TNF-α为结局指标。共纳入502例患者,其中试验组252例,对照组250例,异质性检验(2=47%,=0.11)提示纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以降低TNF-α的水平0.74 ng/L,差异有统计学意义[MD=−0.74,95%CI(−0.83,−0.66),=17.47,<0.000 01]。见图22。
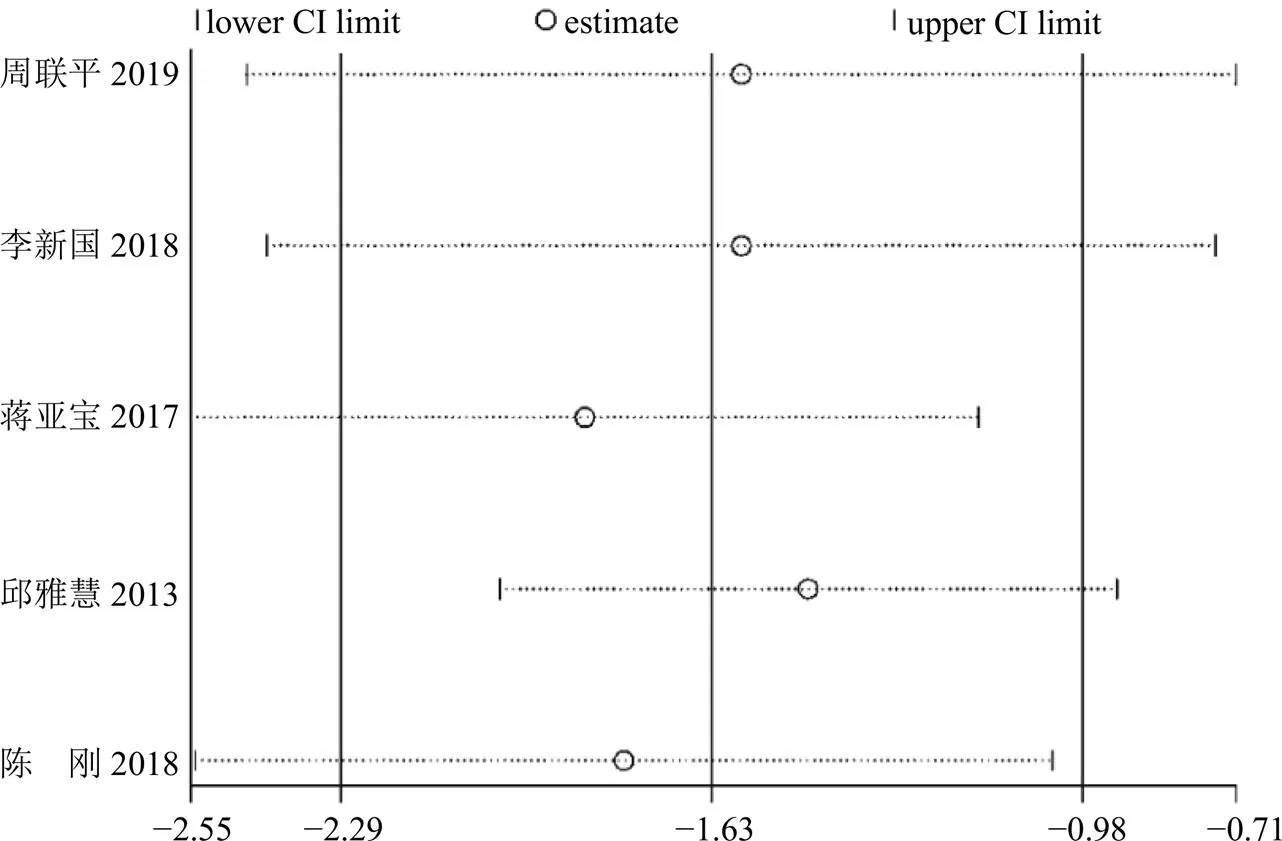
图20 IL-6的敏感性分析

图21 IL-6的Meta分析森林图
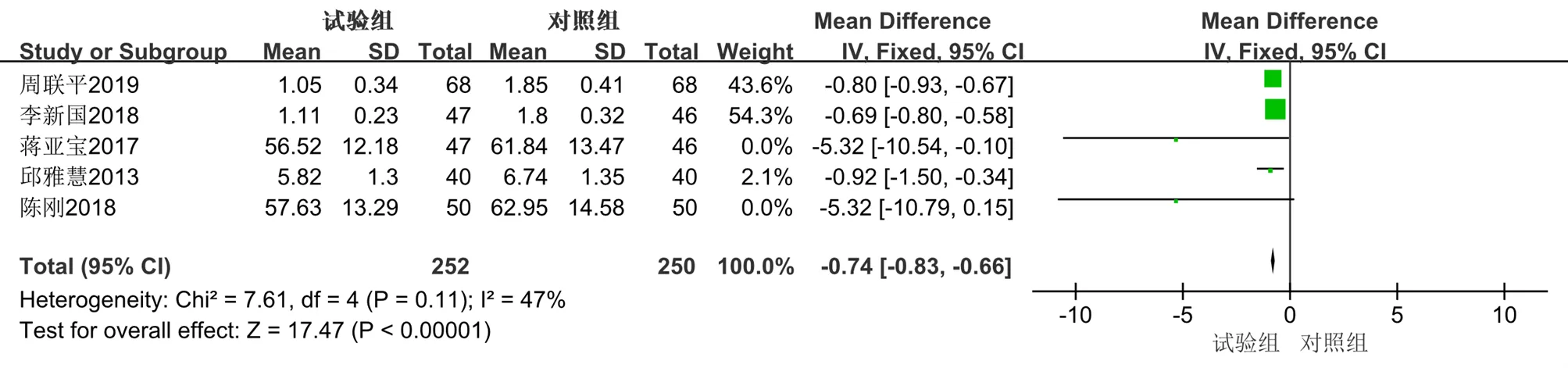
图22 TNF-α的Meta分析森林图
(3)hs-CRP:共有5篇[14,16-17,20,28]文献以hs-CRP为结局指标。共纳入502例患者,其中试验组252例,对照组250例,总体异质性检验提示异质性较高(2=68%,=0.01),敏感性分析发现周联平[14]的研究是造成异质性高的原因,可能与该研究的对照组在西医治疗基础上联合了厄贝沙坦有关。去除该项研究后,数据异质性较之前明显降低(2=39%,=0.18),采用固定效应模型分析。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以降低hs-CRP的水平0.97 mg/L,差异有统计学意义[MD=−0.97,95%CI(−1.27,−0.67),=6.36,<0.000 01]。见图23、24。
2.3.7 血清H-FABP 共有3篇[11,21,27]文献以H-FABP为结局指标。共纳入305例患者,其中试验组155例,对照组150例,异质性检验(2=0,=0.94)提示纳入文献无明显异质性,选用固定效应模型进行Meta分析。结果显示,与单用西医常规治疗相比,联合丹参多酚酸盐注射液可以降低H-FABP水平9.74 ng/mL,差异有统计学意义[MD=−9.74,95%CI(−12.21,−7.27),=7.74,<0.000 01]。见图25。

图23 hs-CRP的敏感性分析
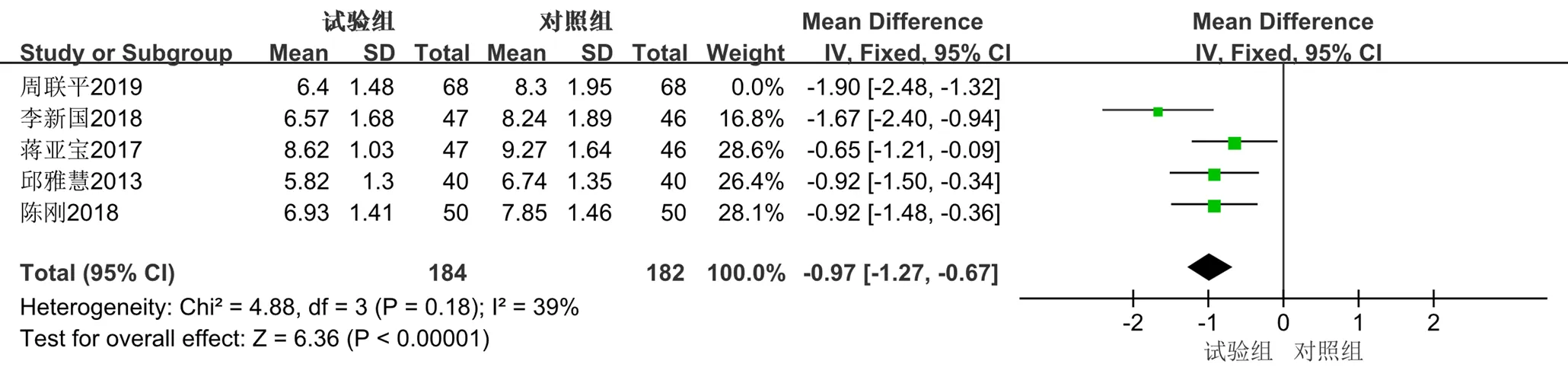
图24 hs-CRP的Meta分析森林图
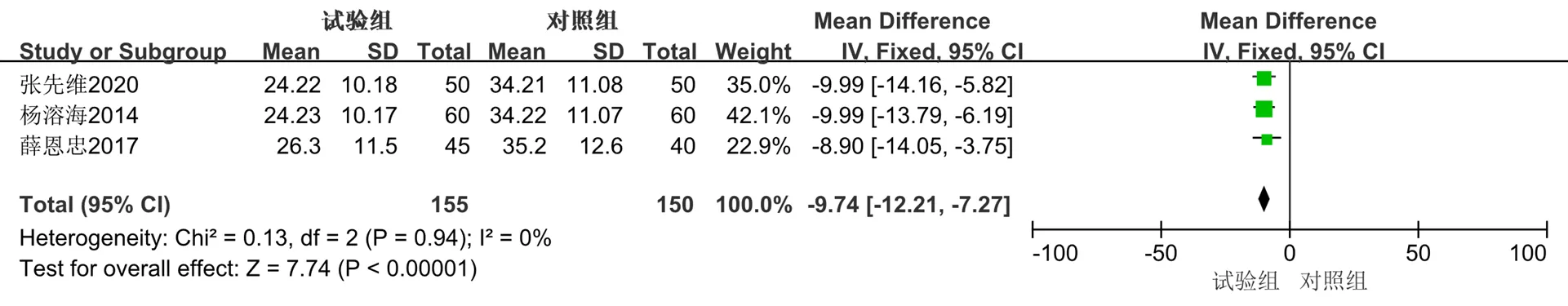
图25 H-FABP的Meta分析森林图
2.3.8 不良反应发生率 共有8篇[12,14,18,24-25,29-30,33]文献有不良反应报告,其中6篇文献显示未见明显不良反应,2篇[14,18]文献报告了西医常规治疗联合丹参多酚酸盐注射液出现的不良反应,包括9例心悸,头晕6例,头痛1例,恶心呕吐2例;同时也报告了对照组出现不良反应,包括12例心悸,头晕7例,头痛3例,恶心呕吐2例。各研究结果间异质性较高(2=67%,=0.08),采用随机效应模型。Meta分析结果显示,试验组在不良反应发生率方面与对照组差异无统计学意义[RR=0.63,95%CI(0.18,2.17),=0.73,=0.47],提示西医常规治疗联合丹参多酚酸盐注射液与单用西医常规治疗相比,不良反应发生率无显著差异。见图26。
2.3.9 心率变异性指标 只有1篇[23]文献以心率变异性指标为结局指标,在此只做描述性分析。结果显示,在治疗14 d后,试验组较对照组能显著改善心率变异性指标,包括全程所有窦性R-R间期的标准差(standard deviation of NN intervals,SDNN)[MD=−20.00,95%CI(−27.92,−12.08),=4.95,<0.000 01]、全程每5 min的R-R间期平均值的标准差(standard deviation of the averages of NN intervals in all 5-minute segments of the entire recording,SDANN)[MD=−12.20,95%CI(−18.77,−5.63),Z=3.64,=0.000 3]、相近窦性R-R间期差值的均方根(square root of the mean of the sum of the squares of differences between adjacent NN intervals,RMMSD)[MD=−7.50,95%CI(−9.56,−5.44),=7.13,<0.000 01]、相邻两个窦性R-R间期差值大于50 ms的心搏数占所分析总心搏数的百分比(NN50 count divided by the total number of all NN intervals,PNN50)[MD=−1.00,95%CI(−1.40,−0.60),=4.84,<0.000 01]、频域参数中的低频范围功率(low frequencies,LF)和高频范围功率(high frequencies,HF)的比值(LF/HF)[MD=0.75,95%CI(0.61,0.89),=10.37,<0.000 01],见图27。
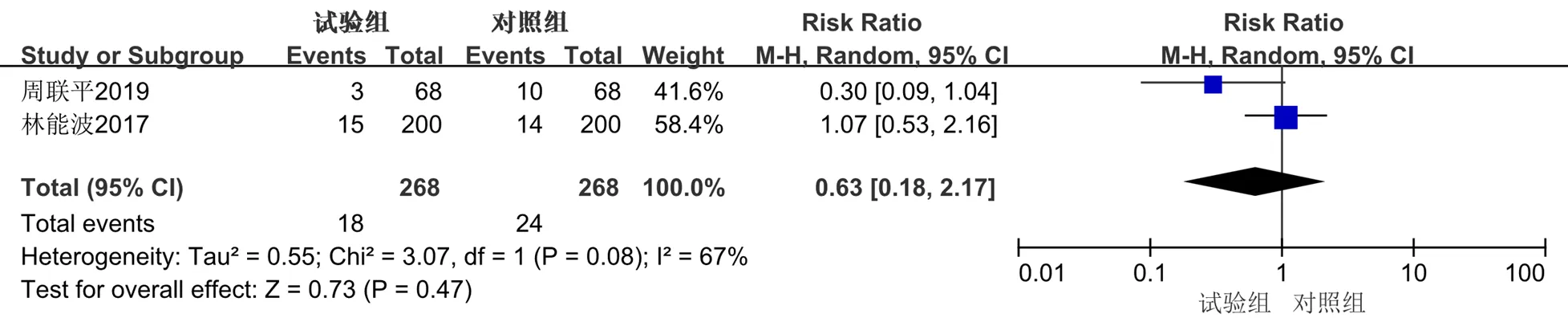
图26 不良反应的Meta分析森林图
2.4 发表偏倚
对临床总有效率、IVEDD、LVEF 3项结局指标进行Egger检验,结果显示临床总有效率(=0.120)、LVEDD(=0.216)、LVEF(=0.002)可能存在发表偏倚。见图28。
2.5 试验序贯分析
试验序贯分析(trial sequential analysis,TSA)能克服传统Meta分析存在的不足之处,使统计分析结果更具有稳健性。此外,TSA还可以估算出Meta分析得到稳定的结论所期望的信息量(required information size,RIS),即为临床试验提供了一个达到样本量的终止标准[34]。本研究对临床总有效率的19项研究、LVEF的19项研究进行TSA分析,设置type 1 error=0.05,power=0.80,RIS为Meta分析所需要的样本量[35]。

图27 心率变异性各项指标分析

图28 临床总有效率(A)、LVEDD (B) 和LVEF (C) 的Egger检验图
2.5.1 临床总有效率 根据临床总有效率的Meta分析结果,本研究设相对危险降低度(relative risk reduction,RRR)为10%,对照组相对事件发生率为76.28%,对19项研究进行TSA。结果累计值曲线(蓝色曲线)在纳入第5项研究[27]后穿过了传统界值(蓝色虚线,=1.96)和TSA曲线(红色曲线),RIS=1077;在纳入第13项研究[20]后样本量已超过RIS,这表明西医常规治疗联合丹参多酚酸盐注射液在提高慢性心力衰竭患者的临床总有效率方面优于对照组,且足已达到所需的病例数。惩罚后的曲线(绿色实线)在纳入第3项研究[28]后超过了传统界值(蓝色虚线,=1.96),进一步肯定了该结论。见图29、30。
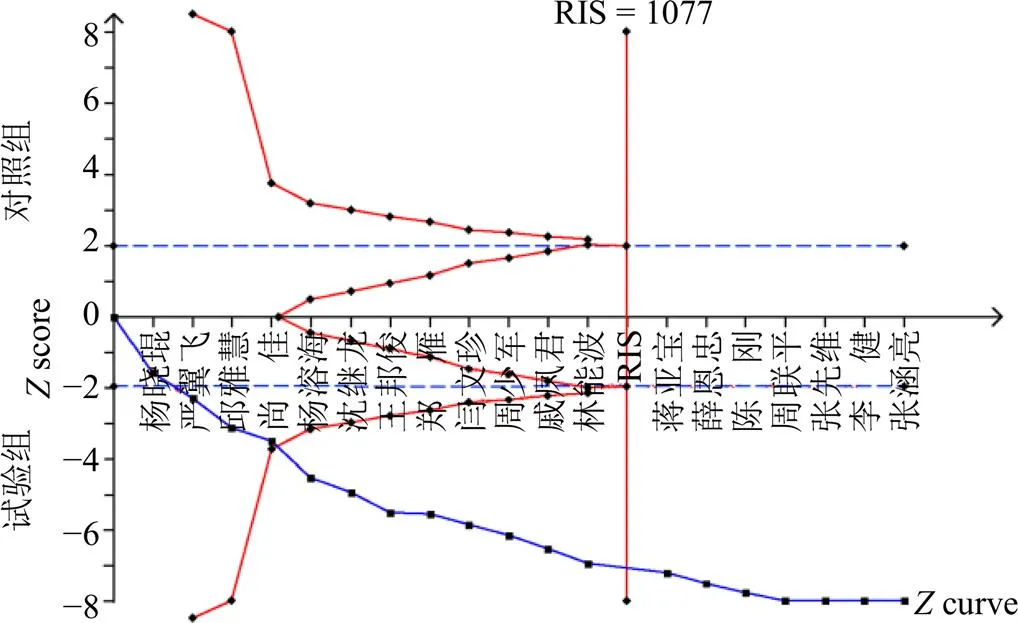
图29 临床总有效率的试验序贯分析

图30 临床总有效率的惩罚统计量分析
2.5.2 LVEF 根据LVEF的Meta分析结果,选用经验值(empirical)对19项研究进行TSA。结果累计值曲线(蓝色曲线)在纳入第2项研究[28]后同时穿过了传统界值(蓝色虚线,=1.96)与TSA界值(红色曲线),RIS=128;在纳入第3项研究[25]前样本量已超过RIS,这表明西医常规治疗联合丹参多酚酸盐注射液在提高慢性心力衰竭患者的LVEF方面优于对照组,且足已达到所需的病例数。惩罚后的曲线(绿色实线)在纳入第2项研究[28]后超过了传统界值(蓝色虚线,=1.96),进一步肯定了该结论。见图31、32。

图31 LVEF的试验序贯分析

图32 LVEF的惩罚统计量分析
2.6 证据质量的GRADE评价
根据GRADE标准,从纳入研究的局限性、不一致性、间接性、不精确性、发表偏倚5个方面对结局指标进行评估,结果显示临床总有效率为中等质量证据,Lee心衰评分、LVESD、LVEDD、LVST、CO、CI、TNF-α、H-FABP 8项结局指标均为低质量证据,6 min步行试验、BNP、LVEF、SV、IL-6、hs-CRP、不良反应发生率7项指标均为极低质量证据,降级的主要原因包括纳入的研究盲法缺失、分配隐藏不充分、部分研究间异质性较大及置信区间跨过临床决策阈值、存在发表偏倚等。见表3。
表3 西医常规治疗联合丹参多酚酸盐注射液对慢性心力衰竭患者疗效Meta分析的GRADE证据质量评价
Table 3 GRADE evidence quality evaluation of Meta-analysis on efficacy of conventional western medicine combined with Salvia Miltiorrhiza Polyphenols Injection in treatment of chronic heart failure
结局指标研究数量/篇研究类型研究的局限性不一致性间接性不精确性发表偏倚样本量效应量(95%CI)证据质量试验组对照组 临床总有效率19RCT严重①不显著不显著不显著不显著866860OR=3.95(2.92,5.35)中等质量 Lee心衰评分 3RCT严重①不显著不显著严重③怀疑116111MD=−0.95(−1.37,−0.52)低质量 6 min步行试验 3RCT严重①严重②不显著严重③怀疑156146MD=44.50(32.02,56.97)极低质量 BNP 4RCT严重①严重②不显著严重③怀疑126126MD=−74.78(−89.24,−60.33)极低质量 LVEF19RCT严重①严重②不显著不显著严重⑤883879MD=5.33(4.33,6.32)极低质量 LVESD 9RCT严重①严重②不显著不显著怀疑456458MD=−5.73(−8.04,−3.43)低质量 LVEDD12RCT严重①严重②不显著不显著不显著573570MD=−5.12(−7.16,−3.08)低质量 LVST 3RCT严重①不显著不显著严重③怀疑149148MD=−1.12(−1.60,−0.64)低质量 CO 4RCT严重①不显著不显著严重③怀疑189184MD=1.12(1.00,1.23)低质量 CI 3RCT严重①不显著不显著严重③怀疑155150MD=1.12(1.00,1.25)低质量 SV 5RCT严重①严重②不显著严重③怀疑225220MD=9.34(5.39,13.29)极低质量 IL-6 5RCT严重①严重②不显著严重③怀疑252250MD=−1.84(−2.36,−1.31)极低质量 TNF-α 5RCT严重①不显著不显著严重③怀疑252250MD=−0.74(−0.83,−0.66)低质量 Hs-CRP 5RCT严重①严重②不显著严重③怀疑252250MD=−0.97(−1.27,−0.67)极低质量 H−FABP 3RCT严重①不显著不显著严重③怀疑155150MD=−9.74(−12.21,−7.27)低质量 不良反应发生率 2RCT严重①严重②不显著严重③④怀疑268268RR=0.63(0.18,2.17)极低质量
OR-比值比 MD-均数差 RR-相对危险度 ①盲法缺失、分配隐藏不充分 ②2>50% ③样本量小 ④置信区间跨过临床决策阈值 ⑤Egger检验(=0.016)
OR-odds ratio MD-mean difference RR-relative risk ①missing blinding, insufficient allocation concealment ②2> 50% ③small sample size ④confidence interval crossing the clinical decision threshold ⑤Egger test (= 0.016)
3 讨论
慢性心力衰竭是各种心血管疾病发展的终末阶段,具有住院率高、病死率高、经济负担重等特点,其病因与神经内分泌激活、持续炎症反应、心室重构等因素有关。其中,神经内分泌-细胞因子系统的激活是心力衰竭发病的启动因素,IL-1、IL-6及TNF-α炎症因子的释放是炎症状态持续的原因,能刺激内皮细胞分泌炎性介质,增加炎性渗出及氧自由基产生,加重炎症反应,导致血管内皮功能下降、微循环障碍、心肌细胞损伤,加快心肌细胞的坏死、凋亡,促进心衰的进展,若不及时干预,会导致患者病情不断恶化。因此,保护心肌细胞、抑制炎症、延缓心室重构是目前心力衰竭治疗上的主要手段[36]。慢性心力衰竭属于祖国医学“心衰”“喘证”“水肿”“胸痹”等治疗范畴,其核心病机为气虚血瘀水停。其中,血瘀既为致病因素,也为病理产物,是慢性心力衰竭发病的关键环节[37]。丹参多酚酸盐注射液具有活血、化瘀、通脉的功效,有研究表明,丹参多酚酸盐注射液的主要有效成分为丹参乙酸镁,可通过Toll样受体4(Toll-like receptor 4,TLR4)-白细胞介素6(interleukin-6,IL-6)-信号传导及转录激活蛋白3(signal transduction and activator of transcription 3,STAT3)通路、过氧化物酶体增殖子活化受体γ(peroxisome proliferator activated receptor γ,PPARγ)- 核转录因子E2相关因子2(nuclear factor erythroid-2 related factor 2,Nrf2)-抗血红素加氧酶-1(heme oxygenase-1,HO-1)、烟酰胺腺嘌呤二核苷酸磷酸氧化酶(nicotinamide adenine dinucleotide phosphate oxidase,NOX)-细胞内活性氧(reactive oxygen species,ROS)-胞外信号调节激酶(extracellular signal-regulated kinase,ERK)等通路起到抑制炎症反应、抗脂质过氧化、减轻细胞损伤、保护内皮功能、保护心肌细胞、抑制心室重构的作用[38-42]。
本研究系统评价了西医常规治疗联合丹参多酚酸盐注射液治疗慢性心力衰竭的疗效及安全性,与西医常规治疗相比,联合丹参多酚酸盐注射液能显著提高临床疗效,无明显不良反应。以上研究结果对临床治疗慢性心力衰竭有一定的指导意义。相较于传统Meta分析,TSA的优势在于可以通过样本量的估算计算Meta分析中获得显著性差异所需的病例数,最大程度避免因随机误差而产生的假阳性错误[34-35]。本研究选取了临床总有效率和LVEF进行TSA,结果发现二者的累计均穿过了传统界值和RIS,证明西医常规治疗联合丹参多酚酸盐注射液在降低患者临床总有效率、提高LVEF上,得到了肯定的结论,并达到了所需的病例数,进一步证实了该结论的准确性。
GRADE评价系统采用高度结构化的方式对证据等级进行了划分,并通过逐条罗列的方式清晰地展示出评价项目,以便于临床医生自行了解干预措施的有效性及可行性,进而做出临床决策[43]。本研究各项指标中,临床总有效率为中等质量证据,Lee心衰评分、LVESD、LVEDD、LVST、CO、CI、TNF-α、H-FABP 8项结局指标均为低质量证据,6 min步行试验、BNP、LVEF、SV、IL-6、hs-CRP、不良反应发生率7项指标均为极低质量证据,表明本研究所预测的疗效可能与真实疗效存在一定的差距,原因主要在于纳入的研究盲法缺失、分配隐藏不充分、部分研究间异质性较大及置信区间跨过临床决策阈值、存在发表偏倚有关,这也是当前同类型系统评价研究中亟待解决的重要问题,未来仍需纳入更高质量的RCT来提高证据级别。在临床治疗慢性心力衰竭上,仍需要综合考虑患者的整体情况作出临床决策。
本研究尚有以下不足:(1)纳入的研究方法学质量不高,多数研究存在随机方法不明确、盲法缺失及分配隐藏不充分的情况,可能导致选择性偏倚;(2)由于近50%的文献未报告病程及基础用药不明确,可能造成临床异质性的因素,难以进一步探索研究间异质性的来源,除临床总有效率、Lee心衰评分、LVST、CO、CI、TNF-α、H-FABP外,其余指标中各研究间的异质性较大,影响了结果的可靠性;(3)由于病情轻重不同或病程不同,丹参多酚酸盐注射液的疗效可能有所不同,患者原发疾病不同,不同级别医疗机构的临床医师对心力衰竭的严重程度判断不同,临床习惯用药不同等,由于大部分研究未完整报告研究对象的临床情况,从而也会影响探讨丹参多酚酸盐注射液在慢性心力衰竭治疗中的地位,可能会影响到最终结果的准确性;(4)全部文献均未替代指标,未有相关再住院率、生存率等终点事件的报道,也未报到与患者生活质量相关的指标,治疗后随访情况均不详;(5)本研究中仅有8项研究[12,14,18,24-25,29-30,33]报道了不良反应,需要进一步验证药物安全性。因此,在今后的研究中,应注意加强临床试验方案设计的严谨性,提高中医药研究结果的可靠性和安全性,以进一步提高证据强度。
综上,在西医常规治疗的基础上联合丹参多酚酸盐注射液,在提高慢性心力衰竭患者的总体临床疗效、改善临床症状、提高心功能、降低炎症因子表达等方面具有显著优势,安全性方面与单用西医常规治疗相比无明显差异。然而证据等级不高,期待未来开展更多高质量、大样本、多中心的RCTs,为丹参多酚酸盐注射液治疗慢性心力衰竭提供更充分的循证证据。
利益冲突 所有作者均声明不存在利益冲突
[1] 《中国心血管健康与疾病报告》编写组. 《中国心血管健康与疾病报告2020》要点解读 [J]. 中国心血管杂志, 2021, 26(3): 209-218.
[2] 中华医学会心血管病学分会心力衰竭学组, 中国医师协会心力衰竭专业委员会, 中华心血管病杂志编辑委员会. 中国心力衰竭诊断和治疗指南2018 [J]. 中华心血管病杂志, 2018, 46(10): 760-789.
[3] 郑思道, 李珂辉, 马学竹, 等. 芪苈强心胶囊治疗心力衰竭的Meta分析 [J]. 疑难病杂志, 2022, 21(1): 84-89.
[4] 王天园, 王彦博, 冯硕, 等. 大株红景天注射液联合常规、西医疗法治疗冠心病合并心力衰竭有效性和安全性的系统评价 [J]. 中国全科医学, 2022, 25(2): 236-242.
[5] 王梦玺, 曹培华, 吴晨洁, 等. 温阳利水中药治疗心力衰竭合并利尿剂抵抗疗效及安全性的Meta分析 [J]. 中国全科医学, 2021, 24(29): 3734-3741.
[6] 谢锋, 段广靖, 王斌, 等. 芪参益气滴丸联合曲美他嗪治疗慢性心力衰竭的meta分析 [J]. 海南医学院学报, 2021, 27(9): 689-694.
[7] 安琪, 赵佳, 刘佩东, 等. 电针联合丹参多酚酸盐对急性心肌梗死大鼠心功能及药物组织分布的影响 [J]. 中国中西医结合杂志, 2022, 42(3): 334-340.
[8] 李铭, 侯雯莉, 杨国红, 等. 丹参多酚酸盐治疗心力衰竭的进展 [J]. 武警后勤学院学报: 医学版, 2018, 27(10): 885-888.
[9] Higgins J P T, Green S. Cochrane handbook for systematic reviews of interventions (Version 5.1.0.) [EB/OL]. (2011-03-01) [2020-03-09]. http://handbook-5-1.cochrane.org/.
[10] Guyatt G H, Oxman A D, Vist G E,. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations [J]., 2008, 336(7650): 924-926.
[11] 张先维. 丹参多酚酸盐注射液治疗冠心病心力衰竭的疗效及对患者左心功能的影响 [J]. 现代诊断与治疗, 2020, 31(10): 1581-1582.
[12] 李健, 李春霞. 丹参多酚酸盐与磷酸肌酸钠治疗冠心病心力衰竭的效果 [J]. 中国继续医学教育, 2020, 12(12): 141-143.
[13] 刘爱根. 注射用丹参多酚酸盐联合瑞舒伐他汀治疗冠心病合并慢性心衰的临床疗效观察 [J]. 临床医药文献电子杂志, 2019, 6(A4): 112-113.
[14] 周联平. 丹参多酚酸盐注射液联合厄贝沙坦对慢性心衰患者左心室射血分数的影响 [J]. 实用心脑肺血管病杂志, 2019, 27(S1): 231-233.
[15] 骆玉玲, 臧清华, 吴昕, 等. 丹参多酚酸盐联合缬沙坦对慢性心力衰竭患者心功能及血浆脑钠肽的影响 [J]. 深圳中西医结合杂志, 2018, 28(12): 32-34.
[16] 陈刚. 丹参多酚酸盐对慢性心力衰竭患者心功能及炎症因子的影响效果观察 [J]. 中西医结合心血管病电子杂志, 2018, 6(14): 153-154.
[17] 李新国, 赵娟. 丹参多酚酸盐联合西药对慢性心力衰竭患者心功能及炎性因子水平的影响 [J]. 临床医学研究与实践, 2018, 3(2): 7-8.
[18] 林能波, 郑炜华, 林永欢. 磷酸肌酸钠联合丹参多酚酸盐治疗冠心病心力衰竭疗效观察 [J]. 海峡药学, 2017, 29(12): 189-190.
[19] 戚凤君, 董志, 郭文娟, 等. 丹参多酚酸盐联合缬沙坦对慢性心力衰竭患者血浆BNP及高敏肌钙蛋白T的影响 [J]. 辽宁中医杂志, 2017, 44(11): 2341-2343.
[20] 蒋亚宝. 丹参多酚酸盐对慢性心力衰竭患者心功能及炎症因子的影响 [J]. 中国初级卫生保健, 2017, 31(11): 72-73.
[21] 薛恩忠, 屈丽娜, 刘春丽. 丹参多酚酸盐联合磷酸肌酸钠对冠心病合并心力衰竭患者心功能的影响 [J]. 中国慢性病预防与控制, 2017, 25(8): 615-617.
[22] 周少军. 注射用丹参多酚酸盐联合常规西药治疗慢性心力衰竭疗效观察 [J]. 新中医, 2016, 48(5): 20-22.
[23] 梅芳, 吴志勇. 丹参多酚酸盐对缺血性心力衰竭患者心率变异性和窦性心律震荡的影响 [J]. 江西医药, 2016, 51(3): 203-206.
[24] 王邦俊, 王志芳, 周利民. 丹参多酚酸盐治疗老年冠心病合并心力衰竭的临床观察 [J]. 蚌埠医学院学报, 2014, 39(12): 1644-1646.
[25] 尚佳, 曲凌光, 葛利军. 磷酸肌酸联合丹参多酚酸盐治疗冠心病心力衰竭的疗效观察 [J]. 北方药学, 2014, 11(12): 74-75.
[26] 郑雁, 李艳辉, 陈海燕. 丹参多酚酸盐对老年慢性心力衰竭患者心功能及氨基末端B型钠尿肽前体浓度的影响 [J]. 中国老年学杂志, 2014, 34(18): 5121-5122.
[27] 杨溶海, 方长庚, 梁建光. 丹参多酚酸盐对冠心病心力衰竭患者左心功能及血清心型脂肪酸结合蛋白的影响 [J]. 中国老年学杂志, 2014, 34(9): 2323-2325.
[28] 邱雅慧, 薛凌, 高夏青. 丹参多酚酸盐对慢性心力衰竭患者心功能及炎症因子的影响 [J]. 中国实验方剂学杂志, 2013, 19(7): 321-323.
[29] 严翼飞, 周琛, 何世安, 等. 丹参多酚酸盐治疗老年多病因心力衰竭22例临床观察 [J]. 内科, 2013, 8(1): 29-30.
[30] 杨晓琨. 丹参多酚酸盐注射液对血瘀型充血性心力衰竭中医证侯及心功能的影响 [J]. 湖南中医药大学学报, 2009, 29(9): 36-38.
[31] 张涵亮, 高健雄, 徐红岩, 等. 丹参多酚酸盐联合磷酸肌酸钠对老年冠心病心力衰竭患者tP A、PAI-1、GDF-15及NGAL水平的影响 [J]. 中国老年学杂志, 2021, 41(11): 2247-2249.
[32] 沈继龙, 朱克军, 李增男, 等. 丹参多酚酸盐治疗慢性心力衰竭患者的临床效果及对血浆脑钠肽的影响 [J]. 中国综合临床, 2014, 30(8): 840-844.
[33] 闫文珍, 黄淑田. 磷酸肌酸钠联合丹参多酚酸盐治疗冠心病心力衰竭疗效观察 [J]. 中国基层医药, 2015, 22(18): 2827-2829.
[34] 邵明, 陈雨婷, 许伟, 等. 试验序贯分析原理及其在meta分析中的应用 [J]. 中国卫生统计, 2022, 39(1): 47-51.
[35] 翁鸿, 李胜, 曾宪涛, 等. 试验序贯分析软件在Meta分析中的应用 [J]. 中国循证医学杂志, 2016, 16(5): 604-611.
[36] 陈素丽, 吴域. 芪参益气滴丸联合参松养心胶囊对气虚血瘀型CHF患者心肌保护、炎症状态的影响 [J]. 中国药物滥用防治杂志, 2021, 27(6): 932-935.
[37] 周艳. 从血瘀论治慢性心力衰竭的探讨 [J]. 中国中医急症, 2014, 23(6): 1090-1091.
[38] 张立新, 刘晓丽, 聂晓博, 等. 丹参多酚酸盐对动脉粥样硬化大鼠TLR4/IL-6/STAT3通路的影响 [J]. 上海中医药大学学报, 2020, 34(4): 61-65.
[39] 李兵. 丹参多酚酸盐对H2O2所致心肌细胞氧化应激损伤及PPARγ/Nrf2/HO-1通路的影响 [J]. 中西医结合心脑血管病杂志, 2021, 19(20): 3493-3499.
[40] 李涛, 王婀莉, 李年生, 等. 丹参乙酸镁通过抑制NOX/VPO1通路阻止肺动脉高压大鼠右心室重构 [J]. 中国药理学与毒理学杂志, 2019, 33(9): 710-711.
[41] 李涛, 罗秀菊, 王婀莉, 等. 丹参乙酸镁通过抑制NADPH氧化酶阻止肺动脉高压大鼠血管平滑肌细胞表型转化 [J]. 中国药理学与毒理学杂志, 2019, 33(9): 750-751.
[42] 陈素枝, 陈文军, 张卓, 等. 丹参多酚酸盐对阳离子化牛血清白蛋白致膜性肾病大鼠的影响 [J]. 中草药, 2018, 49(8): 1877-1883.
[43] 黄桥, 任相颖, 张蓉, 等. GRADE在我国临床实践指南/专家共识中的应用研究 [J]. 中国循证医学杂志, 2021, 21(12): 1457-1462.
Systematic review and trial sequential analysis of efficacy and safety of Salvia Miltiorrhiza Polyphenols Injection combined with conventional western medicine in treatment of chronic heart failure
ZHANG Yao1, YANG Ji1, MU Li-ting2, ZHAO Ying-qiang2, WANG Bao-he2
1. Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China 2. The Second Affiliated Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300250, China 3. First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300381, China
To systematically evaluate the efficacy and safety of conventional western medicine combined with Salvia Miltiorrhiza Polyphenols Injection in the treatment of chronic heart failure.Relevant RCTs in CNKI, Wanfang, VIP, PubMed and other databases were searched by computer, and the search time was limited from the establishment of the database to March 20, 2022. The risk of bias assessment tool was used to evaluate the quality of the literature, RevMan 5.3 and Stata15.0 software were used for Meta-analysis, and TSA 0.9.5.10 Beta software was used for trial sequential analysis (TSA), and the quality of evidence was evaluated according to GRADE standards.A total of 23 RCTs (2421 patients) were finally included, and the overall methodological quality of the included studies was low. Meta-analysis results showed that compared with conventional western medicine, combined with Salvia Miltiorrhiza Polyphenols Injection could significantly improve the clinical total effective rate [OR = 3.95, 95% CI (2.92, 5.35),< 0.000 01], reduce Lee heart failure score [MD = −0.95, 95%CI (−1.37, −0.52),< 0.000 1], increase 6 min walking distance [MD = 44.50, 95% CI (32.02, 56.97),<0.000 01], decrease plasma B-type natriuretic peptide (BNP) concentration [MD = −74.78, 95% CI (−89.24, −60.33),< 0.000 01], improve cardiac function indicators, including increased left ventricular ejection fraction (LVEF) [MD = 5.33, 95% CI (4.33, 6.32),< 0.000 01], decreased left ventricular end systolic diameter (LVESD) [MD = −5.73, 95% CI (−8.04, −3.43),< 0.000 01], left ventricular end diastolic diameter (LVEDD) [MD = −5.12, 95% CI (−7.16, −3.08),< 0.000 01] and interventricular septal thickness (IVST) [MD = −1.12, 95% CI (−1.60, −0.64),< 0.000 01], increased cardiac output (CO) [MD = 1.12, 95% CI (1.00, 1.23),< 0.000 01], cardiac index (CI) [MD = 1.12, 95% CI (1.00, 1.25),< 0.000 01] and stroke volume (SV) [MD = 9.34, 95% CI (5.39, 13.29),< 0.000 01], reduced inflammatory markers, including interleukin-6 (IL-6) [MD = −1.84, 95% CI (−2.36,−1.31),< 0.000 01], tumor necrosis factor-α (TNF-α) [MD = −0.74, 95% CI (−0.83, −0.66),< 0.000 01] and high-sensitivity C-reactive protein (hs-CRP) [MD = −0.97, 95% CI (−1.27, −0.67),< 0.000 01], decreased heart fatty acid binding protein (H-FABP) expression [MD = −9.74, 95% CI (−12.21, −7.27),< 0.000 01], there was no statistical difference in the incidence of adverse reactions between the two groups [RR = 0.63, 95% CI (0.18, 2.17),= 0.47]. TSA further affirmed the efficacy of the combined with Salvia Miltiorrhiza Polyphenols Injection in treatment of chronic heart failure. The GRADE evidence quality classification showed that the total effective rate was moderate quality evidence, the Lee heart failure score, LVESD and other eight outcome indicators were all low-quality evidence, and the rest were very low-quality evidence.Compared with conventional western medicine treatment, combined with Salvia Miltiorrhiza Polyphenols Injection could significantly improve the clinical efficacy without obvious adverse reactions. However, the level of evidence is insufficient, and we look forward to conducting more high-quality, large-sample, multi-center RCTs to provide more sufficient evidence-based evidence for Salvia Miltiorrhiza Polyphenols Injection in the treatment of chronic heart failure.
Salvia Miltiorrhiza Polyphenols Injection; chronic heart failure; systematic review; trial sequential analysis; GRADE evidence quality evaluation
R285.64
A
0253 - 2670(2022)19 - 6139 - 20
10.7501/j.issn.0253-2670.2022.19.020
2022-04-20
天津市卫生局课题:基于证候及SBAR模式的终末期心衰医护一体化管理方案研究(2021112);国家重点研发计划:东部中心城市社区心脑血管疾病中医防控模式研究及示范基地建设(2019YFC1710005)
张 垚(1994—),女,汉族,河北保定人,博士研究生,研究方向为心脑血管疾病中医药防治、中药临床药理研究及中药临床评价。E-mail: 443902877@qq.com
穆丽婷 E-mail: mu.lt@163.com
赵英强 E-mail: zhaoyingqiang1000@126.com
[责任编辑 潘明佳]
