木质素及其衍生物在药物制剂中的应用研究进展
2022-10-08卢富源傅英娟倪书振陈晓倩
卢富源,傅英娟,倪书振,陈晓倩
木质素及其衍生物在药物制剂中的应用研究进展
卢富源,傅英娟,倪书振,陈晓倩*
(齐鲁工业大学(山东省科学院) 生物基材料与绿色造纸国家重点实验室,山东 济南 250353)
简述了近年来木质素及其衍生物在药物制剂领域的国内外研究进展,介绍了木质素的结构、活泼性反应基团的特点。总结了木质素类制剂的抗菌、抗氧化性和抗癌作用,以及其作为片剂辅料在药物传递和控制性释放领域的应用和木质素与其它抗菌性金属材料协同作用在给药和抗菌领域应用的发展前景。提出了木质素在体内给药时潜在的药物副作用、运载药物的精准靶向释放等亟待解决的问题。
木质素;木质素衍生物;药物制剂;金属纳米复合材料;医药科学
木质素作为自然界唯一富含苯环结构的植物资源,是制备功能材料的优质原料,主要基于其含量丰富、生态环境友好、无毒性、生物相容性好且具有较强的抗菌、抗氧化和吸收紫外线等特性。虽然木质素在自然界中含量丰富并且可再生,但对其利用程度并不高,世界上每年木质素制品的量也仅仅占排出废液中木质素总量的2%左右。将木质素进行改性制备高附加值的功能材料可以大大的提高其利用价值,保护环境的同时带了更多的经济效益。
目前,随着各类药物使用的日益增多,人们对于药物的安全使用问题也得到越来越广泛的关注。例如双氯芬酸钠、布洛芬、扑热息痛等疏水性药物的生物相容性差且容易对胃肠道以及肝脏造成不同程度的损伤,为了提高药效并降低药物的副作用,需要解决药物溶解性、稳定性、生物利用度等问题,因此,开发新型功能材料来改善药物制剂的性能对医药行业技术突破至关重要。而木质素的抗菌和抗氧化性使其在该领域表现出巨大的应用潜力。相关研究显示,基于木质素自身的结构特性和功能,将木质素单体及其衍生物改性后用于药物制备或药物辅助添加剂中,可以有效增强药物的崩解性和提高药物生物利用度[1]。另外,木质素存在各种有机官能团、较高的表面积、较强的金属连接反应特性以及优良的结构修饰能力,利用结构中丰富的活性位点引入抗菌性的金属离子制备木质素基金属纳米复合材料,可以增强药物疗效,提高抗菌和抗病毒的效果。
本文对木质素及其衍生物在医药领域的国内外研究进展与发展趋势进行了综述,总结了木质素及其衍生物在药物制剂合成和片剂辅料领域的应用以及木质素基金属纳米复合材料在抗菌抗病毒药物制剂中的研究进展。
1 木质素的结构
木质素的结构单元是苯基丙烷,主要连接方式为醚键和碳-碳键等,具有三维空间结构[2](如图1)。不同种类植物中木质素的芳香核结构也会随着植物的进化和种属的差异而不同,目前主要分为三种类型:对羟苯基型木质素(H型)、愈创木基型木质素(G型)和紫丁香基型木质素(S型)(见图1a)。木质素含有大量的甲氧基、酚羟基、醇羟基、羧基等基团,其中具备较高反应活性的游离酚羟基易发生离子化,使酚羟基的对、邻位得到活化。目前,对于木质素改性常用的方法主要包括:磺化改性、聚合改性、胺化改性、枝接改性和降解改性。不同的改性方法制备出具有不同化学结构的木质素衍生物,合成的木质素衍生物在各自具备独特的特性之外也保留了木素本身具有的抗菌、抗氧化和良好的生物相容性等特性,从而使其在医药领域可以发挥作用。

图1 木质素的三种结构单元类型及其连接方式[3]
2 木质素及其衍生物在药物制剂中的应用
木质素具有的芳香环和侧链上的一些基团结构是许多天然分子的生物活性基团[4],使其具有良好的抗氧化能力和自由基清除能力,随着对木质素结构的深入研究,基于木质素自身结构得到的木质素衍生物逐渐引起研究人员的重视,木质素及其衍生材料在医药科学领域的研究具有良好的前景。木质素及其衍生材料可直接用于制作抗诱变剂和抗癌剂,或者与药物混合制作木质素类药物制剂来增强药物疗效、达到抗菌和抗病毒效果,另外,将木质素或其衍生物作为片剂药物合成处方中的辅料可以提高药物的生物利用度和崩解度、溶解度等[5]。
2.1 木质素类制剂的抗菌和抑制作用
木质素类制剂可以取代有机合成的化合物成为预防癌症和其他疾病的天然药物组分。Oeyen等[6]针对多种木质素磺酸盐对人体细胞内免疫缺陷病毒(HIV)和单纯疱疹病毒(HSV)传播复制能力的影响进行了测定,发现其可抑制HIV-1、HIV-2、HSV-1、HSV-2不同菌株的复制,还可以抑制HIV-1/HSV-2的双重感染,其抗病毒活性与木质素磺酸盐和病毒包膜糖蛋白的相互作用有关。该研究为实现艾滋病治疗开辟了新的路径。碱木质素作为羟基自由基清除剂在治疗癌症领域也占有重要地位,Lu等[7]通过给动物喂食木质素类饲料,对比发现碱木质素表现出的抗自由基性能可以抑制自由基相关酶的反应,达到阻碍癌细胞(HeLa S3细胞)繁殖和生存的效果,当碱木质素的IC50为59.08mg/mL时,可抑制与超氧阴离子自由基产生有关的酶之一黄嘌呤氧化酶的活性,并呈现混合型非竞争性抑制模式,此外碱木质素还可以阻碍葡萄糖-6-磷酸脱氢酶的活性,并以剂量依赖方式阻碍癌细胞的生长和生存。此研究在木质素的高值化利用和癌症治疗领域都具有广阔的应用前景。Košıková等[8]使用多种生物质木质素作为原材料与N-亚硝基二乙胺和胆汁酸进行结合制得木质素制剂,其中改性木质素制剂和预水解木质素制剂对4-硝基喹啉-N-氧化物诱导产生的致病突变表现出优异的抑制作用。同时,由于木质素具有抗氧化特性,以上木质素制剂对经过氧化氢处理的仓鼠V79细胞和人体VH10、CaCo-2结肠癌细胞的脱氧核糖核酸(DNA)具有保护作用且可以降低DNA的烷基化突变程度。
Yasushi Ito等[9]对竹子木质素进行改性,制得其酚类衍生物Lig-8。研究发现Lig-8对氧化应激诱导的细胞凋亡具有强烈的抑制作用,且在浓度为30 μM和静息条件下对任何蛋白酶体活性都没有影响。该研究还证实了Lig-8可降低视网膜损伤,可通过抑制过度的内质网应激反应来保护神经元免受损伤,该研究将在临床视力呵护和神经元保护等领域发挥重要作用。除此之外,Czaikoski等[10]针对工业木质素(木质素磺酸钙和硫酸盐木质素)对Caco-2和HT-29细胞系的毒理作用进行了研究,进一步促进了木质素这种可生物降解材料的聚合形式在医药等领域的应用。Pigarev等[11]以钼酸铵为原料合成新型木质素多酚类化合物BP-C2,使用BP-C2处理动物的血白细胞和骨髓样本,结果显示,TDNA%略高于阴性对照(载体)但显著低于阳性对照(MMS),因此BP-C2对甲基磺酸甲酯(MMS)诱导的DNA损伤具有基因保护作用,可以将其作为一种基因保护剂应用于职业环境或生活环境长期暴露于有致癌风险的领域中,现已在医疗领域的辐射防护剂/抑制剂中得到广泛应用。
2.2 木质素类制剂作为片剂辅料在药物传递和控制释放领域的应用
除了利用木质素与及其衍生物自身所具有的特性来对某些疾病进行治疗或者防护以外,将木质素作为片剂口服药物合成处方中的辅料,以提高片剂的崩解度和生物利用度也非常的具有研究前景。当今制药工业中,片剂因其制备工艺简单、药物溶出速度快且具有良好的身体稳定性等特点成为主要制备工艺之一。由于生物利用度在药物开发中起着至关重要的作用,因此,提高药物的生物利用度正成为制药行业的主线任务之一。而释药速度对片剂的生物利用度[12]影响很大,药物的释放速度越快,则其生物利用度越高,带来的副作用就越小。辅料是药物生产中用于辅助生产和控制用量、质量、稳定性、生物利用度、毒性和功效的惰性物质[12-13]。随着辅料性质的变化,片剂的硬度、崩解度、加工性和生物利用度等均会随着发生变化。目前,很多研究人员利用天然生物聚合物木质素所具有的抗菌、抗氧化性以及来源广泛、价格低廉等特点将其作为片剂生产过程中的辅料,同时,木质素可以通过化学修饰来提高药物的传递和实现药物的控制释放。Pishnamazi等[14]将乙醇黑液木质素进行羧化改性后,将其作为辅料添加到非甾体抗炎药的合成中,研究其对药物释放行为的影响(见图2)。羧化木质素的加入导致原药和木质素的相互作用程度降低,使药物的崩解速度变快、释药量增高,该研究将木质素及其衍生物成功应用于口服药物辅料合成领域中。

图2 木质素羧化机理[14]
Pishnamazi等[15]使用乙醇黑液木质素作为辅料,乙酰水杨酸(阿司匹林)作为活性药物成分(API),将其混合制成片剂,并对药片的溶出速率进行表征。实验结果显示含有木质素作为辅料的片剂具有较快的释药、崩解速度以及较高的片剂硬度。该研究成功为低水溶性药物生物利用度的提高开创了新途径。Domínguez-Robles等[16]选取木质素和微晶纤维素(MCC)作为制备抗菌类药物四环素(TC)片剂的辅料,研究表明单独使用木质素或MCC作为赋形剂制得的片剂的密度和破碎强度不高,而将木质素和MCC混合作为辅料可显著改变片剂的释放曲线和最大释放量,此外木质素自身特性为TC片剂提供了抗氧化性能。因此,利用木质素―其他辅料混合体系作为合成片剂制剂这一领域正不断得到重视,并在生物医药等领域实现了初步应用。另外,将木质素及其衍生物应用于膳食添加剂或者肥料片剂辅助剂也很具有一定的研究价值。
2.3 木质素基金属纳米材料与药物制剂
除了单独作为抗菌添加剂外,木质素还可与其他抗菌材料结合以产生协同作用。木质素可作为绿色还原剂基于其自身的丰富活性官能团,无需添加外源还原剂就可以将Pd、Ag、Au和Pt等金属离子还原为金属纳米粒子[2]。金属纳米粒子具有杀菌、抗病毒、抗真菌、抗癌和抗氧化特性[17-24],与木质素结合制得木质素金属纳米颗粒,使其在给药领域和抗菌领域具有巨大的应用潜力。

图3 木质素还原Ag+的过程[25]
例如,Shen等[25]在研究中选取生物质木质素作为反应的稳定剂和还原剂,在微波照射下用Tollens试剂制备直径在24 nm左右的球形木质素基Ag纳米颗粒,所制备的Ag-NPs对Hg2+表现出高选择性的传感检测,该研究提供了一种绿色、快速合成Ag-NPs的方法,可进行有针对性的检测有毒离子Hg2+,可应用在临床重金属中毒检测领域,木质素还原Ag+的过程如图3。当木质素取代银纳米颗粒的核心时,其表现出良好的抗菌性能,而不产生会对生态带来不利影响的银离子的释放[26-27](图4)。
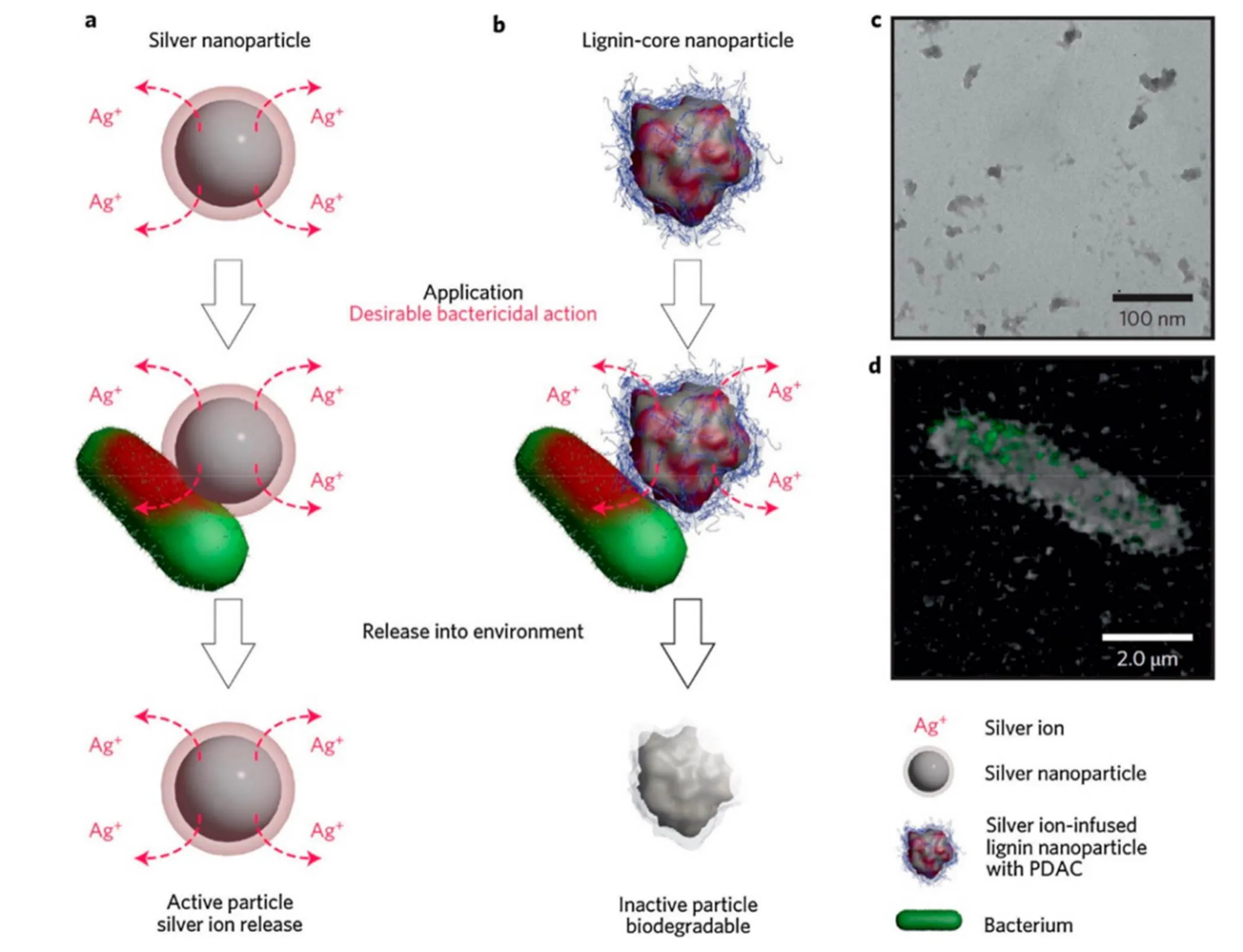
图4 银纳米颗粒和木质素银纳米颗粒的杀菌作用示意图[26-27]
Pletzer等[28]选择木质素作为还原剂和封端剂,采用微波辅助方法合成木质素银纳米颗粒(Ag-LNPs)。抗菌性实验表明Ag-LNPs对革兰氏阳性菌和革兰氏阴性菌均表现出广谱的抗菌活性,对单核细胞THP-1的细胞毒性≤20%,表明Ag-LNPS具有对细胞无明显毒性作用、对病原菌耐受性良好等优异特性。突出了木质素银纳米颗粒作为治疗耐药性病原菌的替代或药物辅助方面有潜在的应用价值。另外,经木质素还原得到的Ag纳米颗粒对大肠杆菌表现出极佳抗菌活性[29](图5),结果表明,含有木质素/Ag纳米颗粒复合材料的琼脂板上的细菌生长完全受到抑制。

图5 培育大肠杆菌的琼脂板:(a) 未含木质素/Ag纳米颗粒;(b)含木质素/Ag纳米颗粒;(c) 含木质素/Ag纳米颗粒复合膜[29]
Saratale等[30]使用麦秸中纯化的木质素制成溶液与AgNO3溶液混合得到银纳米粒子(Li-AgNPs),合成的Li-AgNPs尺寸在15~20 nm之间,且其表面被木质素酚基、羟基和羧基覆盖。抗菌性实验表明该粒子对人类病原体(即金黄色葡萄球菌和大肠杆菌)显示出明显的抑制效果,Li-AgNPs在ABTS和DPPH自由基清除试验方面也表现出明显抗氧化活性。Li-AgNPs的体外细胞毒性试验显示其对SKOV3卵巢癌细胞具有显著的抗癌作用,增强了其在医药领域的实践性。利用木质素银纳米颗粒(Ag-LNPS)的抗菌特性及极低的细胞毒性等特点,可以有效地打破某些抗生素及病菌的耐药性,从而提高药物的治疗效果。Kaur等[31]使用生物质木质素与氧化锌(ZnO)采取环保有效的方法合成氧化锌纳米复合材料(ZnO-NCs),基于木质素与ZnO纳米粒子的协同作用,ZnO-NCS表现出优异的紫外屏蔽和抗菌性能。将ZnO-NCS作为添加剂加入到医用乳霜中,可以赋予其紫外线阻隔和抗菌特性。Wang等[32]使用碱木质素(AL)改性得到的季铵化碱木质素(QAL)与六水硝酸锌和六亚甲基四胺的水溶液混合,水热法制备季铵化碱木质素/氧化锌(QAL/ZnO)纳米复合材料,该材料具有优良的紫外线吸收性能和稳定性(图6),为木质素在医药功能材料领域的高附加值应用开辟了一条新道路。

图6 纯ZnO(a)和QAL/ZnO纳米复合材料的SEM图像[32]
(b)QAL/ZnO-0.5;(c)QAL/ZnO-1.0;和(d)QAL/ZnO-1.5
Lü等[33]以N-甲基苯胺为原料,木质素磺酸盐(LS)为分散剂制备聚N-甲基苯胺-木质素磺酸盐(PNMA-LS)复合微球,PNMA-LS复合微球对Ag+具有优异的吸附特性,通过吸附Ag+制备得到新型三元复合材料(PNMA-LS-Ag),其对人类病原体具有抗菌性能,对金黄色葡萄球菌和大肠杆菌的抗菌率分别达到99.95%和99.99%。Shankar等[34]利用有机溶剂木质素制备银纳米粒子(Ag-NPs),并将其加入到聚乳酸(PLA)聚合物中制备复合膜,该复合膜对大肠杆菌和单细胞李斯特菌表现出明显的抗菌活性,进一步证实了其在医用抗菌领域的应用潜能。随着木质素基金属纳米复合材料应用方面的研究的日渐深入,其所具有的绿色环保、高附加值等的特点逐渐浮现。此外,木质素基金属纳米复合材料的制备也为木质素的高端应用提供了创新途径。
3 结语
尽管木质素生物基材料在生物医学、药物载体等领域的利用率越来越高,在该领域的研究也相应取得了很多进展。但由于木质素自身错综复杂的结构,导致木质素的长期稳定性以及当其在体内给药时潜在的药物副作用、运载药物的精准靶向释放等问题仍亟待解决。利用木质素特有的两亲性、化学通用性和良好生物性能来探索医药、化妆品乳化剂以及水凝胶和气凝胶等方面潜在价值,以及具有不同结构的木质素在细胞水平、激素、蛋白质和免疫系统等方面的生物学效应等领域的研究必将受到越来越多研究人员的重视。
[1] Arafa M F, El-Gizawy S A, Osman M A,. Xylitol as a potential co-crystal co-former for enhancing dissolution rate of felodipine: preparation and evaluation of sublingual tablets[J]. Pharm Dev Technol, 2018, 23(5): 454-463.
[2] 储晶晶, 张莉莉, 王志国. 木质素基金属纳米粒子复合材料的制备及其应用研究进展[J]. 复合材料学报, 2020, 37(11): 2657-2673.
[3] Gall D L, Ralph J, Donohue T J,. Biochemical transformation of lignin for deriving valued commodities from lignocellulose[J]. Current Opinion in Biotechnology, 2017, 63(2): 120-126.
[4] 任建鹏, 李鹏辉, 蒋政伟, 等. 木质素在吸附材料领域中的应用研究进展[J]. 功能材料, 2022, 53(6): 6060-6066.
[5] 汤潜潜. 木质素磺酸盐的浓溶液行为研究及纳米木质素微球的制备[D]. 华南理工大学, 2015.
[6] Oeyen M, Noppen S, Vanhulle E,. A unique class of lignin derivatives displays broad anti-HIV activity by interacting with the viral envelope[J]. Virus Research, 2019, 274: 197760.
[7] Lu F J, Chu L H, Gau R J. Free radical-scavenging properties of lignin[J]. Nutr Cancer, 1998, 30(1): 31-8.
[8] Košı́Ková B, Slameňová D, Mikulášová M,. Reduction of carcinogenesis by bio-based lignin derivatives[J]. Biomass and Bioenergy, 2002, 23(2): 153-159.
[9] Ito Y, Akao Y, Shimazawa M,. Lig-8, a highly bioactive lignophenol derivative from bamboo lignin, exhibits multifaceted neuroprotective activity[J]. Cns Drug Reviews, 2007, 13(3): 296-307.
[10] Czaikoski A, Gomes A, Kaufmann K C,. Lignin derivatives stabilizing oil-in-water emulsions: Technological aspects, interfacial rheology and cytotoxicity[J]. Industrial Crops and Products, 2020, 154(15):112762.
[11] Pigarev S E, Trashkov A P, Panchenko A V,. Evaluation of the genotoxic and antigenotoxic potential of lignin-derivative BP-C2 in the comet assay in vivo[J]. Environmental Research, 2021, 192:110321.
[12] Torrado S, Cadorniga R, Torrado J J. Effect of drug release rate on bioavailability of different aspirin tablets[J]. International Journal of Pharmaceutics, 1996, 133(1): 65-70.
[13] Zhenhao D, Xingxing D, Xinyuan S,. Design and development of pharmaceutical excipients database[J]. World Science and Technology, 2011, 13(4): 611-615.
[14] Pishnamazi M, Hafizi H, Shirazian S,. Design of controlled release system for paracetamol based on modified lignin[J]. Polymers, 2019, 11(6): 1059-1069.
[15] Pishnamazi M, Iqbal J, Shirazian S,. Effect of lignin on the release rate of acetylsalicylic acid tablets[J]. International Journal of Biological Macromolecules, 2019, 124(1): 354-359.
[16] Dominguez-Robles J, Stewart S A, Rendl A,. Lignin and cellulose blends as pharmaceutical excipient for tablet manufacturing via direct compression[J]. Biomolecules, 2019, 9(9): 423-440.
[17] Gurunathan S, Raman J, Malek N A,. Green synthesis of silver nanoparticles using Ganoderma neo-japonicum Imazeki: A potential cytotoxic agent against breast cancer cells[J]. International Journal of Nanomedicine, 2013, 8(1): 4399-4413.
[18] Jeong S H, Yeo S Y, Yi S C. The effect of filler particle size on the antibacterial properties of compounded polymer/silver fibers[J]. Journal of Materials Science, 2005, 40(20): 5407-5411.
[19] Kaviya S, Santhanalakshmi J, Viswanathan B,. Biosynthesis of silver nanoparticles using citrus sinensis peel extract and its antibacterial activity[J]. Spectrochimica Acta Part a-Molecular and Biomolecular Spectroscopy, 2011, 79(3): 594-598.
[20] Khandelwal N, Kaur G, Chaubey K K,. Silver nanoparticles impair Peste des petits ruminants virus replication[J]. Virus Research, 2014, 190: 1-7.
[21] Moldovan B, David L, Achim M,. A green approach to phytomediated synthesis of silver nanoparticles using Sambucus nigra L. fruits extract and their antioxidant activity[J]. Journal of Molecular Liquids, 2016, 221: 271-278.
[22] Prucek R, Tucek J, Kilianova M,. The targeted antibacterial and antifungal properties of magnetic nanocomposite of iron oxide and silver nanoparticles[J]. Biomaterials, 2011, 32(21): 4704-4713.
[23] Satyavani K, Gurudeeban S, Ramanathan T,. Biomedical potential of silver nanoparticles synthesized from calli cells of Citrullus colocynthis (L.) Schrad[J]. Journal of Nanobiotechnology, 2011, 9: 43-51.
[24] Wang L Y, Luo J, Shan S Y,. Bacterial inactivation using silver-coated magnetic nanoparticles as functional antimicrobial agents[J]. Analytical Chemistry, 2011, 83(22): 8688-8695.
[25] Shen Z, Luo Y, Wang Q,. High-value utilization of lignin to synthesize ag nanoparticles with detection capacity for Hg2+[J]. ACS Applied Materials & Interfaces, 2014, 6(18): 16147-16155.
[26] Richter A P, Brown J S, Bharti B,. An environmentally benign antimicrobial nanoparticle based on a silver-infused lignin core[J]. Nature Nanotechnology, 2015, 10: 817-823.
[27] Shu F, Jiang B, Yuan Y,. Biological activities and emerging roles of lignin and lignin-based products: A review[J]. Biomacromolecules, 2021, 22(12): 4905-4918.
[28] Pletzer D, Asnis J, Slavin Y N,. Rapid microwave-based method for the preparation of antimicrobial lignin-capped silver nanoparticles active against multidrug-resistant bacteria[J]. International Journal of Pharmaceutics, 2021, 596: 120299.
[29] Hu S X, Hsieh Y L. Synthesis of surface bound silver nanoparticles on cellulose fibers using lignin as multi-functional agent[J]. Carbohydrate Polymers, 2015, 131(20): 134-141.
[30] Saratale R G, Saratale G D, Ghodake G,. Wheat straw extracted lignin in silver nanoparticles synthesis: Expanding its prophecy towards antineoplastic potency and hydrogen peroxide sensing ability[J]. International Journal of Biological Macromolecules, 2019, 128(1): 391-400.
[31] Kaur R, Thakur N S, Chandna S,. Development of agri-biomass based lignin derived zinc oxide nanocomposites as promising UV protectant-cum-antimicrobial agents[J]. Journal of Materials Chemistry B, 2020, 8(2): 260-269.
[32] Wang H, Qiu X, Liu W,. A novel lignin/ZnO hybrid nanocomposite with excellent UV-absorption ability and its application in transparent polyurethane coating[J]. Industrial & Engineering Chemistry Research, 2017, 56(39): 11133-11141.
[33] Lu Q F, Zhang J Y, Yang J,. Self-assembled poly(N-methylaniline)-lignosulfonate spheres: From silver-ion adsorbent to antimicrobial material[J]. Chemistry-a European Journal, 2013, 19(33): 10935-10944.
[34] Shankar S, Rhim J-W, Won K. Preparation of poly(lactide)/lignin/silver nanoparticles composite films with UV light barrier and antibacterial properties[J]. International Journal of Biological Macromolecules, 2018, 107: 1724-1731.
Recent Advances in the Utilization of Lignin and Lignin-based Products in Pharmaceutic Preparation
LU Fu-yuan, FU Ying-juan, NI Shu-zhen, CHEN Xiao-qian*
(State Key Laboratory of Biobased Materials and Green Papermaking,Qilu University of Technology (Shandong Academy of Sciences), Jinan 250353, China)
The recent progress of domestic and international research on lignin and its derivatives in the field of pharmaceutical formulations is briefly described. The structure of lignin and the characteristics of the active reactive groups are introduced. The antibacterial, antioxidant and anticancer effects of lignin preparations and the application of lignin as tablet excipients in drug delivery and controlled release of drugs are summarized. The recent investigations of the synergistic effects of lignin with antibacterial metal materials are discussed. The applications and development prospects of lignin based metal materials in the fields of biomedical and antibacterial are reviewed. The potential drug side effects of lignin delivery in vivo and the precise targeted release of the delivered drugs are presented.
lignin; lignin derivative; pharmaceutic preparation; metal nanocomposite; pharmaceutical science
1004-8405(2022)03-0036-09
10.16561/j.cnki.xws.2022.03.01
2022-05-04
山东省自然科学基金青年项目(ZR2020QB137);生物基材料与绿色造纸国家重点实验室开放基金资助项目
(ZZ20190110)。
卢富源(1999~),男,硕士;研究方向:木质化生物质资源特性及其应用。
通讯作者:陈晓倩(1989~),女,博士,讲师;研究方向:木质化生物质资源特性及其应用、生物基材料及绿色造纸。chenxiaoqian@qlu.edu.cn
TS7
A
